Молекулярные и кристаллические структуры карбоксилатов три- и тетраарилсурьмы
Автор: Шарутин Владимир Викторович, Сенчурин Владислав Станиславович, Шарутина Ольга Константиновна, Чагарова Ольга Викторовна
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Органическая химия
Статья в выпуске: 33 (250), 2011 года.
Бесплатный доступ
Взаимодействием триарилсурьмы с карбоновой кислотой в присутствии пероксида водорода (1:2:1 мольн.) в эфире синтезированы дикарбоксилаты триарилсурьмы: Ph3Sb[OC(O)C6H4OMe-2]2 (I), Ph3Sb[OC(O)CH2C6H4NO2-4]2 (II), Ph3Sb[OC(O)cyclo-C3H5]2 (III), Ph3Sb[OC(O)C6H4NO2-2]2 (IV), (3-MeC6H4)3Sb[OC(O)C6H4OMe-2]2 (V). Карбоксилаты тетрафенилсурьмы: Ph4SbOC(O)C6H4OMe-2 (VI), Ph4SbOC(O)CH2C6H4NO2-4 (VII), Ph4SbOC(O)cyclo-C3H5 (VIII) и Ph4SbOC(O)C6H4NO2-2 (IX) получены из пентафенилсурьмы и дикарбоксилатов трифенилсурьмы (1:1 мольн.) в толуоле. По данным РСА, атомы сурьмы в молекулах I, II, III, V имеют искаженную тригонально-бипирамидальную координацию с атомами кислорода карбоксильных групп в аксиальных положениях. Аксиальные углы OSbO в I-III, V равны 173,30(6)° (I), 173,35(11)° (II), 176,46(4)° (III), 173,58(19)° (V), валентные углы CSbC составляют 104,30(5)°, 104,30(5)°, 151,39(10)° (I); 110,04(9)°, 110,04(9)°, 139,91(17)° (II); 104,44(6)°, 106,38(5)°, 149,18(6)° (III); 105,3(3)°, 105,9(3)°, 148,8(3)° (V). Интервалы изменения длин связей Sb-O и Sb-C составляют 2,106(2)-2,137(5) A и 2,082(2)-2,1258(16) A. Внутримолекулярные расстояния Sb???O=С равны 2,611(3)-3,012(3) A. В молекулах карбоксилатов тетрафенилсурьмы (VII,IX), имеющих искаженную тригональнобипирамидальную конфигурацию, аксиальные углы CSbO, длины связей Sb-C, Sb-O и внутримолекулярные контакты Sb???O=С составляют 176,26(8)°, 2,115(2)-2,168(3), 2,220(2) и 3,247(3) A (VII); 176,39(8)°, 2,115(3)-2,167(2), 2,325(2) и 3,318(3) A (IХ).
Строение, карбоксилаты, тетрафенилсурьма, трифенил-сурьма
Короткий адрес: https://sciup.org/147160205
IDR: 147160205 | УДК: 546.863+546.865+547.152+547.53.024+548.312.5
Molecular and crystal structures of tri- and tetraarylantimony carboxylates
Triarylantimony interaction with a carboxylic acid in ether medium in the presence of hydrogen peroxide (1:2:1 mol.) has synthesized triarylantimony dicarboxylates: Ph3Sb[OC(O)C6H4OMe-2]2 (I), Ph3Sb[OC(O)CH2C6H4NO2-4]2 (II), Ph3Sb[OC(O)cyclo-C3H5]2 (III), Ph3Sb[OC(O)C6H4NO2-2]2 (IV), (3-MeC6H4)3Sb[OC(O)C6H4OMe-2]2 (V). Tetraphenylantimony carboxylates: Ph4SbOC(O)C6H4OMe-2 (VI), Ph4SbOC(O)CH2C6H4NO2-4 (VII), Ph4SbOC(O)cyclo-C3H5 (VIII) и Ph4SbOC(O)C6H4NO2-2 (IX) have been obtained from pentaphenylantimony and triphenylantimony dicarboxylates (1:1 mol.) in toluene. According to the X-ray diffraction analysis, antimony atoms in the molecules I, II, III, V have a distorted trigonal-bipyramidal coordination with the oxygen atoms of the carboxyl groups in axial positions. Axial OSbO angles in I-III, V are equal to 173.30(6)° (I), 173.35(11)° (II), 176.46(4)° (III), 173.58(19)° (V), CSbC angles are 104.30(5)°, 104.30(5) °, 151.39(10)° (I); 110.04(9)°, 110.04(9)°, 139.91(17)° (II); 104.44(6)°, 106.38( 5)°, 149.18(6)° (III); 105.3(3)°, 105.9(3)°, 148.8(3)° (V). Ranges of Sb-O and Sb-C bond lengths are 2.106(2)-2.137(5) A and 2.082(2)-2.1258(16) A. Intramolecular distances Sb???O=C are equal to 2.611(3)-3.012 (3) A. In the molecules of tetraphenylantimony carboxylates (VII, IX), which have a distorted trigonal-bipyramidal configuration, the axial CSbO angles, Sb-C and Sb-O bond lengths and intramolecular contacts Sb???O =C are 176.26(8)°, 2.115(2 )-2.168 (3), 2.220(2) and 3.247 (3) A (VII); 176.39(8)°, 2.115(3)-2.167(2), 2.325(2) and 3.318 (3) A (IX).
Текст научной статьи Молекулярные и кристаллические структуры карбоксилатов три- и тетраарилсурьмы
Известно, что лиганды в карбоксилатах тетра- и в дикарбоксилатах триорганилсурьмы, как правило, проявляют бидентатные свойства [1–8], поскольку имеют место невалентные взаимодействия центрального атома сурьмы с атомами кислорода карбонильных групп Sb···O=С. При этом асимметрия координации лигандов в зависимости от природы радикала в остатке кислоты и типа сурьмаорганического производного достаточно сильно различается. Установлено, что наличие внутримолекулярного контакта Sb···O=С приводит к увеличению угла CSbC в экваториальной плоскости [2].
C целью установления возможности проявления других внутри- и межмолекулярных взаимодействий в кристаллах нами синтезированы и структурно охарактеризованы дикарбоксилаты триарилсурьмы (Ar 3 Sb(OC(O)R) 2 ) и карбоксилаты тетрафенилсурьмы (Ph 4 SbOC(O)R), в R -группах которых присутствуют функциональные группы с гетероатомами.
Экспериментальная часть
Синтез бис (2-метоксибензоата) трифенилсурьмы (I). К смеси 0,50 г (1,42 ммоль) трифе-нилсурьмы и 0,43 г (2,83 ммоль) 2-метоксибензойной кислоты в 20 мл диэтилового эфира прибавляли 0,16 г 30 %-ного водного раствора пероксида водорода и выдерживали 24 ч при 20 °С. Образовавшиеся кристаллы фильтровали и сушили. Получили 0,84 г (90 %) неокрашенных игольчатых кристаллов I с т. пл. 166 °С.
Найдено, %: С 62,23, Н 4,57.
Для C34H29O6Sb вычислено, %: С 62,31, Н 4,43.
ИК-спектр ( ν , см‾1): 3071, 3054, 2989, 2964, 2939, 2833, 1601, 1559, 1486, 1480, 1464, 1436, 1356, 1268, 1250, 1179, 1167, 1145, 1047, 1022, 996, 862, 748, 741, 697, 690, 666, 561, 536, 455.
Аналогично осуществляли синтез других дикарбоксилатов триарилсурьмы.
Бис (4-нитрофенилацетат) трифенилсурьмы (II) – бесцветные кристаллы, выход 98 %, т. пл. 168 °С.
Найдено, %: С 57,09, Н 3,84.
Для C34H27N2O8Sb вычислено, %: С 57,22, Н 3,79.
ИК-спектр ( ν , см‾1): 3097, 3074, 3060, 2986, 2934, 2849, 1653, 1605, 1597, 1520, 1511, 1479, 1435, 1349, 1342, 1316, 1303, 1154, 1106, 934, 854, 824, 767, 749, 734, 690, 669, 597, 451.
Бис (циклопропанкарбоксилат) трифенилсурьмы (III) – бесцветные кристаллы, 96 %, т. пл. 154 °С.
Найдено, %: С 59,47, Н 4,87.
Для C26H25O4Sb вычислено, %: С 59,66, Н 4,78.
ИК-спектр ( ν , см‾1): 3058, 1615, 1598, 1479, 1434, 1381, 1304, 1260, 1251, 1184, 1073, 1061, 1031, 1021, 996, 944, 898, 820, 742, 738, 691, 678, 536, 465, 456.
Бис (2-нитробензоат) трифенилсурьмы (IV) – бесцветные кристаллы, 90 %, т. пл. 184 °С.
Найдено, %: С 55,86, Н 3,57.
Для C32H23O8N2Sb вычислено, %: С 56,08, Н 3,36.
ИК-спектр (ν, см‾1): 3061, 2989, 1665, 1610, 1576, 1527, 1481, 1437, 1361, 1315, 1263, 1137, 1075, 996, 861, 835, 795, 784, 737, 701, 689, 650, 593, 565, 447.
Бис (2-метоксибензоат) три( м -толил)сурьмы (V) – бесцветные кристаллы, 97 %, т. пл. 136 °С.
Найдено, %: С 63,54, Н 5,17.
Для C37H35O6Sb вычислено, %: С 63,70, Н 5,02.
ИК-спектр ( ν , см‾1): 3074, 3032, 2977, 2944, 2843, 1595, 1567, 1487, 1466, 1437, 1401, 1297, 1276, 1236, 1186, 1164, 1104, 1049, 1022, 854, 784, 763, 723, 662, 578, 463, 441.
Синтез 2-метоксибензоата тетрафенилсурьмы (VI). Смесь 0,25 г (0,49 ммоль) пентафе-нилсурьмы, 0,32 г (0,49 ммоль) бис (2-метоксибензоата) трифенилсурьмы и 5 мл толуола в стеклянной ампуле нагревали на кипящей водяной бане в течение 3 ч. После испарения растворителя получили 0,53 г (93 %) неокрашенных кристаллов VI с т. пл. 126 ° С, ИК-спектр и температура плавления которых были идентичны характеристикам вещества, полученного из пентафенил-сурьмы и 2-метоксибензойной кислоты.
Найдено, %: С 66,06, Н 4,79.
Для C32H27O3Sb вычислено, %: С 66,12, Н 4,65.
ИК-спектр ( ν , см‾1): 3072, 3054, 2989, 2965, 2939, 2834, 1601, 1558, 1486, 1480, 1464, 1436, 1356, 1269, 1250, 1179, 1167, 1147, 1048, 1023, 863, 748, 741, 697, 691, 666, 456.
Аналогично осуществляли синтез других карбоксилатов тетраарилсурьмы.
Сольват 4-нитрофенилацетата тетрафенилсурьмы с толуолом Ph 4 SbOC(O)CH 2 C 6 H 4 NO 2 -4·0,5C 6 H 5 CH 3 (VII) - желтые кристаллы, 91 %, т. разл. 128 ° С.
Найдено, %: С 64,76, Н 4,36.
Для C35,5H30O4NSb вычислено, %: С 64,94, Н 4,57.
ИК-спектр ( ν , см‾1): 3061, 1646, 1511, 1435, 1344, 1322, 1253, 1065, 1020, 995, 852, 818, 745, 732, 716, 692, 663, 466, 459, 445.
Циклопропанкарбоксилат тетрафенилсурьмы – бесцветные кристаллы, 93 %, т. пл. 148 °С.
Найдено, %: С 65,07, Н 4,93.
Для C28H25O2Sb вычислено, %: С 65,27, Н 4,86.
ИК-спектр ( ν , см‾1): 3060, 1626, 1574, 1478, 1429, 1395, 1251, 1187, 1064, 996, 939, 848, 759, 737, 690, 652, 516, 473, 455, 445.
2-Нитробензоат тетрафенилсурьмы - бесцветные кристаллы, 93 %, т. пл. 215 ° С.
Найдено, %: С 62,25, Н 3,98.
Для C31H24O4NSb вычислено, %: С 62,44, Н 4,03.
ИК-спектр (ν, см‾1): 3060, 3045, 2987, 1635, 1602, 1576, 1531, 1479, 1435, 1366, 1337, 1257, 1188, 1146, 1064, 1020, 998, 860, 831, 781, 737, 697, 647, 474, 456, 448, 429.
ИК-спектры записывали на ИК Фурье-спектрометре ФСМ 1201 в таблетке из KBr.
Рентгеноструктурный анализ кристаллов выполнен на автоматическом четырехкружном дифрактометре Bruker–Nonius X8Apex (двухкоординатный CCD-детектор, Мо К α -излучение, λ = 0,71073 Å, графитовый монохроматор). Интенсивности отражений измерены методом ф -сканирования узких (0,5°) фреймов до 26 = 50°. Структура расшифрована прямым методом и уточнена полноматричным МНК в анизотропном для неводородных атомов приближении (SHELX-97) [9]. Поглощение учтено эмпирически (SADABS) [10]. Положения атомов водорода рассчитаны геометрически и включены в уточнение в модели «наездника». Основные кристаллографические данные и результаты уточнения структур приведены в табл. 1, основные длины связей и валентные углы – в табл. 2.
Таблица 1
Кристаллографические данные, параметры эксперимента и уточнения структур I–III, V, VII, IX
|
Параметр |
Значение |
|||||
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
|
Соединение |
I |
II |
III |
V |
VII |
IX |
|
Формула |
C 34 H 29 O 6 Sb |
C 34 H 27 N 2 O 8 Sb |
C 26 H 25 O 4 Sb |
C 37 H 35 O 6 Sb |
C 35,5 H 30 NO 4 S b |
C 31 H 24 NO 4 Sb |
|
М |
655,32 |
713,33 |
523,21 |
697,40 |
656,35 |
596,26 |
|
Т , K |
100 |
150 |
100 |
100 |
100 |
150,0(2) |
|
Сингония |
Моноклинная |
Моноклинная |
Моноклинная |
Моноклинная |
Моноклинная |
Моноклинная |
|
Пр. группа |
C 2/ c |
C 2/ c |
P 2 1 / n |
P 2 1 /n |
C 2/ c |
P 2 1 / n |
|
a , Å |
15,5396(3) |
11,8606(6) |
13,6739(4) |
17,3462(9) |
33,7092(9) |
10,2050(2) |
|
b, Å |
9,5332(2) |
16,1033(8) |
10,1444(3) |
9,2707(4) |
10,3496(3) |
14,7868(4) |
|
c, Å |
19,4588(4) |
16,5519(7) |
17,0699(6) |
19,6375(9) |
17,1559(5) |
17,1745(5) |
|
α, ° |
||||||
|
β, ° |
90,5800(10) |
102,846(2) |
110,3520(10) |
91,554(2) |
99,6910(10) |
101,0680(10) |
|
γ, ° |
||||||
|
V , Å3 |
2882,52(10) |
3082,2(3) |
2220,01(12) |
3156,8(3) |
5899,9(3) |
2543,42(11) |
|
Z |
4 |
4 |
4 |
4 |
8 |
4 |
|
р (выч.), г/см3 |
1,510 |
1,537 |
1,565 |
1,467 |
1,478 |
1,557 |
|
ц , мм-1 |
1,002 |
0,951 |
1,273 |
0,920 |
0,976 |
1,123 |
|
F (000) |
1328 |
1440 |
1056 |
1424 |
2664 |
1200 |
|
Форма кристалла (размер, мм) |
Обломок (0,30 х 0,25 х 0,15) |
Иголка (0,05 х 0,05 х 0,40) |
Призма (0,40 х 0,40 х 0,38) |
Обломок (0,20 х 0,12 х 0,04) |
Обломок (0,18 х 0,18 х 0,10) |
Пластинка (0,05 х 0,30 х 0,60) |
|
Область сбора данных по 6 , град |
2,09–31,58 |
2,30–27,50 |
2,36–31,32 |
2,07–25,00 |
2,06–31,62 |
2,56–31,63 |
|
Интервалы индексов отражений |
-19 < h < 21, -9 < к < 13, -21 < l < 28 |
-15 < h < 14, -15 < к < 20, -14 < l < 21 |
-18 < h < 14, -9 < к < 14, -24 < l < 24 |
-19 < h < 20, -11 < к < 11, -23 < l < 22 |
-48 < h < 32, -12 < к < 10, -23 < l < 24 |
-12 < h < 14, -21 < к < 16, -15 < l < 25 |
|
Измерено отражений |
40 590 |
7995 |
15 968 |
27 646 |
18 288 |
16 621 |
|
Независимых отражений |
10 118 |
3530 |
6092 |
5497 |
7875 |
6945 |
|
Переменных уточнения |
188 |
205 |
280 |
402 |
403 |
334 |
|
GOOF |
1,065 |
1,043 |
1,008 |
1,273 |
0,991 |
1,039 |
Окончание табл. 1
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
|
R -факторы по F 2 > 2 σ ( F 2) |
R 1 = 0,0272, wR 2 = 0,0555 |
R 1 = 0,0407, wR 2 = 0,0691 |
R 1 = 0,0207, wR 2 = 0,0500 |
R 1 = 0,0695, wR 2 = 0,1673 |
R 1 = 0,0397, wR 2 = 0,0658 |
R 1 = 0,0346, wR 2 = 0,0746 |
|
R -факторы по всем отражениям |
R 1 = 0,0326, wR 2 = 0,0577 |
R 1 = 0,0553, wR 2 = 0,0747 |
R 1 = 0,0238, wR 2 = 0,0516 |
R 1 = 0,0872, wR 2 = 0,1753 |
R 1 = 0,0646, wR 2 = 0,0732 |
R 1 = 0,0458, wR 2 = 0,0794 |
|
Остаточная электронная плотность (min/max), e / A 3 |
0,565 / –0,523 |
0,874 / –0,730 |
0,620 / –0,502 |
2,893 / –0,918 |
0,609 / –0,699 |
1,140 / –0,488 |
Таблица 2
Длины связей (Å) и валентные углы (град) соединении I
|
Связь |
d, Å |
Угол |
ω , град |
|
1 |
2 |
3 |
4 |
|
I |
|||
|
Sb(1)–O(1) |
2,1305(11) |
O(1)Sb(1)O(1)#1 |
173,30(6) |
|
Sb(1)–C(21) |
2,1255(16) |
C(21)#1Sb(1)O(1) |
90,43(5) |
|
Sb(1)–C(31) |
2,106(2) |
C(21)Sb(1)O(1) |
91,22(5) |
|
O(1)–C(11) |
1,300(2) |
C(21)#1Sb(1)C(21) |
151,39(10) |
|
O(2)–C(11) |
1,240(2) |
C(31)Sb(1)O(1) |
86,65(3) |
|
C(31)Sb(1)C(21) |
104,30(5) |
||
|
II |
|||
|
Sb(1)–O(1) |
2,106(2) |
O(1)Sb(1)O(1)#1 |
173,35(11) |
|
Sb(1)–C(21) |
2,111(3) |
O(1)Sb(1)C(21) |
92,80(10) |
|
Sb(1)–C(31) |
2,108(4) |
O(1)#1Sb(1)C(21) |
89,48(10) |
|
O(1)–C(11) |
1,293(3) |
O(1)Sb(1)C(31) |
86,67(6) |
|
O(2)–C(11) |
1,229(4) |
C(21)Sb(1)C(21)#1 |
139,91(17) |
|
O(3)–N(1) |
1,230(4) |
C(31)Sb(1)C(21) |
110,04(9) |
|
III |
|||
|
Sb(1)–O(11) |
2,1315(11) |
O(21)Sb(1)O(11) |
176,46(4) |
|
Sb(1)–O(21) |
2,1228(10) |
O(21)Sb(1)C(31) |
87,94(5) |
|
Sb(1)–C(31) |
2,1258(15) |
O(21)Sb(1)C(42) |
90,40(5) |
|
Sb(1)–C(42) |
2,1241(15) |
O(21)Sb(1)C(51) |
90,08(5) |
|
Sb(1)–C(51) |
2,1232(14) |
C(42)Sb(1)O(11) |
91,55(5) |
|
O(11)–C(11) |
1,3094(18) |
C(42)Sb(1)C(31) |
104,44(6) |
|
O(12)–C(11) |
1,2425(18) |
C(51)Sb(1)C(31) |
106,38(5) |
|
O(21)–C(21) |
1,3126(19) |
C(51)Sb(1)C(42) |
149,18(6) |
|
V |
|||
|
Sb(1)–O(11) |
2,137(5) |
O(21)Sb(1)O(11) |
173,58(19) |
|
Sb(1)–O(21) |
2,136(5) |
C(31)Sb(1)O(11) |
91,6(3) |
|
Sb(1)–C(31) |
2,110(8) |
C(31)Sb(1)O(21) |
90,2(3) |
|
Sb(1)–C(41) |
2,082(7) |
C(31)Sb(1)C(51) |
148,8(3) |
|
Sb(1)–C(51) |
2,125(8) |
C(41)Sb(1)O(11) |
87,2(3) |
|
O(11)–C(11) |
1,297(9) |
C(41)Sb(1)O(21) |
86,4(3) |
|
O(12)–C(11) |
1,244(10) |
C(41)Sb(1)C(31) |
105,3(3) |
|
O(21)–C(21) |
1,299(9) |
C(41)Sb(1)C(51) |
105,9(3) |
|
O(22)–C(21) |
1,238(10) |
C(51)Sb(1)O(11) |
91,0(3) |
|
VII |
|||
|
Sb(1)–O(1) |
2,2199(18) |
C(11)Sb(1)O(1) |
176,26(8) |
|
Sb(1)–C(11) |
2,168(3) |
C(21)Sb(1)C(11) |
95,85(10) |
|
Sb(1)–C(21) |
2,115(2) |
C(21)Sb(1)C(31) |
117,45(10) |
Окончание табл. 2
|
1 |
2 |
3 |
4 |
|
Sb(1)–C(31) |
2,119(2) |
C(31)Sb(1)O(1) |
81,92(9) |
|
Sb(1)–C(41) |
2,108(3) |
C(31)Sb(1)C(11) |
94,53(10) |
|
O(1)–C(51) |
1,307(3) |
C(41)Sb(1)O(1) |
85,74(9) |
|
O(2)–C(51) |
1,222(3) |
C(41)Sb(1)C(11) |
94,80(10) |
|
O(3)–N(1) |
1,232(3) |
C(41)Sb(1)C(21) |
124,32(9) |
|
O(4)–N(1) |
1,227(3) |
C(41)Sb(1)C(31) |
115,90(10) |
|
IX |
|||
|
Sb(1)–O(1) |
2,3252(16) |
C(211)Sb(1)O(1) |
82,33(8) |
|
Sb(1)–C(211) |
2,122(2) |
C(211)Sb(1)C(411) |
98,30(9) |
|
Sb(1)–C(311) |
2,116(2) |
C(311)Sb(1)O(1) |
83,11(7) |
|
Sb(1)–C(411) |
2,167(2) |
C(311)Sb(1)C(211) |
115,11(9) |
|
Sb(1)–C(511) |
2,115(3) |
C(311)Sb(1)C(411) |
93,43(9) |
|
N(1)–O(3) |
1,234(3) |
C(411)Sb(1)O(1) |
176,39(8) |
|
N(1)–O(4) |
1,233(3) |
C(511)Sb(1)O(1) |
84,22(8) |
|
N(1)–C(112) |
1,436(4) |
C(511)Sb(1)C(211) |
113,25(9) |
|
O(1)–C(117) |
1,285(3) |
C(511)Sb(1)C(311) |
127,51(9) |
|
O(2)–C(117) |
1,228(3) |
C(511)Sb(1)C(411) |
98,75(9) |
Полные таблицы координат атомов, длин связей и валентных углов депонированы в Кембриджском банке структурных данных (№ 814679–814681, 814984–814986; ; .
Результаты и их обсуждение
Дикарбоксилаты триарилсурьмы синтезированы нами из триарилсурьмы и карбоновой кислоты в присутствии пероксида водорода методом, описанным в работах [11–18]. Реакции протекали в эфире по обычной схеме окислительного присоединения с выходом дикарбоксилата триа-рилсурьмы до 98 %:
Ar 3 Sb + 2 НOC(O)R + Н 2 О 2 → Ar 3 Sb[OC(O)R] 2 + 2 H 2 O
Ar = Ph, R = C 6 H 4 OMe-2 (I), CH 2 C 6 H 4 NO 2 -4 (II), cyclo- C 3 H 5 (III), C 6 H 4 NO 2 -2 (IV)
Ar = C 6 H 4 Me-3, R = C 6 H 4 OMe-2 (V)
Молекулярные и кристаллические структуры соединений I–III, V установлены методом РСА. Атом сурьмы имеет в молекулах искаженную тригонально-бипирамидальную координацию с аксиально расположенными карбоксилатными лигандами (рис. 1–4).
Симметрию координационного узла С3SbO2 в молекулах I и II можно приблизительно охарактеризовать как С 2 v : ось 2-го порядка проходит через атомы Sb и С(31). В I аксиальный угол O(1)SbO(1а) равен 173,30(6) ° , сумма углов в экваториальной плоскости составляет 359,99 ° , но при этом значения индивидуальных углов СSbC различны: углы С(21)SbC(31) и С(21)SbC(31а) равны 104,30(5) ° , тогда как угол С(21)SbC(21а) увеличен до 151,39(10) ° (см. табл. 2). Значения аналогичных параметров в II составляют 173,35(11) ° , 359,99 ° , 110,04(9) ° , 110,04(9) ° , 139,91(17) ° , в III - 176,46(4) ° , 360 ° , 104,44(6) ° , 106,38(5) ° , 149,18(6) ° , в V - 173,58(19) ° , 360 ° , 105,3(3) ° , 105,9(3) ° , 148,8(3) ° . Группировки атомов SbC3 имеют практически плоское строение. Валентные углы между аксиальными и экваториальными заместителями OSbC мало отличаются от теоретического значения (90 ° ) и изменяются в интервалах 86,65(6)-91,22(6) ° (I), 86,67(6)-92,80(10) ° (II), 87,94(3)-91,55(5) ° (III), 86,67(6)-92,80(10) ° (V).
В других структурно охарактеризованных дикарбоксилатах триарилсурьмы интервал изменения аксиальных углов OSbO составляет 169,92-178,39 ° [2]. Углы между аксиальными и экваториальными связями, как правило, отличаются от теоретического значения не более чем на 5 ° . Суммы углов в экваториальной плоскости равны 360 ° или меньше этой величины на 0,01-0,5 ° . Значения углов CSbC, чаще всего, заметно отличаются от теоретического (120 ° ).
В молекулах II и III средние значения экваториальных связей Sb–C 2,110(3) и 2,1243(15) Å) практически совпадают со средними значениями аксиальных связей Sb–О (2,106(2) и 2,1271(10) Å),
В молекулах I и V экваториальные связи (2,1255(16), 2,1255(16), 2,106(2) и 2,082(7), 2,110(8), 2,125(8) Å) короче аксиальных связей (2,1305(11) и 2,136(5), 2,137(5) Å). Отметим, что в структурно охарактеризованных дикарбоксилатах триарилсурьмы средние значения длин аксиальных связей Sb–О варьируют от 2,105 до 2,156 Å [2].
В молекулах I и V, которые отличаются между собой арильными заместителями, валентные углы при атоме сурьмы имеют близкие значения (см. табл. 2). Отметим, что в фенильном производном среднее значение длин связей Sb–C (2,119(2) Å) немного длиннее, а связей Sb–О (2,1305(11) короче, чем в толильном (2,110(8) и 2,136(5) Å).
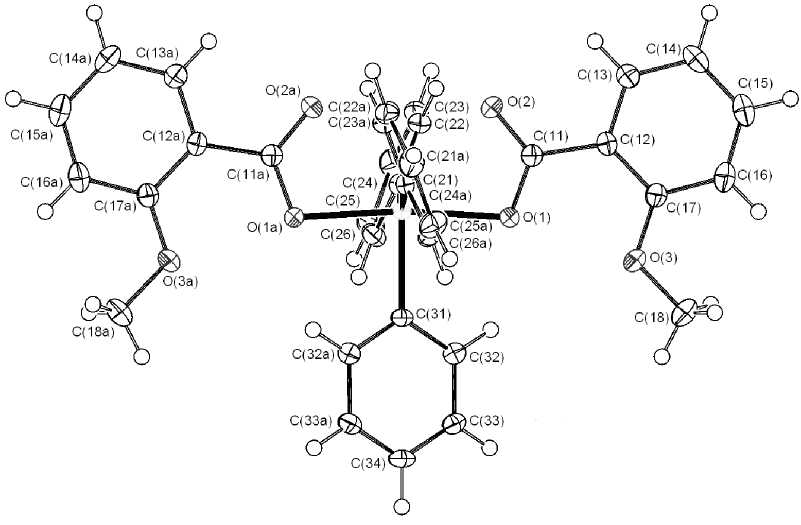
Рис. 1. Общий вид молекулы бис (2-метоксибензоата) трифенилсурьмы (I)
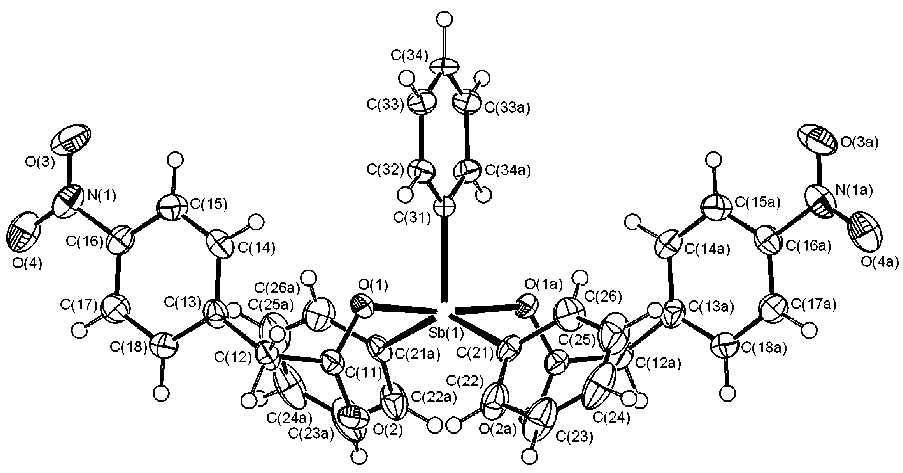
Рис. 2. Общий вид молекулы бис (4-нитрофенилацетата) трифенилсурьмы (II)
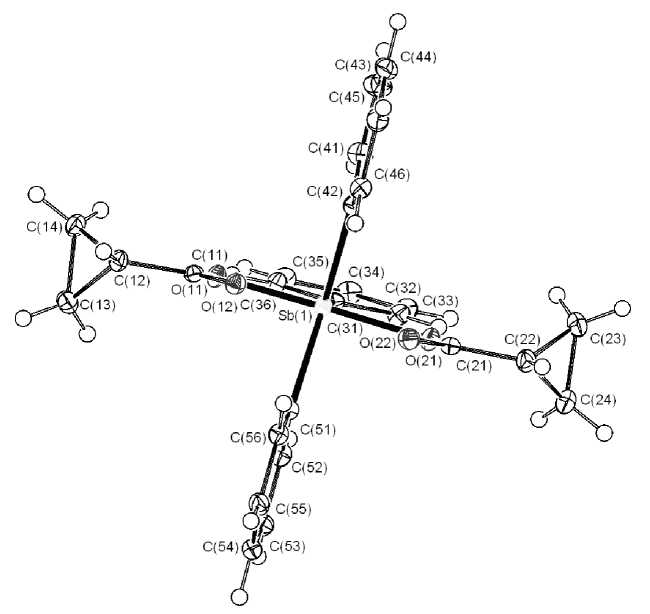
Рис. 3. Общий вид молекулы бис (циклопропанкарбоксилата) трифенилсурьмы (III)
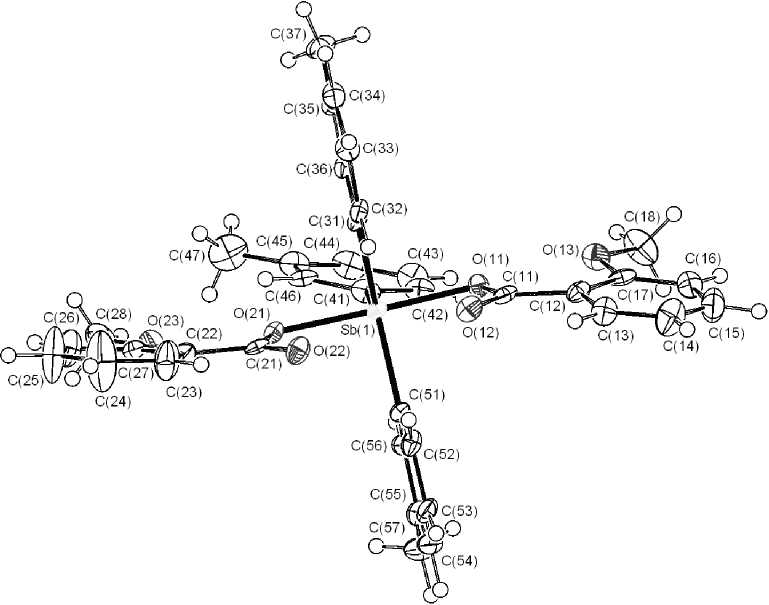
Рис. 4. Общий вид молекулы бис (2-метоксибензоата) три- м -толилсурьмы (V).
В дикарбоксилатах триарилсурьмы имеет место взаимодействие центрального атома с атомами кислорода карбонильных групп. Средние расстояния Sb···O=C составляют 2,664–3,219 Å, при этом закономерного изменения расстояния Sb⋅⋅⋅O=C при изменении длины связи Sb–O не наблюдается. Отношения расстояния Sb···O=C к длине связи Sb–O, определяемые как мера асимметрии бидентатного карбоксилатного лиганда, в дикарбоксилатах триарилсурьмы составляют, как правило, 1,31–1,52 [2].
В соединениях I-III, V расстояния Sb-"O=C и отношения d (Sb--Q=C)Z d (Sb-О) равны соответственно 2,715(2) Å, 1,27; 3,012(3) Å, 1,43; 2,611(3), 2,869(4) Å, 1,23, 1,35; 2,680(4), 2,785(5) Å, 1,25, 1,30.
Карбоксилатные лиганды в дикарбоксилатах триарилсурьмы имеют относительно фрагмента SbC3, как правило, цис- ориентацию и двугранные углы между плоскостями карбоксильных групп не превышают 15 ° . Поэтому один из экваториальных углов СSbC со стороны контактов Sb--Q=C значительно больше по сравнению с двумя другими углами. В молекулах I–III, V карбонильные атомы кислорода, координирующиеся на атом сурьмы, также находятся напротив одного и того же экваториального угла, что приводит к его значительному увеличению (151,39(10) ° в I, 139,91(17) ° в II, 149,18(6) ° в III, 148,8(3) ° в V). При этом выявленная в работе [2] закономерность, что при уменьшении расстояний между центральным атомом и карбонильными атомами кислорода увеличивается экваториальный угол со стороны контактов, подтверждается.
Согласно литературным данным, длина одинарной связи C–O в карбоновых кислотах составляет 1,293–1,308 Å, а длина двойной связи С=О равна 1,214–1,229 Å [19]. Расстояния С(1)–О(1) и С(1)–О(2) в карбоксилатных группах соединения I равны 1,300(2) и 1,240(2) Å соответственно. В II, III и V аналогичные величины составляют 1,293(3), 1,229(4) Å, 1,3094(18), 1,3126(19), 1,2356(19), 1,2425(18) Å и 1,297(9), 1,299(9), 1,244(10), 1,238(10) Å. В дикарбоксилатах триарил-сурьмы подобные расстояния изменяются, как правило, в интервалах 1,290–1,310 Å и 1,210–1,240 Å соответственно.
В ИК-спектрах синтезированных дикарбоксилатов триарилсурьмы полосы поглощения карбонильной группы смещены в длинноволновую область на 20–80 см–1 по сравнению с полосами поглощения соответствующих кислот, что согласуется с наличием внутримолекулярных контактов Sb···O=С, приводящих к удлинению связей О=С.
В молекуле I фенильные радикалы расположены в наиболее энергетически выгодной «пропеллерной» конформации, торсионные углы О(1)Sb(1)C(21)C(26), O(1)Sb(1)C(31)C(32), O(1)Sb(1)C(21)C(22) равны 108,31, 150,93, 115,69°. Карбоксилатные лиганды лежат приблизительно в одной плоскости, метокси- и карбонильные группы находятся относительно связи С(11)-С(12) в транс- положении. В кристалле молекулы образуют цепочки, расположенные вдоль кристаллографической оси b . Межмолекулярные взаимодействия обусловлены водородными связями С=О(2, 2а)···Н–С(34) (2,42 Å). Между плоскостями арильных колец С(12)–С(17) соседних цепочек расстояния составляют 3,376, 3,384 Å, что свидетельствует о возможности п - п-взаимодействий. Атомы кислорода метокси-групп участия в межмолекулярных взаимодействиях не принимают.
В молекуле II торсионные углы О(1)Sb(1)C(21)C(26), O(1)Sb(1)C(31)C(32), O(1)Sb(1)C(21)C(22) равны 45,59, 28,51, 49,73°. В карбоксилатных лигандах плоскости нитрогрупп и фенильных колец практически совпадают, тогда как угол между плоскостями О(1)С(11)О(2) и С(13)–С(18) составляет 116°. Торсионный угол С(12)С(11)С(11а)С(12а) равен 106,84°. Структурная организация кристалла обусловлена водородными связями типа О(2)···Н–С(33), О(2)···Н–С(18), О(2)···Н–С(17) (2,66, 2,70, 2,54 Å соответственно); О(3)···Н–С(34), О(4)···Н–С(32), О(4)···Н–С(32) (2,59, 2,55, 2,64 Å), посредством которых формируется трехмерная сетка.
Плоскости фенильных лигандов С(42)–С(46) и С(51)–С(56) в молекуле III практически совпадают с экваториальной плоскостью [SbC 3 ] (торсионные углы О(11)SbC(42)C(46) и О(11)SbC(51)C(52) равны 99,10 и 88,96° соответственно), тогда как плоскость C(31)–C(36) перпендикулярна ей (торсионный угол О(11)SbC(31)C(32) 177,74°). Циклопропановые радикалы и крбонильные группы относительно связей С(11)–С(12) и С(21)–С(22) находятся в транс положениях, при этом плоскости [C 3 ] и карбокси-групп перпендикулярны друг другу (соответствующие углы составляют 89 и 91°). Две соседние молекулы объединены двумя слабыми водородными связями О(12)···Н(13В)–С(13) (О···Н 2,66 Å). Димеры связаны посредством связей О(22)···Н(53А)–С(53) (2,58 Å).
Аналогичное расположение толильных групп наблюдается в молекуле V: плоскости двух колец незначительно отклоняются от экваториальной плоскости (торсионные углы
О(11)SbC(31)C(36) и О(11)SbC(51)C(52) равны 85,28 и 92,28° соответственно), тогда как плоскость третьего кольца практически перпендикулярна этой плокости (торсионный угол О(11)SbC(41)C(42) 18,78°). Конформация карбоксилатных лигандов в молекулах I и V одинакова. Молекулы в кристалле V образуют цепочки, в межмолекулярных водородных связях участвуют атомы кислорода метокси-групп: МеО(13)···Н(37С)–С(37) (2,68 Å), МеО(23)···Н(57А)–С(57) (2,57 Å). Посредством взаимодействий С=О(12)···Н(53)–С(53) (2,53 Å) и С=О(22)···Н(33)–С(33) (2,49 Å) цепочки связаны между собой.
В литературе описана реакция перераспределения лигандов, когда из пентафенилсурьмы и производного пятивалентной сурьмы типа Ph 3 SbX 2 (X = OC(O)R, ON=CRR’, OAr, OSO 2 R, OP(O)R 2 , NO 3 , NO 2 ) с высоким выходом образуются соединения сурьмы общей формулы Ph 4 SbX [12, 13, 20–40].
Карбоксилаты тетрафенилсурьмы нами были синтезированы по аналогичной методике из пентафенилсурьмы и дикарбоксилатов трифенилсурьмы (I–IV). Реакции проводили при нагревании (1–3 ч) в растворе ароматического углеводорода, окончание реакции контролировали методом ТСХ по исчезновению пятна, характерного для пентафенилсурьмы.
Ph 5 Sb + Ph 3 Sb[OC(O)R] 2 → 2 Ph 4 SbOC(O)R
R = C 6 H 4 OMe-2 (VI), CH 2 C 6 H 4 NO 2 -4 (VII), cyclo- C 3 H 5 (VIII), C 6 H 4 NO 2 -2 (IX)
ИК спектры и температуры плавления полученных карбоксилатов тетрафенилсурьмы совпадали с аналогичными физико-химическими характеристиками веществ, синтезированных из пен-тафенилсурьмы и карбоновой кислоты.
Ph 5 Sb + HOC(O)R → Ph 4 SbOC(O)R + PhH
Молекулярная и кристаллическая структуры соединений VII и IX исследованы методом РСА. Соединение VII кристаллизуется в виде сольвата с толуолом Ph 4 SbOC(O)CH 2 C 6 H 4 (NO 2 -4)∙0,5C 6 H 5 CH 3 . Сольватная молекула толуола разупорядочена по двум позициям с равным весом, связанным между собой осью второго порядка.
Атомы сурьмы в молекулах VII и IX имеют искаженную тригонально-бипирамидальную координацию с аксиально расположенными карбоксилатным и фенильным лигандами (рис. 5, 6).
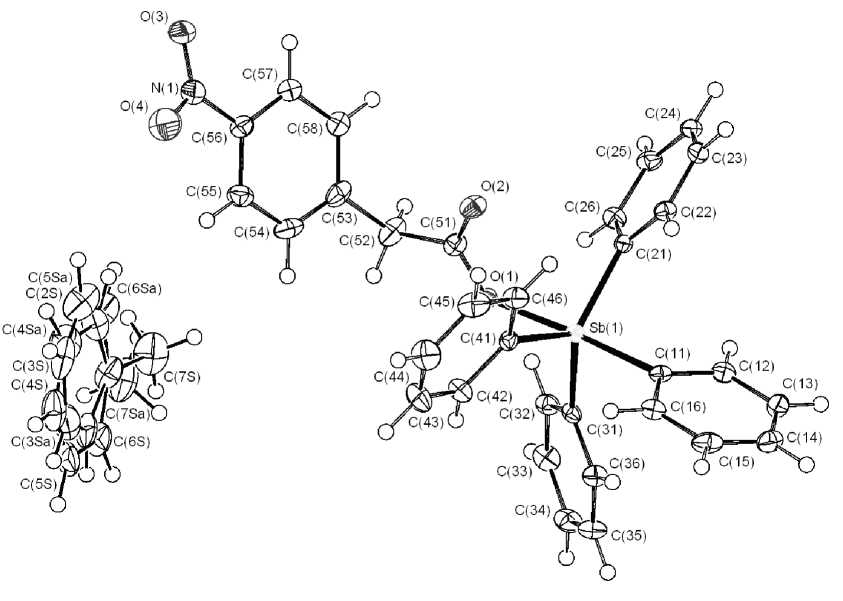
Рис. 5. Общий вид сольвата 4-нитрофенилацетата тетрафенилсурьмы с толуолом (VII)
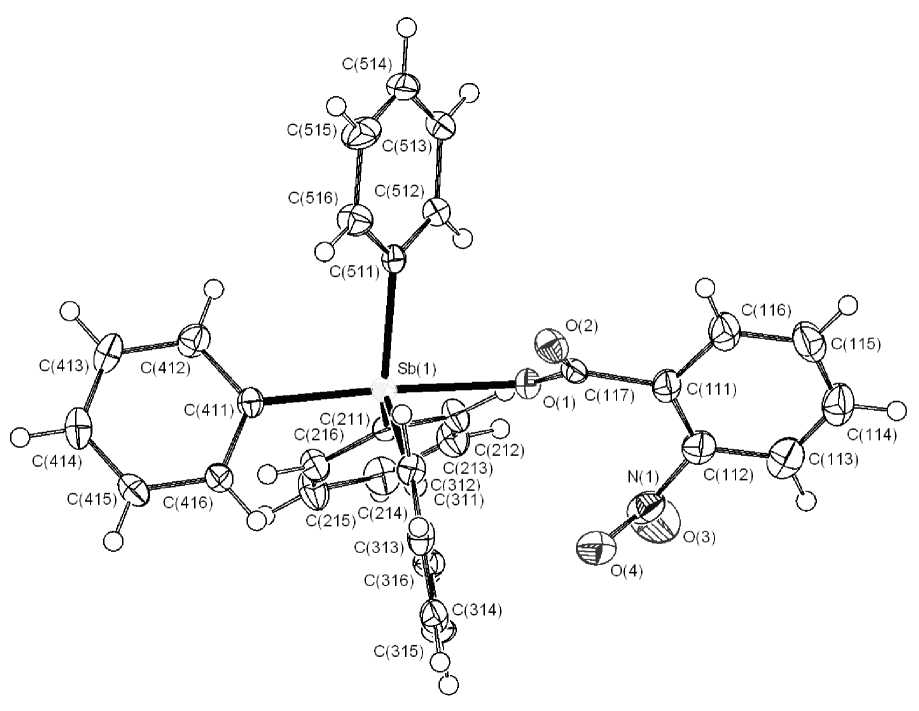
Рис. 6. Общий вид 2-нитробензоата тетрафенилсурьмы (IX)
Общая конформация фенильных колец в экваториальной плоскости молекулы VII является «пропеллерной» из-за поворота в одном направлении вокруг связей Sb–C, что наиболее часто встречается в арильных соединениях пентакоординированной сурьмы. Значения торсионных углов O(1)SbC(31)C(32), O(1)SbC(41)C(42), O(1)SbC(21)C(22) равны 30,16, 70,97, 142,70° соответственно. В молекуле IX наиболее распространенная конформация фенильных колец не наблюдается, соответствующие торсионные углы O(1)SbC(311)C(312), O(1)SbC(511)C(512), O(1)SbC(211)C(212) составляют 105,79, 50,60, –17,02°.
Аксиальные углы OSbCакC равны 176,26(8) ° (VII), 176,39(8) ° (IX). Суммы углов СэKвSbCэKв в экваториальной плоскости составляют 357,67 ° (115,90(10), 117,45(10), 124,32(9) ° ) и 355,87 ° (115,11(9), 113,25(9), 127,51(9) ° ) в VII и IX соответственно. Атом сурьмы выходит из экваториальной плоскости в сторону аксиально расположенного атома углерода. Валентные углы OSbC экв меньше 90° (81,92(9)–86,88(9)° VII и 82,33(8)–84,22(8)° IX), при этом углы С акс SbC экв больше 90° (94,53(10)–95,85(10)° VII и 93,43(9)–98,75(9)° IX).
Длины связей Sb–C экв изменяются в интервалах 2,108(3)– 2,119(2) Å и 2,115(3)–2,122(2) Å в VII и IX соответственно. Расстояния Sb–C акс (2,168(3) и 2,167(2) Å в VII и IX) длиннее, чем средние значения экваториальных связей Sb–C экв . Длина связей Sb–O (2,220(2) и 2,3252(16) Å в VII и IX) превышает сумму ковалентных радиусов сурьмы и кислорода (2,07 Å [41]).
В комплексах VII и IX расстояния Sb—O(=C) составляют 3,247(3) и 3,318(4) А (сумма ван-дер-ваальсовых радиусов сурьмы и кислорода равна 3,70 Å [41]). В структурно охарактеризованных карбоксилатах тетрафенилсурьмы внутримолекулярные контакты изменяются в широком интервале значений (2,594–3,509 Å [3]).
В молекуле VII длина одинарной связи С–О (1,307(3) Å) больше длины двойной связи С=О (1,222(3) Å). В молекуле IX связи С–О (1,285(3) Å) и С=О (1,228(3) Å) различаются не столь существенно. Наблюдаемые значения межъядерных расстояний в карбоксильной группе согласуются с литературными данными для карбоновых кислот [19].
В отличие от молекулы II в органических радикалах карбоксилатных лигандов молекул VII и IX углы между плоскостями арильного кольца и группы NO2 составляют 29 и 54° соответствен- но, что свидетельствует о невозможности полного π-π-сопряжения в системе арильное кольцо – функциональная группа. Таким образом, NO2-группа влияет на смещение электронной плотности в основном за счет индуктивного эффекта. Длины связей N–O составляют 1,227(3), 1,232(3) (VII) и 1,234(3), 1,233(3) Å (IX) (среднее значение аналогичных расстояний для фрагментов Ar–NO2 в органических соединениях 1,217 Å [19]).
Молекулы VII расположены вдоль кристаллографической оси b. Функциональная группа NO 2 принимает участие в образовании межмолекулярных водородных связей типа N(1)–O(3)···H(46A) (2,50 Å) и N(1)–O(2)···H(24A) (2,66 Å) с двумя соседними молекулами (рис. 7).
Кроме того, имеют место межмолекулярные Н-связи с участием атомов кислорода карбоксильной группы С–О(1)···H(23A) (2,66 Å) и С=О(2)···H(57A) (2,62 Å). Наряду с водородными связями, благодаря которым в кристалле формируется трехмерная структура, наблюдаются мно-
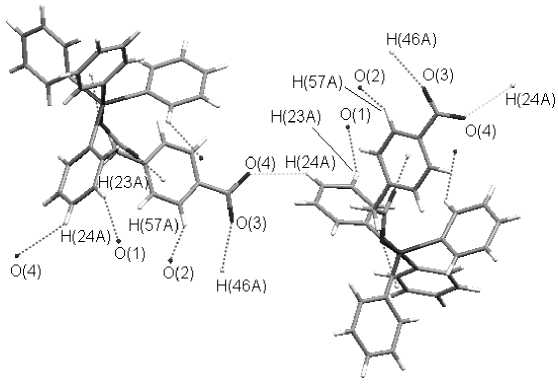
Рис. 7. Система водородных связей в кристалле VII
жественные контакты С–Н···π-типа.
В кристалле IX также наблюдаются межмолекулярные водородные связи типа N(1)–O(3)···H(31B) (2,70 Å) и N(1)–O(4)···H(31D) (2,46 Å) и О(2)···H(51C) (2,44 Å), О(2)···H(21B) (2,46 Å), обусловливающие образование пространственной сетки (рис. 8).
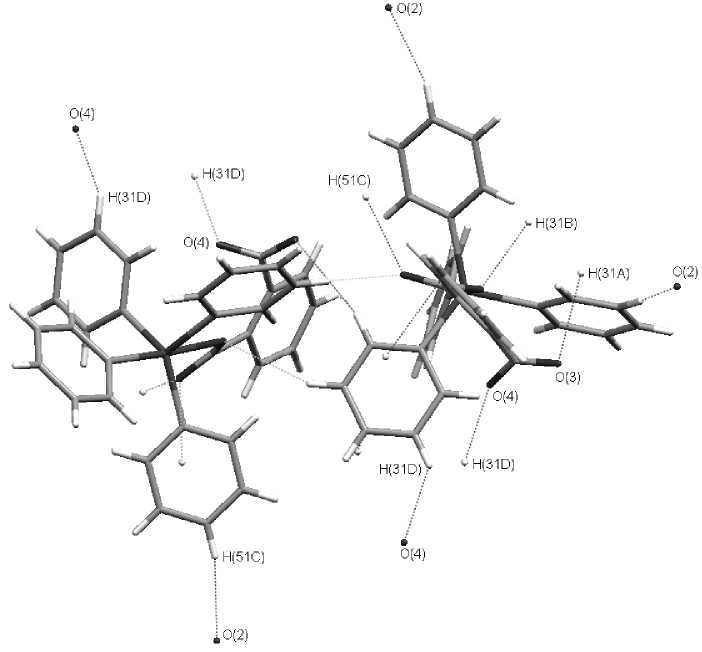
Рис. 8. Система водородных связей в кристалле IX
Выводы
В дикарбоксилатах трифенилсурьмы искажение тригонально-бипирамидальной координации центрального атома проявляется, в основном, в увеличении одного из экваториальных углов из-за внутримолекулярных взаимодействий Sb—O(=C). В карбоксилатах тетрафенилсурьмы наблюдается значительное изменение тригонально-бипирамидальной конфигурации молекул, сопровождающееся возрастанием углов CаксSbCэкв по сравнению с 90 ° и уменьшением суммы экваториальных углов, что указывает на приближение группы Ph4Sb к тетраэдрической структуре. Степень искажения тригонально-бипирамидального полиэдра атома сурьмы коррелирует с увеличением расстояния Sb–O по сравнению с суммой ковалентных радиусов атомов-партнеров связи. Внутримолекулярных контактов с участием функциональных групп в органическом радикале карбоксилатного лиганда не выявлено. Наличие функциональных групп обусловливает формирование трехмерной структуры в кристалле.
Список литературы Молекулярные и кристаллические структуры карбоксилатов три- и тетраарилсурьмы
- Cambridge Crystallographic Data Center. 2011.
- Шарутин, В.В. Строение органических соединений сурьмы R3SbX2 (X -электроотрицательный лиганд)/В.В.Шарутин, О.К. Шарутина//Бутлеровские сообщения. -2007.-Т. 12, № 6. -С. 34-57.
- Шарутин, В.В., Строение органических соединений сурьмы R4SbX (X -электроотрицательный лиганд)/В.В. Шарутин, О.К. Шарутина//Бутлеровские сообщения. -2007. -Т. 12, № 6. -С. 58-65.
- Bone, S.P. The crystal structure of tetraphenylantimony (V) formate/S.P. Bone, D.B. Sowerby//J. Chem. Res., Synop. -1979. -Nо. 3.-P. 82-83.
- Bone, S.P. The crystal structures of tetraphenylantimony acetate and its acetic acid adduct/S.P. Bone, D.B. Sower//Phosphorus, Sulfur, Silicon. Relat. Elem. -1989. -Vol. 45, nо. 1-2. -P. 23-29.
- Ma, Y. Synthesis, characterization and antitumor activity of some arylantimony triphenylgermsnylpropionates and crystal structures of Ph3GeCH(Ph)CH2CO2SbPh4 and [Ph3GeCH(Ph)CH2CO2]2Sb(4-ClC6H4)3/Y. Ma, J. Li, Z. Xuan, R. Liu//J. Organomet. Chem. -2001. -Vol. 620, nо. 2. -P. 235-242.
- Synthesis and structure of the carboxylates tetraphenylantimony/Quan Li, Yin Han-dong, Cui Jichun et al.//J. Organometal. Chem. -2009. -Vol. 694. -P. 3683-3689.
- Synthesis and structure of the dicarboxylates triphenylantimony/Quan Li, Yin Han-dong, Cui Jichun et al.//J. Organometal. Chem. -2009. -Vol. 694. -P. 3708.
- Sheldrick G.M. SHELX-97 Release 97-2. Univ. of Göttingen, Germany, 1998.
- Sheldrick G.M. SADABS, Program for empirical X-ray absorption correction, Bruker-Nonius, 1990-2004.
- Improved methods for the synthesis of antimony triacetate, triphenylantimonyldiacetate and pentaphenylantimony/T.C. Thepe, R.J. Garascia, M.A. Selvoski, A.N. Patel//Ohio J. Sci. -1977. -Vol. 77, nо. 3. -P. 134-135.
- Синтез фторбензоатов тетра-и триарилсурьмы/В.В. Шарутин, О.К. Шарутина, Е.А. Бондарь и др.//Журн. общ. химии. -2002. -Т. 72, № 3. -С. 419-420.
- Синтез и строение фторбензоатов тетра-и триарилсурьмы/В.В. Шарутин, О.К. Шарутина, Е.А. Бондарь и др.//Коорд. химия. -2002. -Т. 28, № 5. -С. 356-363.
- Синтез и строение дикарбоксилатов триарилсурьмы Ar3Sb[OC(O)R]2 (Ar = Ph, n-Tol; R = 2-C4H3O, 3-C5H4N/В.В. Шарутин, О.К. Шарутина, А.П. Пакусина и др.//Коорд. химия. -2003. -Т. 29, № 10. -С. 750-759.
- Особенности строения дикарбоксилатов триорганилсурьмы R3Sb[OC(O)R')]2/В.В. Шарутин, О.К. Шарутина, А.П. Пакусина и др.//Коорд. химия. -2003. -Т. 29, № 11. -С. 843-851.
- Синтез и строение ниацината тетрафенилсурьмы/В.В. Шарутин, А.П. Пакусина, Т.П. Платонова и др.//Журн. общ. химии. -2004. -Т. 74, № 2. -С. 234-237.
- Синтез и строение бис(1-адамантанкарбоксилато)трифенилсурьмы/О.К. Шарутина, А.П. Пакусина, О.В. Молокова и др.//Журн. неорган. химии. -2008. -Т. 53, № 8. -С. 1335-1341.
- Шарутин, В.В. Синтез и строение дигалогенидов трис(N,N-диметиламинофенил)сурьмы/В.С. Сенчурин, О.К. Шарутина, Е.В. Акулова//Журн. общ. химии. -2008. -Т. 78, № 12. -С. 1999-2003.
- Способ получения солей тетрафенилстибония общей формулы Ph4SbX [X=Cl, Br, OC(O)Ph, SCN]/В.В. Шарутин, В.С. Сенчурин, О.К. Шарутина и др.//Журн. общ. химии. -1996. -Т. 66, № 10. -С. 1755-1756.
- Реакции пентаарилсурьмы с диацилатами триарилсурьмы/В.В. Шарутин, О.К. Шарутина, А.П. Пакусина, В.К. Бельский//Журн. общ. химии. -1997. -Т. 67, № 9. -С. 1536-1541.
- Реакции пентафенилвисмута и -сурьмы с элементоорганическими соединениями Ph3EX2 (E = Sb, Bi; X = F, Cl, Br, NO3/В.В. Шарутин, О.К. Шарутина, И.В. Егорова, Л.П. Панова//Журн. общ. химии. -1998. -Т. 68, № 2. -С. 345-346.
- Синтез и строение 4-метилбензолсульфоната тетра-п-толилсурьмы/В.В. Шарутин, О.К. Шарутина, Т.А. Тарасова и др.//Журн. общ. химии. -1999. -Т. 69, № 12. -С. 1979-1981.
- Синтез и строение 2,4-диметилбензолсульфоната тетрафенилсурьмы/В.В. Шарутин, О.К. Шарутина, Т.А. Тарасова и др.//Журн. общ. химии. -2000. -Т. 70, № 8. -С. 1311-1314.
- Синтез и строение бензоата тетрафенилсурьмы/В.В. Шарутин, Г.К. Фукин, Л.Н. Захаров и др.//Журн. общ. химии. -2000. -Т. 70, № 12. -С. 1997-1999.
- Новый метод синтеза арокситетраарильных соединений сурьмы/В.В. Шарутин, О.К. Шарутина, П.Е. Осипов, О.В. Субачева//Журн. общ. химии. -2001. -Т. 71, № 6. -С. 1045-1046.
- Синтез и строение оксиматов тетра-и триарилсурьмы/В.В. Шарутин, О.К. Шарутина, О.В. Молокова и др.//Журн. общ. химии. -2001. -Т. 71, № 8. -С. 1317-1321.
- Карбонат тетраарилсурьмы. Синтез и строение/В.В. Шарутин, О.К. Шарутина, Т.П. Платонова и др.//Журн. общ. химии. -2001. -Т. 71, № 10. -С. 1637-1640.
- Синтез и строение нитрата тетрафенилсурьмы/В.В. Шарутин, О.К. Шарутина, Л.П. Панова и др.//Журн. общ. химии. -2002. -Т. 72, вып. 1. -С. 45-48.
- Синтез и строение оксиматов тетра-и триарилсурьмы/В.В. Шарутин, О.К. Шарутина, О.В. Молокова и др.//ЖОХ. -2002. -Т. 72, № 6. -С. 956-961.
- Синтез и строение оксиматов тетра-и триарилсурьмы/В.В. Шарутин, О.К. Шарутина, О.В. Молокова и др.//Коорд. химия. -2002. -Т. 28, № 8. -С. 581-590.
- Синтез и строение 2-фуроината и бензоата тетрафенилсурьмы/В.В. Шарутин, А.П. Пакусина, Т.П. Платонова и др.//Коорд. химия. -2002. -Т. 28. -№ 11. -С. 803-808.
- Синтез и строение нитрита тетрафенилсурьмы/В.В. Шарутин, А.П. Пакусина, И.В. Егорова и др.//Коорд. химия. -2002. -Т. 28, № 12. -С. 883-886.
- Шарутин, В.В. Особенности строения арильных соединений сурьмы Ar4SbX/В.В Шарутин, А.П. Пакусина, О.К. Шарутина//Бутлеровские сообщения. -2003. -№ 1. -С. 22-30.
- Сурьмаорганические производные 2,4,6-трибромфенола/В.В. Шарутин, А.П. Пакусина, М.А. Пушилин и др.//Журн. общ. химии. -2003. -Т. 73, № 4. -С. 573-577.
- Синтез и строение органосульфонатов тетра-и трифенилсурьмы/В.В. Шарутин, О.К. Шарутина, А.П. Пакусина и др.//Коорд. химия. -2004. -Т. 30, № 1. -С. 15-24.
- Оксиматы тетра-и триарилсурьмы. Синтез и строение/О.В. Молокова, В.В. Шарутин, О.К. Шарутина, Е.А. Алябьева//Бутлеровские сообщения. -2004. -Т. 5, № 3. -С. 28-33.
- Синтез и строение дифенацилфосфината тетрафенилсурьмы/В.В. Шарутин, А.П. Пакусина, С.А. Смирнова, Г.К. Фукин//Коорд. химия. -2004. -Т. 30, № 6. -С. 421-425.
- Синтез и строение сурьма-и висмуторганических производных 4-сульфофенола и 2,4-дисульфофенола/В.В. Шарутин, И.В. Егорова, А.П. Пакусина и др.//Коорд. химия. -2007. -Т. 33, № 3. -С. 176-183.
- Бацанов, С.С. Атомные радиусы элементов/С.С. Бацанов//Журн. неорг. хим. -1991. -Т. 36, № 12. -С. 3015-3037.


