Молекулярные маркеры системы гемостаза после эндопротезирования крупных суставов на фоне антитромботической профилактики низкомолекулярным гепарином
Автор: Антропова Ирина Петровна, Осипенко Артур Васильевич, Рейно Елена Викторовна, Бабушкин Василий Николаевич
Журнал: Гений ортопедии @geniy-ortopedii
Рубрика: Оригинальные статьи
Статья в выпуске: 3, 2010 года.
Бесплатный доступ
Проведено изучение показателей гемостаза у 83 пациентов, перенесших эндопротезирование крупных суставов. Было показано, что использование молекулярных маркеров позволяет выявить предоперационную дисфункцию коагуляции и фибринолиза, исследовать динамику фазовых изменений гиперкоагуляционного синдрома, проследить интенсивность и вариабельность тромбинемии на фоне стандартной антитромботической профилактики эноксапарином.
Гемостаз, эндопротезирование, эноксапарин
Короткий адрес: https://sciup.org/142121326
IDR: 142121326
Molecular markers of hemostasis system after total large joint endoprosthetics through antithrombotic prevetion with heparin of low molecular weight
The analysis of hemostasis indices was performed in 83 patients that had major joint arthroplasty. It showed that using molecular markers enabled to reveal preoperative coagulation and fibrinolysis dysfunction, to investigate the dynamics of hypercoagulation syndrome phase changes, to trace the intensity and variability of thrombinemia by standard antithrombotic prophylaxis with enoxaparin.
Текст научной статьи Молекулярные маркеры системы гемостаза после эндопротезирования крупных суставов на фоне антитромботической профилактики низкомолекулярным гепарином
Операции по эндопротезированию крупных суставов, несмотря на совершенствование хирургической техники, анестезиологического пособия и внедрения в практику современных антикоагулянтных препаратов, сопровождаются повышенным риском развития тромбозов глубоких вен и тромбоэмболии легочной артерии [8, 10]. Основное значение для возникновения тромба, его размеров и физических свойств, наряду с повреждением сосудистой стенки и нарушением кровотока, имеют сдвиги в системе гемостаза [9].
Поэтому необходимы надежные критерии комплексной оценки системы гемокоагуляции, в первую очередь плазменного гемостаза, состояние которого определяется сбалансированным функционированием свертывающего, противосвертывающего и фибринолитического звеньев [5].
Учитывая важность дисфункции коагуляционного звена в процессе формирования венозных тромбов, адекватная антикоагулянтная терапия является приоритетным направлением в предупреждении развития тромбоэмболических осложнений у хирургических больных [6, 14]. В настоящее время использование антикоагулянт- ных препаратов, в частности низкомолекулярных гепаринов (НМГ), специфически действующих на систему гемостаза, основано на принадлежности хирургических пациентов к той или иной группе риска без учета выраженности гемокоагуляционных нарушений [7, 10]. Это делает актуальным изучение вариабельности проявлений и эффективности коррекции гиперкоагуляционного синдрома на фоне стандартного действия НМГ.
Использование современных лабораторных технологий позволяет дополнить базовые тесты высокоспецифичными и чувствительными методами, которые не только определяют индивидуальные компоненты гемостаза, но и оценивают степень активации системы.
Превращение протромбина в активный тромбин является ключевым событием в процессе свертывания крови. Тромбин взаимодействует с различными компонентами коагуляционного каскада и ингибируется антитромбином, в результате чего образуется неактивный комплекс (ТАТ), который удаляется из циркуляции в течение нескольких минут. Повышение концентрации ТАТ в плазме свидетельствует об усилении образования тромбина и наличии гиперкоагуляции непосредственно в момент взятия крови на исследование [4, 11].
Повышенное формирование фибринмономерных комплексов (РФМК) свидетельствует о стадии образования растворимого фибрина. Увеличение в крови Д-димера (Д-д) отражает интенсивность образования и лизиса нерастворимого фибрина и характеризует активность свертывающей и фибринолитической систем. Систему физиологических антикоагулянтов оценивают по активности ее основных компонентов – антитромбина и протеина С [3]. Использование молекулярных маркеров сущест- венно расширяет возможности изучения механизмов гемокоагуляционных нарушений, их диагностики и определения степени медикаментозной коррекции.
Вместе с этим, динамика взаимодействия основных звеньев системы плазменного гемостаза при эндопротезировании крупных суставов остается недостаточно исследованной, что и обусловило проведение данной работы, целью которой стал анализ динамики молекулярных маркеров системы гемостаза и оценка их информативности у пациентов, перенесших эндопротезирование крупных суставов, на фоне анти-тромботической профилактики НМГ.
МАТЕРИАЛ И МЕТОДЫ
В работу было включено 83 пациента (35 мужчин и 48 женщин) в возрасте от 33 до 72 лет, перенесших неосложненные операции первичного эндопротезирования тазобедренного или коленного сустава.
Критерии исключения составили: наличие в анамнезе патологии системы гемостаза, неконтролируемого артериального давления, почечной, печеночной недостаточности, онкологических, наркологических заболеваний, сахарного диабета, ревматоидного артрита, количество тромбоцитов менее 100×109 , противопоказания к антикоагулянтной терапии.
Антитромботическую медикаментозную профилактику проводили НМГ-эноксапарином. Первая инъекция за 12 часов до операции, при планировании общей анестезии вводили 40 мг препарата, при планировании комбинированной спинально-эпидуральной анестезии 20 мг. Вторая инъекция – через 12 часов после операции, впоследствии эноксапарин вводили 1 раз в сутки в дозе 40 мг в течение 14-20 дней.
Отбор проб для анализов проводили до операции, через 30 минут после ее окончания и на 1-е, 3-и, 7-е, 14-е, 20-23-и сутки после эндопротезирования.
Определение комплексов ТАТ проводили с помощью иммуноферментного анализа (ИФА) [11, 12] наборами Enzygnost TAT фирмы Dade
Behring на иммуноферментном анализаторе Stat Fax-2100 (США). Д-димер также определяли с помощью ИФА наборами Asserachrom D-dimer фирмы Roche [13]. Активность образования растворимого фибрина оценивали ортофенантролиновым методом наборами фирмы Технология–Стандарт [3]. Для оценки системы фибринолиза проводили определение времени XIIa-зависимого эуглобулинового лизиса наборами фирмы Технология–Стандарт [3]. Определение фибриногена проводили по Клауссу с помощью наборов Multifibren фирмы Dade Behring на коа-гулометре CA-50 (Sysmex, Япония). Активности антитромбина и плазминогена определяли хромогенным методом наборами фирмы Технология-Стандарт [3] на биохимическом анализаторе Stat Fax-3300 (США). Общие клоттинговые тесты (АЧТВ, тромбиновое время, протромбиновое время) выполняли реактивами фирмы Dade Behring на коагулометре CA-50 (Sysmex, Япония). В качестве контролей использовались Standart Human Plasma, Control Plasma N и Control Plasma P фирмы Dade Behring.
Статистический анализ проводили с использованием t-критерия Стьюдента. Проверялись условия нормальности распределения по критерию Колмогорова-Смирнова и равенство дисперсий по критерию Фишера.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
Исследования, проведенные до операции, показали, что результаты клоттинговых тестов – АЧТВ, ПВ, ТВ не выходили за пределы физиологической нормы. Однако повышенное формирование комплексов ТАТ и Д-Д свидетельствовало об усилении образования тромбина и продуктов деградации нерастворимого фибрина у 43,8 % и 46,0 % обследованных пациентов соответственно. Это указывает на активацию и коагуляционного, и фибринолитического звеньев системы гемостаза у значительной части обследованных уже в предоперационном периоде, что является фактором повышенного риска интра- и послеоперационного развития как тромботических, так и геморрагических осложнений.
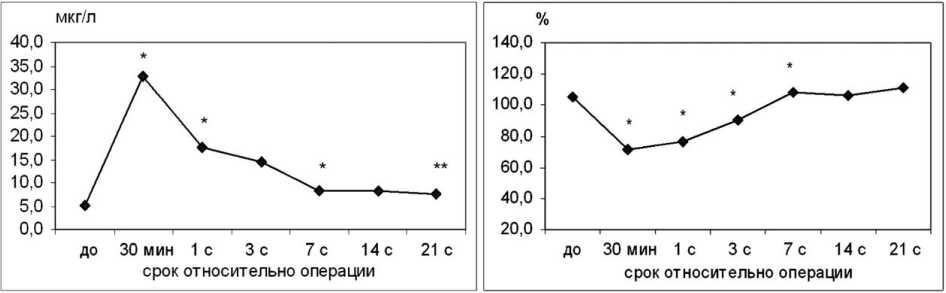
Интраоперационное массивное выделение тканевого фактора приводило к значительному усилению активности свертывающей системы, что выражалось в увеличении формирования комплексов ТАТ (рис. 1, а). Непосредственно по окончании эндопротезирования уровень тромбина в целом по группе увеличивался в 6,4 раза, несмотря на предоперационное введение НМГ, действие которого направлено на ингибирование формирования тромбина и снижение активности коагуляции [2]. Анализ вариабельности показал, что 29,8 % пациентов имели 4-кратное превышение нормы, 31,9 % 5-7 кратное, 38,3 % более чем 7-кратное. Высокая активность свертывания приводила к снижению на 35 % уровня антитромбина, одного из основных ингибиторов коагуляционного процесса (рис. 1, б).
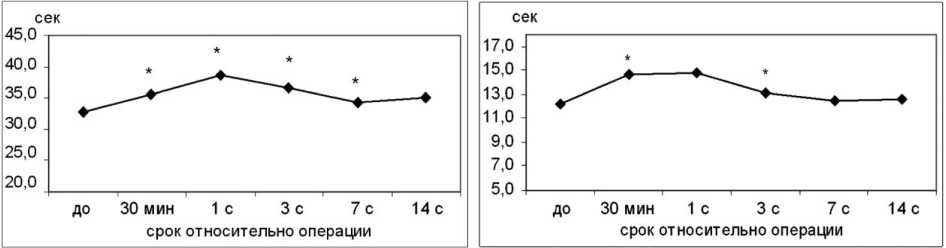
Глобальные тесты показали существенное снижение факторов свертывания, что свидетельствовало об их активном потреблении и выражалось в увеличении АЧТВ (рис. 2, а) и ПВ (рис. 2, б).
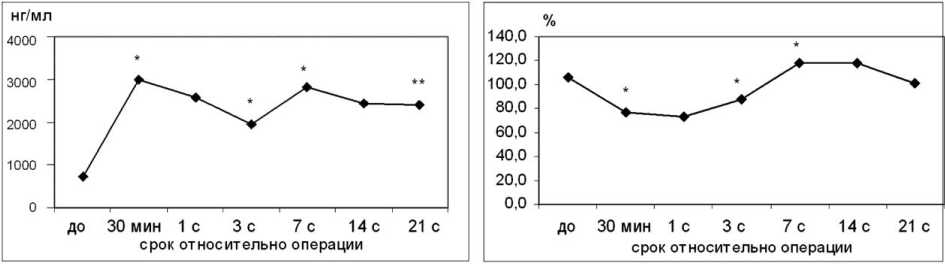
Интраоперационное усиление гемокоагуляционной активности приводило к компенсаторному усилению фибринолиза, о чем свидетельствовало практически пятикратное увеличение концентрации продуктов плазминовой деградации фибрина (рис. 3, а) и снижение на 29 % уровня плазминогена (рис. 3, б).
Полученные данные указывают на высокую активность всех звеньев плазменного гемостаза непосредственно после эндопротезирования крупных суставов и повышенный риск нарушения равновесия в их функционировании, что может приводить к развитию тромботических осложнений при существенном сдвиге в сторону свертывания и к кровоточивости в случае сдвига в сторону фибринолиза [9].
Через сутки после операции активность про- цессов свертывания существенно понижается, о чем свидетельствует уменьшение концентрации комплекса ТАТ (рис. 1, а). Вместе с тем, с 1-х суток увеличивается уровень белка острой фазы воспаления фибриногена (рис. 4, а). К 3-м суткам концентрация фибриногена достигает максимума и сохраняется на высоком уровне до 7-х суток. Это существенно усиливает протромбо-тический статус, так как происходит увеличение концентрации субстрата фибринообразования и повышается вязкость плазмы, тем самым ухудшаются реологические свойства крови.
Положительным фактором снижения тромбогенного риска является восстановление к 5-м суткам уровня физиологического антикоагулянта антитромбина (рис. 1, б).
С первых суток послеоперационного периода в формировании тромбогенного статуса усиливается вклад фибринолитического звена плазменного гемостаза с одновременным снижением геморрагического риска. После выраженной интраоперационной активации фибринолиза происходит его депрессия, что является физиологическим механизмом, направленным на сокращение кровопотери и следствием понижения активности плазминогена. О торможении фибринолиза свидетельствует снижение формирования Д-д (рис. 3, а) и увеличение времени эуглобулинового лизиса (рис. 4, б).
а
б
Рис. 1. Динамика ТАТ (а) и антитромбина (б) после эндопротезирования крупных суставов: * р<0,05 – различия достоверны по сравнению с предыдущим сроком, ** р<0,05 различия достоверны по сравнению с исходными данными
б
Рис. 2. Динамика АЧТВ (а) и ПВ (б) после эндопротезирования крупных суставов:* р<0,05 – различия достоверны по сравнению с предыдущим сроком, ** р<0,05 различия достоверны по сравнению с исходными данными
б
Рис 3. Динамика Д-д (а) и плазминогена (б) после эндопротезирования крупных суставов: * - р<0,05 - различия достоверны по сравнению с предыдущим сроком, ** - р<0,05 - различия достоверны по сравнению с исходными данными
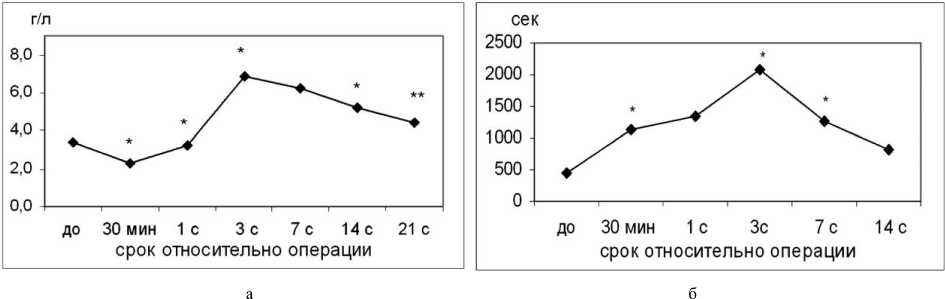
Рис. 4. Динамика фибриногена (а) и ХИа-зависимого фибринолиза (б) после эндопротезирования крупных суставов: * -р<0,05 - различия достоверны по сравнению с предыдущим сроком, ** - р<0,05 - различия достоверны по сравнению с исходными данными
На 7-е сутки содержание плазминогена не только восстанавливалось, но и превышало до-операционные значения (рис. 3, б). Это приводило к усилению репарационного фибринолиза и выражалось в повторном увеличении продукции Д-д (рис. 3, а), снижении времени эуглобулинового лизиса (рис. 4, б), что положительно влияло на уменьшение тромбогенного риска. Через неделю после операции тромбинемия существенно понижалась (рис. 1, а).
На 14-е сутки повышенная концентрация острофазного фибриногена (рис. 4, а) имела существенный сдвиг к нормализации. Таким образом, уменьшался тромбогенный риск, связанный с плазменным звеном гемостаза в целом по группе. Однако анализ индивидуальной вариабельности концентрации комплекса ТАТ через 14 суток после операции показал, что формирование тромбина снижалось до нормального уровня только у 16,4 % обследованных. Умеренная активация тромбинообразования (превышение нормы в 2 раза) выявлена у 58 % пациентов, 3-4 кратное превышение нормы сохранилось в 21,8 % случаев, более чем 5-кратное - у 3,6 % обследованных. Это свидетельствует о том, что более четверти пациентов на 14 -е сутки после эндопротезирования крупных суставов и по окончании срока, который отводится в большинстве рекомендаций для антитромботической профилактики [1, 10], сохраняют выраженный гиперкоагуляционный статус и нуждаются в пролонгировании антикоагулянтной терапии.
В целом по группе повышенное образование тромбина сохранялось до конца исследования, оставался повышенным и уровень фибриногена, что свидетельствует о сохранении гиперкоагуляционного состояния до трех недель после операции эндопротезирования.
ВЫВОДЫ
Таким образом, использование молекулярных маркеров позволило:
-
• выявить у пациентов с дегенеративнодистрофическими заболеваниями суставов предоперационную дисфункцию плазменного гемостаза, которая проявлялась в повышенной активности процессов свертывания и фибринолиза;
исследовать динамику фазовых изменений гиперкоагуляционного синдрома и вклад в его развитие различных звеньев плазменного гемостаза: значительную активацию свертывания, снижение антикоагуляционного потенциала и торможение фибринолиза после эндопротезирования крупных суставов;
проследить интенсивность тромбинемии, которая имела максимальную выраженность непосредственно после оперативного вмешательства и сохранялась до 14 суток у 83,6 % об- следованных после тотальной артропластики крупных суставов при использовании стандартной дозы НМГ.


