Молекулярные вариации гена BTC1 Beta vulgaris L
Автор: Хуссейн Ахмад Садун, Михеева Наталья Ростиславовна, Черепухина Ирина Вячеславовна, Фомина Анастасия Сергеевна, Налбандян Арпине Артаваздовна
Журнал: Вестник Красноярского государственного аграрного университета @vestnik-kgau
Рубрика: Агрономия
Статья в выпуске: 12, 2022 года.
Бесплатный доступ
Раннее цветение растений сахарной свеклы в первый год вегетации значительно снижает продуктивность культуры. Поэтому изучение и молекулярно-генетический отбор исходного материала, устойчивого к цветушности, является актуальным. Для изучения гена, контролирующего время цветения сахарной свеклы, были использованы листовые пластинки отечественных поддерживающих линий (О-тип) и зарубежных гибридов, отобранных в полевых условий, где проявлялся данный признак. При проведении полимеразно-цепной реакции в экспериментах применяли специфическую пару праймеров F9/R9. Обработка результатов секвенирования и сравнительный анализ проводился в программе Geneious Prime. В данной работе представлены результаты изучения гена BTC1 (bolting time control 1), регулирующего процесс цветения культуры Beta vulgaris L. Контроль происходит через регулирование деятельности двух генов, относящихся к семейству FT: ингибитора (Flowering Time 1) и активатора (Flowering Time 2) физиологического процесса - цветения. В генотипах, восприимчивых к цветушности, в гене BTC1 были обнаружены новые однонуклеотидные замены в экзоне 10, инициирующие замены в аминокислотном составе полипептидной цепи, что в итоге приводит к экспрессии функционально другого белка. Наличие определенных SNPs в гене BTC1 сахарной свеклы позволяет с высокой долей вероятности характеризовать те или иные генотипы как чувствительные к раннему цветению. Полученные экспериментальные данные позволяют на ранних этапах селекционного процесса отбирать генотипы, устойчивые к раннему цветению. Знания о генетической природе раннего цветения значимы при использовании культуры Beta vulgaris в разных географических поясах.
Сахарная свекла, цветушность, пцр-анализ, молекулярно-генетические маркеры, днк
Короткий адрес: https://sciup.org/140297463
IDR: 140297463 | УДК: 633.63:575.2 | DOI: 10.36718/1819-4036-2022-12-10-16
Genetic variation of BTC1 gene in Beta vulgaris L
Early flowering of sugar beet plants in the first year of vegetation significantly reduces the productivity of the crop. Therefore, the study and molecular genetic selection of the source material resistant to boltering is relevant. To study the gene that controls the flowering time of sugar beet, leaf blades of domestic supporting lines (O-type) and foreign hybrids selected in the field where this trait was manifested were used. When carrying out the polymerase chain reaction in the experiments, a specific pair of primers F9/R9 was used. Processing of sequencing results and comparative analysis was carried out in the program Geneious Prime. This paper presents the results of studying the BTC1 gene (bolting time control 1), which regulates the flowering process of Beta vulgaris L. Control occurs through the regulation of the activity of two genes belonging to the FT family: an inhibitor (Flowering Time 1) and an activator (Flowering Time 2) of the physiological process - flowering. In genotypes susceptible to flowering, new single nucleotide substitutions in exon 10 were found in the BTC1 gene, initiating substitutions in the amino acid composition of the polypeptide chain, which ultimately leads to the expression of a functionally different protein. The presence of certain SNPs in the BTC1 gene of sugar beet makes it possible with a high degree of probability to characterize certain genotypes as sensitive to early flowering. The experimental data obtained make it possible to select genotypes resistant to early flowering at the early stages of the breeding process. Knowledge about the genetic nature of early flowering is significant when using Beta vulgaris culture in different geographical zones.
Текст научной статьи Молекулярные вариации гена BTC1 Beta vulgaris L
Введение. Сахарная свекла (Beta vulgaris L.) – ценная сельскохозяйственная культура, на долю которой приходится производство около 30 % мирового сахара. Перспективы дальнейшего развития и повышения эффективности селекции сельскохозяйственных культур связаны с развитием геномики, использующей для проведения геномных исследований новейшие методы молекулярной генетики [1]. У сахарной свеклы установлен ряд маркерных признаков, которые определяются отдельными генами или олигогенами и подчиняются менделевскому наследованию. К моногенным, нежелательным признакам относится, например, цветушность, или раннее стрелкование, присущее диким однолетним и рудеральным формам/видам свеклы. Локус В, координирующий ранний выход в стрелку без прохождения яровизации, был картирован на второй хромосоме, в области центромеры [2, 3]. Переход от вегетативного к генеративному росту в течение жизни цветкового растения запускается рядом генов вместе с эндогенными стимулами, а также сигналами окружающей среды, такими как изменение температуры или продолжительности светового дня. Для обеспечения оптимального репродуктивного успеха у цветковых растений существует разный жизненный цикл. Сахарная свекла – двулетнее растение, которое растет вегетативно в первый год и начинает уд- линение (стрелкование) побегов и цветение вследствие яровизации после зимы [4–6]. Обнаружено, что однолетность (закрепление без яровизации) контролируется геном BTC1 посредством регуляции двух генов-гомологов семейства FT – BvFT1 (репрессор цветения) и BvFT2 (индуктор цветения). В однолетней свекле преобладает аллель BTC1, который репрессирует BvFT1 и одновременно активирует BvFT2, чтобы вызвать побеги и цветение. Напротив, у двулетней свеклы экспрессия рецессивного аллеля BTC1 постепенно увеличивается до уменьшения активности BvFT1 во время яровизации, что позволяет стимулировать экспрессию BvFT2 для инициации цветения [7–10]. Толерантность к цве-тушности – важный признак сахарной свеклы. Перенос пыльцы от диких видов свеклы на участки получения семян влечет перемещение В-аллеля в возделываемые двухлетние растения свеклы. Чтобы понять факторы, контролирующие это свойство, мы изучали молекулярногенетические вариации гена BTC1, ключевого гена, связанного с одно- и двулетним жизненным циклом. Следовательно, молекулярная изменчивость (полиморфизм) BTC1 может быть мишенью для улучшения устойчивости культуры к цветушности. В настоящее время молекулярнобиологическими методами установлено, что слаженная работа вышеуказанных 2 генов осущест- вляется под строгим контролем гена-регулятора BTC1 (Bolting time control 1). Предполагается, что кодируемые им белки оказывают контролирующее воздействие на экспрессию генов BvFT1 и BvFT2. Доказано, что небольшие, но весьма значимые изменения в нуклеотидной последовательности BTC1 (SNPs) являются достаточным фактором, чтобы превратить однолетний генотип в двулетний [11–13].
Таким образом, создание устойчивых к цве-тушности гибридов сахарной свеклы является одной из важных и актуальных проблем в современной селекции.
Цель исследований – скрининг и детекция значимых мутаций в гене BTC1 .
Материалы и методы. Для изучения гена устойчивости к цветушности в качестве материалов были использованы листовые пластинки растения опылителя О-типа, отечественных и иностранных гибридов, отобранные в полевых условиях по проявлению данного признака.
Геномную ДНК выделяли с использованием стандартного протокола экстракции 7,5М ацетатом аммония [14, 15]. Качество экстрагированной НК оценивали электрофорезом в 2 % агарозном геле в 1 × TBE-буфере и определяли ее концентрацию с использованием набора для анализа ДНК HS QubitR (Thermo Fisher Scientific, США).
Для идентификации нуклеотидных последовательностей выполняли сравнение схожих последовательностей в базе данных NCBI. Дополнительный поиск генов и исследование их функций выполнены с использованием KAAS с параметрами по умолчанию [16]. Функции некоторых генов проверяли вручную, с использованием алгоритма BLAST (Basic local alignment search tool) [17].
Классическую полимеразно-цепную реакцию ставили в термоциклере SimpliAmp (Thermo
Fisher Scientific, США). Оптимизацию температуры отжига олигонуклеотидов проводили применяя метод температурного градиента. Реакцию амплификации проводили согласно следующему протоколу:
-
1: 94,0 °C в течение 4 мин (предварительная денатурация для активации «Hotstart» ДНК-полимеразы);
-
2: 94,0 °C в течение 30 с (денатурация в начале амплификационного цикла);
-
3: 58,0 °C в течение 1 мин 20 с (отжиг праймеров);
-
4: 72,0 °C в течение 1 мин 30 с (элонгация), количество циклов 30;
-
5: 72,0 °C в течение 5 мин (конечная элонгация).
Для обнаружения гена, контролирующего время цветения, в работе использовалась пара праймеров F.9/R.9, дизайн которых проводили в Primer BLAST (URL: primer-blast):
F.9 – 5, TGCAAGCAATCATGGGAGCA 3,
R.9 – 5, GTTTCCGGAATCGCGTTTGA 3,
Для регистрации продуктов ПЦР-ампли-фикации проводили аналитический электрофорез в 1,5 % агарозном геле c бромистым этидием. Визуализацию осуществляли под действием УФ-излучения на трансиллюминаторе Vilber (Франция). Секвенирование полученных продуктов амплификации осуществляли по методу Сэнгера на генетическом анализаторе Applied Biosystems 3500.
Результаты и их обсуждение. В результате проведенного ПЦР-анализа 5 селекционноценных образцов сахарной свеклы с использованием сконструированной нами пары праймеров F.9/R.9 у всех генотипов выявлен ожидаемый единичный бэнд, размером 1000 пн (рис. 1).
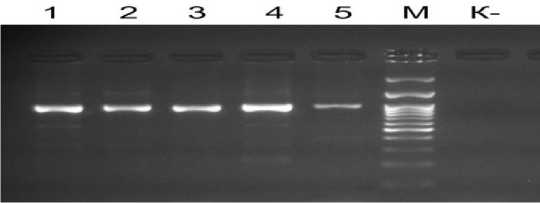
Рис. 1. ПЦР-амплификация генотипов свеклы с праймерами F.9/R.9:
1 – Медина (KWS, цветушное раст.); 2 – F 1 19153 (нецветушное раст.); 3 – РФ709 (нецветушное раст.); 4 – РМС127 (цвет. раст.); 5 – дикая свекла B. corolliflora Zoss.; М – маркер длин ДНК GeneRuler™ (Thermo Scientific, США); К- – (ПЦР-смесь без ДНК)
Среди генотипов, где обнаружен ПЦР-продукт, присутствуют как цветушные, так и не-цветушные растения. Объясняется это наличием в гене BTC1 определенных SNPs (однонуклеотидные замены), в данном случае в экзонах 9 и 10, что способствует преобразованию цветушно-го генотипа в нецветушный. Для точного подтверждения данного явления некоторые ампликоны (№ 3 и 4) были просеквенированы. Результаты прочтения нуклеотидных последовательностей части 9-го и 10-го экзонов отобранных образцов были проанализированы в программе Geneious Prime. В селекционном номере 4 (гибрид РМС 127) было подтверждено наличие известной однонуклеотидной замены – A/G, где присутствие аденина в данной позиции (10 экзон, 72) характерно для устойчивых генотипов [9]. Также в данных генотипах были выявлены новые SNPs в экзоне 10. На рисунке 2 представлен фрагмент генетического анализа по Сэнгеру, где наглядно продемонстрировано положение однонуклеотидных замен G/A в четырех позициях, а также в двух – A/G. При выравнивании нуклеотидных последовательностей интрона исследуемого генотипа с контрольным устойчивым генотипом с двулетним циклом развития (GenBank, Acc. No HQ709091.1) была выявлена вставка (insertion) длиной в 22 п.н. Для подтверждения того, что данная вставка в интроне может быть характерной для чувствительных генотипов, требуется изучение большого количества образцов, склонных к цветушности. Но изученный ранее нами гибрид Хамбер, характеризующийся проявлением цветушности, также содержал в интроне между 9-м и 10-м экзонами аналогичную вставку в 22 п.н., но с другой нуклеотидной последовательностью.
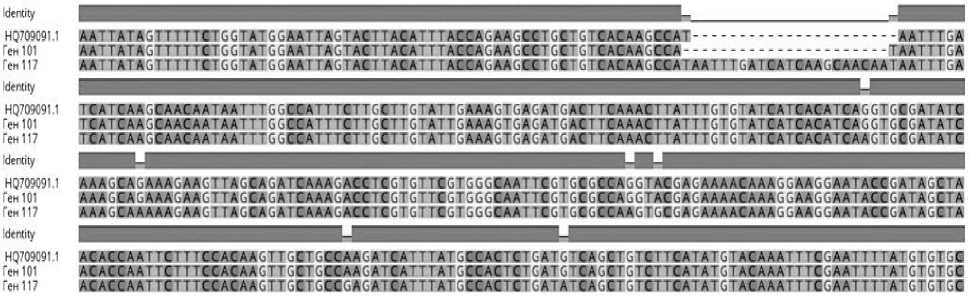
Рис. 2. Фрагмент локализации SNP s в 10-м экзоне и вставки/делеции в интронах образцов № 3 (101) и № 4 (117)
Не все SNPs являются интересными с точки зрения молекулярной биологии, так как многие из них могут относиться к так называемым synonymous SNP или нонсенс-мутациям и на выходе не менять аминокислотный состав белка. Лишь некоторые однонуклеотидные замены являются функционально значимыми (nonsynonymous), когда происходит замена аминокислоты в полипептидной цепи (в сравнении с нормой), в результате чего происходит экспрессия уже функционально другого белка. Из теоретического расчета в программе Geneious Prime следует, что только одна нуклеотидная замена не является ключевой (G/A – вторая по счету), так как не вносит изменения в аминокислотную последовательность пептида. Остальные 5 SNPs являются nonsynonymous и провоцируют замещение аминокислот. В двух случаях замен G/A (первая и третья по счету) вместо глицина синтезируется серин, шестая замена G/A способствует синтезу изолейцина вместо валина. Четвертая SNP (A/G) замещает треонин на аланин, а пятая SNP (A/G) – глутамин на аргинин (рис. 3).
Для селекции данные молекулярногенетические исследования очень актуальны и практически значимы. Они могут помочь селекционеру спрогнозировать вероятность проявления признака цветушности у разных генотипов. Знания о генетической природе раннего цветения полезны при использовании культуры Beta vulgaris в разных географических поясах.
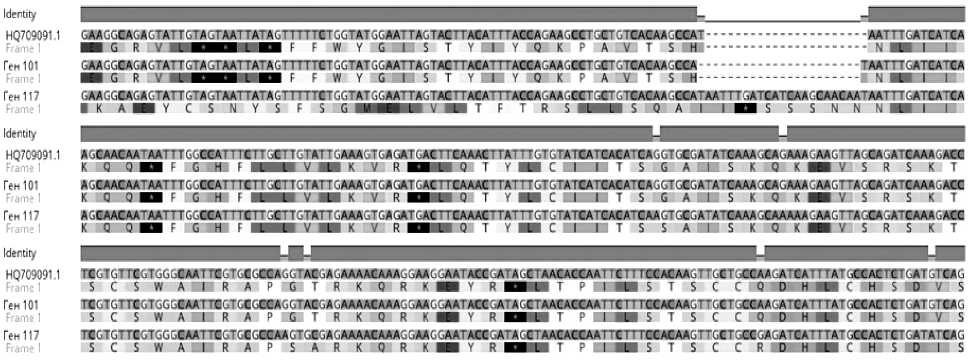
Рис. 3. Дедуктивные аминокислотные последовательности, кодируемые полиморфными вариантами фрагмента экзона 10 гена BTC1: HQ709091.1 – контроль, нецветушный генотип; ген 101 ‒ № 3 (РФ709 нецветушное раст.); ген 117 ‒ № 4 (РМС 127 цветушное раст.)
Заключение. Результаты проведенного мо-лекулярного-генетического анализа свидетельствуют, что данные генотипы сахарной свеклы содержат в своем геноме полноценный ген, контролирующий работу двух генов-кандидатов цветушности ( FT1, FT2 ). В гибриде РМС-127 (№ 4) было подтверждено наличие известных SNP s в 10-м экзоне, характерных для цветуш-ных генотипов, и выявлены новые. В полевых условиях около 5 % растений данного гибрида проявляли цветушность в первый год вегетации. В растениях закрепителя стерильности О-типа РФ-709 не было выявлено данных однонуклеотидных замен. В поле растения данного генотипа не проявляли цветушности.
Это имеет важное теоретическое и практическое значение, так как позволяет на ранних этапах селекционного процесса выявлять генотипы со склонностью к цветушности. В дальнейшем будет продолжено изучение данного актуального вопроса для выявления всех значимых SNPs во всех десяти экзонах гена BTC1.
Список литературы Молекулярные вариации гена BTC1 Beta vulgaris L
- DNA molecular markers in plant breeding: cur-rent status and recent advancements in ge-nomic selection and genome editing. Review / M. Nadeem [et al.] // Biotechnology & Biotech-nological equipment. 2018. Vol. 32. No. 2. P. 261–285. DOI: 10.1080/13102818.2017. 1400401.
- High resolution mapping of the bolting gene B of sugar beet / A. El-Mezawy [et al.] // Theor Appl Genet. 2002. Vol. 105. P. 100–105. DOI: 10.1007/s00122-001-0859-z.
- A bacterial artificial chromosome (BAC) library of sugar beet and physical map comprising the bolting gene B / U. Hohmann [et al.] // Mol Gen Genom. 2003. Vol. 269. P. 126-136. DOI: 10.1007/s00438-003-0821-7.
- Sugar beet (Beta vulgaris L.) / H. Kagami [et al.] // Methods Mol Biol. 2015. P. 335–347. DOI: 10.1007/978-1-4939-1695-5_27.
- Two CONSTANS-LIKE genes jointly control flowering time in beet / N. Dally [et al.] // Sci Rep. 2018. Vol. 8:16120. DOI: 10.1038/ s41598-018-34328-4.
- Gauley A., Boden S. Stepwise increases in FT1 expression regulate seasonal progression of flowering in wheat (Triticum aestivum) // New Phytologist. 2021. V. 229. P. 1163–1176. DOI: 10.1111/nph.16910.
- Genetic analysis of bolting after winter in sugar beet (Beta vulgaris L.) / N. Pfeiffer [et al.] // TheorAppl Genet. 2014. Vol. 127. P. 2479–2489. DOI: 10.1007/s00122-014-2392-x.
- A detailed analysis of the BR1 locus suggests a new mechanism for bolting after winter in sugar beet (Beta vulgaris L.) / C. Tränkner [et al.] // Front. Plant Sci. 2016. Vol. 7:1662. DOI: 10.3389/fpls.2016.01662.
- Haplotype Variation of Flowering Time Genes of Sugar Beet and Its Wild Relatives and the Impact on Life Cycle Regimes / N. Höft [et al.] // Front Plant Sci. 2018. Vol. 8:2211. DOI: 10.3389/fpls.2017.02211.
- Transcriptomic study of the night break in Chenopodium rubrum reveals possible up-stream regulators of the floral activator CrFTL1 / D. Guti´errez-Larruscain [et al.] // Journal of Plant Physiology. 2021. V. 265. Arti-cle 153492.
- The Role of a Pseudo-Response Regulator Gene in Life Cycle Adaptation and Domestica-tion of Beet / P. Pin [et al.] // Current Biology. 2012. Vol. 22. P. 1095–1101. DOI: 10.1016/j. cub.2012.04.007.
- Höft N., Dally N., Jung Ch. Sequence variation in the bolting time regulator BTC1 changes the life cycle regime in sugar beet // Plant Bree-ding. Original article. 2018. Vol. 137. P. 412–422. DOI: 10.1111/pbr.12579.
- Validation of suitable genes for normalization of diurnal gene expression studies in Chenopodium quinoa / N. Maldonado-Taipe [et al.] // PLoS ONE. 2021. V. 16 (3). DOI: 10.1371/journal.pone.0233821.
- Development of an Ammonium Sulfate DNA Extraction Method for Obtaining Amplifiable DNA in a Small Number of Cells and Its Application to Clinical Specimens / S. Young [et al.] // BioMed Research International. 2013. Article ID 546727:1-10. DOI: 10.1155/2013/546727.
- Efficient and nontoxic DNA isolation method for PCR analysis / A.S. Hussein [et al.] // Rus-sian Agricultural Sciences. 2014. No 40 (3). P. 177–178.
- KAAS: an automatic genome annotation and pathway reconstruction server / Y. Moriya [et al.] // Nucleic Acids Research. 2007. Vol. 35. P. 182–185. DOI: 10.1093/nar/gkm321.
- Basic local alignment search tool / S. Altschul [et al.] // Journal of molecular biology. 1990. Vol. 215(3). P. 403–410. DOI: 10.1016/S0022-2836(05)80360-2.


