Мониторинг динамики активности злокачественного роста методом структурного анализа неклеточной ткани
Автор: Шабалин В.Н., Шатохина С.Н., Дедова М.Г.
Журнал: Ульяновский медико-биологический журнал @medbio-ulsu
Рубрика: Клиническая медицина
Статья в выпуске: 3, 2021 года.
Бесплатный доступ
Исследован состав биокристаллических структур (анизоморфонов) сыворотки крови больных раком гортани, которые формируются при переходе сыворотки крови в твердую фазу в процессе ее краевой дегидратации. Выявленные анизоморфоны представляют собой три вида маркерных структур: маркер активного роста злокачественной опухоли - агрегация макросферолита и зернистого микросферолита с одинаковой степенью анизотропии; маркер дегенеративно-дистрофического процесса - агрегация макросферолита с низкой степенью анизотропии и микросферолита с высокой степенью анизотропии; маркер прогрессии злокачественного роста - волнистый микросферолит вне агрегации. Цель - выявить диагностические маркеры активности злокачественного процесса в структурах твердой фазы сыворотки крови больных раком гортани и оценить их значение для выбора эффективного вида лечения. Материалы и методы. В качестве основного метода исследования использован метод краевой дегидратации сыворотки крови, являющийся разделом диагностической технологии «Литос-система» (Разрешение ФС № 155 от 2009 г. на применение в клинической практике). Результаты. Показано, что фаза развития рака гортани (активный рост или дегенеративно-дистрофический процесс) служит важным критерием выбора вида лечения: в фазу дегенеративнодистрофического процесса опухоли наиболее благоприятный эффект дает хирургическое лечение, а в период активной фазы злокачественного роста - лучевая терапия.
Рак гортани, сыворотка крови, краевая дегидратация биологических жидкостей, маркеры фазы активности опухолевого роста
Короткий адрес: https://sciup.org/14121670
IDR: 14121670 | УДК: 616-006.04 | DOI: 10.34014/2227-1848-2021-3-89-96
Monitoring of malignant growth dynamics by structural analysis of non-cellular tissue
The authors examined the composition of biocrystalline structures (anisomorphones) of blood serum in patients with laryngeal cancer. Such structures are formed when blood serum becomes solid, i.e. during its marginal dehydration. The revealed anisomorphones represent three types of marker structures: a marker of a malignant tumor active growth (the aggregation of macroferolite and granular microspherolite with the same degree of anisotropy); a marker of a degenerative-dystrophic process (the aggregation of a macro-spherolite with a low degree of anisotropy and microspherolite with a high degree of anisotropy); a marker of a malignant growth progression (a wavy microspherolite without aggregation). The aim of the study is to identify diagnostic markers of the malignant process activity in the solid phase structures of the blood serum in patients with laryngeal cancer and to assess their importance for choosing an effective therapy. Materials and Methods. Marginal dehydration of blood serum was used as the main research method. It is a part of the "Litos-system" diagnostic technology (Marketing authorization FS No. 155, of2009). Results. It has been shown that the developmental phase of laryngeal cancer (active growth or degenerative-dystrophic process) is an important criterion for choosing treatment options. Surgical treatment is the most effective during the degenerative-dystrophic tumor process, while radiation therapy is preferable during the active phase of malignant growth.
Текст научной статьи Мониторинг динамики активности злокачественного роста методом структурного анализа неклеточной ткани
Введение. Рак гортани является наиболее частым видом злокачественных опухолей лор-органов [1]. Ежегодно в России первичный рак гортани устанавливают у 6–7 тыс. пациентов [2]. В последние годы разработаны новые подходы к лечению и реабилитации больных раком гортани, как консервативные, так и хирургические. Однако вопрос о выборе метода лечения остается дискутабельным [3]. Успех лечения онкологических больных во многом зависит от стадии выявления опухоли [4]. В связи с тем что в 30-35 % случаев заболевание протекает бессимптомно, диагностика злокачественного роста запаздывает [5, 6]. В то же время опухолевый процесс имеет фазовое течение: активная фаза сменяется фазой покоя. Фаза активности опухолевого роста имеет принципиальное значение для выбора вида лечения. На сегодняшний день не существует общепризнанного молекулярного маркера, позволяющего с высокой долей вероятности прогнозировать инвазию и метастазирование опухоли у больных раком гортани [7].
Разработанная нами новая технология диагностики различных видов патологических процессов, в т.ч. и злокачественного роста, базирующаяся на морфологических признаках структур неклеточных тканей организма -биологических жидкостей, открывает значительные перспективы. При исследовании структур сыворотки крови больных с различной локализацией опухолей (т.е. с помощью нового вида жидкостной биопсии) нами были открыты морфологические маркеры доброкачественной и злокачественной неоплазии [8], показано соотношение процессов пролифера- ции и дегенерации в течении злокачественного роста [9].
Цель исследования. Выявить диагностические маркеры активности злокачественного процесса в структурах твердой фазы сыворотки крови больных раком гортани и оценить их значение для выбора эффективного вида лечения.
Материалы и методы. Под наблюдением находились 64 больных раком гортани в возрасте от 47 до 83 лет, среди них было 59 мужчин и 5 женщин. По данным гистологического заключения у всех больных диагностирован плоскоклеточный рак. По стадиям заболевания: Т1N0М0 – 4 чел., Т2N0M0 – 19, Т3N0M0 – 32, Т3N2М0 – 5, Т4N0М0 – 4.
В качестве основного метода исследования использован метод краевой дегидратации сыворотки крови, являющийся разделом диагностической технологии «Литос-система» (разрешение ФС на применение новой медицинской технологии № 2009/155 от 15 июня
2009 г.). Взятие крови у пациента проводили натощак из локтевой вены в объеме 2 мл. Кровь собирали в сухую пробирку (без стабилизатора), после свертывания центрифугировали при 3000 об/мин в течение 10 мин. Полученная сыворотка крови являлась основным объектом исследования. Полуавтоматической пипеткой-дозатором наносили каплю сыворотки крови (0,02 мл) в аналитическую ячейку тест-карты ТК4 (рис. 1), накрывали покровным стеклом. Далее тест-карты выдерживали в течение 7 сут при температуре 20–25 °С и относительной влажности 55–60 %. При этом в процессе медленного перехода в твердую фазу в сыворотке крови формировались отдельные биокристаллы (морфоны). Морфоны могли иметь изо- или анизотропную структуру. В настоящей работе нас интересовали только анизоморфоны. Их исследование проводили с помощью микроскопа DM2500 фирмы Leica в поляризованном свете при увеличении ×100, ×200, ×400, ×800.
Рис. 1. Тест-карта (ТК4) диагностического набора «Литос-система»
Fig. 1. Test card (TC4), "Litos-system" diagnostic kit
Исследование анизоморфонов сыворотки крови больных раком гортани проводили периодически на протяжении всего периода наблюдения: при поступлении пациента в стационар, в процессе лучевой терапии – после доз 46 и 70 Гр, при хирургическом вмешательстве – до и в послеоперационном периоде, да- лее при амбулаторном наблюдении – через каждые 1–2 мес. на протяжении двух лет.
Статистическую обработку полученных данных проводили при помощи программы Statistica for windows v.8.0. Для концевых точек (0 и 100 %) применялся t-критерий Стьюдента с поправкой на концевые точки. Для вы- явления зависимости эффективности лечения от исходного состояния опухолевой ткани (активный рост или дегенеративно-дистрофическое состояние) использовался корреляционный анализ Пирсена (r).
Результаты и обсуждение. При поступлении в стационар анизоморфоны сыворотки крови больных раком гортани были представлены двумя видами: маркером злокачественного роста (МЗР) и маркером дегенеративнодистрофического процесса (МДД) [10].
МЗР представлял собой агрегацию базисного сферолита, в центре которого располагался микросферолит с зернистой структурой (рис. 2а). Данная агрегация имела равномерную степень выраженности анизотропии. МДД также был представлен агрегацией базисного сферолита с зернистым микросферолитом. Однако отличие этой агрегации от МЗР состояло в более низкой степени анизотропии базисного сферолита при резко выраженной анизотропии встроенного в него микросферолита, который имел вид ярко светящегося «глазка» (рис. 2б).
При первичном исследовании 64 больных раком гортани МЗР был выявлен у 36 (56 %), а МДД – у 28 (44 %) чел. На основании клинико-лабораторных показателей 23 больным было проведено хирургическое лечение, а 41 больной получил курс лучевой терапии по радикальной программе. В ходе дальнейших исследований в сыворотке крови наблюдаемых больных была отмечена смена видов ани-зоморфонов на этапах лечения и в процессе последующего амбулаторного наблюдения.
Сопоставление клинических данных и результатов морфологических исследований показало, что эффективность определенного вида лечения зависела от стадии развития опухолевого процесса, которая устанавливалась по онкомаркерам: МЗР и МДД (табл. 1).

а
Рис. 2. Анизоморфоны сыворотки крови:
а) маркер злокачественного роста; б) маркер дегенеративно-дистрофического процесса.
Ув. ×200. Микроскопия в поляризованном свете

б
-
Fig. 2. Blood serum anisomorphone:
-
a) malignant growth marker; b) marker degenerative-dystrophic process marker.
Zoom×200. Polarized light microscopy
Данные табл. 1 показывают значительные различия результатов хирургического лечения и лучевой терапии в зависимости от вида онкомаркеров в сыворотке крови больных раком гортани. Так, из 23 пациентов, которым было проведено хирургическое лечение, 14 пациентов имели МЗР. Из них 9 чел. после операции оставались живыми в течение двух лет наблюдения, а 5 погибли (трое – через 2 мес. после операции, 2 – через 4 и 6 мес.). Больные, в сыворотке крови которых выявлялся МДД (9 пациентов), оставались в живых в течение всего срока наблюдения.
Таблица 1
Table 1
Результаты лечения больных раком гортани в зависимости от вида структурных онкомаркеров в сыворотке крови
Treatment outcomes of laryngeal cancer patients depending on structural tumor markers in blood serum
|
Результат лечения Treatment outcomes |
Хирургическое лечение Surgical treatment (n=23) |
Лучевая терапия Radiotherapy (n=41) |
||
|
МЗР Malignant growth marker (n=14) |
МДД Degenerative-dystrophic process marker (n=9) |
МЗР Malignant growth marker (n=22) |
МДД Degenerative-dystrophic process marker (n=19) |
|
|
Положительный Positive |
9 |
9 |
22 |
8 |
|
Летальный исход Mortality |
5 |
0 |
0 |
11 |
В группе больных, получивших курс радикальной лучевой терапии (41 чел.), у 22 пациентов до начала лечения в сыворотке крови был выявлен МЗР. После проведенной лучевой терапии все они оставались в живых в течение всего срока наблюдения. У 19 пациентов до начала лечения был выявлен МДД. Здесь наблюдался значительно худший результат лечения: только 8 больных оставались живыми на конец срока наблюдения, а остальные 11 погибли: 7 – через 1–2 мес., 4 – через 5–7 мес. после проведенного курса лечения.
При исследовании морфологической картины сыворотки крови 11 больных раком гортани после курса лучевой терапии с последующим летальным исходом у всех были выявлены особые, не обнаруживаемые до лечения маркеры в виде волнистых микросферолитов (ВМС). Они располагались изолированно, т.е. не были встроены в базисные сферолиты, а вместо зернистости (рис. 3а) в них определялись волнообразные структуры (рис. 3б). Следует отметить, что у двух пациентов данный маркер обнаруживался одновременно с выявлением клинических признаков прогрессии злокачественного роста, а у девяти – на два месяца раньше их клинической манифестации. Появление ВМС в сыворотке крови больных после курса лучевой терапии указывает на продолженный рост опухоли. То есть используемая доза лучевого воздействия на опухолевую клетку, находящуюся в фазе покоя
(МДД) и имеющую резистентность к любым внешним воздействиям, оказывает не угнетающий, а стимулирующий эффект. Это вызывает мутацию исходного пула клеток с последующим возникновением более злокачественного клона. Структура ВМС формируется специфическими белковыми молекулами, которые вырабатываются клетками нового злокачественного клона. Наши исследования показали, что появление ВМС указывает на неблагоприятное течение онкологического процесса (р=0,043).
При сопоставлении результатов лечения больных с наличием МЗР выявлено, что эффективность лучевой терапии по сравнению с хирургическим лечением достоверно выше (р=0,02).
При сравнении результатов лечения больных с МДД установлена обратная зависимость: эффективность лучевой терапии оказалась достоверно ниже, чем при хирургическом лечении (р=0,01).
При помощи корреляционного анализа Пирсена в группах хирургического лечения выявлена прямая умеренная зависимость между фазой процесса в опухоли (злокачественный рост или дегенеративно-дистрофический процесс) и эффективностью лечения (r=0,447; р=0,013). В группе лучевой терапии установлена прямая зависимость между активностью опухоли и эффективностью лечения (r=0,247; р<0,05).
а
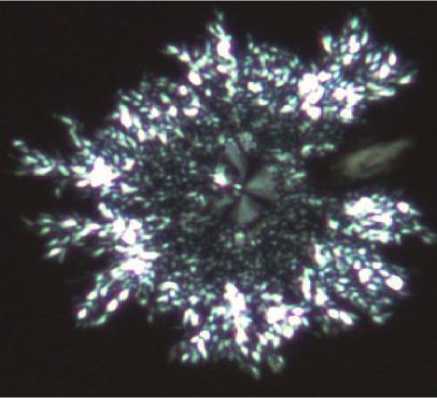
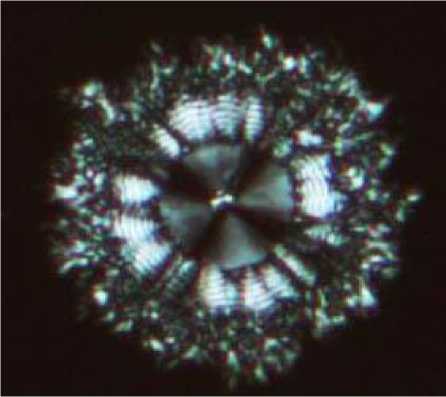
Рис. 3. Анизоморфоны сыворотки крови: а) зернистый микросферолит; б) волнистый микросферолит. Ув. ×800. Микроскопия в поляризованном свете
б
Fig. 3. Blood serum anisomorphone:
-
a) granular microspherolite; b) wavy microspherolite. Zoom×800. Polarized light microscopy
Таким образом, среди анизоморфонов сыворотки крови больных раком гортани выявлены три вида маркерных структур: маркер активного роста злокачественной опухоли (патологическая агрегация базисного сферолита и зернистого микросферолита с одинаковой степенью анизотропии); маркер дегенеративно-дистрофического процесса (аналогичная агрегация, но с низкой степенью анизотропии базисного сферолита при высокой анизотропии встроенного микросферолита); маркер прогрессии злокачественного роста (волнистый микросферолит вне агрегации).
Полученные результаты показывают, что состояние активности опухоли (активный рост или дегенеративно-дистрофический процесс) служит важным критерием выбора вида лечения: в фазу дегенеративно-дистрофического процесса рака гортани наиболее благоприятный эффект достигается при хирургическом лечении, а в период активной фазы зло- качественного роста – при помощи лучевой терапии.
Выводы:
-
1. Морфологическое исследование сыворотки крови больных раком гортани методом краевой дегидратации позволяет выявить специфические маркеры злокачественного роста, указывающие на фазу его активности.
-
2. При наличии в сыворотке крови больных раком гортани маркера дегенеративнодистрофического состояния опухоли показано хирургическое лечение, а выявление маркера активности злокачественного роста указывает на необходимость применения лучевой терапии.
-
3. Выявление в сыворотке крови больного раком гортани в процессе лучевой терапии маркерной структуры в виде волнистого микросферолита указывает на отрицательный результат лечения – продолженный рост опухоли.
Список литературы Мониторинг динамики активности злокачественного роста методом структурного анализа неклеточной ткани
- Раджабова З.А., Котов М.А., Эберт М.А., Митрофанов А.С., Раджабова М.А., Левченко Е.В. Распространенный рак гортани: обзор литературы. Сибирский онкологический журнал. 2019; 18 (5): 97-107. =-5-97-107. DOI: 10.21294/1814-4861-2019-18
- Каприн А.Д., Старинский В.В., Петрова Г.В., ред. Злокачественные новообразования в России в 2018 году (заболеваемость и смертность). М.; 2019. 250.
- Кожанов А.Л. Современные аспекты лечения и реабилитации больных при раке гортани. Опухоли головы и шеи. 2016; 6 (2): 17-26.
- Edge S.B., Bynd D.R., Compton C. C., Fritz A.L., Trolti A. Laryngs AJCC Cancer Staging Mfnual. 7th ed. New York: Springer; 2010: 57-62.
- Медведева А.А., Чернов В.И., Зельчан Р.В., Синилкин И.Г., Фролова И.Г., Чижевская С.Ю., Чойнзонов Е.Л., Черемисина О.В., Гольдберг А.В. Радионуклидные методы исследования в диагностике рака гортани и гортаноглотки. Сибирский онкологический журнал. 2017; 16 (6): 57-66.
- Paget-Boilly S., Cyr D., Luce D. Ocupational expozures and cancer of the larings-systematic review and meta analysis. J. Occup. Environ. Med. 2012; 54 (I): 71-84.
- Немцова М.В., Кушлинский Н.Е. Молекулярно-биологические маркеры в практической онкологии. Лабораторная служба. 2014; 3 (1): 14-22.
- Шатохина С.Н., Шабалин В.Н. Атлас структур неклеточных тканей человека в норме и патологии (в 3 томах). Т. II. Морфологические структуры сыворотки крови. М.; 2013. 238.
- Шатохина С.Н., Шабалин В.Н. Маркеры злокачественного роста в морфологической картине биологических жидкостей человека. Вестник онкологии. 2010; 3 (56): 293-300.
- Шабалин В.Н., Шатохина С.Н. Функциональная морфология неклеточных тканей человека. М.: РАН; 2019. 360.


