Морфологическая трансформация стенки артериализованной вены
Автор: Калинин Р.Е., Пшенников А.С., Деев Р.В., Виноградов С.А., Самбурин В.А.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 3 т.18, 2023 года.
Бесплатный доступ
Цель исследования изучить и сравнить патоморфологические изменения стенки артериализованной вены у больных после аутовенозного бедренно-подколенного шунтирования по методике «in situ» и реверсированной веной, а также артериализации поверхностного венозного русла стопы. Материалом для исследования послужили фрагменты стенки артериализованной вены (n = 7), полученные при повторных оперативных вмешательствах. Микропрепараты исследованы с помощью гистологического (окраска гематоксилин и эозин, орсеин и по Маллори) и иммуногистохимического (Ki-67, CD31, a-SMA) методов. Выявленные патоморфологические изменения артериализованных вен являются характерными для дезадаптивного ремоделирования венозной стенки и включают утолщение стенки, повреждение эндотелия с формированием мозаичного монослоя и его пролиферацию, т.н. неоинтимальную фиброзную и гладкомышечную гиперплазию в результате миграции и пролиферации лейомиоцитов и образования коллагена, ремоделирование соединительнотканного матрикса и воспалительную инфильтрацию стенки.
Заболевания периферических артерий, большая подкожная вена, окклюзия шунта, артериализация вены, венозное шунтирование, шунтирование «in situ», реверсированное шунтирование, атеросклероз
Короткий адрес: https://sciup.org/140301236
IDR: 140301236 | DOI: 10.25881/20728255_2023_18_3_30
Pathological changes in the wall of the vein adapted to arterial circulation
The aim of the study is evaluation and comparison of pathomorphological changes in vein wall adapted to arterial circulation with patients after autogenous femoral-popliteal bypass using the "in situ” and reversed vein technique, as well as arterialization of the superficial foot vein. The material for this study was parts of arterialized venous (n = 7) wall obtained during repeated surgery. Micropreparations studied by histological (stain hematoxylin and eosin, orcein and according to Mallory) and immunohistochemical (Ki-67, CD31, a-SMA) methods. The identified pathomorphological changes in vein wall adapted to arterial circulation are characteristic of nonadaptive remodeling of the venous wall and include its thickening, endothelial damage with the formation of a mosaic monolayer and its proliferation, neointimal fibrous and smooth muscle hyperplasia as a result of migration and proliferation of leiomyocytes and increase in collagen production, remodeling of the connective tissue matrix and inflammatory infiltration.
Текст научной статьи Морфологическая трансформация стенки артериализованной вены
Заболевания периферических артерий занимают весомое место в структуре сердечно-сосудистой патологии и остаются ведущей причиной инвалидизации [1; 2]. Зарекомендовавшие себя методики аутовенозного бедренно-подколенного шунтирования (БПШ) уже на протяжении более полувека остаются «золотым стандартом» открытой реконструктивной сосудистой хирургии [3–5]. В отличие от синтетических протезов, уступающих по проходимости в отдаленном периоде, венозный шунт из большой подкожной вены (БПВ) является аутологичным биологическим кондуитом, который имеет функциональную эндотелиальную выстилку и соединительнотканный каркас и реагирует как на местные, так и системные клеточные, молекулярные и гемодинамические стимулы, регулируя сосудистый тонус и гомеостаз [6]. Адаптация аутологичной вены к артериальной гемодинамике, исторически определенная как «артериализация», характеризуется сложным патофизиологическим процессом, включающим повреждение, воспаление, ремоделирование стенки и изменение морфофункционального состояния венозного эндотелия [7]. Согласно проведенным исследованиям у 30–50% больных в течение пяти лет эти реакции приобретают патологический дезадаптивный характер, обуславливая нарушение проходимости трансплантата в результате тромбоза и потерю конечности [8].
Цель исследования — изучить и сравнить патомор-фологические изменения стенки артериализованной вены у больных после аутовенозного БПШ по методике «in situ» и реверсированной веной, а также артериализа-ции поверхностного венозного русла стопы.
Материал и методы исследования
Материалом для исследования послужили фрагменты артериализованной венозной стенки, полученные при повторных оперативных вмешательствах (n = 7) в связи с тромбозом шунта, нагноением или прогрессированием заболевания. В трех наблюдениях изучена стенка аутовенозного БПШ «in situ», проходимого 1, 3 и 5 месяцев. В трех случаях исследована реверсированная вена БПШ, проходимая в течение 1 суток, 4 и 6 месяцев. В одном наблюдении — стенка артериализованной БПВ через 3 месяца после артериализации поверхностного венозного русла стопы. Фиксированный в 10% нейтральном

формалине тканевый материал подвергался стандартной гистологической обработке. Микропрепараты для световой микроскопии окрашивали гематоксилином и эозином, орсеином и по Маллори. Иммуногистохимическое исследование проводили с антителами (АТ) к Ki-67, CD-31 и α-SMA; продукт реакции выявлялся при помощи полимерной системы EnVision (DAKO).
Результаты и обсуждения
Стенка реверсированной вены , исследованная через 1 сутки после операции, имбибирована кровью. На поверхности t. intima эндотелиальные клетки (ЭК) отсутствуют во всех полях зрения. На обнаженном соединительнотканном субэндотелиальном матриксе определяются пристеночные тромбы, в некоторых участках полностью обтурирующие просвет шунта. Отмечается выраженный отек t. media еt adventitia, неспецифическая инфильтрация стенки клетками лимфогистиоцитарного ряда. Т. adventitia разрыхлена и фрагментирована, vasa vasorum не определяются (Рис. 1А).
При более длительном нахождении под воздействием потока артериальной крови структуры сосудистой стенки подвергаются существенным изменениям. Через 4 месяца стенка вены резко утолщена за счет комплекса тканей, входящих в состав t. intima еt media. Внутренний слой представлен слоем ЭК с подлежащим уплотненным фибриновым слоем. В некоторых локусах эндотелиоциты отсутствуют, что свидетельствует о мозаичности выстилки t. intima даже через 4 месяца после операции. В этих участках отмечаются пристеночные микротромбы. ЭК характеризуются выраженной пролиферацией, выявленной по Ki-67 (Рис. 1Б). В t. media имеются морфологические признаки повреждения и гибель гладкомышечных клеток (ГМК). Они замещаются участками молодой «незрелой» грануляционной соединительной тканью с большим количеством тонкостенных мелких кровеносных сосудов, которая не подверглась рубцеванию к указанному сроку наблюдения. Грануляционная соединительная ткань располагается между пучками сохранившихся ГМК и зрелых волокон коллагена (Рис. 1В, Г). Т. adventitia разрыхлена, фрагментирована, представлена богатоваскуляризованной соединительной тканью, обнаруживаются vasa vasorum (Рис. 1Д).
В более поздний период — через 6 месяцев стека вены выраженно утолщена за счет фиброзной и гладкомышечной неоинтимальной гиперплазии, в результате чего просвет сосуда резко сужен. В нем сформирован пристеночный, организующийся тромб, практически полностью обтурирующий просвет вены (Рис. 1Е, Ж, З). В t. intima отмечен выраженный отек. Следует констатировать, что в течение 6 месяцев сохраняется мозаичность эндотелия: клеточный монослой интимы нарушен. Сохранившиеся ЭК пролиферируют. В некоторых участках определяются волокна коллагена и эластин субэндотелиального матрикса, неспецифическая инфильтрация клетками лимфогистиоцитарного ряда (Рис. 1И). В утолщенном субинтимальном слое зарегистрировано большое количество ГМК. В результате фрагментации эластической мембраны эти клетки мигрируют в субинтимальный слой и активно пролиферируют, принимая непосредственное участие в утолщении стенки шунта (Рис. 1К). В t. media et adventitia поддерживается выраженный отек. В некоторых фрагментах отмечается частичный некроз лейомиоцитов. Для оставшихся ГМК характерна зернистая и гидропическая дистрофия. Между группами сохранившихся ГМК формируются фиброзные септы (Рис. 1Л). Таким образом, выраженное ремоделирование соединительнотканного матрикса отмечается во всех слоях стенки вены, заключающееся в утолщении эластических волокон и разрастании коллагеновых волокон между пучками ГМК (Рис. 1Ж). Деструкция эластического каркаса проявляется фрагментацией и разрушением внутренней и наружной эластической мембран, что благоприятствует миграции воспалительных клеток крови, ГМК, миофибробластов и прогениторных клеток в стенку вены, опосредующих ремоделирование аутовенозного шунта (Рис. 1З).
Т. intima аутовены «in situ» через 1 месяц после операции представлена монослоем ЭК, что подтверждается ИГХ исследованием к CD31. Стенка утолщена за счет субинтимального слоя и t. media, которая представлена пучками лейомиоцитов между волокнами зрелой соединительной ткани. Т. adventitia содержит vasa vasorum и грануляционную соединительную ткань, количество которой увеличивается ближе к анастомозу (Рис. 2А).
Патоморфологические изменения стенки аутовенозного шунта «in situ», эксплантированного при аррозивном кровотечении через 3 месяца после операции (проходим на момент повторной операции), характеризуются отсутствием гиперплазии неоинтимы. Вместе с тем, в t. intima эндотелиальная выстилка мозаичная, ЭК встречаются лишь в единичных участках. Стенка вены значимо не утолщена за счет пластических процессов, но имеется отек всех слоев и лейкоцитарная инфильтрация. Множество vasa vasorum в t. adventitia сохранены (Рис. 2Б). T. intima et media обычных размеров; сохранен широкий просвет для кровотока.
Через 5 месяцев стенка вены резко утолщена за счет неоинтимы. На люминальной поверхности t. intima встречаются ЭК. К большей части поверхности эндотелия прилежит пристеночный красный тромб. Стенка инфильтрирована воспалительными клетками. Внутренняя оболочка и подлежащий субинтимальный слой с выраженной фиброзной неоинтимальной гиперплазией, характеризующейся разрастанием зрелой соединительной ткани между небольшими участками, занятыми ГМК (Рис. 2В). Дезоблитерированная неоинтима представляет собой зрелую рубцовую соединительную ткань. На просветной поверхности ЭК отсутствуют. На участке с внешней стороны сосуда визуализируется небольшое количество клеток соединительнотканного ряда и участки грануляционной ткани с мелкими кровеносными сосудами (Рис. 2Г). В t. media наблюдается выраженный

А
В
Г
K
Л
11 1
З
Ж
И
Е
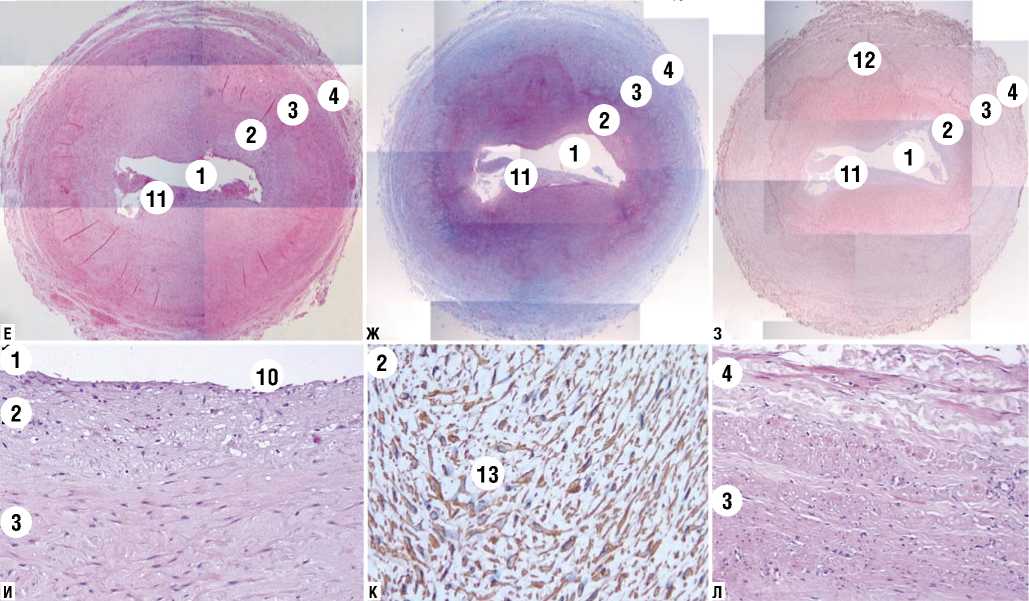
Рис. 1. Патоморфологические изменения стенки артериализованного реверсированного венозного БПШ. А — Стенка вены на 1 сутки; Б, В, Г, Д — стенка вены через 4 месяца; Е, Ж, З, И, К, Л — стенка вены через 6 месяцев. 1 — просвет шунта, 2 — t. intima, 3 — t. media, 4 — t. adventitia, 5 — фибриновый слой, 6 — грануляционная соединительная ткань, 7 — волокна коллагена, 8 — кровеносные сосуды, 9 — vasa vasorum, 10 — ЭК, 11 — пристеночный тромб, 12 — эластическая мембрана, 13 — ГМК. Окраска: А, Б, В, Е, И, Л — гематоксилин и эозин; Г, Ж — по Маллори; Д — ИГХ реакция с АТ к CD31; З — орсеин; К — ИГХ реакция с АТ к a -SMA. Ув.: А, Б, И х 100; В, Г, К, Л х 200; Д х 400; Е, Ж, З х 4.

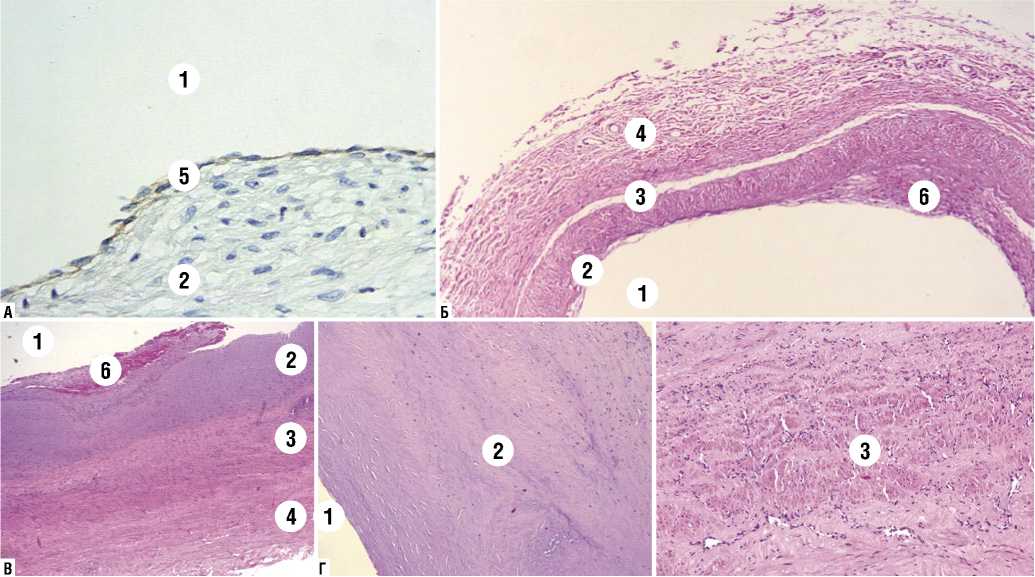
Рис. 2. Патоморфологические изменения стенки артериализованного венозного БПШ «in situ». А — стенка вены через 1 месяц; Б — стенка вены через 3 месяца, В, Г, Д — Стенка вены через 5 месяцев. 1 — просвет шунта, 2 — t. intima, 3 — t. media, 4 — t. adventitia, 5 — ЭК, 6 — пристеночный тромб. Окраска: А — ИГХ реакция с АТ к CD31; Б, В, Г, Д — гематоксилин и эозин. Ув.: А, Д х 200; Б, В, Г х 100.
отек и набухание стромы. Пучки ГМК окружены волокнами межклеточного соединительнотканного матрикса. Внутренняя и наружная эластические мембраны четко не прослеживаются. Присутствует выраженная лейкоцитарная инфильтрация стенки. В t. adventitia большое количество vasa vasorum (Рис. 2Д).
Стенка артериализованной БПВ, изученная через 3 месяца после операции, резко утолщена, преимущественно за счет t. intima еt media, в которых развилась выраженная неоинтимальная гиперплазия. Из-за этого просвет вены резко сужен. В нем имеется обтурирующий тромб, перекрывающий не менее % просвета сосуда (Рис. 3А). T. intima утолщена за счет субинтимального слоя. На просветной поверхности вены обнаружены ЭК. В некоторых локусах эндотелиоциты отсутствуют, что приводит к обнажению субэндотелиального соединительнотканного матрикса (Рис. 3Б). Утолщение t. intima et media происходит в результате неоинтимальной гладкомышечной и фиброзной гиперплазии. При ИГХ-иссле-довании с АТ к α-SMA в субинтимальном слое показано диффузное скопление лейомиоцитов и миофибробластов между волокнами соединительной ткани (Рис. 3В, Г). Гипертрофированные коллагеновые волокна между пучками продольных и циркулярных ГМК указывают на фиброзную перестройку стенки вены (Рис. 3Д, Е). Во всех слоях развилась деструкция эластического каркаса. Внутренняя и наружная эластическая мембраны фрагментированы, с участками эластолиза (Рис. 3Ж). В t. adventitia выявляется большое количество vasa vasorum (Рис. 3И).
Несмотря на то, что исследованию подвергнуты образцы сосудов, полученные через разные сроки после операции, сопоставляя морфологические находки, удается проследить динамику ремоделирования венозной стенки. Важной находкой является тот факт, что весьма пластичная и динамичная ткань — эндотелий, находится в состоянии значительного повреждения и целостность его монослоя в представленных наблюдениях не восстановлена даже через полгода после операции. Нарушение эндотелиального монослоя, обнажение волокон соединительнотканного субэндотелиального матрикса и адгезия клеток крови к просветной поверхности вены создает предпосылки для тромбоза шунта в раннем послеоперационном периоде. В экспериментальных работах, выполненных на различных животных, эндотелиальный монослой восстанавливается в течение 2 недель [7], в то время как в изученных образцах мозаичность эндотелия сохраняется до 6 месяцев.
Обнаружение лейкоцитарной инфильтрации свидетельствует в пользу развертывания воспалительной реакции, причиной которой является плазматическое пропитывание (отек) структур t. media, необратимыми изменениями (некроз) ее клеточных элементов. Повреждение ГМК приводит к замещению t. media соединительной тканью и фиброзной перестройке. В стенке
Б
В
Е
Д
Г
З
Ж
И
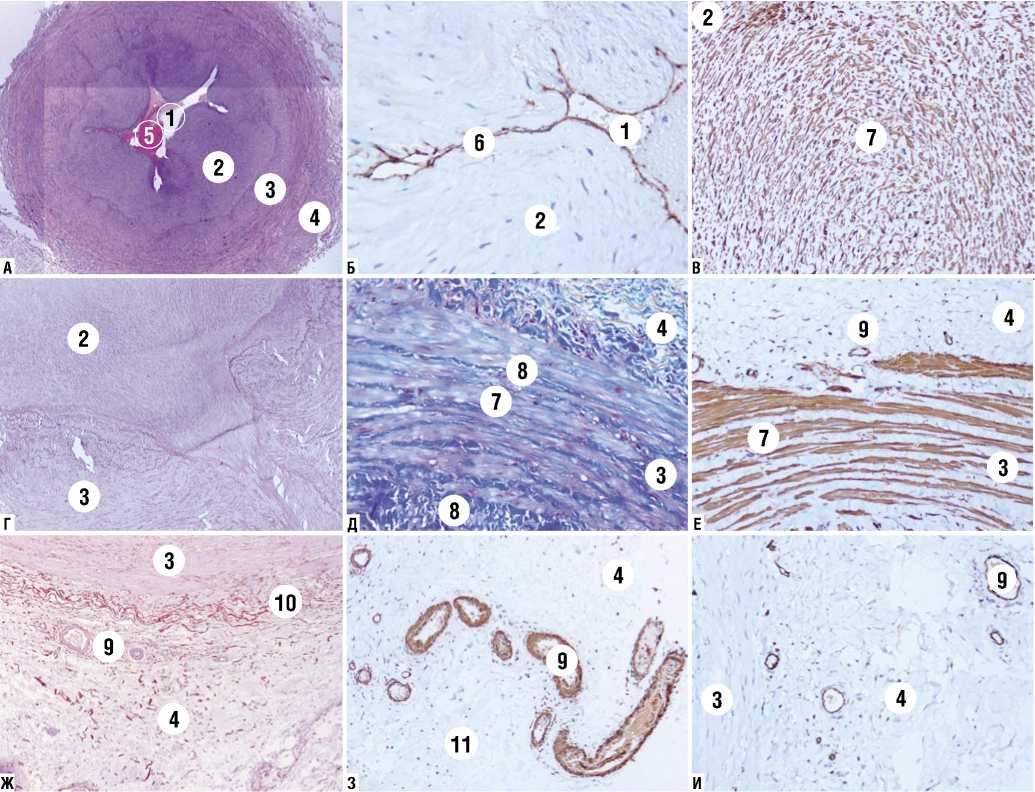
Рис. 3. Патоморфологические изменения стенки артериализованной БПВ через 3 месяца (А, Б, В, Г, Д, Е, Ж, З, И). 1 — просвет вены, 2 — t. intima, 3 - t. media, 4 — t. adventitia, 5 — пристеночный тромб, 6 — эндотелиоциты, 7 — гладкомышечные клетки, 8 — коллагеновые волокна, 9 — vasa vasorum, 10 — наружная эластическая мембрана, 11 — соединительная ткань. Окраска: А, Г — гематоксилин и эозин; Б, И — ИГХ реакция с АТ к CD31; В, Е, З — ИГХ реакция с АТ к a -SMA; Д — по Маллори; Ж — орсеин. Ув.: А х 4; Б, В, Д, Е х 400; Г, Ж х 200; З, И х 250.
реверсированной вены участки грануляционной ткани встречаются даже через 6 месяцев после операции, что может указывать на более интенсивную травму ГМК. В работе Owens C.D. и соавт. (2006) УЗИ венозных шунтов выявило увеличение жесткости стенки вены практически в два раза в течение 3 месяцев после операции [9], что объясняется увеличением волокон коллагена и реорганизацией эластического каркаса. Деструкция базальной и эластических мембран способствует миграции клеток крови в стенку вены, а также ГМК t. media и миофибробластов в субинтимальный слой, что проводит к неоинтимальной гиперплазии и утолщению стенки вены. Ригидный кровеносный сосуд теряет возможность реагировать на регуляторные сигналы. Было показано, что артериализованные вены утрачивают маркеры венозной специфичности без приобретения артериальных, что указывает на сложные клеточные и молекулярные взаимодействия, участвующие при артериализции стенки вены [10].
Таким образом, выявленные изменения структуры вены при артериализации носят дезадаптивный характер и обусловлены механическим (периоперационная травма), гемодинамическим (артериальная гемодинамика), клеточным и молекулярным повреждением всех слоев венозной стенки. Вместе с тем, нельзя не отметить, что подвергнутые исследованию образцы венозного шунта являются примером неблагоприятных исходов хирургического лечения, поэтому описанные изменения, развивающиеся в них наиболее глубокие и приведшие к окклюзии шунта. Однако, очевидно, что они в значительной степени отражают динамику клеточных и тканевых реакций, развивающихся при артериализации сосуда.
Заключение
Выявленные патоморфологические изменения дезадаптивного ремоделированния стенки артери-
ализованной вены имеют схожие изменения при аутовенозном шунтировании по методике «in situ» и реверсированной веной и включают: воспаление стенки, повреждение эндотелия с формированием мозаичного монослоя; пролиферацию эндотелиоцитов, направленную на реэндотелизацию просвета; повреждение гладкомышечных клеток t. media и замещение ее фиброзной тканью; утолщение стенки за счет комплекса тканей, входящий в t. intima et media, в результате неоинти-мальной фиброзной и гладкомышечной гиперплазии; ремоделирование соединительнотканного матрикса и фиброзную перестройку стенки вены. Детальное понимание клеточно-тканевых изменений в стенке сосуда при артериализации будет способствовать определению новых таргетов для влияния сопутствующей фармацевтической терапии, направленной на улучшение прогноза у оперированных больных.
Дополнительная информация
Источник финансирования . Исследование выполнено при финансовой поддержки гранта РФФИ №18-315-00129 и стипендии Президента РФ молодым ученым и аспирантам, осуществляющим перспективные научные исследования и разработки по приоритетным направлениям модернизации российской экономики № СП-2164.2018.4.
Согласие на публикацию . Исследование одобрено локальным этическим комитетом ФГБОУ ВО РязГМУ Минздрава России (протокол №3, от 04.10.2018). Все пациенты подписали информированное добровольное согласие на участие.
Авторы заявляют об отсутствии конфликта интересов (The authors declare no conflict of interest).
Список литературы Морфологическая трансформация стенки артериализованной вены
- Fowkes FGR, Aboyans V., Fowkes FJI, et al. Peripheral artery disease: Epidemiology and global perspectives. Nat Rev Cardiol. 2017; 14(3): 156-70.
- Desai U., Kharat A., Hess CN, et al. Incidence of Major Atherothrombotic Vascular Events among Patients with Peripheral Artery Disease after Revascularization. Ann Vasc Surg. 2021; 75: 217-26. 10.1016/j.avsg. 2021.02.025.
- Conte MS, Bradbury AW, Kolh P., et al. Global Vascular Guidelines on the Management of Chronic Limb-Threatening Ischemia. Eur J Vasc Endovasc Surg. 2019; 69(6): S1-S109.e33.
- Aboyans V., Ricco JB, Bartelink MLEL, et al. 2017 ESC Guidelines on the Diagnosis and Treatment of Peripheral Arterial Diseases, in collaboration with the European Society for Vascular Surgery (ESVS). Eur Heart J. 2018; 39(9): 763-816.
- Бокерия Л.А., Покровский А.В. Национальные рекомендации по диагностике и лечению заболеваний артерий нижних конечностей // Ангиология и сосудистая хирургия. - 2019. - Т.25. - №2. - С.1-110.
- Lu DY, Chen EY, Wong DJ, et al. Vein graft adaptation and fistula maturation in the arterial environment. J Surg Res. 2014; 188(1): 162-73.
- Owens CD, Gasper WJ, Rahman AS, Conte MS. Vein graft failure. J Vasc Surg. 2015; 61(1): 203-16.
- Ambler GK, Twine CP. Graft type for femoro-popliteal bypass surgery. Cochrane Database Syst Rev. 2018; 2: CD001487. 10.1002/14651858. CD001487.pub3.
- Owens CD, Wake N., Jacot JG, et al. Early biomechanical changes in lower extremity vein grafts-distinct temporal phases of remodeling and wall stiffness. J Vasc Surg. 2006; 44(4): 740-6.
- Isaji T., Hashimoto T., Yamamoto K., et al. Improving the Outcome of Vein Grafts: Should Vascular Surgeons Turn Veins into Arteries? Ann Vasc Dis. 2017; 10(1): 8-16.


