Морфологические и функциональные изменения в печени у больных с острой кишечной непроходимостью
Автор: Амаханов А.К., Федосеев А.В., Муравьев С.Ю., Бударев В.Н., Инютин А.С.
Журнал: Московский хирургический журнал @mossj
Рубрика: Клинические исследования
Статья в выпуске: 2 (42), 2015 года.
Бесплатный доступ
Острая кишечная непроходимость сопровождается изменениями в морфологии и функциональной активности печени. Изменения эти в значительной степени определяют развитие синдрома энтеральной недостаточности, сопутствующего непроходимости. По этой причине для снижения риска развития полиорганной недостаточности при острой кишечной непроходимости необходимо корректировать компенсаторные возможности печени.
Острая кишечная непроходимость, синдром энтеральной недостаточности, функциональное состояние печени
Короткий адрес: https://sciup.org/142211211
IDR: 142211211 | УДК: 616.381-002-089.168.1-06-089.85
Текст научной статьи Морфологические и функциональные изменения в печени у больных с острой кишечной непроходимостью
Актуальность исследования
Актуальность исследований, связанных с острой кишечной непроходимостью, не вызывает сомнений [1]. Она обусловлена высокой распространенностью данного заболевания и не всегда благоприятными исходами его лечения [11]. Современный уровень развития медицины таков, что любой позитивный сдвиг в улучшении лечебного процесса может быть достигнут лишь при глубоком понимании всех тонких патологических процессов, сопровождающих ту или иную патологию [6]. Не является исключением и острая кишечная непроходимость [2].
В своем исследовании мы решили подробно изучить изменения в морфологии и функциональном состоянии печени у рассматриваемой группы больных. Эндогенная интоксикация у больных с острой кишечной непроходимостью влечет за собой активацию фильтрационных ме- ханизмов печени и почек [7, 8]. Поэтому компенсаторные возможности этих органов являются основополагающим для послеоперационной выживаемости и реабилитации больных в ургентной хирургии [4, 9]. При этом существующая взаимосвязь патологических процессов, происходящих в печени и почках, позволила авторам объединить их в так называемый гепаторенальный синдром [5]. Но поскольку с одной стороны именно ретикулоэндотелиальная система печени участвует в сдерживании бактериальной агрессии, а с другой – синтезирующая функция печени поддерживает гомеостаз организма, то и главенствующая роль в развитие гепаторенального синдрома отводится именно печени [3, 10].
Цель исследования. Изучить характер и направленность изменений в морфологии и функциональном состоянии печени у больных с острой кишечной непроходимостью.

Материалы и методы
Предметом исследования стало наблюдение 129 пациентов с механической острой кишечной непроходимостью, сопровождающейся СЭН, проходивших лечение в больнице скорой медицинской помощи города Рязани в период с 2012 по 2014 год. Среди пациентов, включенных в исследование, был 61 мужчина и 68 женщин. 50 пациентов (38,8%) имели возраст моложе 60 лет, 4 пациента (3,1%) – старше 85 лет, а основная масса (75 человек, 58,1%) – возраст 61– 85 лет. Среди причин, вызвавших кишечную непроходимость, преобладали обтурация опухолью толстой кишки (45,7% случаев) и спаечная болезнь (22,5% случаев). На все остальные причины вместе взятые (опухоль, заворот, инвагинация, обтурация безоаром тонкой кишки, непроходимость в грыжевом мешке) пришлось 31,8% случаев наблюдения. В нашем исследовании использовалась схема оценки тяжести СЭН, предложенная профессором Завада Н.В. с соавторами. Согласно ей, I степень СЭН встречалась у 40 (31%) пациентов, II степень – у 57 (44,2%), III степень – у 32 (24,8%) пациентов.
Специфика исследования потребовала применения ряда специфических диагностических методик.
У 43 пациентов, отобранных методом случайной выборки, интраоперационно бралась пункционная биопсия печеночной ткани. Срезы ткани окрашивали гематоксилин-эозином.
При анализе выраженности некрозовоспалительных изменений в печени использовали индекс гистологической активности (ИГА), который оценивался в соответствии с классификационной системой METAVIR.
Для определения функциональных возможностей печени при синдроме энтеральной недостаточности (СЭН) использовалась шкала MELD.
Также производился парамецийный тест крови, забранной из локтевой и брыжеечной вены.
Результаты и их обсуждение
По данным гистологического исследования, в соответствии с оценочной шкалой METAVIR, легкое лобулярное воспаление с отсутствием некрозов (А0) было зарегистрировано в 16 (36,4%) случаях. Однако в 63,6% наблюдениях отмечалось более выраженное повреждение паренхимы печени. Из них умеренное лобулярное воспаление без или в сочетании с единичными ступенчатыми некрозами (А1) отмечалось в 15 (34,1%) случаях. В четверти случаев, то есть у 11 человек, наблюдалось лобулярное воспаление различной выраженности, включая ступенчатые некрозы, достигающие умеренной интенсивности (А2). Примечательно, что выраженное воспаление в сочетании с обширными ступенчатыми некрозами (А3) отмечено только в 2 (4,5%) случаях биоптата печени.
При сопоставлении морфологических изменений в печени с тяжестью СЭН мы получили следующее распределение (табл. 1).
Наблюдающееся увеличение некрозовоспалительного повреждения печеночной морфологии при прогрессировании СЭН получило статистическое подтверждение в виде сильной корреляционной связи (r=0,826, p<0,05).
Функциональные резервы печени исследовались опосредованно, путем сравнения показателей крови, забранной из локтевой и брыжеечной вены, с полученным индексом гистологической активности METAVIR.
Полученные данные свидетельствовали о том, что при отсутствии выраженных морфологических нарушений в печени, соответствующих ИГА степени А0, токсичная кровь, с уровнем парамецийного теста, равного 15,7±1,204 минуты, полностью обезвреживалась в гепаторенальной зоне. Поскольку у этих пациентов в кубитальной фракции значения парамецийного теста в среднем были в норме, и составляли 18,3±0,372 минуты. В то же время при легком воспалении с элементами невыраженной деструкции, соответствующих ИГА степени А1, в обеих фракциях отмечался токсический сдвиг парамецийного теста, который был более выражен в портальном кровотоке, нежели в системном (tСт=-2,139, p<0,05).
У пациентов с выраженным лобулярным воспалением, сопровождающимся очаговыми некрозами (А2), выявлена достоверная идентичность по токсичности крови как в брыжеечном кровотоке (9,4±1,173 минуты), так в системном (10,9±1,364 минуты). Аналогичный результат зарегистрирован и при более обширных некрозах гепатоцитов (А3) на фоне выраженного гепатита.
При статистической обработке полученных данных нами установлена корреляционная связь между увеличением токсичности крови в портальном кровотоке и увеличением деструктивных изменений в морфологии печени (r=0,554, p<0,05). Одновременно с этим выявлена корреляционная зависимость прогрессирования эндогенной интоксикации на фоне усугубления патологических процессов в печеночной паренхиме (r=0,699, p<0,05).
При изучении распространенности гепаторенального синдрома как составной части полиорганной недостаточности мы выявили, что его тяжесть по шкале MELD менее
Таблица 1
Распределение больных по выраженности ИГА с учетом тяжести СЭН
|
Степень СЭН |
ИГА по шкале METAVIR, Абс., (%) |
Корреляция |
|||
|
A0 (n=16) |
A1 (n=15) |
A2 (n=11) |
A3 (n=2) |
||
|
I (n=14) |
14 (100) |
0 |
0 |
0 |
r=0,826 p<0,05 |
|
II (n=19) |
2 (11,8) |
11 (64,7) |
6 (35,3) |
0 |
|
|
III (n=11) |
0 |
4 (36,4) |
5 (45,5) |
2 (18,2) |
|
10 баллов встречалась в 21 (61,8%) случае, 10–19 баллов – в
9 (26,5%) случаях, 20 и более – в 4 (11,7%) (рис. 1).
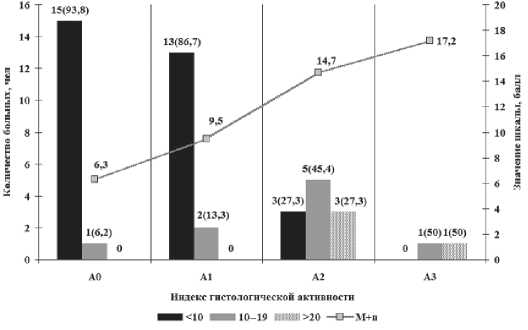
Рис. 1. Изменения показателей шкалы MELD в зависимости от выраженности печеночной деструкции
При легкой степени воспалительных изменений и без некротических очагов в печени (А0) из 16 случаев в 15 (93,8%) у больных имелось менее 10 баллов, и лишь в одном (6,2%) – 12 баллов. При этом среднее значение шкалы MELD при данном состоянии печени составило 6,3±1,217 балла.
При выявлении легкого или тяжелого лобулярного воспаления с единичными некрозами (А1) распределение больных в соответствии с показаниями шкалы MELD менялось незначительно (рис. 1). Так, например, в диапазоне 10 баллов находилось 13 (86,7%) пациентов, а увеличение до 10– 14 баллов имели только двое (13,3%) из них, при этом средний уровень шкалы по подгруппе составил 9,5±2,811 балла. Таким образом, при легком или умеренном воспалительном процессе в печени с незначительным количеством очагов некроза показатели шкалы MELD находятся в благоприятном для исхода диапазоне.
Одновременно с этим при развитии умеренного или выраженного воспаления с увеличением зоны некроза в паренхиме печени (А2) количество больных с уровнем шкалы менее 10 баллов резко снижается (рис. 1). Так, в результате анализа данных у этой подгруппы пациентов менее 10 баллов по шкале MELD имели три (27,3%) человека, попадали в диапазон от 10 до 14 баллов – пятеро (45,4%) пациентов. Вместе с тем неблагоприятный прогноз исхода заболевания, то есть при значении шкалы MELD более 20 баллов, имели трое (27,3%) больных. Однако в среднем по выборке уровень шкалы MELD имел 14,7±1,259 балла, что соответствует относительно благоприятному исходу.
При выраженном воспалительно-деструктивном процессе в печени показатели шкалы MELD менее 10 баллов не регистрировались. При этом у одного пациента было 15 баллов, у другого – 21 балл, а в среднем по подгруппе получилось – 17,2±2,337.
При анализе зависимости прогрессирования гепаторенального синдрома от тяжести деструктивных изменений в печени нами выявлено, что она существует, причем является корреляционной (r=0,704, p<0,05).
Выводы
-
1. Между увеличением выраженности некрозовоспалительных изменений печеночной морфологии и прогрессированием СЭН имеется статистически достоверная прямая сильная корреляционная связь (r=0,826, p<0,05).
-
2. Между увеличением токсичности крови в портальном кровотоке и увеличением деструктивных изменений в морфологии печени имеется корреляционная связь (r=0,554, p<0,05).
-
3. Имеется корреляционная зависимость прогрессирования эндогенной интоксикации и усугубления патологических процессов в печеночной паренхиме (r=0,699, p<0,05).
-
4. Имеется корреляционная связь (r=0,704, p<0,05) между прогрессированием гепаторенального синдрома и тяжестью деструктивных изменений в печени.
-
5. Для снижения риска развития полиорганной недостаточности при острой кишечной непроходимости необходимо корректировать компенсаторные возможности печени на фоне СЭН.
Список литературы Морфологические и функциональные изменения в печени у больных с острой кишечной непроходимостью
- Беляев Л.Б., Юдин Е.В., Скоробогатов В.М. Острая кишечная непроходимость как проблема неотложной хирургии //Неотложная медицинская помощь (состояние, проблемы, перспективы развития): тез. докл. науч.-практ. конф. М., 1998. С. 3738.
- Гостищев В.К. и др. Бактериальная транслокация в условиях острой непроходимости кишечника //Вестн. РАМН. 2006. № 9-10. С. 34-38.
- Борзунов М.А., Милюков В.Е. Анатомо-экспериментальное исследование морфофункциональных изменений печени при острой кишечной непроходимости и после ее устранения//Современные технологии диагностики и лечения, раненых и больных в поликлинике и стационаре: тез. докл. 2-й науч.-практ. конф. 574-го Воен. клинич. госпиталя (20 мая 1999 г.). М., 1999. С. 118-119.
- Гельфанд БЛ*., Матвеев Д.В., Сергеева Н.А. Роль портальной бактериемии и эпдотоксинемии в патогенезе полиорганной недостаточности при перитоните//Вестн. хирургии им. И.И. Грекова. 1992. Т. 148, № 1. С. 21-27.
- Дибиров М.Д. и др. Диагностика, профилактика и лечение гепаторенального синдрома при острой Хирургической патологии органов брюшной полости//Хирург. 2010. №5. C. 11-17.
- Федосеев А.В. и др. К вопросу диагностики ранних признаков полиорганной дисфункции у больных с синдромом энтеральной недостаточности//Вестн. эксперим. и клинич. хирургии. 2012. Т. 5, № 1. С. 60-64.
- Мишнев О.Д., Щеголев А.И., Лысова Н.Л. Печень и почки при эндотоксикозе. М., 2003. 210 с.
- Bounous G. The intestinal factor in MOF and shock//Surgery. 1990. Vol. 107, № 1. P. 118-119.
- Brearly S. et al. Endotoxin levels in portal and systemic blood//Dig. Surg. 1985. Vol. 2. P. 70-72.
- Bahrami S. et al. Involvement of bacteria endotoxin translocation in the development of multiple organ failure//Wien. Klin. Wschr. 1998. Suppl. 1. P. 2-10.
- Duron J.J. et al. Prevalence and risk factors of mortality and morbidity after operation for adhesive postoperative small bowel obstruction//Am J Surg. 2008. Vol. 195. P. 726-734.


