Морфологические и молекулярно-генетические предикторы рецидива лейомиомы матки у женщин репродуктивного возраста после органосохраняющего лечения
Автор: Карамян Р.А., Ордиянц И.М., Демура Д.А., Крот М.А., Рыженков К.В., Мамыкин А.И.
Журнал: Ульяновский медико-биологический журнал @medbio-ulsu
Рубрика: Клиническая медицина
Статья в выпуске: 1, 2026 года.
Бесплатный доступ
Лейомиома матки (ЛМ) характеризуется высокой частотой рецидивирования после органосохраняющих операций (до 70–80 % через 8 лет). Существующие прогностические модели немногочисленны и имеют ограничения. Цель. Выявить морфологические и молекулярно-генетические факторы, предопределяющие развитие рецидивов ЛМ у пациенток репродуктивного возраста. Материалы и методы. Обследовано 75 женщин, оперированных по поводу ЛМ: 52 без рецидива и 23 с рецидивом. Рецидивом считалось возникновение ЛМ у женщин, которые уже перенесли миомэктомию на момент включения в исследование, либо обнаружение миоматозных узлов на контрольном осмотре через 1 год после произведенной миомэктомии. С целью определения предикторов рецидивирования ЛМ участки удаленного миометрия и миоматозные узлы после операции были направлены на морфологическое, иммуногистохимическое (VEGF, TGF-β) и молекулярно-генетическое (микроРНК: Let 7, miR-92a, miR-146b) исследование. Для создания базы данных и математической обработки был применен пакет модулей IBM SPSS STATISTICS v.26.0 for Windows (IBM Corporation, Somers, USA), Jamovi version 1.2.27, StatTech v.1.2.0 (номер регистрации 2020615715). Результаты. Установлены ключевые предикторы рецидива ЛМ: макроскопические – размер матки 10–15 нед., диаметр узла 60–80 мм, быстрый рост новообразования; микроскопические – снижение гиалиноза, увеличение фибриноидного некроза, наличие зон роста; иммуногистохимические – гиперэкспрессия VEGF и TGF-β; молекулярные – дисбаланс микроРНК (повышение Let-7 и miR-92a, снижение miR-146b). Разработана математическая модель прогнозирования риска рецидива с высокой точностью (AUC=0,99, чувствительность 95,5 %, специфичность 97,6 %).
Лейомиома матки, молекулярно-генетические предикторы рецидивирования
Короткий адрес: https://sciup.org/14134856
IDR: 14134856 | УДК: 618.3: 618.14-006.36-089 | DOI: 10.34014/2227-1848-2026-1-88-97
Morphological and molecular genetic predictors of uterine leiomyoma recurrence in women of reproductive age after organ-preserving treatment
Uterine leiomyoma (ULM) is characterized by a high recurrence rate after organ-preserving surgery (up to 70–80 % after 8 years). Existing prognostic models are limited in number and have certain constraints. Objective. The aim of the study is to identify morphological and molecular genetic factors that predetermine the development of ULM recurrences in patients of reproductive age. Materials and Methods. The study involved 75 women who underwent myomectomy: 52 without recurrence and 23 with recurrence. Recurrence was defined as the occurrence of myomectomy in women who had already undergone myomectomy at the time of enrollment, or the detection of myomatous nodes during a follow-up examination 1 year after myomectomy. To identify predictors of myomectomy recurrence, samples of the excised myometrium and myomatous nodes were subjected to morphological, immunohistochemical (VEGF, TGF-β), and molecular genetic (microRNA: Let 7, miR-92a, miR-146b) analysis. Data management and statistical processing were performed using the IBM SPSS STATISTICS v.26.0 for Windows (IBM Corporation, Somers, USA), Jamovi version 1.2.27, and StatTech v.1.2.0 (registration number 20206157150. Results. Key predictors of ULM recurrence were identified: macroscopic – uterine size 10–15 weeks, node diameter 60–80 mm, and rapid tumor growth; microscopic – decreased hyalinosis, increased fibrinoid necrosis, development of growth zones; immunohistochemical – hyperexpression of VEGF and TGF-β; molecular – microRNA imbalance (increased Let-7 and miR-92a, decreased miR-146b). A high-accuracy mathematical model for predicting recurrence risks was developed (AUC=0.99, sensitivity 95.5 %, specificity 97.6 %).
Текст научной статьи Морфологические и молекулярно-генетические предикторы рецидива лейомиомы матки у женщин репродуктивного возраста после органосохраняющего лечения
Введение. Лейомиома матки (ЛМ) является заболеванием, склонным к прогрессированию, росту и рецидивированию. Так, по данным M.P. Radosa et al., после лапароскопической миомэктомии риск рецидива составляет 4,9 % через 24 мес. и 21,4 % через 60 мес. после операции. Возраст женщины 30–40 лет и наличие более чем одного узла ЛМ на мо- мент первичной лапароскопической миомэктомии были определены как факторы, значительно повышающие риск симптоматического рецидива ЛМ (31,25 % и 38,71 % соответственно, p<0,01) [1]. Y. Kotani et al. показали, что кумулятивная частота рецидивов ЛМ через 8 лет после миомэктомии составляет 70– 80 % [2]. Согласно наблюдениям Verena M.C.
Reichert et al. случайное удаление лейомиосаркомы матки влияет на выживаемость без рецидивов, но не оказывает негативного влияния на общую выживаемость [3].
С учетом высокой распространенности ЛМ у женщин репродуктивного возраста и мультифакторности заболевания прогнозирование риска рецидива опухоли в настоящее время является одной из ключевых задач, решение которой смогло бы улучшить не только качество жизни пациенток, но и снизить риск развития осложнений беременности после миомэктомии. Однако в настоящее время подобные прогностические модели представлены лишь в единичных публикациях.
Патентный поиск за последние 7 лет показал, что в отечественной литературе способ прогнозирования рецидива ЛМ представлен лишь в работе М.Г. Николаевой с соавт. [4]. Безусловно, он вызывает заслуженный практический интерес, однако применим лишь в случае использования в качестве метода лечения эмболизации маточных артерий.
Имеющаяся зарубежная прогностическая модель (X. Ming et al.) включает в расчет такой клинический показатель, как наличие эндометриоза. Это либо сужает область применения модели (только для сочетанной патологии), либо требует уточнения, насколько универсальным является этот фактор для всех случаев рецидива ЛМ [5].
Фундаментальные механизмы развития заболевания остаются не до конца ясными и дискуссионными (контраверсионными), что затрудняет поиск мишеней для терапии. Роль микроРНК в механизмах рецидивирования ЛМ изучена недостаточно, хотя их идентификация открывает перспективы для разработки новых методов лечения и профилактики повторного роста узлов. Это особенно актуально для тех пациентов репродуктивного возраста, хирургическое лечение которых может являться малоэффективным. Целенаправленная терапия также может предотвратить рецидивирование миомы матки, а следовательно, повторное хирургическое вмешательство.
Таким образом, радикальное лечение ЛМ (гистерэктомия) неприемлемо для женщин, планирующих беременность, а другие методы не всегда эффективны и не предотвращают рецидивы.
Цель исследования. Установить морфологические и молекулярно-генетические детерминанты рецидивирующей лейомиомы матки у женщин репродуктивного возраста.
Материалы и методы. Обследовано 75 женщин, оперированных по поводу ЛМ: 52 без рецидива и 23 с рецидивом. Рецидивом считалось возникновение ЛМ у женщин, которые уже перенесли миомэктомию на момент включения в исследование, либо обнаружение миоматозных узлов на контрольном осмотре через 1 год после произведенной миомэктомии.
С целью определения предикторов реци-дивирования ЛМ участки удаленного миометрия и миоматозные узлы после операции были направлены на морфологическое, иммуногистохимическое (VEGF, TGF-β) и молекулярно-генетическое (микроРНК: Let 7, miR-92a, miR-146b) исследование.
Материал для гистологической и иммуногистохимической оценки фиксировался в 10 % забуференном формалине. Фиксация и гистологическая проводка выполнялись по стандартным протоколам. Затем материал заливался в парафин, из полученных парафиновых блоков изготавливались серийные срезы толщиной 4–5 мкм. Для гистологического исследования срезы были окрашены гематоксилином и эозином.
Измерение уровней экспрессии микроРНК (Let 7, miR-92a, miR-146b) методом ПЦР в реальном времени проводили на ам-плификаторе CFX96 (Bio-Rad Laboratories, США). Данный этап был выполнен в ФГБУН Институт молекулярной и клеточной биологии Сибирского отделения РАН в лаборатории молекулярной генетики отдела структуры и функции хромосом (заведующий лабораторией – доктор биологических наук А.В. Вершинин).
Для создания базы данных и математической обработки был применен пакет модулей IBM SPSS STATISTICS v.26.0 for Windows (IBM Corporation, Somers, USA), Jamovi version 1.2.27, StatTech v.1.2.0 (номер регистрации 2020615715).
Результаты. Результаты морфологических и молекулярно-генетических исследований позволили установить возможные предикторы рецидивирующей ЛМ. Ключевыми макроскопическими факторами являются увеличение размеров матки до 10–15 нед. (73,9 % пациенток с рецидивом против 46,2 % больных с первичной ЛМ, р=0,052), диаметр наибольшего миоматозного узла 60–80 мм (у 65,2 % против 36,5 % женщин соответственно, р=0,051), быстрый рост новообразования – до 6 мес. (17,4 % больных против 9,6 % соответственно, р=0,051).
Микроскопическими предикторами можно считать снижение гиалиноза (34,8 % пациенток с рецидивом против 65,4 % без такового, р=0,044), уменьшение отека стромы (13,0 % женщин против 25,0 % соответственно, р=0,024), увеличение фибриноидного некроза в 2 раза (30,4 % больных против 15,4 % соответственно, р=0,027), частые зоны роста (69,6 % пациенток против 57,7 % соответственно, р=0,033). Выявлена прямая корреляционная зависимость между количеством узлов и гиалинозом (r=0,452, p=0,001).
Среди иммуногистохимических предикторов рецидива ЛМ необходимо указать ангиогенные факторы: увеличение концентрации VEGF (88,5 % женщин с рецидивом против 39,1 % с первичной ЛМ) в рецидивирующих узлах и гиперэкспрессия TGF-β (57,1 % против 24,0 % женщин соответственно), способствующая стимуляции фиброза. То есть рост ЛМ после миомэктомии связан с высокой экспрессией факторов роста (TGF-β, VEGF), что приводит не столько к пролиферации ЛМ, сколько к ее гипертрофии.
Таким образом, источниками рецидива ЛМ являются периваскулярные «зачатки» ЛМ в миометрии, микроскопические остаточные узлы и рубцовые изменения после миомэктомии, а критериями агрессивного течения – быстрый рост и множественные узлы (6 тип по FIGO), преобладание фибриноидного некроза над гиалинозом, а также высокая плотность зон роста.
Дисбаланс микроРНК (увеличение экспрессии Let-7 (2,73 против 1,85 отн. ед.), miR-92a
(1,63 против 1,45 отн. ед.) и снижение экспрессии miR-146b (0,59 против 0,73 отн. ед.)) играет ключевую роль в патогенезе рецидивирования ЛМ после органосохраняющих операций.
Таким образом, рецидивирующие лейомиомы – это не случайные новые узлы, а проявление системной биологической предрасположенности миометрия к опухолевой трансформации. Основными факторами, оказывающими влияние на рецидив лейомиомы матки в репродуктивном возрасте после органосохраняющего лечения, являются генетическая предрасположенность и остаточные клетки после миомэктомии. Патогенез рецидива ЛМ после миомэктомии представляет собой последовательный каскад нарушений, начинающийся на молекулярном уровне и завершающийся клиническими проявлениями на органном уровне.
С учетом выбора тактики хирургического лечения пациенток с впервые выявленной ЛМ, а также прогноза риска развития рецидива и вероятности успеха его преодоления была разработана и обоснована персонифицированная модель морфологических и молекулярно-генетических предикторов ре-цидивирования лейомимы матки в репродуктивном возрасте. В прогностическую модель включены возможные морфологические, молекулярно-генетические детерминанты рецидива ЛМ.
P=1/(1+e-Z)×100 %.
Z=-15,4+5,13×X микроРНК-let7 –4,8×X микроРНК-92а –
33,2×X микроРНК-146b +14,8×X VEGF в узле +5,6×
XTGF-β в узле+3,2×X гиалиноз–4,8×Xразмеры матки +1,4×Xразмер миоматозного узла+4,3×Xскорость роста узла, где: P – вероятность рецидива ЛМ (%), e – число Эйлера – математическая константа (≈2,718), z – score – линейный предиктор всех факторов риска, Xразм. матки – размер матки (нед.); Xразм. миом. узла – размер миоматозного узла (мм); Xск.рост.узла – скорость роста узла (на 2 см за 12 мес.), Хгиалиноз –замещенная ткань (%), XTGF-β – TGF–β (% позитивных клеток H-score, 0–300), XVEGF – VEGF (% позитивных клеток H-score, 0–300), XмикроРНК-146b – экспрессия микроРНК-146b в миоматозном узле (отн. ед.), XмикроРНК-let7 – экспрессия мик-роРНК-Let7 в миоматозном узле (отн. ед.), XмикроРНК-92а – экспрессия микроРНК-92а в ми-оматозном узле (отн. ед.).
ROC-кривая прогнозирования риска рецидива ЛМ, построенная на основе морфологических и молекулярно-генетических предикторов, представлена на рис. 1.
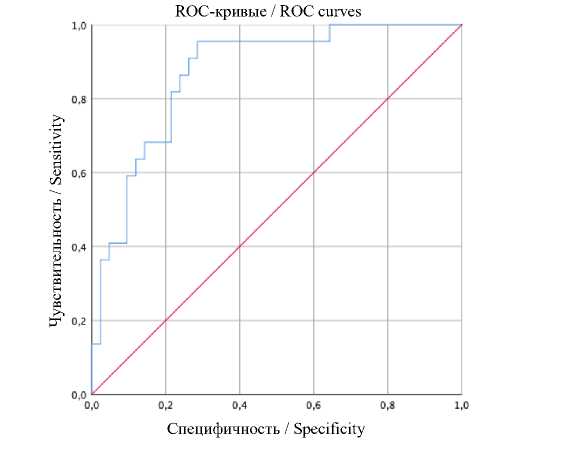
Рис. 1. ROC-кривая прогнозирования риска рецидива ЛМ, построенная на основе морфологических и молекулярно-генетических предикторов
Fig. 1. ROC curve for predicting the risk of LM recurrence based on morphological and molecular genetic predictors
Площадь под ROC-кривой, соответствующая взаимосвязи прогноза рецидива ЛМ и значения логистической регрессионной функции, равнялась 0,99±0,011 (95 % ДИ 0,97–1,0). Пороговое значение функции P в точке cut-off составляло 0,4. Значения, равные или превышающие указанное, соответствовали высокому риску рецидива ЛМ. Чувствительность модели составила 95,5 %, специфичность – 97,6 %.
Обсуждение. Проблема рецидивирования лейомиомы матки после органосохраняющих операций остается одной из наиболее дискуссионной в гинекологии [6]. Наше исследование было направлено на поиск морфологических и молекулярно-генетических предикторов рецидива, что позволило не только выявить группу риска, но и обосновать патогенетические механизмы повторного роста опухоли. Полученные результаты демонстрируют высокую прогностическую значимость разработанной модели, что требует их сопоставления с актуальными научными данными [7–9].
Нами было подтверждено, что агрессивный фенотип ЛМ, склонной к рецидиву, характеризуется определенными макроскопическими чертами: тенденцией к увеличению размеров матки и диаметра доминантного узла, а также быстрым ростом. Эти наблюдения согласуются с выводами крупного ретроспективного исследования [10], в котором диаметр и множественность узлов включены в финальную номограмму для прогнозирования рецидива. Авторы также подчеркивают важную роль семейного анамнеза и наличия резидуальных узлов, что коррелирует с нашей концепцией о роли микроскопических остаточных «зачатков» в миометрии. Однако если в работе Emmanuel N Kontomanolis et al. подслизистая локализация узла рассматривалась как протек-тивный фактор [11], то в нашем исследовании акцент сделан на интерстициальные и субсерозные узлы (включая FIGO 6 тип), что указывает на различную этиологию рецидивов в зависимости от исходного типа роста опухоли.
Гистологическое исследование позволило выявить ключевые микроскопические маркеры неблагоприятного прогноза. Снижение гиалиноза и отека стромы на фоне двукратного увеличения частоты фибриноидного некроза и зон роста указывает на преобладание процессов пролиферации над инволютивными изменениями. Эти данные расширяют классические представления о патоморфозе ЛМ, предлагая рассматривать соотношение некроза и гиалиноза в качестве диагностический критерия агрессивности.
Центральным звеном предложенного нами патогенеза рецидива является дисбаланс факторов роста (гиперэкспрессия VEGF и TGF-β), ведущий не столько к гиперплазии, сколько к гипертрофии гладкомышечных клеток и фиброзу. Так, в обзоре М.И. Ярмолинской и соавт., посвященном опухолям матки, особое внимание уделено сигнальным путям, участвующим в регуляции основных клеточных процессов, возникновении и прогрессировании заболевания. Отмечено, что значимую роль в развитии миомы матки играет активация таких сигнальных путей, как Wnt/β-катенин, MAPK/ERK, TGF-β/SMAD [12].
Наше исследование вносит существенный вклад в понимание роли микроРНК при ЛМ. Выявленный нами дисбаланс (повышение экспрессии Let-7, miR-92a и снижение miR-146b) является одним из первых описаний специфического рецидивассоциированного профиля микроРНК для доброкачественной патологии. Эти данные перекликаются с выводами Ni et al., которые показали, что повышение уровня онкогенной miR-499a-5p в клетках ЛМ активирует Wnt/β-катениновый сигнальный путь, способствуя пролиферации и миграции клеток. Важно подчеркнуть, что если в злокачественных опухолях (uLMS) наблюдается супрессия семейств miR-29 и miR-200, то паттерн рецидивирующих лейомиом иной, что подтверждает их доброкачественную, но биологически активную природу [13–15].
Разработанная нами прогностическая модель объединяет все выявленные разноуровневые предикторы. Высокие показатели чувствительности (95,5 %) и специфичности (97,6 %) отличают наш подход от существующих аналогов.
Так, имеющиеся модели [16, 17] базируются преимущественно на клинических и ультразвуковых данных, тогда как наша модель включает молекулярно-генетические маркеры (микроРНК, факторы роста), что позволяет точнее оценить биологический потенциал ткани.
Таким образом, концепция, согласно которой рецидивирующие лейомиомы являются проявлением системной предрасположенности миометрия к опухолевой трансформации, активируемой хирургическим вмешательством, находит подтверждение в свете новейших данных о роли микроРНК и ангиогенных факторов [18–20]. Внедрение данной прогностической модели в клиническую практику позволит перейти к действительно персонализированному ведению пациенток репродуктивного возраста с ЛМ.
Заключение. Патогенетические механизмы рецидивов лейомиомы матки в репродуктивном возрасте после органосохраняющего лечения представляют собой сложный многоуровневый комплекс процессов, обуславливающих предрасположенность миометрия к опухолевой трансформации: на молекулярном уровне отмечается дисбаланс микроРНК (повышение экспрессии Let-7, miR-92a и снижение miR-146b), который, подавляя апоптоз, создает среду для неконтролируемого роста остаточных клеток после миомэктомии; на клеточном – гиперактивация ключевых факторов роста (TGF-β и VEGF); на тканевом – ги-алиноз, отек, несоответствие темпов роста и васкуляризации, фибриноидный некроз, что на органном уровне объясняет формирование крупных, быстрорастущих, множественных узлов, значительное увеличение матки, т.е. клинические проявления рецидивов.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Вклад авторов
Концепция и дизайн исследования: Карамян Р.А., Ордиянц И.М., Демура Т.А.
Литературный поиск, участие в исследовании, обработка материала: Карамян Р.А.,
Крот М.А., Рыженков К.В.
Статистическая обработка данных: Карамян Р.А., Мамыкин А.И.
Анализ и интерпретация данных: Ордиянц И.М., Демура Т.А., Мамыкин А.И.
Написание и редактирование текста: Карамян Р.А., Демура Т.А., Ордиянц И.М.


