Морфологические изменения миентеральных ганглиев при экспериментальном остром язвенном колите
Автор: Хочанский Дмитрий Николаевич, Макарова Ольга Васильевна, Худоерков Рудольф Михайлович
Журнал: Морфологические ведомости @morpholetter
Рубрика: Оригинальные исследования
Статья в выпуске: 2 т.23, 2015 года.
Бесплатный доступ
Проведено морфологическое исследование энтеральной нервной системы ободочной кишки у мышей линии C57Bl/6 при экспериментальном декстраниндуцированном остром язвенном колите. Изучены клеточный состав миентеральных ганглиев и цитометрические показатели миентеральных нейронов. При колите по сравнению с контролем выявлено снижение числа гипохромных нейронов и глиоцитов, увеличение числа гиперхромных нейронов на ганглий, уменьшение размеров нейронов и их ядер. Выявленные морфологические изменения миентеральных ганглиев ободочной кишки при остром язвенном колите могут обусловливать нарушения моторной и секреторной функции.
Энтеральная нервная система, морфология, колит, нейроны, глия
Короткий адрес: https://sciup.org/143177052
IDR: 143177052
Morhological changes of myenteric ganglia in experimental acute ulcerative colitis
Myenteric ganglia of colon of C57Bl/6 mice with acute DSS-induced colitis were investigated. The cell composition of myenteric ganglia and cytometric values of myenteric neurons were studied. It was found a decrease in number of hypochromic neurons and glial cells and an increase in number of hyperchromic neurons. The area of neurons and their nuclei decreased in colitis. These morphological changes of myenteric ganglia in colitis may cause an impairing of motor and secretory functions of colon.
Текст научной статьи Морфологические изменения миентеральных ганглиев при экспериментальном остром язвенном колите
Введение. По данным клинических исследований в последние годы отмечается увеличение распространенности воспалительных заболева- ний кишечника, таких как болезнь Крона и язвенный колит [1, 2]. В патогенезе этих заболеваний важную роль наряду с иммунной играет энтеральная нервная система (ЭНС) - собственная нервная система желудочно-кишечного тракта, состоящая из двух нервных сплетений - субмукозного и миен-терального, которые содержат нервные ганглии, в их составе различают нейроны и глиальные клетки [3, 4]. ЭНС регулирует функциональное состояние кишечника, его моторную и секреторную функции [5]. Структурные и функциональные нарушения ЭНС играют важную роль в развитии клинических проявлений воспалительных заболеваний кишечника. Однако, литературные данные, посвященные изменениям ЭНС при колитах, особенно у человека, фрагментарны [3, 6]. Авторы, исследовавшие ЭНС у пациентов с воспалительными заболеваниями кишечника и у животных с экспериментальным колитом, чаще всего отмечают уменьшение числа нейронов в миентеральном и субмукозном сплетениях [7]. У больных язвенным колитом выявляется гиперплазия и гипертрофия энтеральных нейронов [3, 6].
Цель исследования - изучить морфологические изменения нейронов и глиоцитов миен-теральных ганглиев ободочной кишки при остром язвенном колите, индуцированном декстрансульфатом натрия у самцов мышей C57Bl/6.
Материалы и методы исследования. Работа выполнена на 10 половозрелых мышах самцах С57Bl/6, массой тела 20-28 г. Животных содержали в клетках при естественном освещении, температуре +20-22 ˚С., со свободным доступом к воде и пище. При работе с экспериментальными животными руководствовались приказом Минздрава СССР № 755 от 12.08.1977. На проведение эксперимента получено разрешение биоэтической комиссии ФГБНУ «НИИ морфологии человека». Для индуцирования острого колита (n=5) питьевую воду в поилках на 5 дней заменяли 2,5% раствором декстрансульфата натрия (40 kDa, ApliChem). Контрольная группа мышей (n=5) получала питьевую воду. В течение эксперимента ежедневно проводили оценку общего состояния животных и проявлений колита, которые характе- ризовались загрязнением фекалиями анальной области, иногда с примесью крови. На 7-ые сутки животных опытной и контрольной групп выводили из эксперимента передозировкой диэтилового эфира. Ободочную кишку извлекали из брюшной полости, отмывали от содержимого фосфатносолевыми буфером комнатной температуры и разделяли на проксимальный, медиальный и дистальный отделы, которые фиксировали в жидкости Буэна и заливали в парафиновые блоки. Изготавливали продольно ориентированные гистологические срезы толщиной 10 мкм, затем окрашивали их гематоксилином и эозином и по методу Ниссля крезиловым фиолетовым.
Для морфометрии и фотосьемки использовали микроскоп Leica DM2500 (обьективы x10, x40, x100), оснащенный цифровой фотокамерой Leica DFC 295 с матрицей с разрешающей способностью 3,2 Мп. Использовали программное обеспечение ImageJ и графический планшет Wacom. Подсчет клеток в миентеральных ганглиях проводили визуально при увеличении 640 под микроскопом по глубине препарата. При оценке клеточного состава в 40 миентеральных ганглиях на каждом препарате подсчитывали нейроны центрального сечения с нормо-, гипо- и гиперхромным тигроидом, с ядром без ядрышка, гиперхромные пикнотические, нейроны с отчетливо визуализируемым тигроидом, но без ядра и глиальные клетки (рис. 1). Нейронами центрального сечения считали те нейроны, в которых определялось ядро с четкой границей и ядрышко (8). Глиальные клетки характеризовались относительно небольшим размером ядра с более плотным хроматином и от- сутствием тигроида. Определяли площадь 15 нейронов центрального сечения и их ядер в каждом препарате. Результаты морфометрии трех отделов ободочной кишки суммировались. Проводили статистическую обработку полученных данных в программах Statistica 8.0, AtteStat. Достоверность различий между показателями устанавливали с использованием непараметрического критерия Манна-Уитни. Различия считали статистически значимыми при p < 0,05.
Результаты исследования и их обсуждение. На 3-5 сутки от начала потребления декстрансульфата натрия общее состояние животных опытной группы по сравнению с контролем прогрессирующее ухудшалось, двигательная активность и потребление пищи снижались, отмечалась пилоэрекция. На 7-ые сутки эксперимента у всех мышей опытной группы выявлялось загрязнение анальной области фекалиями с примесью крови. При вскрытии животных опытной группы отмечалось уменьшение длины толстой кишки с чередованием зон расширения и сужения просвета. Содержимое толстой кишки у мышей опытной группы было жидким и темно-красного цвета, а в контрольной группе желто-коричневого цвета с увеличением плотности содержимого в дистальном отделе ободочной кишки.
При микроскопическом исследовании у животных опытной группы по сравнению с контролем во всех трех отделах ободочной кишки в слизистой оболочке отмечались язвы и эрозии, отек и воспалительная инфильтрация из макрофагов, нейтрофилов и лимфоцитов (рис. 2). Выраженность язвенного поражения была максимальной в
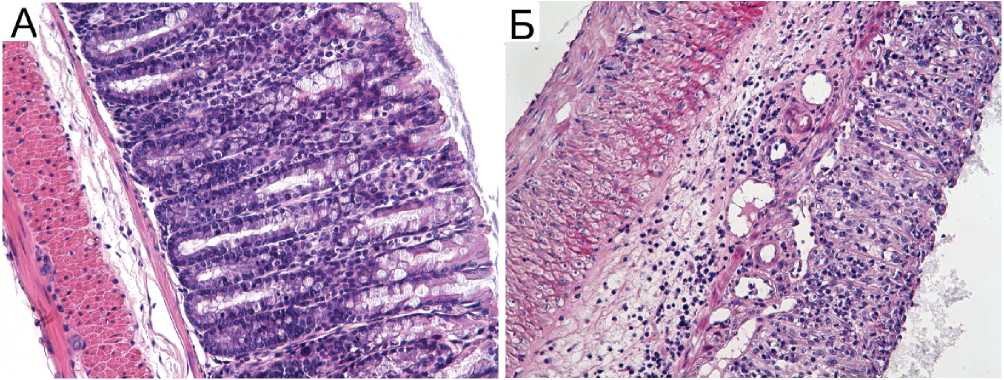
Рис. 1 Стенка дистальной отдела ободочной кишки мыши контрольной группы (А) и с острым язвенным колитом (Б). А - патологических изменений не выявляется; Б - острая язва представлена грануляционной тканью с выраженной воспалительной инфильтрацией. Отек и воспалительная инфильтрация подслизистого слоя. Окраска гематоксилином и эозином. Ув. 200.
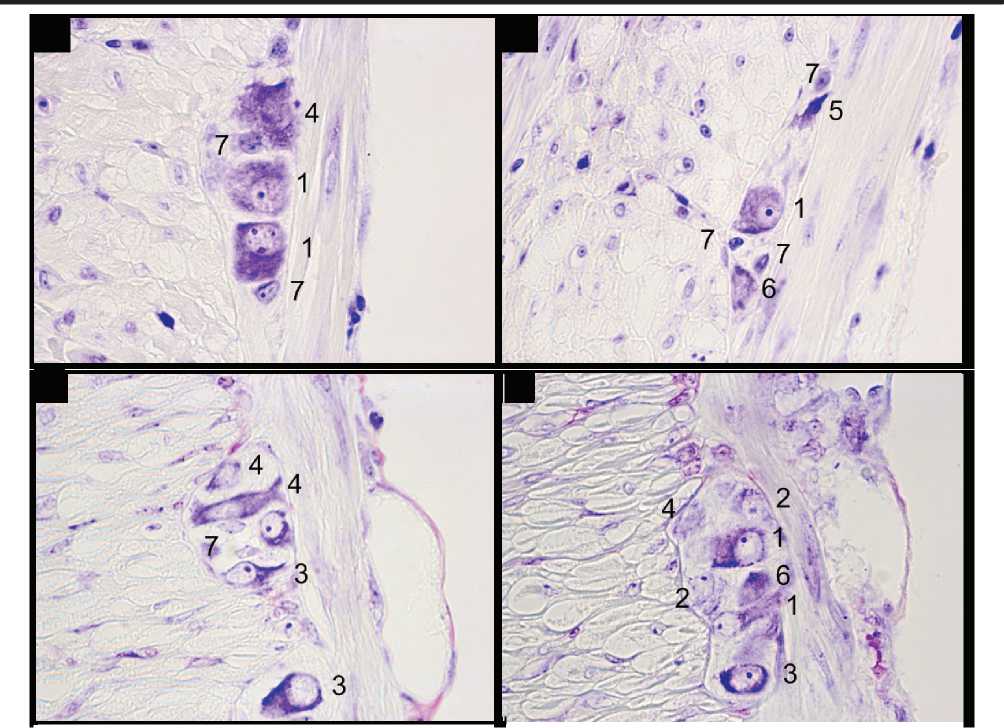
Рис. 2 Миентеральный ганглии ободочной кишки мышей контрольной группы (А, Б) и при остром язвенном колите (В, Г): 1 – нормохромные нейроны; 2 – гипохромные нейроны ; 3 – гиперхромные нейроны;4 – нейроны с ядром без ядрышка;5 – пикнотические гиперхромные нейроны; 6 – нейроны без ядра;7 - глиальные клетки. Окраска по Нисслю. Ув.640.
дистальном отделе ободочной кишки. В мышечной оболочке и миентеральных ганглиях воспалительные изменения отсутствовали.
В миентеральных ганглиях у животных опытной группы по сравнению с контролем определялось очаговое разряжение нейропиля. При анализе клеточного состава миентераль-ных ганглиев выявлено статистически значимое снижение количества гипохромных и увеличение гиперхромных нейронов, снижение числа клеток нейроглии. Общее количество нейронов на ганглий при остром язвенном колите по сравнению с контролем статистически значимо не изменилось (табл.1), а площадь миентеральных нейронов центрального сечения и их ядер статистически значимо уменьшилась (табл. 2). Показатели глио-нейронального индекса миентеральных ганглиев и ядерно-цитоплазматического отношения нейронов при колите не отличались между группами (табл.1, табл. 2) .
В настоящей работе использована окраска гистологических препаратов по Нисслю крези- ловым фиолетовым, которая широко применяется нейроморфологами. Этот метод основан на взаимодействии щелочного красителя, например крезилового фиолетового, с нуклеиновыми кислотами, сконцентрированными в ядре или шероховатом ретикулуме нейронов [9]. Тинкториальные свойства (хромность) цитоплазмы нейронов зависят от состояния тигроида и отражают гетерогенность популяций нейронов [10].
По данным литературы, основанным на исследовании морфологических изменений нейронов в ЦНС, гипохромия нейронов с неизмененной морфологией ядра может быть связана с центральным хроматолизом, острым или гидропическим набуханием нейронов [10]. При центральном хроматолизе отмечается разряжение тигроида в центральных участках клетки, а ядро сдвигается к ее краю. При остром набухании тигроид разряжается и цитоплазма нейрона приобретает гомогенный вид. При гидропичесских изменениях нейронов вокруг ядра выявляются светлые вакуоли. Гиперхромия или сморщивание нейронов в ЦНС
Таблица 1.
Клеточный состав миентеральных ганглиев
|
Показатели на ганглий |
Контроль |
Острый язвенный колит |
Отклонение от контроля, % |
Достоверность различий, p |
|
Нормохромные нейроны |
0,58±0,03 |
0,59±0,03 |
+2% |
0,82 |
|
Гипохромные нейроны |
0,44±0,03 |
0,28±0,02 |
-36% |
<0,05 |
|
Гиперхромные нейроны |
0,08±0,01 |
0,18±0,02 |
+55% |
0,05 |
|
Все нейроны центрального сечения |
1,1±0,05 |
1,05±0,04 |
-5% |
0,37 |
|
Нейроны с ядром не центрального сечения |
0,32±0,03 |
0,34±0,03 |
+6% |
0,49 |
|
Пикнотические нейроны |
0,08±0,02 |
0,08±0,01 |
0% |
0,77 |
|
Нормохромные нейроны без ядра |
1,22±0,05 |
1,09±0,05 |
-11% |
0,2 |
|
Глиоциты |
1,95±0,08 |
1,38±0,06 |
-30% |
<0,05 |
|
Глио-нейрональ-ный индекс |
1,77 |
1,31 |
-26% |
Таблица 2.
Площадь цитоплазмы и ядра миентеральных нейронов центрального сечения
|
Показатели |
Контроль |
Острый язвенный колит |
Отклонение от контроля,% |
Достоверность различий, p |
|
Площадь нейронов в мкм² |
103,11±3,34 |
90,32±2,26 |
-12% |
<0,05 |
|
Площадь ядер в мкм² |
46,88±1,06 |
43,56±0,85 |
-7% |
<0,05 |
|
Ядерно-цитоплазма-тический индекс |
0,48±0,01 |
0,50±0,08 |
+4% |
у человека проявляется в уменьшении размеров нейронов и их ядер, слиянии гранул тигроида в темную массу [10]. Выраженная гиперхромия так называемых темных нейронов традиционно считается признаком их повреждения [11]. Конечным этапом повреждения нейронов является кариоцитолиз с появлением бледных клеток-теней, лишенных ядра. При использовании классических нейрогистологических методов окраски выделяют прогрессивные и регрессивные формы изменения астроцитов. При первом состоянии отмечается гипертрофия астроцитов и нередко их многоядерность, при втором сморщивание клеток и гиперхромия их ядер [10]. Следует отметить что по нашим наблюдениям в большинстве нейронов миентеральных ганглиев мышей опытной и контрольной групп ядро занимает эксцентрическое положение из-за небольшого размера клетки, а детальная оценка морфологии тигроида невозможна из-за небольшого размера цитоплазмы нейронов, вследствие чего экстраполяция данных, полученных на нейронах ЦНС у человека на нейроны миентеральных ганглиев у мышей затруднена. Выявленные при экспериментальном остром колите морфологические изменения ми-ентеральных ганглиев, такие как снижение числа гипохромных нейронов без изменений их ядер и ядрышек, отражают нарушения функционального состояния нейронов, а увеличение числа гиперх-ромных нейронов и уменьшение размеров их ядер и цитоплазмы, уменьшение количества глиоцитов и глиально-нейронального индекса - процессы их альтерации.
Литературные данные об изменении количества энтеральных нейронов и глиоцитов при колите противоречивы. При иммуногистохимическом исследовании энтеральной нервной системы большинство исследователей отмечает снижение количества нейронов при экспериментальном остром и хроническом колите [12 -17].
Ряд авторов указывает что количество нейронов при экспериментальном колите не изменяется [18, 19], имеются сообщения о парадоксальном увеличении числа энтеральных нейронов при колите (20). Количество глиальных клеток по данным литературы может как уменьшаться [17], так и увеличиваться [21 - 22].
Противоречия в результатах исследования количества нейронов и глиальных клеток в энтеральных ганглиях при остром колите может быть связано с тем, что высокоспецифические иммуногистохимические методы, применяемые для выявления клеточных популяций не позволяют идентифицировать клетки с выраженными изменениями в результате потери ими иммунореактивности [23]. Так в зонах некроза слизистой оболочки и подслизистого слоя при остром колите, индуци-рованом тринитробензолсульфоновой кислотой, описывается исчезновение иммунореактивных нейронов и глиальных клеток и постепенное их появление по мере стихания воспалительного процесса [24]. Поэтому оценка патологических изменений энтеральной нервной системы с помощью традиционного метода Ниссля является достаточно информативной.
Выводы. При декстраниндуцированном остром язвенном колите у самцов мышей C57Bl/6 общее количество нейронов на ганглий в ободочной кишке по сравнению с контролем не изменяется, но снижается число гипохромных нейронов и глиоцитов и увеличивается число гиперхромных нейронов на ганглий. Глио-нейрональный индекс уменьшается, что указывает на снижение трофической функции глиоцитов. Размеры нейронов и их ядер уменьшаются. Выявленные морфологические изменения миентеральных ганглиев ободочной кишки при остром язвенном колите могут обусловливать нарушения моторной и секреторной функции.
Список литературы Морфологические изменения миентеральных ганглиев при экспериментальном остром язвенном колите
- Shi X.Z. Differential immune and genetic responses in rat models of Crohn's colitis and ulcerative colitis / Shi X.Z., Winston J.H., Sarna S.K.// Am J Physiol Gastrointest Liver Physiol. 2011 Jan;300(1):G41-51
- Shokrani M. Inflammatory bowel disease: diagnosis and research trends: the clinical lab is playing an increasingly important role. //MLO Med Lab Obs. 2012 Aug; 44(8):8, 10, 12; quiz 14.
- Cirillo C. Ulcerative Colitis - Epidemiology, Pathogenesis and Complications Edited by Mortimer B. O'Connor, Publisher: InTech, Chapters published December 14, - 2011. - P. 29-50. Enteric Nervous System Abnormalities in Ulcerative Colitis By Carla Cirillo, Giovanni Sarnelli and Rosario Cuomo
- Furness J.B. The enteric nervous system and neurogastroenterolog y/ Furness J.B. // Nature Reviews Gastroenterology and Hepatology. - 2012. - № 9. - P. 286-294.
- Furness, J. B. The Enteric Nervous System. Publisher: Blackwell, Oxford. - 2006.
- Geboes K. Structural abnormalities of the nervous system in Crohn's disease and ulcerative colitis / Geboes K., Collins S.// Neurogastroenterol Motil. 1998 Jun;10(3):189-202.
- Moynes D.M. Effects of inflammation on the innervation of the colon / Moynes D.M., Lucas G.H., Beyak M.J., Lomax A.E. // Toxicol Pathol. 2014 Jan;42(1):111-7.
- Худоерков Р.М. Методы компьютерной морфометрии в нейроморфологии. - М.:ФГБУ «НЦН» РAМН, 2014. 53 с.
- Kádár A. Improved method for combination of immunocytochemistry and Nissl staining / Kádár A., Wittmann G., Liposits Z., Fekete C.// J Neurosci Methods. 2009 Oct 30; 184(1): 115-118.
- Ермохин П.Н. Гистопатология центральной нервной системы. М: Медицина -1969 241 с.
- Ooigawa H. The fate of Nissl-stained dark neurons following traumatic brain injury in rats: difference between neocortex and hippocampus regarding survival rate / Ooigawa H., Nawashiro H., Fukui S., Otani N., Osumi A., Toyooka T., Shima K.//Acta Neuropathol 2006 Oct 21;112(4):471-81. Epub 2006 Jul 21.
- Sanovic S., Damage to the Enteric Nervous System in Experimental Colitis /Sanovic S., Lamb D.P., Blennerhassett M.G.//Am J Pathol. 1999 Oct; 155(4): 1051-1057.
- Boyer L. Myenteric plexus injury and apoptosis in experimental colitis /Boyer L., Ghoreishi M., Templeman V., Vallance B.A., Buchan A.M., Jevon G., Jacobson K.// Auton Neurosci. 2005 Jan 15;117(1):41-53.
- Linden D.R. Indiscriminate loss of myenteric neurones in the TNBS-inflamed guinea-pig distal colon. /Linden D.R., Couvrette J.M., Ciolino A., McQuoid C., Blaszyk H., Sharkey K.A., Mawe G.M.// Neurogastroenterol Motil. 2005 Oct;17(5):751-60.
- Lin A. Selective loss of NGF-sensitive neurons following experimental colitis./ Lin A., Lourenssen S., Stanzel R.D., Blennerhassett M.G.// Exp Neurol. 2005 Feb;191(2):337-43.
- Sarnelli G., Myenteric neuronal loss in rats with experimental colitis: role of tissue transglutaminase-induced apoptosis /Sarnelli G., De Giorgio R., Gentile F., Cali G., Grandone I., Rocco A., Cosenza V., Cuomo R., D'Argenio G.//Dig Liver Dis. 2009 Mar;41(3):185-93.
- Sigalet D.L. The effects of glucagon-like peptide 2 on enteric neurons in intestinal inflammation / Sigalet D.L., Wallace L., De Heuval E., Sharkey K.A.// Neurogastroenterol Motil. 2010 Dec;22(12):1318-e350.
- Auli M. Neuromuscular changes in a rat model of colitis /Auli M., Nasser Y,. Ho W., Burgueño J.F., Keenan C.M., Romero C., Sharkey K.A., Fernández E. //Auton Neurosci. 2008 Aug 18;141(1-2):10-21
- Winston J.H. Paradoxical regulation of ChAT and nNOS expression in animal models of Crohn's colitis and ulcerative colitis/ Winston J.H., Li Q., Sarna S.K. //Am J Physiol Gastrointest Liver Physiol. 2013 Aug 15; 305(4): G295-G302.
- Belkind-Gerson J., Colitis induces enteric neurogenesis through a 5-HT4-dependent mechanism /Belkind-Gerson J., Hotta R., Nagy N., Thomas A.R., Graham H., Cheng L., Solorzano J., Nguyen D., Kamionek M., Dietrich J., Cherayil B.J., Goldstein A.M.// Inflamm Bowel Dis. 2015 Apr;21(4):870-8.
- Bradley J.S. Effects of inflammation on cell proliferation in the myenteric plexus of the guinea-pig ileum/Bradley J.S. Jr, Parr E.J., Sharkey K.A. //Cell and Tissue Research, Vol. 289, No. 3,(September 1997), pp. 455-461
- Ippolito C. An integrated assessment of histopathological changes of the Enteric neuromuscular compartment in experimental colitis / Ippolito C., Segnani C., Errede M., Virgintino D., Colucci R., Fornai M., Antonioli L., Blandizzi C., Dolfi A., Bernardini N.//J. Cell. Mol. Med. Vol. XX, No X, 2014 pp. 1-16
- Lomax A.E. Plasticity of the enteric nervous system during in test in alinflammation/Lomax A.E., Fernandez E., Sharkey K.A.//Neurogastroenterol Motil (2005) 17, 4-15
- Poli E., Morphological and functional alterations of the myenteric plexus in rats with TNBS-induced colitis./Poli E., Lazzaretti M., Grandi D., Pozzoli C., Coruzzi G.//Neurochem Res. 2001 Sep;26(8-9):1085-93.


