Морфологические свойства лучевой артерии человека, выделенной в интраоперационный период коронарного шунтирования
Автор: Еременко К.В., Дзюман А.Н., Вечерский Ю.Ю., Затолокин В.В., Андреев С.Л.
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: Клинические исследования
Статья в выпуске: 2 т.28, 2013 года.
Бесплатный доступ
В препаратах лучевой артерии человека, выделенной во время операции коронарного шунтирования, изучали морфологические свойства сосудистой стенки. Установлено, что суммарная толщина tunica intima и tunica media лучевой артерии в проксимальном отделе больше, чем в дистальном за счет увеличения толщины tunica media. При этом объемная плотность tunica media проксимального отдела больше дистального, тогда как объемная плотность tunica intima, напротив, в проксимальном отделе меньше, чем в дистальном. Потому в качестве предпочтительного варианта предлагается анастомозирование дистального отдела лучевой артерии с коронарной артерией.
Лучевая артерия, аортокоронарное шунтирование, гиперплазия гладкомышечных клеток
Короткий адрес: https://sciup.org/14919842
IDR: 14919842 | УДК: 616.127-089.844:615.849.19
The morphologycal properties of the human radial artery, harvested in an intraoperative period of coronary artery bypass grafting
The aim of the study was to examine the histopathological changes of the vascular wall in preparations of human radial artery, harvested during coronary artery bypass surgery. Data showed that the combined thickness of the tunica intima and tunica media in the proximal segment of the radial artery was higher than in the distal segment due to an increase in the thickness of the tunica media. The volumetric density of the tunica media in the proximal segment was higher than in the distal segment, whereas the volumetric density of tunica intima in the proximal segment was lower than in the distal one. Therefore, as a preferred choice for achieving the highquality anastomosis, we propose to create anastomosis between the distal segment of a radial artery and a coronary artery.
Текст научной статьи Морфологические свойства лучевой артерии человека, выделенной в интраоперационный период коронарного шунтирования
Ишемическая болезнь сердца (ИБС) – наиболее распространенная причина смертности и инвалидизации среди населения развитых стран. Основной причиной ИБС является стенозирующее атеросклеротическое поражение коронарных артерий. В мировой практике наиболее распространенным и эффективным методом хирургического лечения данного заболевания является операция аортокоронарного шунтирования (АКШ), позволяющая восстановить кровоснабжение миокарда, а в итоге – повысить выживаемость и качество жизни больных [8].
В практике сердечно-сосудистой хирургии для шунтирования коронарных артерий используются аутоартериальные или аутовенозные шунты [3–6]. Поскольку венозные шунты не всегда обеспечивают стабильность поздних результатов операции коронарного шунтирования, все чаще используются аутоартериальные кондуиты. Наиболее часто используемыми аутоартериальными кондуитами для шунтирования коронарных артерий являются внутренняя грудная и лучевая артерии (ЛА). ЛА стала объектом выбора для таких операций благодаря структуре сосудистой стенки, диаметру просвета, сопоставимому с венечными артериями, достаточной длине и устойчивости к давлению, относительной простоте выделения, хорошим послеоперационным результатам [1].
Основной трудностью, возникающей во время и после операций коронарного шунтирования, является спазм аутоартериальных шунтов, который ведет к серьезным осложнениям, в том числе к возникновению ишемии и периоперационных инфарктов миокарда. Причинами возникновения спазма ЛА во время и после операций коронарного шунтирования может быть как применение препаратов для лечения пациентов до операции, так и механическое повреждение сосудов во время операции [2]. Немалое значение в последнее время уделяется и морфологическим изменениям сосудистой стенки, в частности, гиперплазии внутренней и средней оболочек.
Цель исследования: изучение строения стенки ЛА человека, выделенной в интраоперационный период.
Материал и методы
Объектом исследования явились фрагменты ЛА человека, выделенные во время операции коронарного шунтирования у пациентов со стенозирующим атеросклерозом коронарных артерий и клиническими проявлениями ИБС. Выделение ЛА проводилось методом скелетирования в 0,5–1 см от места бифуркации плечевой артерии. Проанализировано 96 препаратов из ЛА, выделенной в интраоперационный период у 32 пациентов. Гистологическое, морфометрическое исследования и попарное сравнение проводились у 18 пациентов, у которых извлекалось по 2 сегмента артерии (1 – с проксимальной и 1 – с дистальной части). У оставшихся 14 пациентов, у которых извлекалось по 1 сегменту (проксимальный или дистальный) было проведено только гистологическое исследование. Средний возраст больных составил 55,31±1,13 года. Все пациенты были мужского пола. Из сопутствующих заболеваний наиболее часто встречались гипертоническая болезнь III стадии, риск 4 (90% больных), синдром атерогенной дислипидемии (51,6%), ожирение (29%).
Изолированные сегменты ЛА фиксировались в растворе 10%-го формальдегида и заливались в парафин по стандартной методике. Затем на микротоме изготавливались поперечные срезы лучевой артерии толщиной 5 мкм. Микротомные срезы монтировались на предметные стекла и окрашивались 2 способами: 1) гематоксилином и эозином; 2) орсеином и пикриновой кислотой – для выявления эластических волокон. Световую микроскопию проводили на микроскопе Axioscope 40 (Сarl Zeiss, Germany) при увеличении х100, х400 и х600. Морфометрия микропрепаратов ЛА человека осуществлялась с помощью программных пакетов “Image Tool” и “ImageJ”. Измерялись отдельная и суммарная толщина и объемная плотность tunica intima и tunica media, а также диаметр сосуда.
Все пациенты давали письменное согласие на участие в исследовании. Исследование одобрено локальным этическим комитетом.
Результаты исследования обработаны с помощью программного пакета STATISTIСA 6.0, представлены в качестве медианы (Me) и интерквартильного интервала (Q25–Q75). При сравнении групп независимых переменных использовали непараметрический критерий Манна– Уитни. Статистически значимыми считали различия при значении р<0,05.
Результаты и обсуждение
В результате морфологического исследования были выделены следующие изменения в сосудистой стенке: 1. Диффузное утолщение tunica intima (ДУТИ) за счет гиперплазии, отека и гиперэластоза подэндотелиального слоя, проявляющееся увеличением внутренней оболочки по всему внутреннему контуру ЛА (рис. 1 А на 3-й стр. обложки), с преобладанием в интиме эластических структур и мультипликацией, фрагментацией, утолщением, чрезмерной извитостью внутренней эластической мембраны (рис. 1 Б на 3-й стр. обложки);
-
2. Локальное утолщение tunica intima (ЛУТИ), проявляющееся локализованным увеличением толщины интимы на фоне нормально развитой внутренней оболочки (рис. 2 А на 3-й стр. обложки) и изменением внутреннего контура ЛА с локальным сужением просвета сосуда (рис. 2 Б на 3-й стр. обложки);
-
3. Гипертрофия и отек tunica media (ГТМ), представляющие собой выраженное увеличение толщины мышечной оболочки без изменения размеров и формы ГМК (рис. 3 А, Б на 3-й стр. обложки) и уменьшение просвета сосуда.
Наиболее частым сочетанием изменений морфологического строения ЛА, встречающимся у 13 пациентов (41%), явились: гиперплазия, отек, гиперэластоз подэндотелиального слоя tunica intima с мультипликацией, фрагментацией, утолщением, чрезмерной извитостью внутренней эластической мембраны и гипертрофия tunica media (рис. 4 на 3-й стр. обложки).
Данные изменения сосудистой стенки наблюдались как по отдельности, так и сочетанно (рис. 5). Одновременное проявление всех вышеперечисленных изменений сосудистой стенки наблюдалось у 6 пациентов (19%). Реже всего наблюдалось сочетание таких изменений, как диффузное и локальное утолщение tunica intima. Последнее сочетание встретилось у 3 пациентов (9%).
Диффузное утолщение tunica intima как проявление самостоятельного процесса установлено у 9 пациентов (28%). Лишь у одного пациента, подвергшегося операции коронарного шунтирования, изменений в стенке ЛА обнаружено не было.
Возможно, данные изменения могут быть причиной послеоперационных осложнений. В частности, утолщение tunica media может приводить к развитию спастической реакции в раннем послеоперационном периоде, а диффузное и локальное утолщения tunica intima (как варианты развития одного и того же процесса) могут приводить к окклюзии шунта из ЛА в позднем послеоперационном периоде. Кроме того, показано, что локальное утолщение tunica intima является проявлением долипид-ной стадии атеросклеротического поражения ЛА [7]. Этот фактор также влияет на проходимость шунта, а следовательно, и на возникновение осложнений, в том числе периоперационного инфаркта миокарда.
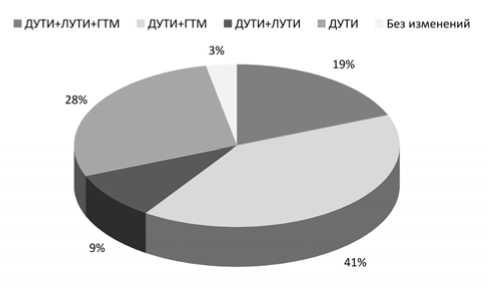
Рис. 5. Соотношения изменений в стенке ЛА человека, выделенной в интраоперационный период
Таблица
Морфометрические показатели внутренней и средней оболочек ЛА у пациентов с ИБС (Me, Q25–Q75)
|
Проксимальный отдел, n=18 |
Дистальный отдел, n=18 |
|||||
|
Q25 |
Me |
Q75 |
Q25 |
Me |
Q75 |
|
|
Толщина tunica intima, мкм |
37,39 |
55,01 |
103,83 |
43,86 |
60,9 |
91,13 |
|
Толщина tunica media, мкм |
265,53 |
309,70 |
391,85 |
238,89 |
281,28 |
339,41 |
|
Объемная плотность tunica intima, % |
6,78 |
10,44 |
15,59 |
9,3 |
12,81 |
17,64 |
|
Объемная плотность tunica media, % |
63,61 |
69,43 |
74,47 |
61,09 |
64,19 |
67,76 |
|
Суммарная толщина tunica intima и tunica media, мкм |
327,68 |
385,68 |
504,08 |
277,86 |
359,51 |
414,75 |
|
Суммарная объемная плотность tunica intima и tunica media, % |
75,4 |
82,54 |
85,94 |
74,15 |
79,11 |
85,17 |
|
Просвет сосуда, мкм |
423,15 |
588,3 |
684,17 |
421,3 |
614,45 |
699,95 |
Примечание: Курсивом выделены статистически значимые отличия (p<0,05) между исследуемыми показателями в проксимальном и дистальном отделах.
В ходе морфометрического исследования проксимального и дистального отделов лучевой артерии человека, выделенной в интраоперационный период, были определены показатели, представленные в таблице.
Суммарная толщина tunica intima и tunica media в проксимальном отделе 385,68 (327,68–504,08) мкм оказалась статистически значимо выше, чем в дистальном 359,51 (277,86–414,75) мкм, преимущественно за счет увеличения толщины tunica media. Последняя в проксимальном отделе составила 309,7 (265,53–391,85) мкм, а в дистальном – 281,28 (238,89–339,41) мкм. Наряду с этим отмечалось статистически значимое отличие в объемной плотности tunica media проксимального и дистального отделов. Она равна 69,43% (63,61–74,47) и 64,19% (61,09– 67,76) соответственно. При этом объемная плотность tunica intima в проксимальном отделе составляла 10,44% (6,78–15,59) и была статистически значимо ниже, чем в дистальном 12,81% (9,3–17,64). Более выраженный мышечный слой в проксимальном отделе ЛА может быть препятствием к использованию этого участка артерии для дистального анастомоза в операциях АКШ из-за высокой вероятности спастической реакции. В этом случае предпочтительным вариантом анастомозирования с коронарной артерией является дистальный отдел ЛА.
Заключение
Таким образом, при морфологическом и морфометрическом исследовании препаратов ЛА, полученных у больных ИБС с выраженным стенозирующим атеросклерозом коронарных артерий, выявлены исходные изменения сосудистой стенки радиальных артерий, используемых в качестве шунтов, которые могут стать причиной ранних и поздних послеоперационных осложнений КШ. Полученные нами данные позволяют предположить, что для создания анастомоза между радиальной и коронарной артериями при выполнении операции коронарного шунтирования следует выбирать дистальный отдел ЛА. В дистальном отделе ЛА менее развиты гладкомышечные клетки в tunica media, которые являются основным субстратом для развития спастических реакций.
Список литературы Морфологические свойства лучевой артерии человека, выделенной в интраоперационный период коронарного шунтирования
- Вечерский Ю.Ю., Андреев С.Л., Затолокин В.В. Сравнительное исследование функционирования различных аутоартериальных и венозных графтов по данным шунтографии после изолированного коронарного шунтирования//Сибирский медицинский журнал (Томск). -2010. -№ 4, вып. 1. -С. 43-49.
- Мамчур С.Е., Вечерский Ю.Ю., Фадеев М.В. Морфология внутренне грудной и лучевой артерий у пациентов, подвергшихся коронарному шунтированию//Бюл. сиб. медицины. -2004. -№ 2. -C. 85-89.
- Шнейдер Ю.А., Толкачев В.В., Жорин С.П. Реваскуляризация миокарда с помощью лучевой артерии//Вестник хирургии. -2004. -№ 3 -С. 14-18.
- Iaco A.L., Teodori G., Di Giammarco G. Radial artery for myocardial revascularization: long term clinical and angiographic results//Ann. Thorac. Surg. -2001. -Vol. 72. -P. 464-468.
- La Villa G., Lazzeri C., Fronzaroli C. et al. Brain natriuretic peptide//Ann. Ital. Med. Mt. -1995. -Vol. 10, No. 4. -P. 233-241.
- Tatoulis J., Buxton B., Fuller J. Patencies of 2127 arterial to coronary conduits over 15 years//Ann. Thorac. Surg. -2004. -Vol. 77. -P. 87-92.
- Wildhirt S.M., Voss B., Von Canal F. et al. Graft function, histopathology and morphometry of radial arteries used as conduits for myocardial revascularization in patients beyond age 70//Eur. J. Cardio thoracic Surg. -2006. -Vol. 30. -P. 333-340.
- Wilson J.M., Ferguson J.J., Hall R.J. Coronary artery bypass surgery and percutaneous coronary revascularization: impact on morbidity and mortality in patients with coronary artery disease//Cardiovascular Medicine. -NY: Springer, 2007. -P. 1073-1112.


