Морфологические варианты болезни Кастлемана и плотность сосудистой сети в ткани лимфатических узлов
Автор: Михайлов Анатолий Михайлович, Раскин Григорий Александрович, Ругаль Виктор Иванович, Семенова Наталья Юрьевна, Бессмельцев Станислав Семенович
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: Лабораторные и экспериментальные исследования
Статья в выпуске: 2 т.32, 2017 года.
Бесплатный доступ
С помощью цифровой гистоморфометрии изучена плотность сосудистой сети в ткани лимфатических узлов у 28 больных с плазмоклеточным и гиалиново-васкулярным типом болезни Кастлемана. Метод позволил количественно оценить плотность сосудистой сети и обработать результаты статистически. Наибольшие показатели плотности сосудов выявлены при плазмоклеточном типе. При гиалиново-васкулярном типе плотность сосудов характеризовалась значительной вариабельностью, что может отражать неоднородность этого варианта болезни
Болезнь кастлемана, лимфатические узлы, сосудистая сеть, цифровая гистоморфометрия
Короткий адрес: https://sciup.org/14920204
IDR: 14920204 | УДК: 616.15;
Morphologic variants of Castleman’s disease and density of vascular net in tissue of lymph nodes
Vascular density was studied in the lymph node biopsies from 28 patients with Castleman’s disease (hyaline vascular and plasma cell types) with the help of digital histomorphometry. The method allowed for quantitative assessments and statistical analysis. Plasma cell type demonstrated the highest vascular density. The data on hyaline vascular Castleman’s disease showed a high statistical spread, suggesting heterogeneity of this particular type of the disease.
Текст научной статьи Морфологические варианты болезни Кастлемана и плотность сосудистой сети в ткани лимфатических узлов
Болезнь Кастлемана (БК) или интерлейкин-6 опосредованная ангио-фолликулярная гиперплазия лимфатических узлов – редкое лимфопролиферативное заболевание. Болезнь получила название в честь автора (B. Castleman), описавшего ее в 1954 г. [4]. Морфологической основой болезни Кастлемана является гиперплазия лимфоидных фолликулов в лимфатических узлах с инволюцией и гиалинозом герминативных центров, и, что наиболее демонстративно, обильным развитием в межфолликулярных зонах узлов капилляров с гиалинозом их стенок. Некоторые сосуды врастают в гиперплазированные фолликулы, напоминая картину “леденца на палочке” [7,8]. Заболевание имеет два основных морфологических варианта: плазмоклеточный (более редкий) и гиалиново-васкулярный (более частый). Ряд авторов выделяет также смешанный тип [1, 2, 4, 5]. Диагностика заболевания только морфологическая – по биопсии лимфатического узла. В части случаев проводится иммуногистохи-
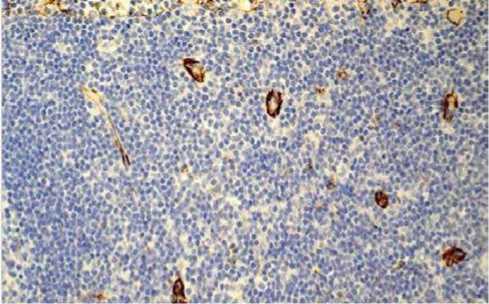
Рис. 1. Развитие сосудистой сети в ткани лимфатического узла у пациентки контрольной группы после мастэктомии. Иммуногистохимическая реакция с антителами к СD34 х 200
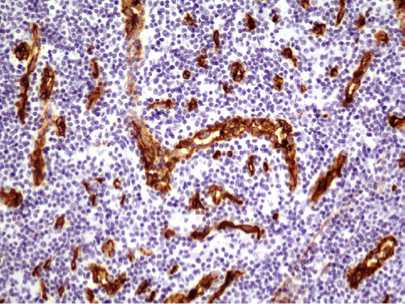
Рис. 2. Сосудистая сеть в ткани лимфатического узла у больного с плазмоклеточным вариантом болезни Кастлемана и РОЕМS-синдромом. Иммуногистохимическая реакция с антителами к СD34 х 200
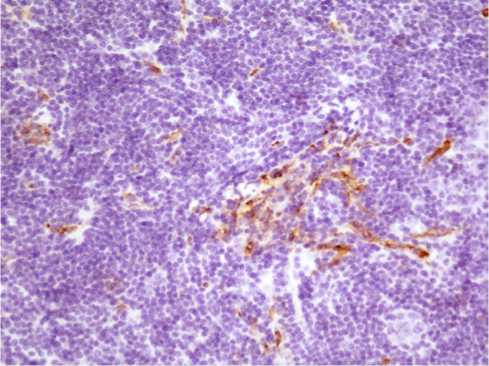
Рис. 3. Слабо развитая сосудистая сеть в ткани лимфатического узла у больного с гиалиново-васкулярным типом болезни Кастлемана. Иммуногистохимическая реакция с антителами к СD34 х 200
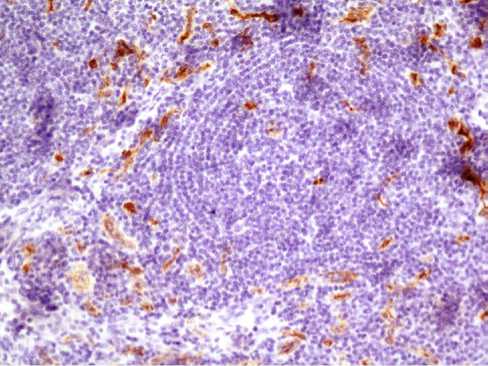
Рис. 4. Увеличение плотности микрососудов в ткани лимфатического узла у больного с гиалиново-васкулярным вариантом болезни Кастлемана. Иммуногистохимическая реакция с антителами к СD34 х 200
мическое исследование – преимущественно для оценки иммуноархитектоники лимфатического узла; она почти не отличается от нормальной. Иногда иммуногистохимическое исследование необходимо для дифференциальной диагностики болезни Кастлемана и В-клеточных лимфом из зрелых клеток (фолликулярной, лимфомы маргинальной зоны, лимфомы из мантийных клеток). Плазмоклеточный вариант характеризуется обилием плазмоцитов в межфолликулярных зонах в виде крупных скоплений или почти полным замещением лимфоцитов плазматическими клетками [4]. В зависимости от характера распределения увеличенных лимфатических узлов выделяют 2 клинических варианта болезни Кастлемана – уни-центрический и мультицентрический [5]. Гиперплазию сосудистого русла обычно оценивали визуально [5, 7, 8], что не позволяло количественно определить площадь сосудов. В отличие от гиалиново-васкулярного при плазмоклеточном варианте присутствуют симптомы интоксикации (потливость, субфебрилитет, слабость) и выявляются изменения лабораторных данных. Так, при плазмоклеточном варианте БК обнаружено 100-кратное увеличение содержания эндотелиального фактора роста сосудов (VEGF) в элюате из лимфатического узла [5], что может оказать заметное влияние на развитие новых сосудов. В предыдущей публикации [3] нами также была показана интенсивная экспрессия VEGF всеми клетками лимфатического узла у больного смешанным типом БК с обилием вновь образованных сосудов.
Целью работы явилось сопоставление морфологического варианта болезни Кастлемана с количественной оценкой процента площади сосудов в ткани лимфатического узла.
Материал и методы
Под наблюдением находилось 28 пациентов с болезнью Кастлемана (мужчины – 14, женщины – 14). Возраст больных колебался от 24 до 65 лет. При обследовании больных использовали метод цифровой иммунной гистоморфометрии. Срезы лимфатических узлов после этапа гистологического и иммуногистохимического подтверждения болезни Кастлемана обрабатывали антителами к СD34 class11 (QBEND10, Dako) для маркировки эндотелия сосудов. Далее препараты подвергали сплошному сканированию на сканнере Panoramic (Zeiss). Процент площади сосудов определяли с помощью программы Panoramic Viewer, что позволяло производить статистическую обработку данных по t-критерию Стьюдента. Содержание и распределение плазматических клеток в ткани лимфатических узлов определяли иммуногистохимическим методом с антителами к СD138 (М115, Dako). Для контроля были использованы 3 операционных лимфатических узла из подмышечной области, взятых у больных с опухолью молочной железы без признаков метастазирования. У всех пациентов при обследовании соблюдались этические стандарты.
Статистическая обработка полученных данных проводилась методом вариационной статистики с определением средней величины М, ее средней ошибки m. Достоверность различий оценивалась с помощью непарамет- рического U-критерия Манна–Уитни для малых выборок с ненормальным распределением. Различие между сравниваемыми показателями считалось статистически значимым при р≤0,05. Математическую обработку результатов исследования проводили с использованием программ Statistica v. 6.0, MedCalc, Microsoft Excel для Windows ХР.
Результаты и обсуждение
Плазмоклеточный вариант болезни Кастлемана был диагностирован у 8 (28,6%) из 28 больных, вошедших в исследование. Увеличение лимфатических узлов у них носило распространенный характер, что позволило всем поставить мультицентрический вариант заболевания. Этот вариант, как известно [5], встречается реже, протекает более агрессивно, характеризуется смешанно-клеточной или плазмоклеточной морфологией. У 5 из 8 больных был установлен РОЕМS-синдром, который характеризовался полинейропатией, органомегалией (гепато- и спленомегалия), эндокринопатиями с изменениями уровня половых гормонов у мужчин по женскому типу (снижение тестостерона, увеличением пролактина), а также появлением низкого уровня инсулина у одной больной, и изменениями кожи в виде обильного развития ангиом или гиперемии, и выявлением M-протеина при электрофорезе сывороточных белков. Полинейропатия была подтверждена проведением электро-нейромиографии, которая выявила нейромышечный сенсорно-моторный блок периферических нервов. Из литературы известно, что в развитии РОЕМS-синдрома ведущую роль играют свободные лямбда-цепи иммуноглобулинов, повреждающие ткани, и гиперпродукция VEGF, что приводит к существенному развитию новых сосудов (неоангиогенез) [6]. Эти два фактора вызывают развитие склероза тканей, истощение организма и гибель больных от респираторного нейро-мышечного блока, проявлявшегося отсутствием самостоятельного дыхания, что произошло с одним из наблюдаемых нами больным. Гиалиново-васкулярный тип БК установлен у 20 (71,4%) из 28 больных. У 16 из них болезнь носила мультицентрический тип (80%). При проведении исследования установлено, что в ткани лимфатических узлов контрольной группы сосуды занимали 10,6±1,0% площади (рис. 1) У больных с плазмоклеточным вариантом заболевания площадь сосудов в ткани узла была увеличена и составила 15,1±1,4% (р ≤ 0,05) (рис. 2). Больные гиалиново-васкулярным типом, в зависимости от величины площади сосудов, были разделены на 2 подгруппы. У 15 (75%) пациентов первой подгруппы процент площади сосудов составил 6,8±2,3% (рис. 3), что оказалось статистически значимо ниже по сравнению с больными плазмоклеточным вариантом болезни Кастлемана (р ≤ 0,05). У 5 (25%) больных гиалиново-васкулярным типом (вторая подгруппа) процент площади сосудов равнялся 12,3±1,5%, что не отличалось от уровня группы контроля и больных плазмоклеточным вариантом, но было выше, чем у пациентов первой подгруппы (р ≤ 0,05) (рис. 4).
Таким образом, полученные результаты свидетельствуют о наиболее выраженном неоангиогенезе в ткани лимфатических узлов при плазмоклеточном варианте болез- ни Кастлемана, в том числе с развитием РОЕМS-синдро-ма у 5 из 8 больных. Гиалиново-васкулярный тип болезни продемонстрировал свою гетерогенность по плотности вновь образующихся сосудов в ткани лимфоузлов. На наш взгляд, это объясняется различием в интенсивности выработки факторов ангиогенеза у этой категории больных. Как уже указывалось выше, наиболее высокая продукция VEGF наблюдается при плазмоклеточном варианте болезни Кастлемана.
Существует множество методов лечения БК: стероиды, химиотерапия, противовирусные препараты, интерферон α , моноклональные антитела к IL-6 и к его рецептору IL-6, моноклональное антитело к CD20 [5]. Установление факта выраженности неоангиогенеза при болезни Кастлемана ассоциируется с высокой агрессивностью данного варианта заболевания и требует проведения цитостатической терапии с включением препаратов-ингибиторов ангиогенеза [5].
Заключение
Проведенное исследование с использованием цифровой гисто-морфометрии площади, занимаемой сосудами в ткани лимфатического узла при болезни Кастлемана, дало возможность количественно оценить этот показатель. Наибольшие показатели плотности сосудов выявлены при плазмоклеточном варианте болезни Кастлема-на. При гиалиново-васкулярном типе плотность сосудов характеризовалась значительной вариабельностью, что может отражать неоднородность этого варианта болезни. Наиболее интенсивный неоангиогенез при плазмоклеточном варианте болезни Кастлемана указывает на необходимость применения у данной категории больных ингибиторов ангиогенеза.
Выводы
-
1. Цифровая гисто-морфометрия позволяет количественно оценить развитие сосудов в ткани лимфатического узла при болезни Кастлемана.
-
2. Неоангиогенез наиболее выражен у больных плазмоклеточным вариантом болезни Кастлемана.
-
3. При гиалиново-васкулярном типе плотность сосудов характеризовалась значительной вариабельностью, что отражает его биологическую гетерогенность и возможные количественные различия выработки факторов неоангиогенеза.
Список литературы Морфологические варианты болезни Кастлемана и плотность сосудистой сети в ткани лимфатических узлов
- Егорова Е.К. Клинико-морфологические особенности различных вариантов болезни Кастлемана: автореф. дис.. канд. мед. наук. -М., 2016. -25 с.
- Меликян А.Л., Капланская Б., Корнева Е.П. и др. Болезнь Кастлемана//Тер. Архив. -2005. -№ 7. -С. 48-53.
- Михайлов А.М., Бессмельцев С.С., Пожарисский К.М. и др. Болезнь Каслмана и РОЕМS-синдром//Клиническая Онкогематология. Фундаментальные исследования и клиническая практика. -2010. -№ 3. -С. 259-269.
- Castleman B., Town V. Case 40011//N. Engl. J. Med. -1954. -Vol. 250, No. 1. -P. 26-30.
- Casper C. The etiology and management of Castleman disease at 50 years: translating pathophysiology to patients care//British J. Haemathology. -2005. -Vol. 129. -P. 3-17.
- Dispenziery A. POEMS-syndrome. Review//Blood Rev. -2007. -Vol. 21, No. 5. -P. 285-299.
- Neoplastic Hematology: 2nd edn/ed. by D.M. Knowles. -Philadelphia: Lippincott Williams & Wilkins, 2000. -P. 1546-1549.
- Yang N.S., Gerson S.L., High K.A. Clinical hematology. -Philadelphia: Lippincott Williams&Wilkins, 2006. -P. 322-324.


