MUC1 антиген как иммунотерапевтическая мишень
Автор: Боженко В.К., Уразаева И.Х., Ранджит Р., Кудинова Е.А.
Журнал: Вестник Российского научного центра рентгенорадиологии Минздрава России @vestnik-rncrr
Рубрика: Обзоры
Статья в выпуске: 4 т.23, 2023 года.
Бесплатный доступ
Резюме: MUC1 является высоко гликозилированным белком. Он имеет две субъединицы, которые играют разные роли в нормальном и патологическом состоянии. В нормальных условиях N- конец служит барьером для защиты клеток от вредных экологических и бактериальных инфекций. В опухолях С-конец локализуется внутри клеток и больше вовлечен в передачу различных сигналов, которые влияют и регулируют рост опухоли, ее выживание, инвазию, миграцию и апоптоз. MUC1 - это онкоген, который провоцирует воспаление в рак, повышает устойчивость к лекарствам, способствует метастазированию опухоли и, как было показано, играет важную роль в прогрессировании рака. Основываясь на этих характеристиках, исследователи разработали различные терапевтические подходы, основанные на использовании MUC1 для лечения рака. В отличие от других органов, чрезмерная экспрессия MUC1 была обнаружена во многих типах рака, что делает его хорошим маркером для диагностики и прогноза в клиническом лечении.В области целенаправленной доставки терапевтических средств в раковые клетки исследователи разработали различные типы вакцин, направленных против чрезмерной экспрессии MUC1, которые могут быть эффективными в профилактике и лечении рака. Сообщалось также о разработке иммунотерапевтических стратегий на основе MUC1. В обзоре раскрываются структурные особенности MUC1 и его основные функции в прогрессировании рака, а также обсуждаются возможности его клинического применения, разработанные за последнее десятилетие.
Муцин 1, muc1, иммунотерапия, онкотерапия, злокачественные опухоли
Короткий адрес: https://sciup.org/149145027
IDR: 149145027
MUC1 antigen as an immunotherapeutic target
MUC1 is a highly glycosylated protein. It has two subunits that play different roles in normal and pathological conditions. In normal state, the N-terminus serves as a barrier to protect cells from harmful environmental and bacterial infections. In tumors, the C-terminus localizes inside the cells and is more involved in transmitting various signals that affect and regulate tumor growth, survival, invasion, migration and apoptosis. MUC1 is an oncogene that provokes inflammation into cancer, increases drug resistance, promotes tumor metastasis and has been shown to play an important role in cancer progression. Based on these characteristics, researchers have developed various therapeutic approaches based on the use of MUC1 to treat cancer. Unlike other organs, MUC1 overexpression has been detected in many cancers, making it a promising marker for diagnosis and prognosis in clinical treatment.In the field of targeted delivery of therapeutic agents to cancer cells, researchers have developed various types of vaccines directed against MUC1 overexpression, which may be effective in cancer prevention and treatment. The development of MUC1-based immunotherapeutic strategies has also been reported. This review reveals the structural features of MUC1 and its major functions in cancer progression, and discusses its clinical applications developed over the past decade.
Текст научной статьи MUC1 антиген как иммунотерапевтическая мишень
Муцины (MUC) — это крупные и высоко гликозилированные белки, которые обеспечивают защиту, гидратацию и смазку эпителиальной поверхности, включая желудочнокишечный, дыхательный и репродуктивный тракты [1]. Муцины подразделяются на два типа: секретированные и трансмембранные (мембранно-связанные) муцины. Секретируемые муцины представлены гелеобразующими (MUC2, MUC5AC, MUC5B, MUC6, MUC19) и не гелеобразующими муцинами (MUC7, MUC8, MUC9 (OVGP1)). Трансмембранные муцины содержат один мембранный домен и цитоплазматический домен, они были идентифицированы как MUC1, MUC3A, MUC3B, MUC4, MUC12, MUC13, MUC14 (эндомуцин), MUC15, MUC16, MUC17, MUC20, MUC21 (эпигликанин) и MUC22 [2,3]. MUC1 был одним из самых первых обнаруженных муцинов [4]. Трансмембранный гликопротеин муцин 1, благодаря своим структурным и биохимическим свойствам, способствует формировании слизи, участвует как смазка и увлажнитель в стенках нормальных клеток, выполняет барьерную функцию и таким образом защищает от инфекций [5]. Опухоль- ассоциированный MUC1 отличается от MUC1 по экспрессии в нормальных клетках, биохимическим характеристикам, клеточному распределению и функции [6]. Однако в раковых клетках MUC1 часто подвергается аберрантному гликозилированию и сверхэкспрессии [5]. Он вовлечен в опухолевую инвазию, метастазирование, ангиогенез и апоптоз за счет участия в процессах передачи внутриклеточных сигналов и регуляции связанных биомолекул. В данном обзоре будет рассмотрено строение и функция MUC1 в нормальных и раковых клетках, а также регуляторные механизмы, отвечающие за эти функции. В настоящее время наблюдается большой прогресс в исследовании и клиническом применении MUC1 в онкотерапии [5,6].
Строение МUC1
MUC1, наиболее изученный трансмембранный муцин, имеет переменное количество высокогликозилированных 20-аминокислотных тандемных повторов (VNTR) , домен спермы белок-энтерокиназы-агарин (SEA) (внеклеточный), трансмембранный домен и 72-аминокислотный цитоплазматический хвостовой домен, выходящий на 200-500 нм за пределы клеточной поверхности (рис. 1A) [4,5]. MUC1 кодируется как единая полипептидная цепь, которая сразу после трансляции подвергается самозащитному расщеплению по мотиву GSVV (расположенному в домене SEA) на два пептидных сегмента: более длинную N-концевую субъединицу (MUC1-N) и более короткую C-концевую субъединицу (MUC1-C) (рис. 1A) [6]. Эти две субъединицы связаны стабильными водородными связями [7]. Тем не менее, в опухоль ассоциированном MUC1 было обнаружено структурное изменение в связи с потерей полярности в эпителиальных клетках, а боковые цепочки углеводов становились незавершенными и образовывали новые углеводные побочные цепи (Thomsen-Friedenreich (TF или T), Tn и Sialyl-Tn (STn)) и воздействие основного пептида (рис. 1В) [8-11].
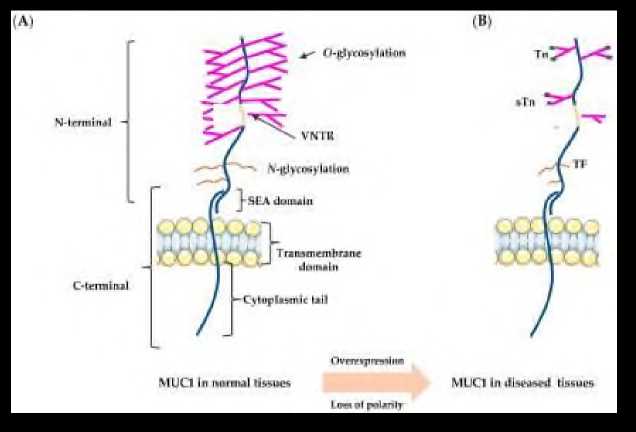
Рис. 1 . Структура MUC1 в нормальных и пораженных тканях. (А) Структура MUC1 в нормальных тканях. (B) Структура MUC1 в пораженных тканях [8].
Функция MUC1 в нормальных тканях
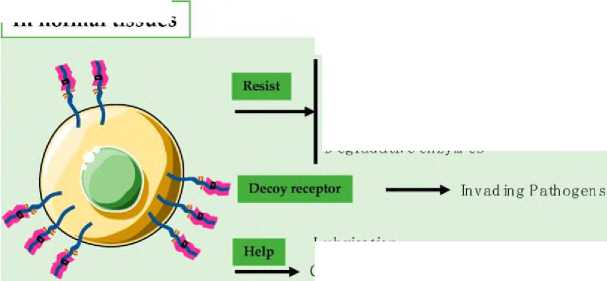
В здоровых тканях MUC1 выполняет барьерную функцию, защищая клетки, в основном благодаря своему внеклеточному домену [12]. Связанный с мембраной MUC1 действует как физический барьер через свой внеклеточный домен SEA, что позволяет ему регулировать кровоток и адгезию клеток при метастазировании; защищать апикальную клеточную мембрану эпителиальных клеток от разрыва, вредных условий и иммунной атаки; обеспечивать устойчивость к стимулам; подавлять иммунные реакции через защиту рецепторов; действовать как рецептор-приманка для вторгающихся патогенов [13]. Он также участвует в смазывании, гидратации клеточной поверхности и защите от деградирующих ферментов (рис. 2A) [14,15]. В нормальном эпителии слизистой оболочки рта MUC1, вместе с MUC5B и MUC7, оказывает антимикробное действие, постоянно смазывая и стабилизируя слизь на поверхности клеток и обеспечивая защиту от протеолиза, тем самым предотвращая дегидратацию [6]. MUC1, трансмембранный продукт расщепления белка MUC1, может помочь в размножении большого количества плюрипотентных стволовых клеток для терапевтических вмешательств [16].
Функции MUC1 при патологииВоспалительная и противовоспалительная функции
MUC1 может выполнять, как и воспалительную, так и функции в различных индуцированных инфекцией видах противовоспалительную рака, действуя как
иммуномодулирующий переключатель [9,10]. При рассеянном склерозе MUC1 играет противовоспалительную роль, ингибируя реакцию дендритных клеток, которые необходимы для возникновения воспаления (рис. 2B) [11]. MUC1 может также влиять на ответные реакции Toll-подобных рецепторов через иммуномодуляцию [12].
In normal tissues
Tm m une a Hack
H arm fu 1 en v iron m en t
Apical cell m em brane rupture
D egradative enzym es
(A)
Lubrication
C e 13 surface h уd ration
C ellshedd ing and adhesion
Or Glycosylation
Pro- or anti-inflammatory role Pharmacodynamic inhibitors
Migration and invasion of cancer cd Is promoters
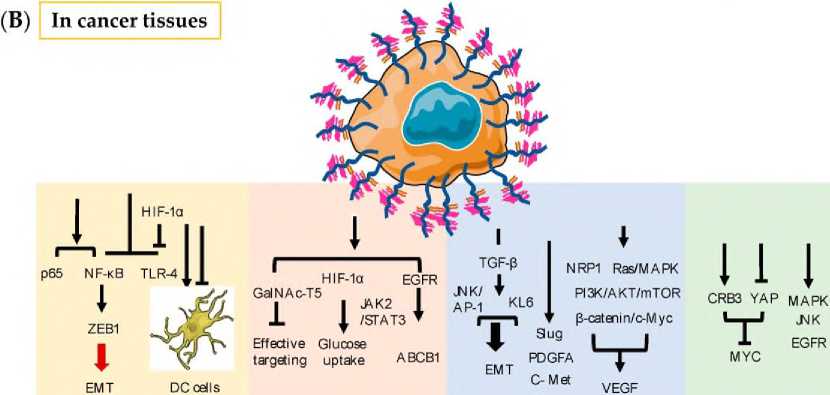
Рис. 2. Различные функции MUC1 в здоровых и раковых тканях. (А) Функция MUC1 в нормальных тканях. (B) Функция и главные пути MUC1 в опухолевых тканях [12].
Фармакодинамические ингибиторы
MUC1 может привести к появлению лекарственной устойчивости во время проведения онкотерапии, так как он обычно в большом количестве выделяется в различных эпителиальных раковых клетках. Сообщалось, что чрезмерная экспрессия MUC1 ограничивает эффективность флюороурацила, снижая внутриклеточное поглощение лекарств и противоопухолевое действие препарата в опухолях поджелудочной железы. Стимулируя активацию и ядерную транслокацию EGFR, MUC1 увеличивает экспрессию АТФ-связывающего кассетного транспортера B1 (ABCB1) . MUC1-опосредованный метаболизм нуклеотидов также играет ключевую роль в резистентности к лучевой терапии при раке поджелудочной железы и может блокировать эффективное таргетирование через гликолиз [13]. В клетках гепатоцеллюлярной карциномы MUC1 может способствовать радиорезистентности, активируя этим янус-киназу-2, которая является преобразователем сигнала и активатором транскрипции-3. Кроме того, MUC1-CT проявляет онкогенную активность, воздействуя на гликозилтрансферазу GalNAc-T5, связанную с функцией опухолевого супрессора при раке поджелудочной железы [14].
MUC1 способствует миграции и распространению рака
MUC1 способствует миграции и инвазии различных видов рака; регуляторные механизмы, отвечающие за это явление избыточны и сложны. Первый механизм заключается в регуляции факторов, тесно связанных с проникновением опухолевых клеток и метастазами. Было показано, что при колоректальном раке олигосахаридная форма MUC1 определяет метастатический потенциал колоректальных раковых клеток и имеет клиникопатологическую значимость при оценке исхода и прогноза пациентов. Раковые клетки выживают в гипоксических условиях, стимулируя экспрессию проангиогенных генов в дальнейшей стимуляции ангиогенеза. Экспрессия MUC1 способствует ангиогенезу при раке и, в определенной степени, способствует миграции и инвазии опухоли. Экспрессия MUC1 и фактора роста эндотелия сосудов в раке молочной железы человека сильно коррелируют, и было показано, что экспрессия MUC1 усиливает ангиогенез в раке молочной железы человека как in vivo , так и in vitro [15].
MUC1 блокирует рост раковой клетки и апоптоза
MUC1 также участвует в регуляции различных путей роста раковых клеток и апоптоза. Трансформация и потеря полярности эпителиальных клеток рака молочной железы приводит к сверхэкспрессии MUC1, который, в свою очередь, индуцирует экспрессию Crumbs homolog-3 (CRB3) и ингибирует экспрессию “ да-ассоциированного белка” (YAP) и YAP/β-связанного белка, опосредованную Myc [8]. Чрезмерная экспрессия MUC1-C, но не MUC1-N достаточна для индуцирования трансформации и устойчивости к вызванному стрессом апоптозу [16]. MUC1 способствует росту и выживанию клеток рака поджелудочной железы, активируя путь митоген-активируемая протеинкиназа; фармакологическое ингибирование этого пути подавляет пролиферацию MUC1-экспрессирующих клеток [8].
MUC1 влияет на различные пути прогрессирования опухоли. Клетки из высокоопухолевой субпопуляции CD133+ клеток поджелудочной железы демонстрируют более высокий уровень экспрессии MUC1, что способствует их опухолевому фенотипу за счет усиления взаимодействия между MUC1-C и β-катенином, которые, в свою очередь, модулируют онкогенные сигнальные каскады [17]. В эпителиальных тканях рака яичников сверхэкспрессия опухоль-ассоциированного MUC1 способствует клеточной адгезии, передаче сигналов, миграции, пролиферации и дифференцировке раковых клеток; таким образом, повышение регуляции MUC1 в злокачественных клетках может изменять пути канцерогенеза [18].
Научные исследования трансмембранных муцинов в онкотерапии
Муцины являются перспективной мишенью для лечения раковых клеток. Благодаря своей роли в трансдукции сигнальных путей раковых клеток, трансмембранные муцины могут иметь важный потенциал в исследованиях противоопухолевой терапии. Внеклеточный домен мембранно-связанных муцинов также может быть хорошей мишенью для антителоопосредованной терапии, основанной на нейтрализующих антителах, химерных антигенных рецепторах, биспецифических активаторах Т-клеток и конъюгатах антитело-лекарство. Специфическая для рака экспрессия некоторых муциновых белков также предполагает возможность разработки противоопухолевой вакцины на основе муцинов [19]. Терапевтические препараты MUC1 находятся в стадии разработки для различных типов рака, включая как твердых опухолей, так и злокачественных патологий крови (табл. 1). Отсутствие ферментативного кармана в белке MUC1 не позволяет нацеливать на него ингибиторы на основе малых молекул, но пептидные ингибиторы и РНК-аптамеры могут быть жизнеспособными вариантами ингибиторов прямого связывания MUC1. Онкопротеин MUC1-C является внутриклеточной мишенью, на которую можно воздействовать с помощью ингибиторов клеточных проникающих пептидов, например GO-203 [20]. Цитоплазматический домен MUC1 связывает ряд ключевых онкогенных белков, и блок димеризации MUC1 может иметь антиопухолевые эффекты через различные механизмы, в зависимости от типа клетки. Так как AKT-S6K1-eIF4A является одним из основных путей, измененных MUC1, GO-203 обладает антиопухолевым потенциалом, блокируя AKT-путь в нескольких типах опухолей, таких как опухоли толстой кишки, пищевода, мочевого пузыря и молочных желез [21,22]. GO-203 также обладает хорошим потенциалом в сочетании со стандартными химиотерапевтическими препаратами в раковых клетках, устойчивых к химиотерапии, или трудноизлечимых [22]. При трижды негативном раке молочной железы GO-203 в комбинации с ингибитором поли (АДФ-рибозы)-полимеразы (PARP) проявляет противоопухолевую активность, блокируя MUC1-C-индуцированное эпигенетическое перепрограммирование и активируя ответ на повреждение ДНК [23]. В KRAS (Kirsten Rat Sarcoma Virus) мутантной аденокарциноме легких GO-203 подавляет MUC1-индуцированную транскрипцию MYC синергически в сочетании с ингибитором JQ-1 BET (Bromodomain and extra-terminal) [24]. GO-203 также показывает синергизм с леналидомидом и бортезомибом против лекарственноустойчивой множественной миеломы, регулируя TCF4/β-катенин (Фактор транскрипции 4) и механизмы ER/окислительного стресса [25]. GO-203 также оказывает противораковое действие на FLT3 (fms-like tyrosine kinase 3)-мутантный лейкоз и Т-клеточную лимфому [26]. В сочетании с иммунным микроокружением опухоли GO-203 подавляет PD-L1 и индуцирует IFN-γ в немелкоклеточном раке легкого [27].
Избирательное связывание РНК-аптамеров с внеклеточным доменом MUC1 - еще одна стратегия, позволяющая с высокой специфичностью воздействовать на MUC1-сверхэкспрессирующие раковые клетки. Были разработаны MUC1-аптамер-гибридные наночастицы для доставки противоопухолевых микроРНК в MUC1- сверхэкспрессирующие раковые клетки. Эти микроРНК-29b-загруженные гибридные наночастицы (MAFMILHNs) демонстрируют противоопухолевые эффекты в модели рака легких мышей, снижая регулирование DNMT3B (ДНК метилтрансферазы 3 beta), прямой мишени полезной нагрузки микро-РНК [28,29]. Кроме того, при двойной нагрузке, гейстин-микро-РНК-29b-биконьюгатные гибридные наночастицы (GMLHNs) показали больший эффект по сравнению с одиночной нагрузкой наночастицами в модели рака легких мыши, снижая уровни экспрессии AKT, PI3K, DNMT3B и MCL-1 (myeloid cell leukemia sequence 1) [29].
Последние достижения в области технологии антител привели к появлению различных методов лечения на основе антител, таких как ADC, BiTE (Bispecific T-Cell engager) и CAR, а также к нейтрализации терапевтических антител. BM7-PE и M-1231 являются ведущими терапевтическими препаратами ADCs MUC1 в текущих клинических испытаниях. Препарат BM7-PE, разработанный в Университетской больнице Осло (Норвегия), содержит антитела BM7 против MUC1, сопряженные с псевдотоксином A. В доклиническом исследовании BM7-PE показал антиметастатическую эффективность и повысил долгосрочную выживаемость в модели рака молочной железы голой крысы [30]. BM7-PE в настоящее время находится в фазе 1/2 клинических испытаний для метастатического колоректального рака (NCT04550897). М1231 является биспецифическим антитело-лекарственным конъюгатом, направленным на рецептор эпидермального фактора роста и MUC1; в настоящее время он находится в фазе 1 клинических испытаний для различных метастатических твердых опухолей. Pab-001 является первым в своем классе терапевтическим антителом к мишени OT-MUC1 (онко-привязанный MUC1). Высокогликозилированная область трансмембраны MUC1 подвержена расщеплению внеклеточными матричными протеазами. Расщепляемая субъединица MUC1-N высвобождается в кровь, тем самым изолируя антитела против MUC1, которые распознают домен MUC1-N. Pab-001 нацелен на внеклеточную часть расщепляемой субъединицы MUC1-C, чтобы преодолеть этот недостаток [31,32]. Pab-001-MMAE ADC показал многообещающие результаты против TNBC и других видов рака в различных доклинических исследованиях. DS-3939 — это PankoMab-GEX (gatipotuzumab) ADC [33], предназначенный для опухолевоспецифического углеводно-белкового эпитопа муцина (TA-MUC1). Биспецифические антитела с использованием PankoMab находятся в стадии разработки. PM-CD3-GEX - это BiTE, который рекрутирует антиопухолевые CD3+ T-клетки в MUC1-экспрессирующие раковые клетки. PM-IL15-GEX - это иммуноцитокин, который сочетает интерлейкин-15 с PankoMab-GEX для стимуляции анти-опухолевых NK или T-клеток. PM-PDL-GEX -трифункциональное антитело, направленное на MUC1, PD-L1 и FcγR. Ингибирование PD-L1 и активация FcγR действуют как иммуностимуляторы противоопухолевых лейкоцитов.
После замечательных достижений в борьбе с диффузной В-крупноклеточной лимфомой и множественной миеломой для химерных антигенных рецепторов (CAR) ищут новые целевые молекулы, чтобы расширить их применение на солидные опухоли. В настоящее время разрабатываются несколько CAR-терапий, направленных на антиген MUC1, поскольку MUC1 является целевым препаратом из-за его способности к аберрантной экспрессии в различных твердых опухолях. Следует отметить, что базальная экспрессия MUC1 в нормальных тканях может вызывать значительные побочные эффекты. Это привело к разработке новых стратегий анти-MUC1 CAR-терапии, которые призваны обеспечить безопасность и эффективность. О последних достижениях в этой области будет рассказано ниже.
Tn-MUC1 CAR, разработанный Tmunity Therapeutics, является ведущим методом клеточной терапии MUC1 CAR-T, который в настоящее время находится на стадии 1 клинических испытаний (NCT04025216). Из-за того, что Tn (GalNAcα1-O-Ser/Thr) является наиболее распространённой аномальной гликоформой в раковых тканях, Tn-гликоформа MUC1 (Tn-MUC1) является перспективной целью для CAR-терапии. Tn-MUC1 CAR-T показал противоопухолевую активность против Т-клеточных лимфом и опухолей поджелудочной железы [34]. MUC-1 pCAR, разработанный Leucid Bio, является параллельной платформой CAR (pCAR), которая представляет два химерных антиген-рецептора бок о бок с различными антигенсвязывающими доменами и ко-стимулирующими доменами или цитокинстимулирующими рецепторами соответственно (WO2020183158). Эта комбинация двойных рецепторов, как ожидается, даст Т-клеткам больше специфичности против MUC1-положительных опухолей и большую эффективность, чем стандартные CAR-T, которые имеют низкий потенциал против твердых опухолей. Клетки huMNC2-CAR44 T, производимые Minerva Biotechnologies Corp, укрывают scFv против расщепленной формы MUC1, присутствующей на твердых раковых клетках. huMNC2-CAR44 находится в фазе 1 клинических испытаний (NCT04020575) для рака молочной железы, яичников, поджелудочной железы и легких, которые являются MUC1-положительными типами опухоли [35,36]. Клетки NK также считаются хорошими «хозяевами» для CAR терапии. ONKT-103 является MUC1 ориентированной клеточной терапией CAR-NK, разработанной ONK Therapeutics. ONKT-103 максимизирует противоопухолевую активность, вводя DR5-TRAIL вариант сигнального пути рецептора смерти. TRAIL в клетках NK стимулирует рецепторы смерти DR5 раковых клеток и приводит к FADD-каспазе-опосредованному апоптозу. ONKT-103 в настоящее время находится на доклинической стадии и тестируется для терапии рака яичников, груди и легких [37].
Табл. 1 . Современные терапевтические препараты, нацеленные на белок MUC1 [1].
|
Название препарата |
Компан ия |
Тип лекарств а |
Направление |
Статус развития |
Идентифика торы |
Статус набора |
Дата начала испытан ия |
|
BM7-PE |
Госпита ль при Универс итете Осло |
ADC |
Метастатичес кий колоректальн ый рак |
Этап 2 |
NCT04550897 |
Рекрутинг |
31 августа 2020 г. |
|
Gatipotuzuma b (PankoMab-GEX) |
Glycotop e GmbH |
Антитела IgG1 |
Рак яичников на поздней стадии |
Этап 2 |
NCT01899599 |
Завершен |
Сентябрь 2013 |
|
M-1231 |
EMD Serono; Sutro Biophar ma |
ADC |
Метастатичес кий рак |
Этап 1 |
NCT04695847 |
Рекрутинг |
13 января 2021 года |
|
Клеточная терапия Анти-CDЗ/анти-MUC1BiTE CIK |
Benhealt h Biophar maceutic al (Shenzhe n) |
BiTE; Клеточна я терапия |
Метастатичес кий рак |
Этап 2 |
NCT03146637 |
Рекрутинг |
1 мая 2017 г. |
|
GO-203-2C |
Genus Oncolog y LLC |
Пептидны й |
R/R AML |
Этап 2 |
NCT02204085 |
Активный, без рекрутинга |
Сентябрь 2014 |
|
GO-203-2C |
Genus Oncolog y LLC |
Пептидны й |
Твердая опухль |
Этап 1 |
NCT01279603 |
Завершенн ый |
19 января 2011 года |
|
huMNC2-CAR44 T cells |
Minerva Biotechn ologies Corp. |
CAR-T |
Рак |
Этап 1 |
NCT04020575 |
Рекрутинг |
15 января 2020 г. |
|
Tn MUC-1 CAR-T |
Tmunity Therapeu tics |
CAR-T |
Рак |
Этап 1 |
NCT04025216 |
Рекрутинг |
10 октября 2019 г. |
|
Клеточнаяте рапияAnti-MUC1 CART (w or w/o) PD-1 knockout T cell |
Guangzh ou Anjie Biomedi cal Technolo gy |
CAR-T |
Метастатичес кий рак |
Этап 2/3 |
NCT03525782 |
Рекрутинг |
1 февраля 2018 г. |
Заключение
Несмотря на активное изучение роли MUC1 в связи с прогрессией рака и его полезности в качестве биомаркера, качественное и количественное обнаружение MUC1 в опухолевых клетках стало возможным только после разработки специфических детекторов. Несмотря на достигнутые успехи, детальные механизмы, с помощью которых MUC1 проявляет свою активность, остаются в значительной степени неизученными. В настоящее время разрабатываются вакцины и антитела против MUC1, и некоторые из них продемонстрировали значительный терапевтический эффект и сейчас проходят I/II фазу клинических испытаний, однако их побочные эффекты и вопросы клинической безопасности требуют дальнейшего изучения и подтверждения.
Вклад авторов. В.К. Боженко: концепция и подбор литературных источников, анализ информации, корректировка рукописи; И.Х. Уразаева: подбор литературных источников, написание текста статьи, корректировка рукописи; Р. Ранджит: подбор литературных источников, корректировка рукописи; Е.А. Кудинова: анализ представленных литературных данных, обоснование актуальности выбранной тематики, корректировка рукописи. Все авторы прочитали и согласились с версией рукописи, представленной для публикации. Все авторы ознакомились и согласились с представленным к публикации вариантом рукописи.
В.К. Боженко и И.Х. Уразаева внесли равный вклад в данное исследование.
Финансирование. Публикация подготовлена в рамках Государственного задания № 1022040800109-5-3.2.21.
Соблюдение прав пациентов и правил биоэтики. Данное обзорное исследование было основано на опубликованных работах и поэтому не требовало одобрения этического комитета.
Список литературы MUC1 антиген как иммунотерапевтическая мишень
- Lee DH, Choi S, Park Y, Jin HS. Mucin1 and Mucin16: Therapeutic Targets for Cancer Therapy. Pharmaceuticals (Basel). 2021 Oct;14(10):1053. doi: 10.3390/ph14101053.
- Bhatia R, Gautam SK, Cannon A, Thompson C, Hall BR, Aithal A, et al. Cancer-associated mucins: role in immune modulation and metastasis. Cancer Metastasis Rev. 2019 Jun;38(1-2):223-236. doi: 10.1007/s10555-018-09775-0.
- Dhanisha SS, Guruvayoorappan C, Drishya S, Abeesh P. Mucins: Structural diversity, biosynthesis, its role in pathogenesis and as possible therapeutic targets. Crit Rev Oncol Hematol. 2018 Feb;122:98-122. doi: 10.1016/j.critrevonc.2017.12.006.
- Hattrup CL, Gendler SJ. Structure and function of the cell surface (tethered) mucins. Annu Rev Physiol. 2008;70:431-457. doi: 10.1146/annurev.physiol.70.113006.100659.
- 5. Syrkina MS, Maslakova AA, Potashnikova DM, Veiko VP, Vassetzky YS, Rubtsov MA. Dual Role of the Extracellular Domain of Human Mucin MUC1 in Metastasis. J Cell Biochem. 2017 Nov;118(11):4002-4011. doi: 10.1002/jcb.26056.
- Khodabakhsh F, Merikhian P, Eisavand MR, Farahmand L. Crosstalk between MUC1 and VEGF in angiogenesis and metastasis: a review highlighting roles of the MUC1 with an emphasis on metastatic and angiogenic signaling. Cancer Cell Int. 2021 Apr;21(1):200. doi: 10.1186/s12935-021-01899-8.
- Nath S, Mukherjee P. MUC1: a multifaceted oncoprotein with a key role in cancer progression. Trends Mol Med. 2014 Jun;20(6):332-342. doi: 10.1016/j.molmed.2014.02.007.
- Chen W, Zhang Z, Zhang S, Zhu P, Ko JK, Yung KK. MUC1: Structure, Function, and Clinic Application in Epithelial Cancers. Int J Mol Sci. 2021 Jun;22(12):6567. doi: 10.3390/ijms22126567.
- Kashyap B, Kullaa AM. Regulation of mucin 1 expression and its relationship with oral diseases. Arch Oral Biol. 2020 Sep;117:104791. doi: 10.1016/j.archoralbio.2020.104791.
- Johansson ME, Sjövall H, Hansson GC. The gastrointestinal mucus system in health and disease. Nat Rev Gastroenterol Hepatol. 2013 Jun;10(6):352-361. doi: 10.1038/nrgastro.2013.35.
- Yen JH, Xu S, Park YS, Ganea D, Kim KC. Higher susceptibility to experimental autoimmune encephalomyelitis in Muc1-deficient mice is associated with increased Th1/Th17 responses. Brain Behav Immun. 2013 Mar;29:70-81. doi: 10.1016/j.bbi.2012.12.004.
- Wang YM, Qi X, Gong FC, Chen Y, Yang ZT, Mao EQ, Chen EZ. Protective and predictive role of Mucin1 in sepsis-induced ALI/ARDS. Int Immunopharmacol. 2020 Jun;83:106438. doi: 10.1016/j.intimp.2020.106438.
- Gunda V, Souchek J, Abrego J, Shukla SK, Goode GD, Vernucci E, Dasgupta A, et al. MUC1-Mediated Metabolic Alterations Regulate Response to Radiotherapy in Pancreatic Cancer. Clin Cancer Res. 2017 Oct;23(19):5881-5891. doi: 10.1158/1078-0432.CCR-17-1151.
- Caffrey T, Sagar S, Thomas D, Lewallen ME, Hollingsworth MA, Radhakrishnan P. The glycoprotein mucin-1 negatively regulates GalNAc transferase 5 expression in pancreatic cancer. FEBS Lett. 2019 Oct;593(19):2751-2761. doi: 10.1002/1873-3468.13532.
- Kitamoto S, Yokoyama S, Higashi M, Yamada N, Takao S, Yonezawa S. MUC1 enhances hypoxia-driven angiogenesis through the regulation of multiple proangiogenic factors. Oncogene. 2013 Sep;32(39):4614-4621. doi: 10.1038/onc.2012.478.
- Bouillez A, Rajabi H, Pitroda S, Jin C, Alam M, Kharbanda A, et al. Inhibition of MUC1-C Suppresses MYC Expression and Attenuates Malignant Growth in KRAS Mutant Lung Adenocarcinomas. Cancer Res. 2016 Mar;76(6):1538-1548. doi: 10.1158/0008-5472.CAN-15-1804.
- Sousa AM, Rei M, Freitas R, Ricardo S, Caffrey T, David L, et al. Effect of MUC1/β-catenin interaction on the tumorigenic capacity of pancreatic CD133+ cells. Oncol Lett. 2016 Sep;12(3):1811-1817. doi: 10.3892/ol.2016.4888.
- Deng J, Wang L, Chen H, Li L, Ma Y, Ni J, Li Y. The role of tumour-associated MUC1 in epithelial ovarian cancer metastasis and progression. Cancer Metastasis Rev. 2013 Dec;32(3-4):535-551. doi: 10.1007/s10555-013-9423-y.
- Chen W, Zhang Z, Zhang S, Zhu P, Ko JK, Yung KK. MUC1: Structure, Function, and Clinic Application in Epithelial Cancers. Int J Mol Sci. 2021 Jun;22(12):6567. doi: 10.3390/ijms22126567.
- Gendler SJ, Lancaster CA, Taylor-Papadimitriou J, Duhig T, Peat N, Burchell J, et al. Molecular cloning and expression of human tumor-associated polymorphic epithelial mucin. J Biol Chem. 1990 Sep;265(25):15286-15293.
- Gao T, Cen Q, Lei H. A review on development of MUC1-based cancer vaccine. Biomed Pharmacother. 2020 Dec;132:110888. doi: 10.1016/j.biopha.2020.110888.
- Singh R, Bandyopadhyay D. MUC1: a target molecule for cancer therapy. Cancer Biol Ther. 2007 Apr;6(4):481-486. doi: 10.4161/cbt.6.4.4201.
- van Putten JPM, Strijbis K. Transmembrane Mucins: Signaling Receptors at the Intersection of Inflammation and Cancer. J Innate Immun. 2017;9(3):281-299. doi: 10.1159/000453594.
- Marczynski M, Jiang K, Blakeley M, Srivastava V, Vilaplana F, Crouzier T, Lieleg O. Structural Alterations of Mucins Are Associated with Losses in Functionality. Biomacromolecules. 2021 Apr;22(4):1600-1613. doi: 10.1021/acs.biomac.1c00073.
- Yin L, Kufe T, Avigan D, Kufe D. Targeting MUC1-C is synergistic with bortezomib in downregulating TIGAR and inducing ROS-mediated myeloma cell death. Blood. 2014 May;123(19):2997-3006. doi: 10.1182/blood-2013-11-539395.
- Jain S, Washington A, Leaf RK, Bhargava P, Clark RA, Kupper TS, et al. Decitabine Priming Enhances Mucin 1 Inhibition Mediated Disruption of Redox Homeostasis in Cutaneous T-Cell Lymphoma. Mol Cancer Ther. 2017 Oct;16(10):2304-2314. doi: 10.1158/1535-7163.MCT-17-0060.
- Bouillez A, Adeegbe D, Jin C, Hu X, Tagde A, Alam M, et al. MUC1-C promotes the suppressive immune microenvironment in non-small cell lung cancer. Oncoimmunology. 2017 Jul;6(9):e1338998. doi: 10.1080/2162402X.2017.1338998.
- Perepelyuk M, Sacko K, Thangavel K, Shoyele SA. Evaluation of MUC1-Aptamer Functionalized Hybrid Nanoparticles for Targeted Delivery of miRNA-29b to Nonsmall Cell Lung Cancer. Mol Pharm. 2018 Mar;15(3):985-993.
- Sacko K, Thangavel K, Shoyele SA. Codelivery of Genistein and miRNA-29b to A549 Cells Using Aptamer-Hybrid Nanoparticle Bioconjugates. Nanomaterials (Basel). 2019 Jul;9(7):1052. doi: 10.3390/nano9071052.
- Engebraaten O, Sivam G, Juell S, Fodstad O. Systemic immunotoxin treatment inhibits formation of human breast cancer metastasis and tumor growth in nude rats. Int J Cancer. 2000 Dec 15;88(6):970-976. doi: 10.1002/1097-0215(20001215)88:6<970::aid-ijc21-3.0.co;2-q.
- Bouillez A, Rajabi H, Pitroda S, Jin C, Alam M, Kharbanda A, et al. Inhibition of MUC1-C Suppresses MYC Expression and Attenuates Malignant Growth in KRAS Mutant Lung Adenocarcinomas. Cancer Res. 2016 Mar;76(6):1538-1548. doi: 10.1158/0008-5472.CAN-15-1804.
- Yamamoto M, Jin C, Hata T, Yasumizu Y, Zhang Y, Hong D, et al. MUC1-C Integrates Chromatin Remodeling and PARP1 Activity in the DNA Damage Response of Triple-Negative Breast Cancer Cells. Cancer Res. 2019 Apr;79(8):2031-2041. doi: 10.1158/0008-5472.CAN-18-3259.
- Danielczyk A, Stahn R, Faulstich D, Löffler A, Märten A, Karsten U, Goletz S. PankoMab: a potent new generation anti-tumour MUC1 antibody. Cancer Immunol Immunother. 2006 Nov;55(11):1337-1347. doi: 10.1007/s00262-006-0135-9.
- Posey AD Jr, Schwab RD, Boesteanu AC, Steentoft C, Mandel U, Engels B, et al. Engineered CAR T Cells Targeting the Cancer-Associated Tn-Glycoform of the Membrane Mucin MUC1 Control Adenocarcinoma. Immunity. 2016 Jun;44(6):1444-1454. doi: 10.1016/j.immuni.2016.05.014.
- Ahmad R, Alam M, Hasegawa M, Uchida Y, Al-Obaid O, Kharbanda S, Kufe D. Targeting MUC1-C inhibits the AKT-S6K1-elF4A pathway regulating TIGAR translation in colorectal cancer. Mol Cancer. 2017 Feb;16(1):33. doi: 10.1186/s12943-017-0608-9.
- Shigeta K, HasegawaM, Kikuchi E, Yasumizu Y, Kosaka T, Mizuno R, et al. Role of the MUC1-C oncoprotein in the acquisition of cisplatin resistance by urothelial carcinoma. Cancer Sci. 2020 Oct;111(10):3639-3652. doi: 10.1111/cas.14574.
- Wu G, Maharjan S, Kim D, Kim JN, Park BK, Koh H, et al. A Novel Monoclonal Antibody Targets Mucin1 and Attenuates Growth in Pancreatic Cancer Model. Int J Mol Sci. 2018 Jul; 19(7):2004. doi: 10.3390/ijms19072004.


