Мультиспиральная компьютерная томография в диагностике лимфедемы нижних конечностей
Автор: Бардаков В.Г., Апханова Татьяна Валерьевна, Бадтиева В.А., Бронов О.Ю.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 3 т.7, 2012 года.
Бесплатный доступ
В статье проанализированы результаты мультиспиральной компьютерной томографии 20 больных лимфедемой нижних конечностей I-III клинических стадий. Целью настоящей работы явилось изучение данных компьютерной томографии больных лимфедемой нижних конечностей для определения закономерностей патологических изменений и их структуры в зависимости от формы и стадии заболевания. Установлено, что МСКТ при лимфедеме позволяет, с высокой степенью разрешения, визуализировать изменения подкожной жировой клетчатки и соединительнотканных образований в над- и субфасциальных пространствах конечностей. Прогрессирование заболевания сопровождается усилением фиброза и склероза кожи, подкожной жировой клетчатки, фасций и перимускулярного ложа. Для определения первичного или вторичного характера заболевания необходимо проведение комплексного обследования с проведением лимфосцинтиграфии и КТ регионарных лимфоузлов и области таза. Данные МСКТ представляет важную информацию для дифференциальной диагностики классической лимфедемы и различных комбинированных форм хронического лимфатического отека. Изменения подкожного пространства в виде «сотовой» структуры, утолщение кожи за счет ее фибросклероза, выявляемые при классической лимфедеме, не характерны для флеболимфедемы и липолимфедемы, что важно для установления причины лимфатического отека и определения тактики ведения больного.
Мультиспиральная компьютерная томография, лимфедемы нижних конечностей, флеболимфедема, липолимфедема
Короткий адрес: https://sciup.org/140188081
IDR: 140188081 | УДК: 616.718-073.756.8
Multispiral computed tomography in diagnosis of lymphedema of lower extremities
The paper analyzes the results of Multislice Computed Tomography in 20 patients with lower extremities lymphedema of I-III clinical stages. The objectiveis to study the CT scans of patients with lymphedema of the lower extremities with certain patterns of pathological changes and their structure depending on the form and stage of disease. Found that MSCT allows for lymphedema, high resolution, to visualize changes in subcutaneous fat and connective tissue formations in the supra-and subfascial space of the limbs. Disease progression was accompanied by increased fibrosis and sclerosis of the skin, subcutaneous fat, fascia and perimuskulyarnogo bed. To determine the primary or secondary nature of the disease is necessary to conduct a comprehensive survey of holding lymphoscintigraphy and CT of regional lymph nodes and pelvis. MSCT data provides important information for differential diagnosis of lymphedema and the classic combination of various forms of chronic lymphatic edema. Changes in the subcutaneous space in the form of "honeycomb” structure, observed in the classical lymphedema, are not typical for flebolymphedema and lipolymphedema and that it was important to establish the cause lymph edema and to determine the tactics of the patient’s treatment. CT as the method can be used to diagnose obstructive lymphedema, demonstrating the presence or absence of changes in the pelvis, which may cause lymphatic obstruction.
Текст научной статьи Мультиспиральная компьютерная томография в диагностике лимфедемы нижних конечностей
Классическая лимфедема нижних конечностей – это хроническое прогрессирующее заболевание, обусловленное лимфатической недостаточностью с низким выбросом, при которой нормальная лимфатическая нагрузка превышает сниженную транспортную емкость измененных лимфатических сосудов. По происхождению выделяют первичную и вторичную лимфедему. Причиной первичного варианта заболевания являются генетически обусловленные дефекты лимфатической системы вследствие дисплазии лимфатических сосудов или узлов. К вторичному поражению приводят нарушение целостности или удаление лимфатических сосудов и узлов – после травм, воспалительных заболеваний (лимфаденитов, лимфангитов), оперативных вмешательств с проведением радикальной лимфаденэктомии регионарных лимфатических узлов или лучевой терапии по поводу злокачественных новообразований [12]. В последнее время в практической работе все чаще встречаются комбинированные формы лимфедемы (флеболимфедема, липолимфедема, комбинированные ангиодисплазии, лимфедема на фоне ревматоидного артрита и др.), которые возникают при сочетании поражения лимфатических сосудов с какой-либо патологией, увеличивающей жидкостную и белковую нагрузку на измененные лимфатические пути.
От постановки правильного и точного диагноза лимфедемы с установлением стадии и формы заболевания зависит выбор адекватной тактики и схемы лечения. Поэтому дифференциальная диагностика первичной и вторичной форм лимфедемы остается актуальной проблемой лимфологии. Несмотря на развитие новых методов визуализации, диагностика расстройств периферического лимфатического транспорта до сих пор основана в основном на клинических исследованиях (жалобы, анамнез, характерные изменения при осмотре, линейный и объемные измерения конечностей). Между тем, в развитых странах ежегодно растет число пациентов с вторичной лимфедемой, обусловленной диссекцией, облучением или метастазированием в регионарные лимфатические узлы рака различной локализации. В странах третьего мира частой причиной лимфедемы по-прежнему являются филяриоз или инфекции [14]. Прежде чем начать лечение, которое скорее всего будет пожизненным и может оказаться неэффективными или даже вредным, если диагноз лимфедема является неполным или неправильным, даже при относительно «простых» ситуациях,

необходимо подтверждение диагноза лимфедемы с точным определением анатомо-физиологических изменений лимфатических сосудов, узлов и мягких тканей пораженной конечности [7].
Согласно рекомендациям Международного общества лимфологов (2009), алгоритм диагностики лимфедемы включает следующие ступени [12]:
-
1. Установление отека конечности (физикальное исследование и анамнез);
-
2. Исключение всех других причин отека, кроме лимфатического (тромбоз глубоких вен, варикозная болезнь, сердечная недостаточность, нефротический синдром, предменструальный синдром, опухоли, инфекции, прием гипотензивных препаратов);
-
3. Определение первичного или вторичного генеза лимфедемы.
Дифференциальный диагноз первичного генеза лимфедемы всегда был связан с проблемами визуализации лимфатической системы [7]. На смену прямой контрастной лимфографии с применением липиодола, являвшейся обязательным методом диагностики до 80-х годов ХХ века, пришла изотопная лимфосцинтиграфия. Прямая лимфография в настоящее время практически повсеместно не используется из-за высокой инвазив-ности (требует хирургического вмешательства) и высокого риска осложнений (инфицирование, повреждение эндотелия лимфатических сосудов жирорастворимыми контрастными препаратами, анафилактические реакции) [13]. Лимфосцинтиграфия (ЛСГ) позволяет выявить функциональные нарушения в лимфатической системе, визуализировать лимфоток без катетеризации лимфатических сосудов, что устраняет риск дополнительного их повреждения. Лимфосцинтиграфия дает возможность получить не только качественные (четкое контрастирование лимфатических сосудов и узлов), но и количественные данные о транспорте лимфы. С помощью ЛСГ возможно диагностировать латентную стадию лимфедемы. При проведении ЛСГ оценивается клиренс радиофармпрепарата (РФП), скорость попадания РФП в лимфатические узлы, а также количество поглощенного ими РФП. За счет минимальной инвазивности, изотопная лимфография (ЛСГ) – в настоящее время является одним из основных методов визуализации при лимфедеме [11, 12].
И все же ЛСГ является инвазивной методикой, так как связана с весьма болезненным внутрикожным введением радиоизотопных меченных коллоидов (Tехнеция 99) в 1-й межпальцевой промежуток стоп пораженной и здоровой конечностей.
Действительно неинвазивным методом диагностики, позволяющим визуализировать патологические изменения мягких тканей и лимфатических узлов при лимфедеме с высокой точностью, в настоящее время является высокотехнологичный метод компьютерной томографии (КТ) [4, 7].
В опубликованных ранее российских исследованиях, посвященных применению КТ для диагностики лимфе- демы нижних конечностей, были исследованы лишь изменения толщины кожи, подкожно-жировой клетчатки, описаны проявления фиброза при разных клинических стадиях. [1, 3, 5, 6]. КТ применялась также для оценки качественных и количественных изменений в тканях конечностей больных лимфедемой после хирургического лечения [1, 4].
Российских исследований, посвященных применению МСКТ для дифференциальной диагностики периферической лимфедемы, в том числе комбинированных форм лимфатических отеков, мы не встретили.
Между тем, по данным зарубежных исследователей, компьютерная томография (КТ) позволяет отличить лимфедему от отёков другой этиологии, а в некоторых случаях установить причину лимфатических отеков [8, 10, 13].
Создание в 1989 г. спиральной технологии и на рубеже веков многосрезовой методики (16, 64- МСКТ) принципиально изменило диагностические подходы ко многим заболеваниям [2, 9].
Спиральная томография дает возможность непрерывно сканировать тело пациента во время постоянного линейного движения стола (спиралевидное движение веерообразного луча через тело пациента) и исследовать одну анатомическую область за один период задержки дыхания с получением тонких соприкасающихся срезов, при этом практически полностью исключаются пропуски небольших патологических объектов. В настоящее время стандартом КТ является обследование с помощью многосрезового томографа с возможностью получения до 64 срезов с временным разрешением 0,1–0,5 сек. (минимально доступная длительность одного оборота рентгеновской трубки составляет 0,3 сек.), Длительность томографии всего тела с толщиной среза менее 1 мм составляет около 10–15 секунд, а результатом исследования являются от нескольких сотен до нескольких тысяч изображений.
Преимущества МСКТ по сравнению с другими диагностическими методами очевидны, что определяет высокую клиническую значимость метода.
Преимущества МСКТ:
-
– высокое пространственное разрешение;
-
– быстрота обследования;
-
– возможность 3-мерной и многоплоскостной реконструкции изображений;
-
– низкая оператор-зависимость метода;
-
– возможность стандартизации исследования;
– возможность визуализации измененных регионарных лимфоузлов и других висцеральных причин лимфатической обструкции (метастазы, лимфомы, лимфоцеле).
Современная МСКТ является практически безопасным методом диагностики, приемлемым для большинства пациентов. Относительными противопоказаниями для КТ-исследования могут быть беременность и непереносимостью контрастных препаратов. Несмотря на
высокую стоимость, присущие МСКТ оптимальное соотношение стоимость/эффективность, высокая клиническая значимость и неинвазивность определяют продолжающееся развитие и распространение метода.
Целью настоящей работы явилось изучение данных компьютерной томографии больных лимфедемой нижних конечностей для определения закономерностей патологических изменений и их структуры в зависимости от формы и стадии заболевания.
Материалы и методы
Обследовано 20 пациентов с лимфедемой нижних конечностей I–III стадий (по классификации Савченко Т.В., Покровского А.В., 2004). Из них 17 женщин и 3 мужчин, в возрасте от 18 до 73 лет (средний возраст – 43 года).
Длительность заболевания составляла от 2 до 48 лет. Двухстороннее поражение конечностей наблюдалось у 8 из них. Первичной лимфедемой страдало 8 больных, вторичной – 12 пациентов (4 с флеболимфедемой, 2 с посттравматической лимфедемой, 2 с лимфедемой на фоне лимфаденита паховых лимфатических узлов, 3 с липолимфедемой и 1 с выраженной двухсторонней лимфедемой после тотальной гистерэктомии с последующей лучевой терапией по поводу рака тела матки). Клинический диагноз первичной лимфедемы был подтвержден методом лимфосцинтиграфии у всех 8 пациентов. 4 больных лечились хирургически (у 2 были выполнены реконструктивные операции на глубоких и перфорантных венах, у 1 пациентки – лимфовенозные анастомозы и в одном случае произведена односторонняя липодер-мофасцэктомия). Результаты хирургического лечения у всех больных не принесли желаемого эффекта, а у 2 пациентов способствовали быстрому прогрессированию заболевания.
МСКТ проводилась на базе рентгенологического отделения отдела лучевой диагностики ФГБУ «НМХЦ им. Н.И. Пирогова» на современном 64-спиральном компьютерном томографе «PHILIPS BRILLIANCE 64», толщина срезов – 3 мм, позволяющем получать мультиспиральные срезы очень высокого разрешения с очень высокой скоростью, что значительно снижало лучевую нагрузку.
Результаты
Результаты проведенного анализа представлены в таблице.
При анализе представленных в таблице данных, во всех случаях у пациентов с лимфедемой (вне зависимости от этиологии) было выявлено утолщение кожи, более выраженное при III стадии (до 4–5 мм). Толщина кожи составила в среднем 3,0 ± 0,36 мм (при норме 1,0 ± 0,10 мм) p < 0,01 (Рис. 1).
Увеличение толщины подкожного пространства наблюдалось также во всех случаях, более выраженное при III-IV стадиях, в среднем до 26,9 ± 3,2 (p < 0,05). В 13 из 20 случаев отмечались характерные изменения подкожной ткани в виде «сотовой» структуры, образованные
КТ-признаки дифференциальной диагностики лимфедемы
Причем, характерная «сотовая» структура была более выраженной при II–III стадиях заболевания. У больного с III–IV стадией вторичной лимфедемы выявлено резкое усиление плотности (D) подкожных тканей до (минус) –7,0 (–3,0) HU, за счет выраженного фибросклероза подкожно-жировой клетчатки, фасций и перимускулярного ложа (Рис. 3, 4).
Расширения субфасциального пространства у больных лимфедемой не отмечалось. При КТ-анализе субфасциального пространства (в том числе мышечного компонента) не выявлено увеличения или отека скелетных мышц, что совпадает с данными других исследователей, и подтверждает, что при лимфедеме в первую очередь наблюдаются патологические фиброзно-склеротические изменения кожи и подкожной клетчатки.
КТ у больных с флеболимфедемой показала расширение подкожного пространства, субфасциального пространства, расширение подкожных вен в исследуемой области и утолщение кожи у всех 3 пациентов, характерное изменение подкожного пространства в виде «сотовой» структуры было выявлено лишь у 1 из 3 пациентов. Плотность подкожного пространства (D), составила –65,1 ±8,4 HU, что соответствует по шкале Хаунсфильда усредненной плотности жира и жидкости с высоким содержанием белка (плотность жидкости от –20 до +25 HU) (Риc. 5).
КT при липолимфедеме выявила расширение подкожного пространства, за счет разрастания жировой ткани, но при этом не отмечалось утолщения кожи и
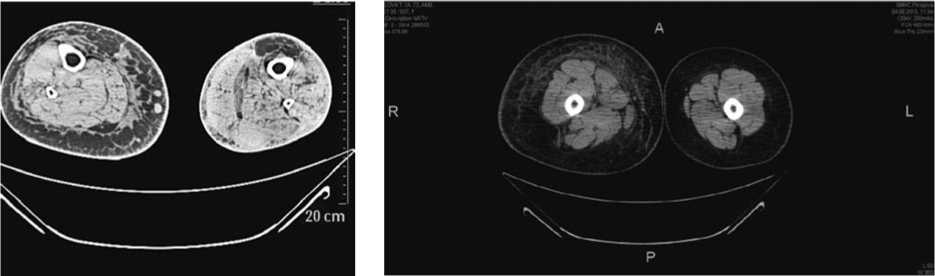
Рис. 1. КТ-изображение Больной первичной лимфедемой нижних конечностей III стадии. Определяется выраженное утолщение кожи, подкожного пространства, «сотовая» структура подкожно-жирового пространства
Рис. 2. КТ-изображение Больной вторичной лимфедемой II стадии. Справа определяется утолщение кожи, подкожного пространства, «сотовая» структура подкожно-жировой клетчатки. Мышечный компонент не изменен
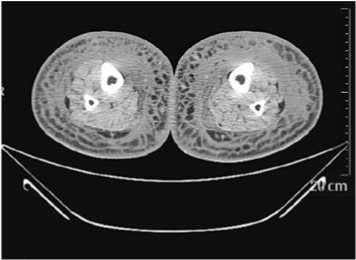
Рис. 3. КТ-изображение больного с III стадией вторичной лимфедемы. Определяется выраженное утолщение кожи, подкожного пространства, выраженный фиброз кожи, подкожно-жировой ткани, фасций
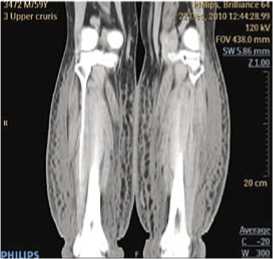
Рис. 4. Фронтальная КТ реконструкция больного с Ш стадией вторичной лимфедемы
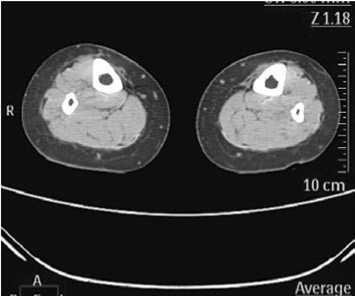
Рис. 5. КТ-изображение больной с флеболифе-демой. Кожа не утолщена, увеличено подкожное пространство, отсутствует» сотовая» структура. Определяются расширенные подкожные вены
расширения субфасциального пространства. Плотность подкожного пространства (D), измеренная по шкале Ха-унсфильда, составила –102,2 ± 0,85 HU, что соответствует плотности жировой ткани (–100 HU) и обусловлено разрастанием подкожно-жировой клетчатки (Рис. 6, 7).
Заключение
С помощью МСКТ при лимфедеме возможна четкая, с высокой степенью разрешения, визуализация изменений подкожной жировой клетчатки и соединительнотканных образований в над- и субфасциальных пространствах конечностей. Выраженность КТ симптомов лимфедемы пропорциональна стадии заболевания. Прогрессирование заболевания сопровождается усилением фиброза и склероза кожи, подкожной жировой клетчатки, фасций и перимускулярного ложа. Однако, КТ-признаки лимфедемы не позволяют выявить ее генез. Для определения первичного или вторичного характера заболевания необходимо проведение комплексного обследования с проведением лимфосцинтиграфии и КТ регионарных лимфоузлов и области таза.
Данные МСКТ представляет важную информацию для дифференциальной диагностики классической лимфедемы и различных комбинированных форм хронического лимфатического отека. Изменения подкожного пространства в виде «сотовой» структуры, утолщение кожи за счет ее фибросклероза, выявляемые при классической лимфедеме, не характерны для флеболимфедемы и липолимфедемы, что важно для установления причины лимфатического отека и определения тактики ведения больного.
Метод КТ может также применяться для диагностики обструктивной лимфедемы, демонстрируя наличие или отсутствие изменений в малом тазу, которые могут быть причиной лимфатической обструкции.
Таким образом, метод МСКТ, как относительно доступный и неинвазивный, необходим для дополнительной визуализации анатомо-физиологических изменений

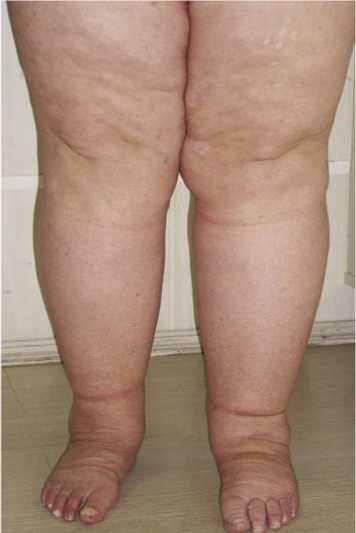
Рис. 6. Фото больной с липолимфедемой
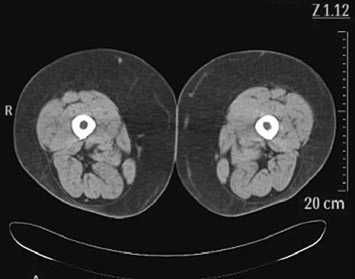
Рис. 7. КТ этой же больной с липолимфедемой. Определяется резкое утолщение подкожножирового пространства за счет разрастания жировой ткани. Утолщения кожи не определяется. «Сотовая» структура подкожного пространства отсутствует
при лимфедеме для установления более точного клинического диагноза (с определением формы и стадии) и определения дальнейшей тактики комплексного лечения.
Список литературы Мультиспиральная компьютерная томография в диагностике лимфедемы нижних конечностей
- Жданова О.А. Магнитно-резонанснотомографическая диагностика лимфедемы нижних конечностей./Автореф. дис..канд.мед.наук. М., 1996. -25 с.
- Кармазановский Г.Г. Компьютерная томография -перспективы развития в третьем тысячелетии.//Медицинская визуализация, апрель-июнь 1998. -С. 24-26.
- Кармазановский Г.Г., Савченко Т.В. Компьютерно-томографическая симптоматика лимфедемы нижних конечностей.//Вестник рентгенологии и радиологии. -1991, № 6. -С. 42-50.
- Кармазановский Г.Г., Савченко Т.В. Оценка результатов хирургического лечения лимфедемы по данным компьютерной томографии.//Хирургия. -1996, № 2. -С. 71-73.
- Поташов Л.В., Бубнова Н.А. и др. Хирургическая лимфология. СПб: Изд-во СПбГЭТУ «ЛЭТИ», 2000. -С. 7-75.
- Фионик О.В., Семенов А.Ю., Бубнова Н.А., Петров С.В. Патогенетические принципы диагностики и лечения лимфедемы нижних конечностей.//Вестник Санкт-Петербургского университета. Сер.11, 2006, вып. 3. -С. 68-72.
- Charles L. Witte, Marlys H. Witte, Evan C. Unger et all. Advances in Imaging of lymph Flow Disorders.//Radiographics, 20, 1697-1719. November 2000.
- E.D. Monnin-Ddelhom, B.P. Gallix,C.Achard et all. High resolution unenhanced computed tomography in patients with swollen legs. Lymphology 35 (2002) 121-128.
- Zonneveld F.W. Современное состояние и будущее компьютерной томографии.//Медицинская визуализация, январь-март 1999. -С. 44-56.
- Hadjis N.S., Carr D.H., Banks Linda at all. The Role of CT in the Diagnosis of Primary Lymphedema of the lower Limb. AJR Am J Roentgenol.1985; 144: 361-364.
- Robert J. Damsrta. Diagnostic and therapeutical aspects of lymphedema./Rabe Medical Publishing, Bonn, Germany. -2010. -Р. 34-44.
- The Diagnosis and Treatment of Peripheral Lymphedema. 2009 Consensus Document of the International Society of Lymphology. Lymphology 42(2009).
- The Diagnosis and Treatment of Secondary Lymphedema. Technology Assessment report by Department of Health and Human Services of USA, 28 May, 2010.
- World Health Report 2002: Reducing Risk and Promoting Healthy Life. World Health Organization, Geneva, Switzerland.


