Научно-методологический подход к утилизации фармацевтических отходов на основе биотехнологий и математического моделирования
Автор: Вихарева Е.В.
Журнал: Российский журнал биомеханики @journal-biomech
Статья в выпуске: 3 (41) т.12, 2008 года.
Бесплатный доступ
Представлен разработанный авторами научно-методологический подход к утилизации некачественных лекарственных средств на основе использования микроорганизмов и математического моделирования, обеспечивающий возможность превращения опасных фармацевтических отходов в безопасные для окружающей природной среды. На примере парацетамола предложен алгоритм биодеструкции лекарственных средств, содержащих фенольную гидроксильную группу, актинобактериями рода Rhodococcus. Алгоритм предусматривает использование математической модели, представляющей собой систему кинетических уравнений, адекватно описывающих процесс биодеструкции свободными и иммобилизованными клетками родококков. Модель позволяет прогнозировать поведение исходных лекарственных средств и продуктов их разложения по установленным схемам реакций и найденным константам скоростей, а также окончание процесса биодеструкции и осуществлять переход к проведению его в полупромышленных и промышленных условиях.
Фармацевтические отходы, парацетамол, p-аминофенол, биодеструкция, родококки, константа скорости реакции, математическое моделирование, кинетические показатели
Короткий адрес: https://sciup.org/146215925
IDR: 146215925 | УДК: 531/534:
Текст научной статьи Научно-методологический подход к утилизации фармацевтических отходов на основе биотехнологий и математического моделирования
Актуальной проблемой, возникающей при уничтожении отходов, является обеспечение экологической безопасности используемых технологий. При выборе наиболее эффективных способов обезвреживания определенных категорий опасных отходов предпочтение отдается биотехнологическим способам. В настоящее время в России и за рубежом отсутствуют биотехнологические способы утилизации опасных фармацевтических отходов, в том числе непригодных к медицинскому использованию лекарственных средств – фальсифицированных, забракованных, с истекшим сроком годности и пр. Данные лекарственные средства относятся в основном к первому или второму классам опасности и подлежат обязательному уничтожению. Однако рекомендуемые методы их утилизации (слив в канализацию, сжигание и захоронение на санитарных полигонах) не являются экологически безопасными.
Как показано нами ранее [5, 6], технологически перспективными для осуществления направленных биотрансформаций лекарственных веществ, содержащих в своей структуре фенольную гидроксильную группу (в частности, парацетамола, ацетилсалициловой кислоты, салициловой кислоты и др.), являются актинобактерии рода Rhodococcus [7]. Для расширения объектов биодеструкции среди лекарственных средств необходим единый методологический подход к утилизации фармацевтических отходов, обеспечивающий возможность превращения их в безопасные для окружающей природной среды соединения.
В связи с этим цель настоящих исследований – разработка научнометодологического подхода к утилизации некачественных лекарственных средств, производных фенола, на основе использования микроорганизмов и математического моделирования.
Материалы и методы
В работе применяли традиционные методы бактериологии, в том числе метод кометаболизма, метод биотрансформации веществ с использованием покоящихся и иммобилизованных бактериальных клеток. Для закрепления клеток использовали способ включения их в криогель поливинилового спирта [10] и сорбционный метод иммобилизации родококков на твердых носителях. С целью повышения сродства поверхности адсорбентов к бактериальным клеткам использовали прием гидрофобизации поверхности носителя с помощью Rhodococcus -биосурфактантов. Оценку интенсивности адгезии бактериальных клеток на модифицированной поверхности твердых носителей проводили методами инфракрасного сканирования и профилометрии высокого разрешения с использованием инфракрасной камеры CEDIP Silver 450 M ( CEDIP Infrared Systems , Франция) и интерференционного микроскопа NewView 5000 ( Zygo Corporation , США) соответственно. Оптимизацию процесса биодеструкции парацетамола с использованием иммобилизованного биокатализатора проводили в условиях лабораторного биореактора. О скорости процесса биодеградации лекарственных веществ судили по степени их убыли из среды культивирования родококков, регистрируемой методом высокоэффективной жидкостной хроматографии с использованием хроматографа модели HP -1090 ( Hewlett Packard , США) и колонки ZORBAX SB–C 18 (4,6×250 мм, 5 µм), заполненной октадецильной привитой фазой [6]. Количественное содержание первичного метаболита p -аминофенола в культуральных жидкостях определяли фотометрическим методом с помощью спектрофотометра типа Lambda EZ 201 ( Perkin-Elmer , США) при λ = 450 нм на основе цветной реакции конденсации p -аминофенола с п -диметиламинобензальдегидом [6]. Класс опасности культуральной жидкости и шлама после биодеструкции парацетамола определяли расчетным методом в соответствии с [11] на основании известных токсикологических [9] и эколого-гигиенических [8] показателей p -аминофенола и значения LD 50 осадка (шлама), определенного по методу В.В. Прозоровского [12].
Результаты и их обсуждение
В результате направленной биодеградации некачественных лекарственных средств, производных хинолина, изохинолина, фенотиазина, пиразола, имидазола, бензимидазола, ацетанилида, фурана, бензгидрола, бензойной, пара-аминобензойной, дифенилуксусной и диэтиламинопропановой кислот нами установлено, что родококки характеризуются наиболее выраженной деструктивной активностью в отношении дротаверина (но-шпы), бензоата натрия и тримекаина. Выявлены основные стадии и отдельные продукты биодеградации исследуемых соединений; определены кинетические и термодинамические параметры; подобраны оптимальные условия биоконверсии лекарственных средств в виде фармацевтических субстанций и лекарственных форм. Разработаны технологические схемы процесса утилизации фармацевтических отходов с использованием коллекционных штаммов R. erythropolis
ИЭГМ 767, R. rodochrous ИЭГМ 647, R. ruber ИЭГМ 77, ИЭГМ 228, ИЭГМ 235 [7] – активных катализаторов процесса биодеградации исследуемых соединений.
Для достижения наибольшей степени эффективности и операционной стабильности данных биокатализаторов использован сорбционный метод иммобилизации целых клеток родококков на модифицированных поверхностях твердых носителей. Экспериментально обоснована возможность оптимизации процесса иммобилизации с использованием Rhodococcus -биосурфактантов. Полученные с помощью интерференционного микроскопа изображения свидетельствуют о том, что иммобилизация родококков имеет монослойный характер, клетки располагаются по всей поверхности носителя. При этом существует предел насыщения носителя бактериальными клетками, после чего резко снижается скорость адсорбции, и клетки практически не оседают на его поверхности. На основании полученных данных определена оптимальная (107 клеток/мл) концентрация клеток родококков в суспензии при проведении процедуры иммобилизации.
Разработанный биокатализатор характеризуется высокой каталитической активностью закрепленных клеток: скорость разложения парацетамола составляет 116 мг/(л∙ч). Использование иммобилизованных на модифицированном древесном опиле клеток родококков, предварительно адаптированных к фенолу, позволяет существенно сократить продолжительность процесса биодеструкции парацетамола – с 4 суток до 20 часов.
Оптимизация процесса биодеструкции парацетамола с использованием разработанного биокатализатора проведена в условиях лабораторного биореактора. Предварительно с помощью математического моделирования определены оптимальные значения температуры в интервале от 28 до 35 °С и скорости перемешивания среды от 160 до 200 об/мин, обеспечивающие максимальную величину константы скорости реакции разложения парацетамола (рис. 1) Штриховыми линиями на горизонтальной плоскости на рис. 1 показаны технологические ограничения на орбитальную скорость и температуру среды инкубации родококков. Коэффициент k 1 имеет явную тенденцию к увеличению с повышением температуры и скорости перемешивания. Максимальное значение k 1 находится на границе допустимой области по температуре и имеет тенденцию роста при этой температуре в сторону увеличения скорости перемешивания. В условиях эксперимента для орбитального шейкера k 1 max = 1,233 сут-1 при Т = 35 °С и n = 200 об/мин.
Полученное решение задачи оптимизации процесса биодеструкции парацетамола использовано для перехода к универсальным характеристикам параметров процесса: температуре и скорости перемешивания культуральной жидкости. После определения этих характеристик возможен переход к реальным управляющим технологическим параметрам для проведения процесса в полупромышленных и промышленных условиях. Это обусловлено тем, что температуру в полупромышленной установке (ферментере) можно привести в соответствие с температурой в лабораторной установке – шейкере, а переход от орбитальной скорости в шейкере к эквивалентной угловой скорости вращения мешалки в ферментере представляется возможным через интенсивность перемешивания культуральной жидкости [2].
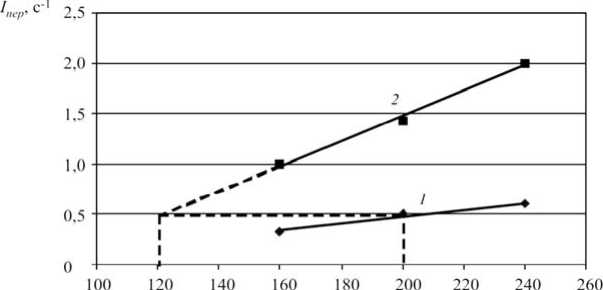
По нашим данным, для реализации оптимального значения k 1 max = 1,233 сут-1 при Т = 35 °С и n = 200 об/мин в лабораторных условиях необходима интенсивность перемешивания I пер = 0,5 с-1. Аппроксимируя точки прямой 2 (рис. 2) в силу
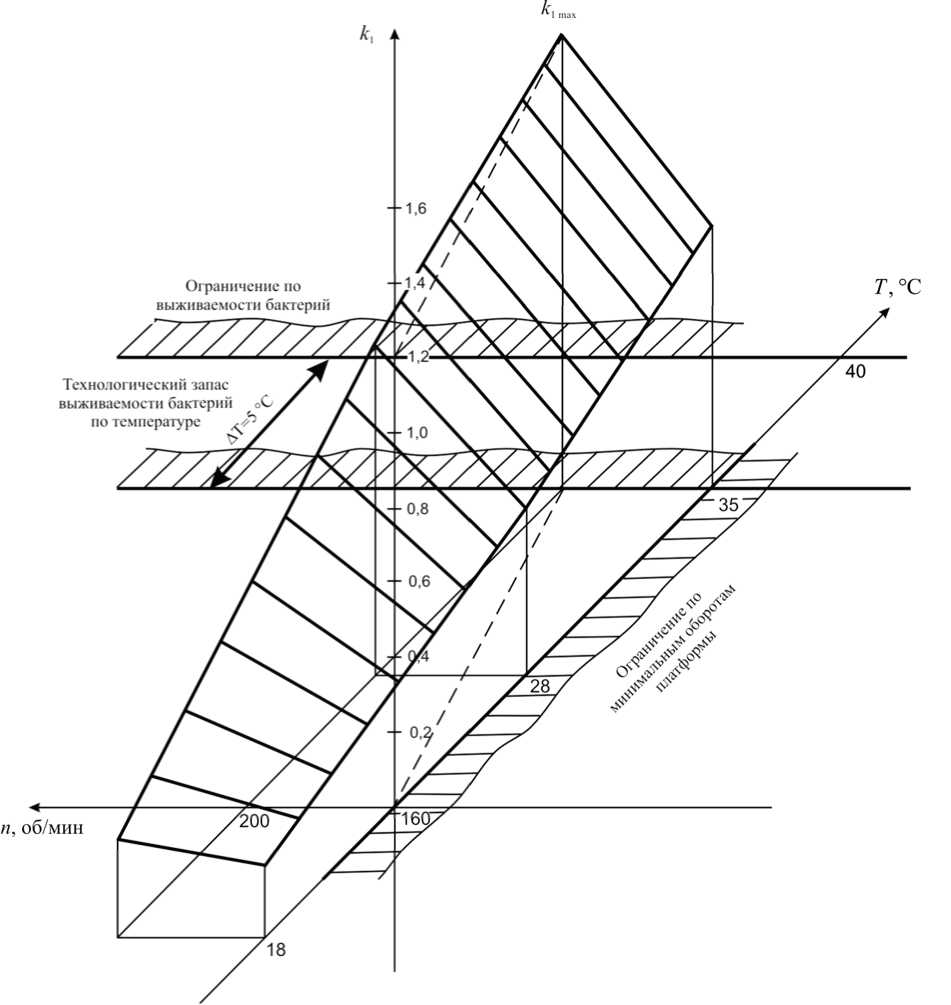
Рис. 1. Зависимость константы скорости реакции k1 биокаталитического окисления парацетамола клетками R. ruber ИЭГМ 77 от орбитальной скорости вращения шейкера и температуры среды инкубации родококков линейности до оптимальной интенсивности перемешивания в колбе (шейкере), находим значение n = 200 об/мин. Это значение можно считать начальной точкой угловой скорости вращения мешалки в ферментере при проведении процесса в полупромышленных условиях. Начальная точка температуры при этом составляет Т = 28 °С. Найденные технологические параметры являются начальным приближением при разработке технологии процесса биодеструкции парацетамола в полупромышленных условиях.
Как показано нами ранее [3], возможность прогнозирования содержания продуктов реакции во времени обеспечивает математическая модель, построенная на основании схемы биодеструкции (рис. 3) и представляющая собой систему дифференциальных уравнений первого порядка, которая имеет вид
—1 = - ( b + k • t ) • X ], dt
d ( x 2 + x, )
----2----— = K • ( b + k • t ) • X - ( c + d • t ) • x 2,
H2O 1 2
d^ = K dt CH3COOH
• K H2O • ( b + k • t) • X 1 ,
—4 = Ko • ( c + d • t) • x7, I dt O2
с начальными условиями
X 1 ^ = o X 1 , x 2 I t = 0 x 3 I t = 0 X 4 I t = 0 0, (2)
где х 1 , х 2 , х 3 , х 4 – концентрации парацетамола, p -аминофенола, уксусной кислоты и остальных продуктов разложения парацетамола соответственно.
n. об/мин
Рис. 2. Зависимость интенсивности перемешивания жидкости в колбе ( 1 ) и ферментере ( 2 ) от скорости вращения шейкера и мешалки ферментера
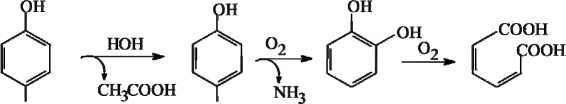
NHCOCH3 NH2
и-аминофенол пирокатехин цис, цис-муконовая кислота
парацетамол
NH3|
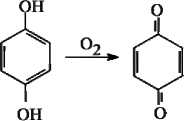
гидрохинон
^*1ТГ-1ЛХУТПТГХП иснзохинин
Рис. 3. Схема биодеструкции парацетамола с использованием клеток R. ruber ИЭГМ 77
Присутствующие в кинетических уравнениях коэффициенты K H2O , K CH3COOH , K O2 для открытой системы рассчитаны на основании закона сохранения молекулярных масс участвующих в реакциях соединений (см. рис. 3). Параметры «констант» скорости реакций b , k и c , d для парацетамола и p -аминофенола соответственно получены на основе экспериментальных данных [3].
Разработанная модель адекватно описывает процесс биодеструкции парацетамола как открытой системы [4] свободными и иммобилизованными клетками родококков и дает возможность прогнозировать его окончание по убыли токсичного метаболита – p- аминофенола (рис. 4, 5). Пунктирными линиями на рис. 4, 5 обозначены содержание p- аминофенола и время окончания процесса.
В процессе биодеструкции парацетамола происходит снижение класса опасности отхода с I до IV и V. Так, по нашим данным, парацетамол и p- аминофенол относятся к I классу опасности для окружающей природной среды [1], то есть являются чрезвычайно опасными отходами. Культуральная жидкость по достижении в ней концентрации p- аминофенола, равной 0,0005 г/мл, становится малоопасным отходом (IV класс опасности для окружающей природной среды) и может быть размещена на санитарном полигоне через 6 суток при использовании свободных клеток родококков (см. рис. 4) или через 19 часов при использовании иммобилизованных клеток (см. рис. 5). При этом после завершения процесса содержание парацетамола в среде становится равным нулю. Образующийся в процессе биодеструкции осадок (шлам) малотоксичен ( LD 50 > 4000 мг/кг), относится к V классу опасности (практически не опасен) для окружающей природной среды и наряду с культуральной жидкостью может быть размещен на санитарном полигоне твердых бытовых отходов.
Таким образом, на примере парацетамола разработан методологический подход к исследованию процесса биодеструкции непригодных к медицинскому использованию лекарственных средств, который включает в себя следующий алгоритм: 1) в результате изучения механизма сложного химического процесса, происходящего при биодеструкции лекарственного вещества, устанавливается схема данного процесса; 2) на основании скрининга производится отбор наиболее активных штаммов-биодеструкторов используемого соединения; 3) экспериментальным путем подбираются рациональные условия проведения процесса биодеструкции (состав среды, концентрация исходного субстрата, температура инкубации, интенсивность перемешивания, добавка косубстрата и др.); 4) проводится ограниченный ряд экспериментов для определения константы скорости реакции биокаталитического окисления исследуемого вещества, а также основных продуктов его разложения как исходных субстратов; 5) по схеме процесса биодеструкции строится математическая модель (система кинетических уравнений) для исходного субстрата и продуктов его разложения с учетом особенностей открытой системы и параллельной (одновременной) биодеградации исследуемого вещества и продуктов его разложения в реальном процессе; 6) в условиях эксперимента проверяется адекватность предложенной модели; 7) определяются начальные значения технологических параметров (температуры, скорости вращения мешалки и др.) для проведения процесса биодеструкции лекарственного вещества в полупромышленных и промышленных условиях.
Заключение
-
1. На примере парацетамола изучена кинетика процесса биодеструкции некачественных лекарственных средств, производных фенола. Установлена зависимость между скоростью процесса биодеструкции парацетамола и условиями
-
2. Разработана математическая модель процесса биодеструкции парацетамола с учетом особенностей открытой системы, позволяющая прогнозировать поведение исходного субстрата и продуктов его разложения, а также окончание процесса биодеструкции парацетамола по убыли p -аминофенола.
-
3. Показано, что в процессе биодеструкции парацетамола происходит снижение класса опасности отхода с I до IV и V, что позволяет размещать фармацевтические отходы на санитарном полигоне твердых бытовых отходов.
-
4. С использованием методов математического моделирования на примере парацетамола разработан методологический подход к изучению процессов биодеструкции некачественных лекарственных средств, производных фенола.
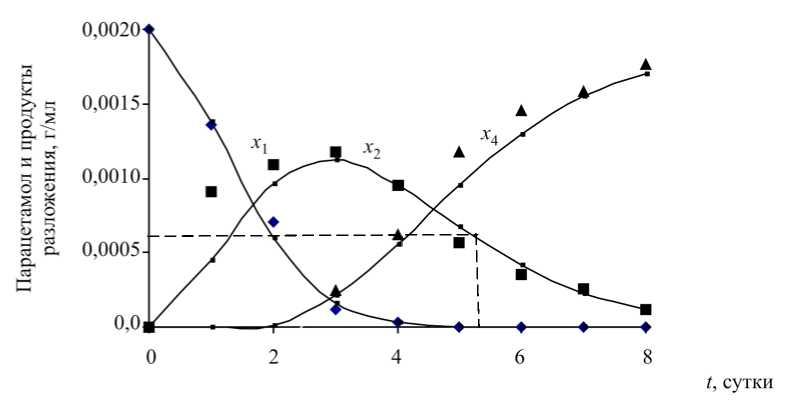
Рис. 4. Экспериментальные (точки) и теоретические (линии) зависимости от времени концентрации парацетамола х 1 , p -аминофенола х 2 и остальных продуктов разложения х 4 в процессе биодеструкции парацетамола свободными клетками R. erythropolis ИЭГМ 767
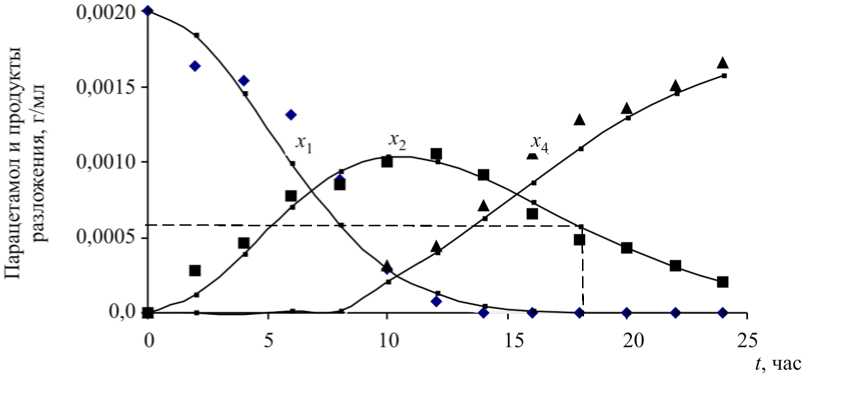
Рис. 5. Экспериментальные (точки) и теоретические (линии) зависимости от времени концентрации парацетамола х 1 , p -аминофенола х 2 и остальных продуктов разложения х 4 в процессе биодеструкции парацетамола иммобилизованными клетками R. erythropolis ИЭГМ 767
его проведения (температурой, интенсивностью перемешивания культуральной жидкости).
Благодарности
Работа выполнена при поддержке Российского фонда фундаментальных исследований (гранты № 04–04–96057–р_Урал_а, № 07–04–96038–р_Урал_а).
Список литературы Научно-методологический подход к утилизации фармацевтических отходов на основе биотехнологий и математического моделирования
- Вихарева, Е.В. Классификатор фармацевтических отходов (непригодных к использованию лекарственных средств) по классам опасности для окружающей природной среды и рекомендации по их уничтожению/Е.В. Вихарева; Перм. гос. фарм. акад. -Пермь, 2008. -118 с.
- Вихарева, Е.В. Математическое моделирование процесса биодеструкции парацетамола актинобактериями рода Rhodococcus/Е.В. Вихарева, А.А. Селянинов, И.Б. Ившина, Ю.И. Няшин//Российский журнал биомеханики. -2007. -Т. 11, № 2. -С. 93-100.
- Вихарева, Е.В. Математическая модель процесса биодеструкции парацетамола как открытой системы/Е.В. Вихарева, А.А. Селянинов, Ю.И. Данилов, И.П. Рудакова, Т.А. Нечеухина, И.Б. Ившина, Ю.И. Няшин//Российский журнал биомеханики. -2008. -Т. 12, № 2. -С. 80-94.
- Денисов, Е.Т. Кинетика гомогенных химических реакций/Е.Т. Денисов. -М.: Высшая школа, 1988. -390 с.
- Ившина, И.Б. Алканотрофные родококки как катализаторы процесса биодеструкции непригодных к использованию лекарственных средств/И.Б. Ившина, М.И. Рычкова, Е.В. Вихарева, Л.А. Чекрышкина, И.И. Мишенина//Прикладная биохимия и микробиология. -2006. -Т. 42, № 4. -С. 443-447.
- Ившина, И.Б. Деградация парацетамола с истекшим сроком годности свободными клетками актинобактерий/И.Б. Ившина, М.И. Рычкова, Е.В. Вихарева, Л.А. Чекрышкина, И.И. Мишенина//Катализ в промышленности. -2006. -№ 2. -С. 44-49.
- Ившина, И.Б. Каталог штаммов Региональной профилированной коллекции алканотрофных микроорганизмов/И.Б. Ившина. -М.: Наука, 1994. -163 с.
- Исаев, Л.К. Контроль химических и биологических параметров окружающей среды/под ред. Л.К. Исаева; Эколого-аналитический центр «Союз». -СПб., 1998. -896 с.
- Колла, В.Э. Дозы лекарственных средств и химических соединений для лабораторных животных/В.Э. Колла, Б.Я. Сыропятов. -М.: Медицина, 1998. -263 с.
- Лозинский, В.И. Криотропное гелеобразование растворов поливинилового спирта/В.И. Лозинский//Успехи химии. -1998. -Т. 67, № 7. -С. 641-652.
- Об утверждении критериев отнесения опасных отходов к классу опасности для окружающей природной среды: Приказ Министерства природных ресурсов Российской Федерации № 511 от 15.06.01.
- Прозоровский, В.В. Экспресс-метод определения средней эффективной дозы и ее ошибки/В.В. Прозоровский, М.П. Прозоровская, В.М. Демченко//Фармакология и токсикология. -1978. -№ 4. -С. 497-502.


