Нейроэндокринная опухоль большого дуоденального сосочка
Автор: Карпов О.Э., Маады А.С., Алексеев К.И., Левчук А.Л., Степанюк И.В., Плотницкий А.В., Судиловская В.В.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Клинические наблюдения
Статья в выпуске: 4 т.9, 2014 года.
Бесплатный доступ
Короткий адрес: https://sciup.org/140188354
IDR: 140188354 | УДК: 616.342-006.6-072.1
Текст статьи Нейроэндокринная опухоль большого дуоденального сосочка
Национальный медико-хирургический Центр им. Н.И. Пирогова
УДК: 616.342-006.6-072.1
NEUROENDOCRINE TUMORSOF THE MAJOR DUODENAL PAPILLA
Нейроэндокринные опухоли (НЭО) представляют собой группу злокачественных новообразований, происходящих из нейроэндокринных клеток, находящихся в любой части тела, характеризующихся положительной иммуногистохимической реакцией со специфическими маркерами (хромогранин А, синаптофизин), сродством к серебру, способностью вырабатывать различные пептидные гормоны и биогенные амины, которые вызывают типичные гормональные синдромы [2].
Как правило, НЭО - медленно растущие опухоли из клеток диффузной эндокринной системы [11]. В литературе используется множество синонимов для обозначения НЭО: карциноидная опухоль, эндокринная опухоль, нейроэндокринная опухоль, АПУДома, опухоль из островковых клеток поджелудочной железы и др. [1].
Термин «карциноид» введен немецким патологом Оберндорфером в 1907 г. для обозначения типа опухоли кишечника, менее агрессивного по сравнению с аденокарциномой. Однако он не признавал эндокринную природу этих опухолей [9].
Стандартизованные показатели заболеваемости НЭО варьируют в разных странах в пределах 0,71–1,36 на 100 000 человек в год. Большинство исследователей отмечают увеличение частоты заболеваемости за последние 30 лет, с ежегодным приростом заболеваемости на 3% [3, 8].
НЭО органов брюшной полости и забрюшинного пространства составляют до 20% всех новообразований желудочнокишечного тракта (ЖКТ), поджелудочной железы и других органов. Общая 5-летняя выживаемость больных НЭО независимо от локализации составляет 67–82%. В пределах ЖКТ большинство опухолей локализуются в тонкой кишке (30%), червеобразном отростке (20%) и прямой кишке (10%). [3]. Одной из самых редких локализаций НЭО в желудочно-кишечном тракте является большой дуоденальный сосочек (БДС). Частота встречаемости этой патологии составляет 0,05–0,1% [4, 5]. В доступной научной литературе встречаются лишь единичные публикации клинических наблюдений НЭО БДС [4–6].
Выбор оптимального хирургического вмешательства при нейроэндокринных опухолях до сих пор остается дискутабельным. Большинством авторов отдается предпочтение панкреатодуоденальной резекции [5, 7, 12], хотя остаются и сторонники локальных резекций [10].
Представляем собственное клиническое наблюдение нейроэндокринной опухоли этой редкой локализации.
Женщина 36 лет поступила в хирургическое отделение НМХЦ им. Н.И. Пирогова с жалобами на боли «опоясывающего» характера в верхней половине живота.
Примерно за год до поступления пациентку госпитализировали в один из московских хирургических стационаров с нарастающей механической желтухой. При обследовании была выявлена опухоль БДС размерами до 1 см; выполнено дренирующее вмешательство в объеме эндоскопической супрапапиллярной хо-ледоходуоденостомии. Тогда пациентка отказалась от радикального лечения, так как за месяц до этого перенесла роды.
В НМХЦ им. Н.И. Пирогова пациентка обследована. Выявлена амилазе-мия до 200 Ед/л и повышение уровня общего билирубина до 35 мкмоль/л. При УЗИ брюшной полости выявлены расширенные общий желчный и главный панкреатический протоки (до 1,9 см и 0,9–1,0 см соответственно), а также мелкие конкременты в желчном пузыре. При дуоденоскопии отмечено увеличение БДС до 2 см (рис. 1).
Эндоскопическая ультрасонография выявила наличие интраампулярного образования в БДС диаметром до 1,5 см, расширение панкреатического протока.
При мультиспиральной компьютерной томографии выявлена опухоль БДС с
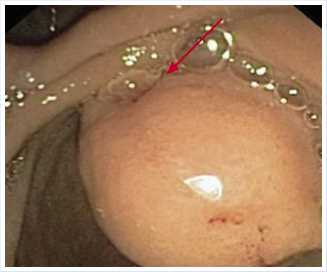
Рис. 1. Дуоденоскопия: БДС увеличен до 2 см, стрелкой указано холедоходуоденосто-мическое отверстие расширением панкреатического протока до 0,9–1,0 см.
В качестве первого этапа лечения выполнена эндоскопическая папиллос-финктеротомия, стентирование панкреатического протока и биопсия БДС. Гистологическое заключение: аденома БДС с дисплазией 1 ст.
Вторым этапом, через две недели после папиллосфинктеротомия выполнена эндоскопическая папиллэктомия, стентирование панкреатического протока. В ходе вмешательства возникло интенсивное кровотечение из краев разреза, которое удалось остановить установкой саморасширяющегося стента в панкреатический проток (рис. 2–6).
Оба стента извлечены на 3-и сутки после вмешательства (рис. 8).
Гистологическое исследование: фрагмент стенки двенадцатиперстной кишки с массивным разрастанием нейроэндокринной опухоли и микрофокусами роста в слизистой оболочке с распространением в непосредственную плоскость резекции (рис. 7).
Иммуногистохимическое исследование: иммунофенотип более всего соответствует нейроэндокринной опухоли (NET, Grade 2).
При эндоскопическом контроле через 5 недель выявлен фокус тканевых разрастаний вокруг устья панкреатического протока (рис. 9).
При эндосонографии выявлены также признаки инфильтративных изменений собственной мышечной оболочки двенадцатиперстной кишки в проекции ранее выполненной папиллэктомии.
Учитывая признаки нерадикального удаления опухоли с умеренным злокачественным потенциалом (Net, Grade 2), ее продолженный рост с распространением за пределы стенки двенадцатиперстной кишки, относительно молодой возраст

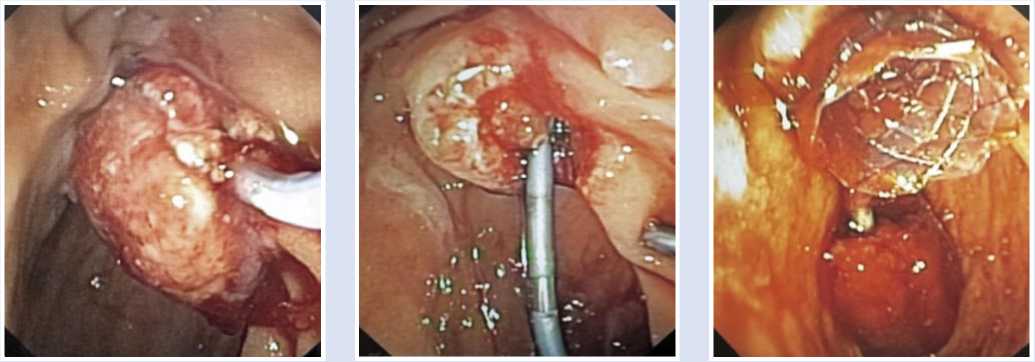
Рис. 2–4. Папиллэктомия. Стентирование панкреатического протока пластиковым и саморасширяющимся стентами.
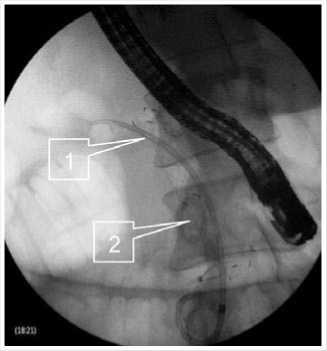
Рис. 5. Рентгенограмма. Видны пластиковый (1) и саморасширяющийся (2) стенты в панкреатическом протоке
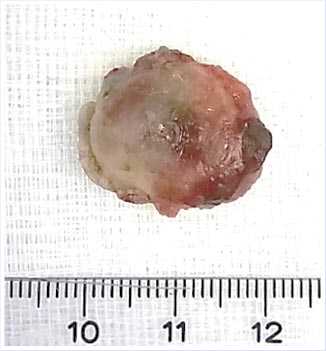
Рис. 6. Макропрепарат: БДС с фрагментом стенки двенадцатиперстной кишки
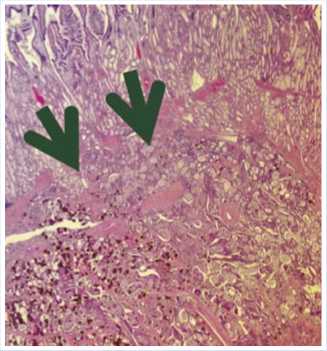
Рис. 7. Микропрепарат: нейроэндокринная опухоль с распространением в плоскость резекции
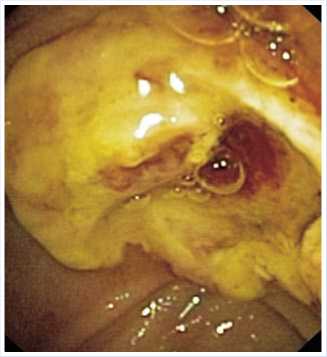
Рис. 8. Эндоскопическая картина после удаления обоих стентов
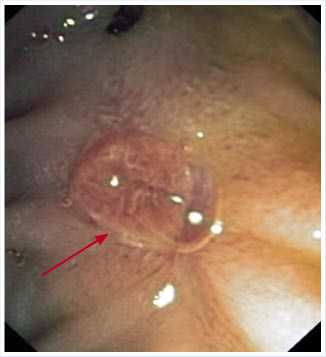
Рис. 9. Эндоскопическая картина через 5 недель после папиллэктомии. Видны тканевые разрастания вокруг устья панкреатического протока
пациентки и благоприятный жизненный прогноз консилиумом с участием онколога признано нецелесообразным выполнение повторного эндоскопического вмешательства. Поэтому пациентке предложено хирургическое лечение в объеме гастропанкреатодуоденальной резекции, которая и была выполнена (рис. 10, 11).
Послеоперационный период протекал без осложнений, пациентка выписана в удовлетворительном состоянии на 12 сут. после хирургического вмешательства.
Таким образом, представлен опыт лечения пациентки с нейроэндокринной опухолью крайне редкой локализации. Показаны возможности и ограничения эндоскопического метода, успешно преодоленные благодаря мультидисциплинарному подходу, доступному лишь в условиях крупных многопрофильных стационаров.

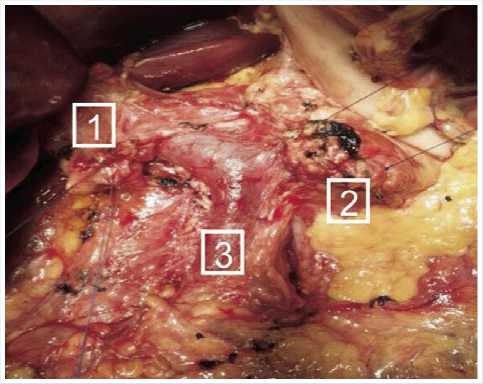
Рис. 10. Панкреатодуоденальная резекция: вид после удаления панкреатодуоденального комплекса (1 – культя общего печеночного протока, 2 – культя поджелудочной железы, 3 – воротная вена)
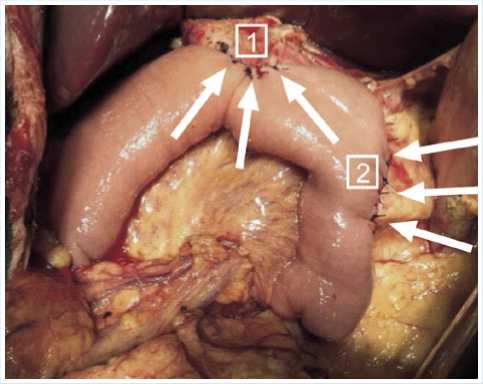
Рис. 11. Панкреатодуоденальная резекция: вид после наложения гепатикоэнтероанастомоза (1) и панкреатоэнтероанастомоза (2) (указаны стрелками)
Список литературы Нейроэндокринная опухоль большого дуоденального сосочка
- Нейроэндокринные опухоли: руководство для врачей /под ред. M. Caplin, L. Kvols. Москва: Практическая медицина, 2011.
- Поликарпова С.Б. и др. Клинико-биохимические аспекты карциноидного синдрома при нейроэндокринных опухолях органов брюшной полости и забрюшинного пространства и его связь с прогнозом болезни//Бюллетень экспериментальной биологии и медицины. 2009. Т. 148. № 11. С. 557-560.
- Bektas H. и др. Neuroendocrine tumors of the stomach. Surgery therapy and prognosis//Chirurg. 2002. Т. 73. № 4. С. 331-335.
- Pyun D.-K. и др. A carcinoid tumor of the ampulla of Vater treated by endoscopic snare papillectomy//Korean J. Intern. Med. 2004. Т. 19. № 4. С. 257-260.
- Gilani N., Ramirez F.C. Endoscopic resection of an ampullary carcinoid presenting with upper gastrointestinal bleeding: a case report and review of the literature//World J. Gastroenterol. 2007. Т. 13. № 8. С. 1268-1270.
- Cakmak A. и др. Carcinoid tumor of the ampulla of Vater presenting as recurrent acute acalculous cholecystitis attacks//Turk. J. Gastroenterol. 2008. Т. 19. № 4. С. 297-299.
- Clements W. Ampullary carcinoid tumors: rationale for an aggressive surgical approach//J. Gastrointest. Surg. 2003. Т. 7. № 6. С. 773-776.
- Modlin I.M., Lye K.D., Kidd M.A. 5-decade analysis of 13,715 carcinoid tumors//Cancer. 2003. Т. 97. С. 934-959.
- Oberndorfer S. Karzinoid Tumoren des Dunndarms//Frankf. Z. Pathol. 1907. № 1. С. 426-429.
- Ricci J.L. Carcinoid of the ampulla of Vater. Local resection or pancreaticoduodenectomy.//Cancer. 1993. Т. 71. № 3. С. 686-90.
- Rindi G., Bordi C. Endocrine tumours of the gastrointestinal tract: aetiology, molecular pathogenesis and genetics//Best Pract. Res. Clin. Gastroenterol. 2005. Т. 19. № 4. С. 519-534.
- Roder J.D. и др. Pylorus-preserving versus standard pancreatico-duodenectomy: an analysis of 110 pancreatic and periampullary carcinomas.//Br. J. Surg. 1992. Т. 79. № 2. С. 152-5.


