Нейроэндокринная опухоль - параганглиома, симулирующая зоб
Автор: Мосин С.В., Тарабрин Е.А., Фейдоров И.Ю., Тигров М.С., Лафишев Э.В., Яковлева Л.П., Кропотов М.А., Петрова А.Л., Глаголев Н.С.
Журнал: Злокачественные опухоли @malignanttumors
Рубрика: Клинический случай
Статья в выпуске: 2 т.9, 2019 года.
Бесплатный доступ
В данной статье представлены два редких клинических наблюдения, имеющих один объединяющий их признак. Пациентам с узловыми образованиями в щитовидной железе, обследованным в полном объеме согласно стандартным алгоритмам, с установленным до операции диагнозом «многоузловой зоб II степени», планировалось хирургическое лечение в объеме тиреоидэктомии. Однако после выполненных операций было установлено, что за многоузловой зоб с компрессией трахеи была ошибочно принята крайне редко встречающаяся нейроэндокринная опухоль - параганглиома, имитировавшая зоб с признаками компрессии органов шеи. При анализе клинических случаев нами были выявлены общие систематические ошибки, допущенные при обследовании с соблюдением общепринятых стандартизированных подходов, что привело к определенным сложностям в лечении этих пациентов.
Многоузловой зоб, щитовидная железа, тиреоидэктомия, нейроэндокринная опухоль, параганглиома
Короткий адрес: https://sciup.org/140243824
IDR: 140243824 | DOI: 10.18027/2224-5057-2019-9-2-64-73
A neuroendocrine tumor, paraganglioma presenting as plunging goiter
This paper presents two rare case reports with one common feature. Patients with thyroid nodules, who had undergone a comprehensive clinical evaluation based on standard algorithms according to their preoperative diagnosis of “Multinodular goiter, grade II”, were scheduled for surgical treatment (thyroidectomy). Postoperative morphological examination revealed, however, the extremely rare neuroendocrine tumor - paraganglioma - that simulated multinodular goiter with tracheal compression. Our analysis of these clinical cases showed common systematic mistakes that were committed during conventional, standardized preoperative examination, resulting in certain difficulties in the treatment of these patients
Текст научной статьи Нейроэндокринная опухоль - параганглиома, симулирующая зоб
Сокращения
ЩЖ — щитовидная железа
НЭО — нейроэндокринная опухоль
ТАБ — тонкоигольная аспирационная пункционная биопсия
АСПД — аналоги соматостатина пролонгированного действия
ОСА — общая сонная артерия
Узловые образования в щитовидной железе (ЩЖ) — распространенное патологическое состояние, встречающееся приблизительно у 10% людей в популяции [1,2]. Термин «узловые образования» включает в себя различные нозологические формы и их варианты, к которым относятся: узловой (многоузловой) коллоидный пролиферирующий зоб, доброкачественные опухоли (аденомы) и рак щитовидной железы. Основные принципы и этапы диагностического поиска, а также тактика лечения всех заболеваний ЩЖ хорошо известны и отражены в многочисленных публикациях и клинических рекомендациях. Большинству пациентов с узлами в ЩЖ не требуется специальное лечение, после проведения необходимых обследований по стандартному алгоритму и исключения состояний, требующих операции, им показано дальнейшее наблюдение у эндокринолога.
Хирургическое лечение узлового зоба в большинстве случаев выполняется в специализированных отделениях эндокринной хирургии, торакальной хирургии или хи- рургических отделениях общего профиля; операции при верифицированном раке ЩЖ в большинстве случаев выполняются в хирургических отделениях онкологических стационаров.
Показания к хирургическому лечению выявляются в среднем у 2–5% пациентов с узловыми образованиями [3]. В большинстве случаев при обнаружении узлового (многоузлового) зоба пациентам показано выполнение тиреоидэктомии, в некоторых случаях (например, при фолликулярной опухоли или раке ЩЖ I стадии) может быть выполнена гемитиреоидэктомия. Хирургическое лечение при узловых образованиях ЩЖ показано в следующих ситуациях:
-
1. Злокачественная опухоль ЩЖ или опухоль с неопределенным злокачественным потенциалом, выявленная при обследовании пациентов с узловым зобом (например, фолликулярная опухоль, соответствующая IV категории цитологического заключения по The Bethesda System for Reporting Thyroid Cytopathology (TBS) [4].
-
2. Гормонально-активный узел (функциональная автономия, или токсическая аденома ЩЖ, на фоне многоузлового зоба);
-
3. Узловой (многоузловой) зоб со значительным увеличением общего объема ЩЖ, приводящий к сдавлению пищевода или трахеи, развитию синдрома компрессии органов шеи, с соответствующей клинической картиной. Экстрафасциальная тиреоидэктомия является стандартной и хорошо отработанной хирургической операцией, с минимальной частотой осложнений при условии выполнения ее в специализированном центре. В большинстве случаев, при правильном планировании хирургической операции, риск осложнений составляет 0,5–5,3% и в основном выражается в послеоперационном гипопаратиреозе [5]. Вероятность возникновения нежелательных последствий оперативного лечения повышается при операции, выполняемой по поводу местнораспространенного рака ЩЖ, или зоба с загрудинным расположением и большим размером узла. Так, вероятность послеоперационного гипопаратиреоза возрастает до 10–15% и повреждения возвратного гортанного нерва до 4,3 % [6].
В целом, при соблюдении всех стандартизированных алгоритмов предоперационного обследования и основных правил проведения хирургической операции, вероятность диагностической ошибки или развития послеоперационных осложнений должна быть минимальной.
В исключительно редких случаях за узловые образования (многоузловой зоб) или аберрантную долю щитовидной железы могут быть приняты другие заболевания со сходной картиной, а именно внеорганные опухоли, локализующиеся в области шеи или верхнего средостения, в непосредственной близости от ЩЖ, по клиническим проявлениям и данным различных методов диагностики сходные с зобом.
Мы обладаем опытом лечения двух пациентов, которым планировалось хирургическое лечение по поводу многоузлового зоба, в результате которого была выявлена нейроэндокринная опухоль (НЭО) шейной или внутри-грудной локализации — параганглиома.
НЭО развиваются из энтерохромаффинных клеток, расположенных в различных тканях и органах. В 80–90% случаев НЭО являются высокодифференцированными опухолями с низким злокачественным потенциалом (Grade 1, реже — Grade 2); в остальных случаях НЭО представляют собой низкодифференцированные злокачественные опухоли Grade 3 [7]. Основная причина возникновения НЭО — генетические мутации (в онкогенезе участвуют такие гены, как MEN1, RET, VHL, TSC1, TSC2 и другие). Большую долю занимают герминативные мутации (гены SDHB, SDHA, SDHAF2, SDHD, SDHC, THEM 127, MAX), у таких пациентов риск метастазирования опухоли значительно выше [7]. По своему эмбриогенезу НЭО могут быть из клеток различных отделов эмбриональной кишечной трубки: верхней (foregut), средней (midgut) и концевой (hindgut) части. В 70% случаев НЭО встречаются в поджелудочной железе и в тонкой кишке (последние часто называются
«карциноидные опухоли»), а НЭО шейной и внутригрудной локализации развиваются из верхнего отдела (foregut).
НЭО внеорганной локализации — параганглиома, относится к редко встречающимся опухолям [8]. Кроме параганглиом, в эту группу отнесены нейробластома, карциноидные опухоли легких. Феохромоцитома надпочечника (частный случай параганглиом надпочечниковой локализации), и медуллярный рак ЩЖ, по устоявшейся практике рассматриваются отдельно, хотя также являются НЭО по своему происхождению. Около 10% феохромоцитом, и до 40% параганглиом обладают высоким злокачественным потенциалом (Grade 2–3), в остальных случаях опухоли Grade 1 расцениваются, как доброкачественные. Феохромоцитомой принято считать гормонально-активную параганглиому, сопровождающуюся типичной клинической картиной. От 10 до 20% всех гормонально-активных феохромоцитом имеют вненадпочечниковую локализацию и могут располагаться в любом месте, где есть парасимпатические ганглии, по ходу позвоночного столба,
Параганглиомы/феохромоцитомы клинически могут проявляться артериальной гипертензией или протекать бессимптомно а также иметь неспецифические проявления. Опухоль может являться причиной кризового повышения артериального давления у 0,05–0,1% всех пациентов с артериальной гипертензией. До 40% параганглиом всех локализаций также являются гормонально-активными опухолями, выделяющими катехоламины и их производные [9].
В стандартный алгоритм обследования при выявлении параганглиом входят определение Хромогранина А (общего маркера НЭО), а также катехоламинов в плазме крови или их метаболитов (метанефрина и норметанефрина) или в суточной моче, как маркеров гормонально активной параганглиомы. Некоторые авторы рекомендуют дополнительное определение допамина для параганглиом шейной локализации. Необходимо учитывать, что до 20% пациентов с феохромоцитомами/параганглиомами могут иметь нормальный уровень катехоламинов. Кроме этих маркеров, для параганглиом (как и для всех НЭО, происходящих из верхней эмбриональной кишки) в лабораторных анализах может наблюдаться низкое содержание серотонина, и высокое содержание гистамина [7,8].
Для визуализации параганглиом рекомендуется применение КТ или МРТ с контрастным усилением и специфическое исследование — сцинтиграфия с метайодбен-зилгуаниином-I123 (МИБГ), имеющим высокое сродство к адренэргическим рецепторам нейронов [9].
Описываемые нами клинические случаи являются сходными по принципу отбора кандидатов на оперативное лечение. Пациентам с установленным диагнозом «многоузловой зоб II степени (по классификации ВОЗ, 2009 г), с компрессией органов шеи», обследованным в полном объеме согласно общепринятым алгоритмам, планировалось хирургические лечение в объеме тиреоидэктомии из классического шейного доступа. В результате ряда диагностических ошибок, допущенных по различным причинам, диагноз «параганглиома» был установлен только после операции. В обоих случаях эта крайне редко встречающаяся опухоль имитировала зоб с признаками компрессии органов шеи, что привело к нежелательным сложностям в лечении этих пациентов.
Клинический случай № 1
Пациент А., 61 года. Обратился в клинику в октябре 2016 года с жалобами на увеличение окружности шеи, чувство дискомфорта в области шеи при глотании. Наблюдался у эндокринолога по поводу многоузлового зоба в течении 2-х лет. В 2015 году была выполнена тонкоигольная аспирационная биопсия (ТАБ) — получена кровь, пункция не повторялась. После этого по данным УЗИ в динамике отмечалось увеличение узла левой доли более чем в 2 раза.
При осмотре: область шеи незначительно деформирована, окружность увеличена, при пальпации определяются узлы в обеих долях, смещаемые, безболезненные. По УЗИ выявлены узлы в обеих долях ЩЖ, соответствующие TIRADS II–III. Также выявлен крупный узел левой доли, расположенный под левой общей сонной артерией, по структуре сходный с тканью ЩЖ.
Пациенту была выполнена ТАБ узла нижнего полюса левой доли и узла правой доли, заключение — цитологическая картина пролифелирующего зоба (TBS II — правая доля), атипия неопределенного значения (TBS III — левая доля). Повторная ТАБ узла левой доли оказалась неинформативной (TBS I).
Выполнено КТ шеи. Щитовидная железа имеет обычную плотность (55 HU), симметрична. Структура железы по данным КТ однородная, узловые образования в ткани не определяются. По нижнему контору левой доли ЩЖ определяется овальной формы образование с четкими, ровными контурами, однородной структуры, плотностью 47 HU, размерами 24 × 27 × 31 мм. Данное образование тесно прилежит к трахее слева, оттесняя его и сужая просвет до 7 мм. Трахея и главные бронхи проходимы, сужены. Сосуды шеи, визуализируемые при КТ— не изменены. Заключение: образование переднего средостения, требующее проведения дифференциального диагноза между увеличенным лимфатическим узлом и узловым зобом с частично загрудинным расположением (рис. 1–2).
В целом, по данным предоперационного обследования имелись неоднозначные данные о характере изменений в ЩЖ. Тем не менее, имелось клинически значимое сдав-
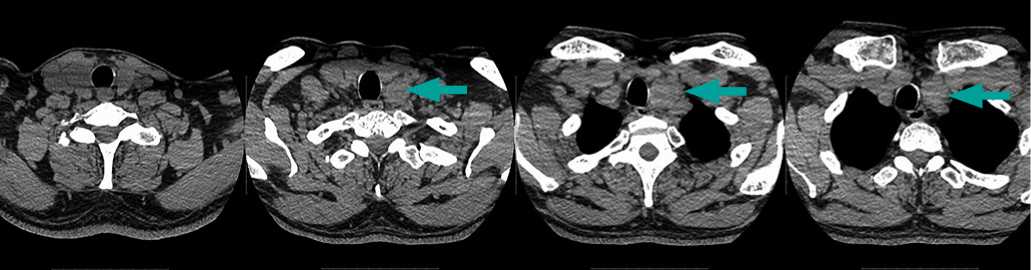
Рисунок 1. КТ шеи до операции, без в/венного контрастного усиления, аксиальный срез. Стрелками указана опухоль, расцениваемая как узловой зоб.
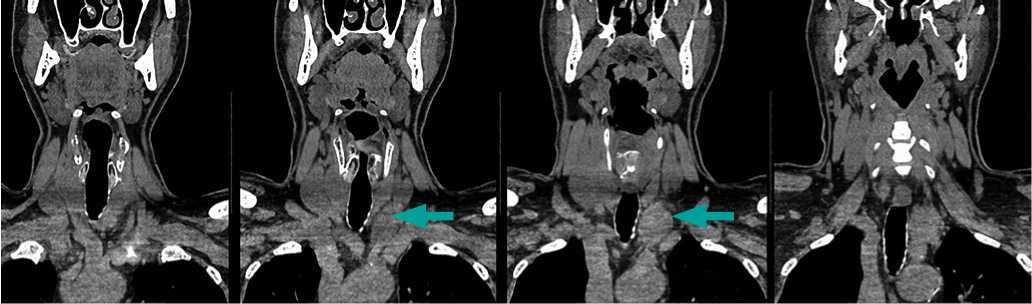
Рисунок 2. КТ шеи до операции, без в/венного контрастного усиления, фронтальный срез. Стрелками указана опухоль, расцениваемая как узловой зоб.
ление трахеи, подтвержденное по данным КТ. При этом выявленные изменения в ЩЖ были расценены как многоузловой зоб, с частично загрудинным расположением, с неопределенным цитологическим заключением ТАБ узла левой доли ЩЖ (TBS III), что в совокупности и явилось показанием к операции.
Операция выполнялась из стандартного шейного доступа (поперечная цервикотомия). Выявлено, что ЩЖ увеличена в размерах за счет обеих долей, более за счет левой. Определяются узловые образования; узел около 3-х см в нижнем полюсе левой доли, вплотную прилежит к трахее, что соответствует предоперационным данным. Выполнена экстрафасциальная тиреоидэктомия, при этом в ложе удаленной щитовидной железы дополнительных образований выявлено не было. В послеоперационном периоде — транзиторная гипокальциемия легкой степени. Выписан на 4-е сутки без осложнений.
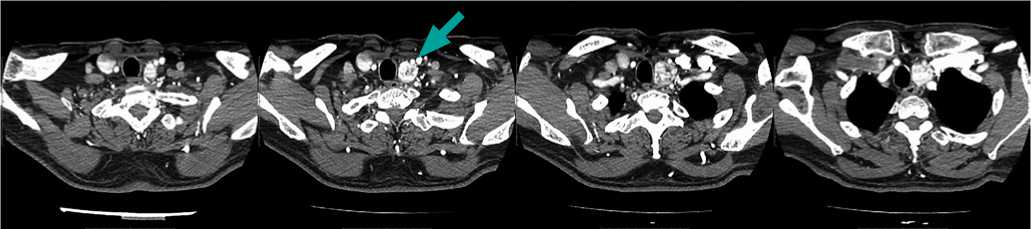
Рисунок 3. КТ шеи до операции, с в/венным контрастным усилением, аксиальный срез. Стрелками указана предполагаемая эктопированная доля ЩЖ.
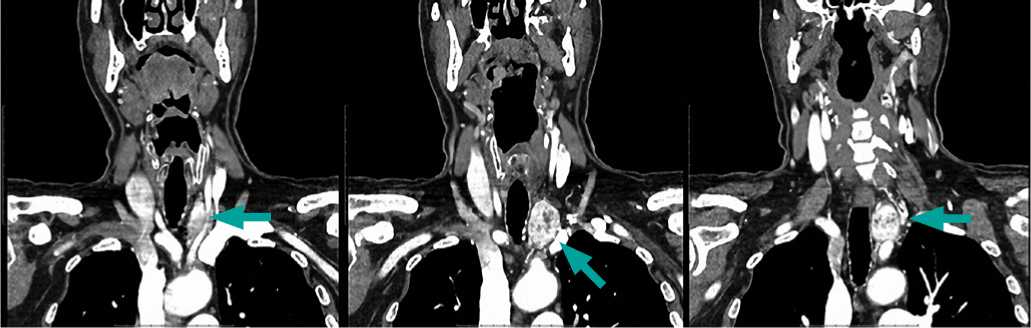
Рисунок 4. КТ шеи до операции, с в/венным контрастным усилением, фронтальный срез. Стрелками указана предполагаемая эктопированная доля ЩЖ.
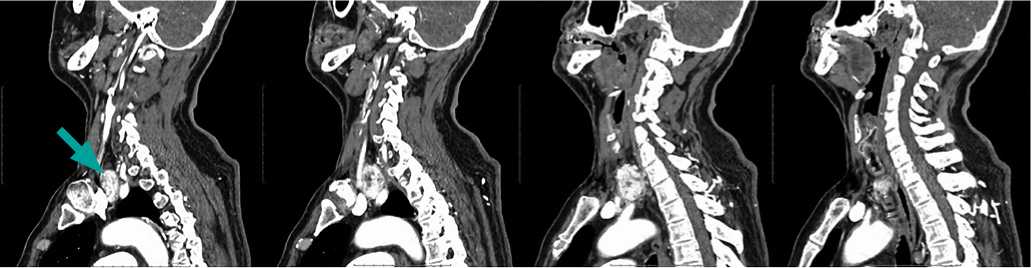
Рисунок 5. КТ шеи до операции, с в/венным контрастным усилением, сагиттальный срез. Стрелками указана предполагаемая эктопированная доля ЩЖ.
При гистологическом исследовании удаленной ЩЖ в левой доле обнаружено два инкапсулированных узла по 0,9 см. Морфологическая картина соответствовала микрофолликулярной аденоме солидного строения с ростом папиллярной карциномы (фолликулярный вариант) в краевых отделах аденомы с инвазией в капсулу ЩЖ. Признаков интравазальной и периневральной инвазии нет. В остальных фрагментах ЩЖ морфологическая картина многоузлового зоба. Инвазия в капсулу ЩЖ была расценена, как стадия T3 (согласно классификации TNM 7), так как сопровождалась минимальными признаками экстратиреоидного распространения.
В результате у пациента, оперированного по поводу многоузлового зоба с загрудинным расположением и компрессией трахеи, при морфологическом изучении удаленной ЩЖ был выявлен дифференцированный рак III стадии (pT3N0M0), не установленный при доопераци-онном обследовании. С учетом того, что объем операции (тиреоидэктомия) был адекватен стадии заболевания, пациент был направлен на консультацию к радиотерапевту. В связи с выявленным папиллярным раком ЩЖ III стадии пациенту было показано проведение терапии радиоактивным йодом, которая в дальнейшем не была проведена вовремя по личным обстоятельствам.
На контрольной КТ с внутривенным контрастным усилением через 4 месяца после операции, перед запланированным курсом радиойодтерапии, было выявлено опухолевидное образование, расположенное в проекции бифуркации общей сонной артерии паратрахеально слева, размером до 3 см.
Из описания КТ: в проекции левой доли удаленной ЩЖ визуализировано образование овальной формы, плотностью до 55–60 НU, размерами до 29 × 27 мм, в котором отмечается активное неравномерное накопление контрастного (соответствующее ткани ЩЖ) с наличием неправильной формы включений пониженной плотности, по задней поверхности образования расположены подключичная и позвоночные артерии, по переднему контуру — ОСА; в области удаленной правой доли ЩЖ дополнительные образования не определяются (рис. 3–5).
В связи с этой находкой необходимо было проводить дифференциальный диагноз между метастатическим поражением лимфатического узла паратрахеальной группы, возникшим после тиреоидэктомии, и эктопированной долей ЩЖ, ошибочно не удаленной при первой операции. Выполнена тонкоигольная пункция образования — получен неинформативный материал (кровь). При сравнении КТ, выполненного до первой операции (рис. 1–2), и контрольного КТ (рис. 3–5), было установлено, что образование было у пациента и до первой операции, тесно прилежало к левой доле ЩЖ и ошибочно не было удалено, так как располагалось под сонной артерией, а интраоперационно в левой доле ЩЖ был выявлен узел, по размерам и локализации напоминавший выявляемый по КТ «узел ЩЖ», сдавливавший трахею. С учетом неинформативной
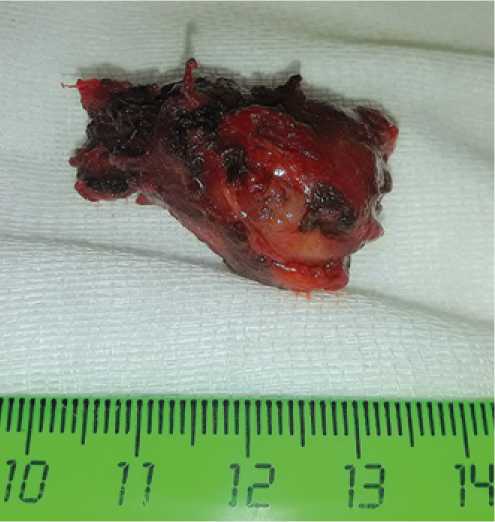
Рисунок 6. Удаленная параганглиома.
пункции образования, и сходной с тканью ЩЖ плотностью по КТ, образование окончательно расценено, как эктопированная доля ЩЖ. Пациенту запланировано удаление образования.
На операции удалена опухоль размерами 3,0 × 2,0 × 1,5 см, расцениваемая, как эктопированная доля ЩЖ (рис. 6).
Опухоль располагалась медиально и кзади от левой общей сонной артерии, в фасциальном футляре, покрывающем сосудисто-нервный пучок, образованным париетальным листком fascia endocervicalis. При гистологическом исследовании был обнаружен рост умереннодифференцированной злокачественной опухоли, окруженной со-единительно-тканной капсулой, местами формирующей альвеолярные и трабекулярные структуры. В утолщенной собственной фиброзной капсуле опухоли отмечено наличие опухолевых депозитов.
При иммуногистохимическом исследовании выявлена позитивная реакция опухолевых клеток с антителами к CD56, Синаптофизину, при этом негативная — к Хромогранину А. Индекс пролиферативной активности Ki-67–1%. Заключение: иммунофенотип нейроэндокринной опухоли (параганглиома), Grade 1.
Таким образом, у пациента на фоне многоузлового зоба II степени с компрессией органов шеи обнаружена параганглиома шейной локализации, прилежащая вплотную к доле ЩЖ, но расположенная в фасциальном футляре, покрывающем сосудисто-нервный пучок, и отделенная от ЩЖ париетальным листком внутренностной (IV) фасции шеи. На КТ опухоль имитировала узел ЩЖ, сдавливающий трахею, и ошибочно не была удалена при тиреоидэктомии, располагаясь в другом фасциальном слое.
Клинический случай № 2
Пациентка А., 72 лет. 12.2017 обратилась к эндокринологу с жалобами на слабость, утомляемость, одышку. Ранее, в 2014 году, при обследовании на МРТу пациентки выявлялось образование в передне-верхнем средостении, размерами 97 × 55 × 43 мм. Рекомендовано проведение МСКТ, которое не было выполнено. При настоящем обращении, с учетом ранее выявленных данных, пациентке сделано УЗИ, на котором подтверждено узловое образование, прилежащее к задней поверхности правой доли ЩЖ, по структуре гипоэхогенное, неоднородное, распространяющееся латерально и загрудинно, 88 × 38 × 54 мм, с пери- и интранодулярным кровотоком. По заключению УЗИ, принадлежность образования к ЩЖ сомнительна.
Для уточнения диагноза 12.2017 выполнено МРТ шеи. Объемные образования в ткани ЩЖ не определяются. В надключичной области справа, а также в верхнем средостении справа определяется образование с четкими контурами, размерами 100 × 51 × 66 мм, по эхогенности соответствует ткани ЩЖ. По заключению МРТ, структура и локализация образования более характерна загрудинной эктопированной доле ЩЖ.
На сцинтиграфии, признаки снижения функциональной активности паренхимы ЩЖ (на фоне приема левотироксина). Описано гетерогенное образование в области шеи
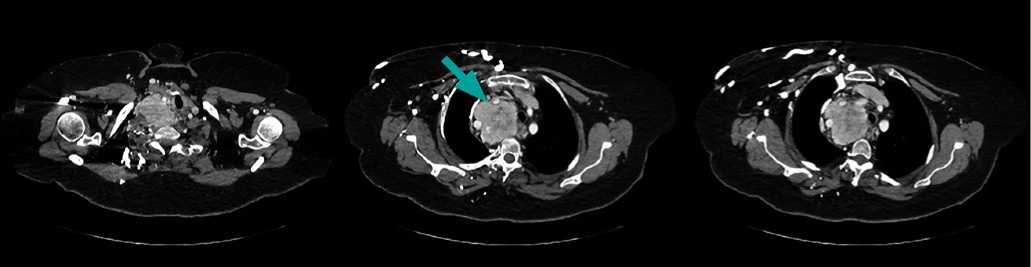
Рисунок 7. КТ шеи до операции, аксиальный срез. Стрелками указана предполагаемый загрудинный зоб.
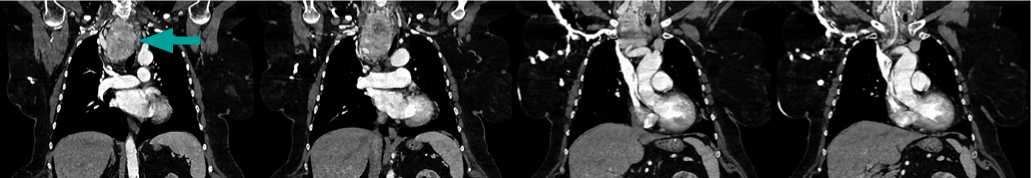
Рисунок 8. КТ шеи до операции, фронтальный срез. Стрелками указана предполагаемый загрудинный зоб.
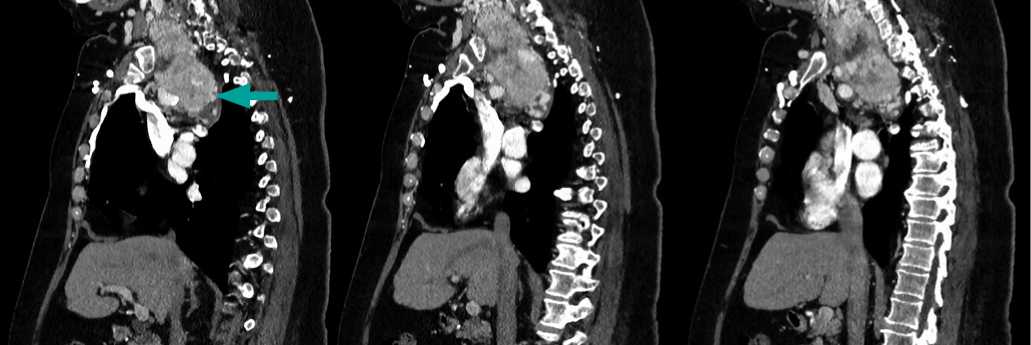
Рисунок 9. КТ шеи до операции, сагиттальный срез. Стрелками указана предполагаемый загрудинный зоб.
и средостения справа, оттесняющее трахею, пищевод, ЩЖ и сосуды влево. Заключение: вероятнее всего определяющееся образование не связанно с тканью ЩЖ.
Из описания МСКТ с в/венным контрастированием: крупное объемное образование, расположенное у нижнего полюса правой доли ЩЖ, размерами 47 × 70 × 119 мм. Контуры образования неровные, бугристые, структура неоднородна, активно накапливает контрастный препарат. Заключение: вероятнее всего, образование исходит из правой доли ЩЖ, с оттеснением прилежащих структур, но без признаков их инвазии. Выраженная компрессия верхней полой вены на фоне сдавления выявленным образованием с формированием обширной сети венозных коллатералей (рис. 7–9).
Выполненные ЭГДС и трахео-бронхоскопия показали локальное сдавление трахеи извне в области мембранозной части подскладочного пространства и задне-правой стенки средней трети трахеи. Признаков сдавления пищевода нет. По данным рентгеноскопии пищевода — оттеснение яуровне Th3-Th4 до 5 мм.
Цитологическая картина соответствовала коллоидному пролиферирующему зобу (TBS II). Учитывая результаты проведенного обследования, образование было расценено, как узловой зоб II степени с загрудинным расположением и симптомами компрессии трахеи, что и явилось показанием к хирургическому лечению.
В январе 2018 г. пациентка была прооперирована, выполнена поперечная цервикотомия. При ревизии установлено, что новообразование располагается справа от трахеи и ЩЖ (и не связано с ней, при этом прилежит к нижнему полюсу правой доли), оттесняя органы средостения влево. Образование тесно спаяно с окружающими тканями и вовлекает правую общую сонную артерию и плечеголовной ствол, опускается в средостение, а нижний полюс не достижим через цервикотомный доступ. Выполнена частичная продольно-поперечная стернотомия, выделены плечеголовной ствол, левая плечеголовная вена, правая общая сонная артерия. С техническими трудностями по причине высокой кровоточивости опухоли она отделена от окружающих тканей и удалена. Тиреоидэктомия не выполнялась (рис. 10–12). Течение послеоперационного периода без особенностей, выписана на 8-е сутки.
При гистологическом исследовании была описана картина эпителиоидноклеточной опухоли с неопределенным злокачественным потенциалом, без признаков инвазивного роста. При иммуногистохимическом исследовании выявлена позитивная реакция опухолевых клеток с антителами к CD56, Синаптофизину, Хромогранину А, GATA3, S100. Индекс мечения Ki-67=2%. Заключение: иммунофенотип нейроэндокринной опухоли (параганглиома), Grade 1.
Обсуждение
Параганглиома Grade 1 — высокодифференцированная НЭО с низким злокачественным потенциалом, в редких случаях обладающая гормональной активностью, инвазивный рост и регионарное метастазирование для нее не характены. Однако, как и при остальных НЭО, даже при высокодифференцированной опухоли Grade 1 возможен локорегионар-ный рецидив или генерализация. Морфологическая верификация с оценкой характеристик опухоли до операции предпочтительна, но не является необходимой, особенно в случае локализованных опухолей без выявленных до операции признаков инвазивного роста или регионарного метастазирования. Предоперационная морфологическая диагностика может быть заменена одним из методов визуализации соматостатиновых рецепторов: сцинтиграфия с In-111-октреотидом, или ПЭТ-КТ с Ga-68-DOTATOC, при этом чувствительность метода значительно зависит от наличия в опухоли рецепторов к соматостатину 2 и 5 типов, характерных для НЭО. Определение уровня Хромогранина А перед операцией является стандартом серологической диагностики при подозрении на НЭО.
Основным методом лечения локализованных опухолей является хирургический. Операция показана как при гормонально-неактивных, так и при гормонально-активных
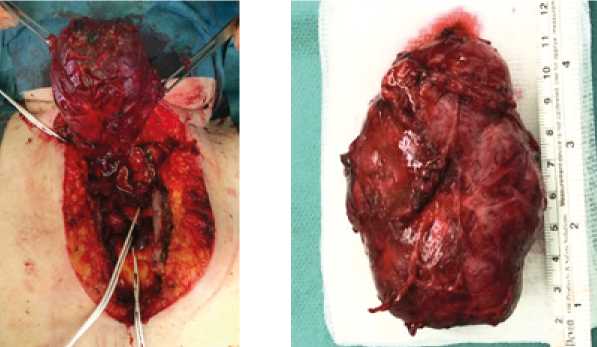
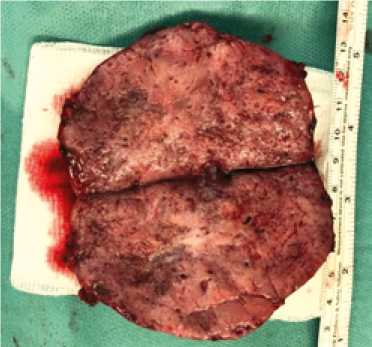
Рисунки 10–12. Этапы операции и удаленная опухоль.
опухолях (например, при гормонально-активной пара-ганглиоме/феохромоцитоме любой вненадпочечниковой локализации, или при параганглиоме с карциноидным синдромом, что встречается крайне редко). Лимфаденэктомия при опухоли Grade 1 не является необходимой, если до операции не выявлены измененные регионарные лимфоузлы. Адьювантное лучевое лечение при Grade 1 не показано.
Лекарственная терапия при НЭО Grade 1 может проводится в адьювантном режиме только по показаниям после радикального хирургического лечения — при наличии не-удалимых метастазов или при прогрессировании, а так же с целью лечения карциноидного синдрома. Адьювантная химиотерапия при локализованной опухоли Grade 1 не рекомендуется. Биотерапия аналогами соматостатина пролонгированного действия (АСПД), обладает как хорошей антисекреторной, так и доказанной умеренной антипро-лиферативной активностью. Терапия АСПД применяется в качестве I линии, если после радикальной операции при дальнейшем наблюдении выявляется биохимический рецидив (повышение уровня Хромогранина А более чем в 4 раза по сравнению с исходным послеоперационным уровнем), или клинический рецидив. Терапия АСПД не показана после радикального удаления гормональнонеактивной опухоли без признаков генерализации [10].
В обоих представленных клинических случаях пациентам было проведено радикальное хирургическое лечение. Дальнейшее специальное лечение им не требуется. В плане наблюдения показано регулярное изучение уровня Хромогранина А (через 3-6-12 месяцев) и наблюдение у онколога для своевременного выявления потенциального рецидива.
При анализе всех особенностей лечения обоих пациентов из описанных нами клинических примеров мы выявили определенные закономерности, повлиявшие на развитие ошибочного суждения о диагнозе.
-
1. Отсутствие онкологической настороженности. При узловом (многоузловом) зобе с признаками компрессии органов шеи, при нетипичном/загрудинном расположении единичного крупного узла последний может являться не узлом ЩЖ, а внеорганной опухолью, вплотную прилежащей к доле ЩЖ. В описанным нами случаях опухоль являлась параганглиомой, хотя могут встречаться и вне-органные опухоли другой природы. Выявляемая при до-операционном обследовании опухоль, тесно прилежащая к ЩЖ, была расценена, как узловой зоб. В определенной мере это ошибочное суждение было обусловлено редкостью подобной опухоли, и частой встречаемостью узлового коллоидного зоба с симптомами компрессии трахеи. Дополнительно заподозрить опухоль также можно было, определив уровень Хромогранина А при стандартном предоперационном обследовании [11].
-
2. Противоречивые данные предоперационных методов визуализации. В обоих случаях до операции были выявлены признаки экстраорганного расположения узла. В первом случае, по данным КТ без в/венного контраст-
- ного усиления, не прослеживалась убедительная связь образования с ЩЖ, но данные УЗИ с высокой вероятностью описывали многоузловой зоб. Во втором случае наоборот, аналогичные сомнения были высказаны по результатам УЗИ и МРТ, но описание КТ явилось более убедительным аргументом в пользу зоба с загрудинным расположением, связанным с нижним полюсом правой доли ЩЖ. Тем не менее, по совокупности полученных результатов, был сделан вывод о принадлежности образования к ткани ЩЖ.
-
3. Нарушение методологии выполнения тонкоигольной аспирационной биопсии (ТАБ). Дополнительными аргументами «в пользу зоба» являлись данные ТАБ. В первом случае, при ТАБ узла левой доли ЩЖ была получена неопределенная атипия (Bethesda III), что в сочетании с размерами узла и явилось показанием к хирургическому лечению. При этом, гистологически действительно был выявлен папиллярный рак ЩЖ. Во втором случае, выполнялась ТАБ загрудинно расположенного образования, и цитологическое заключение (коллоидный зоб — TBS II) подтверждало диагноз коллоидного зоба. Анализируя, очевидно ошибочные факты несовпадения результатов ТАБ и морфологического диагноза удаленных параганглиом, из которых по определению не может быть получен тиреоидный эпителий при ТАБ, мы предположили, что такое заключение могло быть получено в связи с получением «путевого» материала из щитовидной железы, если игла при выполнении пункции образования проходит через ткань ЩЖ. При этом, материал для цитологического исследования забирается не из самой опухоли (или не только из нее), но и частично из ткани ЩЖ, что и нашло отражение в цитологических заключениях. Учитывая объективные сложности ТАБ из «неудобно» расположенных опухолей, выбрать другую трассу для введения иглы в обоих случаях было технически затруднительно.
-
4. Ошибки при выполнении хирургической операции.
-
5. Недостаточная послеоперационная верификация.
Ретроспективно мы проанализировали данные КТ обоих пациентов. В первом случае на КТ без в/венного контрастного усиления была выявлена слабо выраженная прослойка, образованная висцеральным и париетальным листком facsia endocervicalis, между тканью ЩЖ и опухолью, расположенной в фасциальном футляре, покрывающем сосудисто-нервный пучок. На УЗИ эта прослойка дифференцировалась нечетко, опухоль вплотную прилежала к ткани ЩЖ. Во втором случае данные исследований также были противоречивы и неоднозначны, однако мы обратили внимание на то, что образование верхнего средостения имеет неровный контур, «огибающий» крупные артерии, что не характерно для коллоидного зоба и дифференцированного рака ЩЖ с загрудинным расположением, как правило, имеющих ровную и округлую форму на КТ. Кроме этого, по данным УЗИ в первом случае, МРТ и КТ — во втором, плотность образования была аналогична плотности ткани ЩЖ.
В первом клиническом примере параганглиома ошибочно не была удалена при первой операции. Объективными причинами этого являлись два фактора: опухоль располагалась вне ложа ЩЖ, в клетчаточном пространстве вокруг сосудисто-нервного пучка, под сонной артерией, и на операции был выявлен узел в левой доле ЩЖ, по размерам и характеру напоминающий дооперационную картину, и расположенный непосредственно у трахеи. Параганглиома не была обнаружена во время операции, так как находилась в соседнем клетчаточном пространстве шеи, отделенном от зоны операции двумя фасциальными листками: висцеральным и париетальным листком facsia endocervicalis.
В послеоперационном периоде было показано проведение ИГХ с соматостатиновыми рецепторами 2 и 5 типов для того, чтобы определить потенциальную чувствительность опухоли к АСПД.
Описанные объективные трудности диагностики и лечения параганглиом шейной и внутригрудной локализации, по нашему мнению, в первую очередь были связаны с тем, что опухоли прилежали к ЩЖ, имитируя узловой зоб с атипичным расположением узлов. Изначально ошибочная выявленная связь образования с ЩЖ увела диагностический поиск в неверном направлении, что привело к нежелательным сложностям в лечении пациентов и к дополнительным затратам.
Список литературы Нейроэндокринная опухоль - параганглиома, симулирующая зоб
- Carlé, A., Krejbjerg, A. and Laurberg, P. (2014). Epidemiology of nodular goitre. Influence of iodine intake. Best Practice & Research Clinical Endocrinology & Metabolism, 28 (4), pp.465-479
- Li, H., Li, X., Liu, J., Jin, L., Yang, F., Wang, J., Wang, O. and Gao, Y. (2017). Correlation between serum lead and thyroid diseases: papillary thyroid carcinoma, nodular goiter, and thyroid adenoma. International Journal of Environmental Health Research, 27 (5), pp.409-419
- Smith, J., Chen, X., Schneider, D., Broome, J., Sippel, R., Chen, H. and Solórzano, C. (2013). Cancer after Thyroidectomy: A Multi-Institutional Experience with 1,523 Patients. Journal of the American College of Surgeons, 216 (4), pp.571-577
- Cibas, E. and Ali, S. (2017). The 2017 Bethesda System for Reporting Thyroid Cytopathology. Thyroid, 27 (11), pp.1341-1346
- Cannizzaro, M., Lo Bianco, S., Picardo, M., Provenzano, D. and Buffone, A. (2017). How to avoid and to manage postoperative complications in thyroid surgery. Updates in Surgery, 69 (2), pp.211-215
- Surgical management of substernal goitres at a tertiary referral centre: A retrospective cohort study of 2,104 patients. (2016). International Journal of Surgery, 27, pp.46-52
- Кэплин М. Нейроэндокринные опухоли: руководство для врачей//М.: Изд-во Практическая медицина, 2011. С 67-96
- Neuroendocrine Tumors, Version 1.2015. (2015). Journal of the National Comprehensive Cancer Network, 13 (1), pp.78-108. 10.6004/jnccn.2015.0011
- DOI: :10.6004/jnccn.2015.0011
- Tsirlin, A., Oo, Y., Sharma, R., Kansara, A., Gliwa, A. and Banerji, M. (2014). Pheochromocytoma: A review. Maturitas, 77 (3), pp.229-238
- Орел Н.Ф., Горбунова В.А., Дворниченко В.В., Емельянова Г.С., Кузьминов А.Е., Любимова Н.В., Маркович А.А., Орлова Р.В., Трифанов В.С. Практические рекомендации по лекарственному лечению нейроэндокринных опухолей желудочно-кишечного тракта и поджелудочной железы. Коллектив авторов: 10.18027/2224-5057-2017-7-3s2-395-403
- DOI: :10.18027/2224-5057-2017-7-3s2-395-403
- O’Connor, D., Mahata, S., Taupenot, L., Mahata, M., Livsey Taylor, C., Kailasam, M., Ziegler, M. and Parmer, R. (2000). Chromogranin A in Human Disease. Advances in Experimental Medicine and Biology, pp.377-388


