Неоадъювантная химиотерапия в органосохранном лечении мышечно-инвазивного рака мочевого пузыря
Автор: Винтизенко С.И., Слонимская Елена Михайловна, Усынин Е.А., Юрмазов З.А., Хурсевич Н.А.
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Клинические исследования
Статья в выпуске: 2 (32), 2009 года.
Бесплатный доступ
Изучено влияние неоадъювантной полихимиотерапии по схеме MVAC (цисплатин, метотрексат, винбластин, доксору- бицин) на эффективность лечения инвазивных форм рака мочевого пузыря. Установлено, что проведение системной хи- миотерапии у больных мышечно-инвазивным раком мочевого пузыря в предоперационном режиме способствует снижению количества рецидивов опухоли, позволяет отодвинуть сроки их появления, соответственно, увеличить продолжительность жизни без признаков местного проявления опухолевого роста и уменьшить количество выполняемых органоуносящих операций.
Инвазивный рак мочевого пузыря, неоадъювантная химиотерапия, выживаемость, эффективность
Короткий адрес: https://sciup.org/14055129
IDR: 14055129 | УДК: 616.62-006.6+615.28
Neoadjuvant chemotherapy for muscle-invasive bladder cancer
The purpose of the present research was to study the influence of neoadjuvant MVAC (cisplatin, methotrexate, vinblastin, doxorubicin) on the treatment efficacy of muscle invasive bladder cancer. Neoadjuvant chemotherapy for patients with muscle invasive bladder cancer was found to reduce the incidence of local recurrence, to prolong lifetime and to reduce the incidence of radical cystectomies.
Текст научной статьи Неоадъювантная химиотерапия в органосохранном лечении мышечно-инвазивного рака мочевого пузыря
В структуре онкоурологической заболеваемости опухоли мочевого пузыря занимают первое место и составляют 70 % [3]. На долю инвазивного рака мочевого пузыря (РМП), который характеризуется исходно агрессивным течением и неблагоприятным прогнозом, приходится до 60 % новообразований этой локализации, лечение данной категории больных остается одной из наиболее сложных и нерешенных задач онкоурологии [5]. Это касается, прежде всего, выбора объема оперативного вмешательства.
Согласно рекомендациям Европейской ассоциации урологов (2007), стандартным методом лечения мышечно-инвазивного РМП считается радикальная цистэктомия с деривацией мочи в сегмент кишечного тракта. Несмотря на значительный объем оперативного вмешательства, в течение двух лет после радикальной цистэктомии у 50 % больных появляются отдаленные метастазы, а у 25 % местные рецидивы опухоли в полости малого таза [7]. В связи с этим в последнее время растет число сторонников орга- носохранного подхода в лечении инвазивного РМП с использованием химиолучевой терапии [2, 4, 6]. Считается, что органосохранное лечение может быть предложено пациентам с мышечноинвазивным раком, у которых отсутствуют регионарные и отдаленные метастазы, размер солитарной опухоли не более 5 см, нет проявлений гидронефроза, опухоль имеет папиллярное строение, предполагается «видимое» полное удаление новообразования с помощью трансуретральной резекции (ТУР), а также при полной регрессии опухоли после индукционной химиотерапии [4]. Для снижения риска развития местного рецидива опухоли и отдаленных метастазов, с целью увеличения выживаемости, в настоящее время применяют системную лекарственную терапию с использованием различных схем (CMV, MVAC, GC и др.) и режимов, как один из важнейших этапов комбинированного лечения [1].
На сегодняшний день хорошо изучена эффективность адъювантной химиотерапии, она позволяет снизить частоту развития рецидивов почти у трети больных РМП, отодвинуть сроки их появления и увеличить продолжительность жизни. Основным преимуществом этого вида лечения является то, что химиотерапия выполняется после морфологического исследования удаленного препарата. Следовательно, наиболее точно определяются распространенность процесса и прогноз заболевания. К серьезному недостатку послеоперационной химиотерапии следует отнести отсутствие контроля за ее эффективностью, поскольку опухоль, по реакции которой можно было бы судить о действенности лечения, уже удалена [1].
В настоящее время интенсивно изучается роль неоадъювантной химиотерапии (НАХТ) в органосохранном лечении инвазивных форм РМП. Предоперационная химиотерапия имеет ряд преимуществ, которые заключаются в возможности уменьшения размеров опухоли, снижении способности опухолевой ткани к реимплантации во время ее фрагментации при ТУР мочевого пузыря, оценки чувствительности опухоли на проводимое лечение (можно добиться полной регрессии новообразования или прекратить лечение ввиду нечувствительности) [2, 3]. Однако результаты НАХТ противоречивы. Некоторые авторы считают, что она улучшает показатели выживаемости на 10–15 % [3], другие полагают, что результаты НАХТ позволяют только выделять группы больных с хорошим (при полной регрессии опухоли) и плохим (при частичной регрессии и отсутствии эффекта) исходом заболевания и могут трактоваться лишь как дополнительный фактор прогноза [8]. Изучение литературных данных показывает, что единой точки зрения в отношении целесообразности проведения НАХТ у больных инвазивным РМП до сих пор нет.
Целью исследования явилось изучение влияния неоадъювантной полихимиотерапии на эффективность лечения мышечно-инвазивного РМП.
Материалы и методы
В исследование включено 60 больных мышечно-инвазивным РМП T2а-3bN0M0G1–3 без признаков регионального и отдаленного метастазирования, из них мужчин было 52 (87 %), женщин – 8 (13 %). Средний возраст составил 54,5 ± 0,5 года. У всех пациентов морфологи- чески установлен переходно-клеточный рак с разной степенью дифференцировки опухоли. В зависимости от варианта проведения химиотерапии больные были разделены на две группы. В первую (I) вошли 26 больных, которым проводилось 2 курса системной полихимиотерапии в неоадъювантном режиме по стандартной схеме MVAC (метотрексат – 30 мг/м2 в 1-й и 8-й дни, винбластин – 4 мг/м2 в 1-й и 8-й дни, цисплатин – 70 мг/м2 во 2-й день, доксорубицин 30 мг/м2 – во 2-й день), перерыв между курсами – 4–6 нед. В последующем этим пациентам выполнялась ТУР мочевого пузыря и проводились 2 курса адъювантной химиотерапии по вышеуказанной схеме. Во II (контрольную) группу были включены 34 пациента, у которых лечение начиналось с выполнения ТУР мочевого пузыря, а затем проводилось 2 курса системной полихимиотерапии в адъювантном режиме по схеме MVAC. Анализируемые группы пациентов были сопоставимы по возрасту, полу, стадии заболевания, характеру роста и степени дифференцировки опухоли.
Для оценки распространенности процесса выполнялась светооптическая цистоскопия с измерением двух максимальных размеров опухоли, учитывались количество новообразований, характер их роста, с последующим забором биопсийного материла. Дополнительно проводились УЗИ, компьютерная томография. Стадия заболевания определялась в соответствии с международной классификацией TNM 6-го пересмотра (2002). Исследование биопсийного и операционного материала включало определение гистотипа опухоли, степени ее дифференцировки и инвазии, оценку терапевтического патоморфоза после цитостатической терапии. Объективная оценка эффекта предоперационного лечения в I группе проводилась после 2 курсов химиотерапии по шкале RECIST и основывалась на данных УЗИ, компьютерной томографии и цистоскопии. Полученные данные были обработаны с использованием программы Statistica 6,0.
Результаты и обсуждение
Анализ непосредственной эффективности НАХТ у 26 больных I группы показал, что ни в одном наблюдении не было получено полной
Таблица 1
Эффективность НАХТ у больных мышечно-инвазивным раком мочевого пузыря в зависимости от степени дифференцировки опухоли, абс.ч. (%)
У всех пациентов, получавших НАХТ, при морфологическом исследовании операционного материала после выполнения ТУР в опухолевой ткани определялась степень выраженности лекарственного патоморфоза. Было отмечено, что из 13 больных, у которых эффект от проведенного лечения был оценен как стабилизация процесса, у 8 (61,5 %) повреждения злокачественных клеток были незначительными и соответствовали I степени патоморфоза, тогда как II степень патоморфоза достоверно чаще наблюдалась при явлениях частичной регрессии опухоли – у 7 (63,6 %) из 11 пациентов. Эти данные дают основание полагать, что при достижении частичной регрессии опухоли после 2 курсов химиотерапии целесообразно
Таблица 2
|
Группы |
Сроки выявления рецидивов |
||||||
|
0–3 мес |
3–6 мес |
6–9 мес |
9–12 мес |
12–18 мес |
18–24 мес |
Всего |
|
|
I группа (НАХТ) n=26 |
2 (7,8) |
3 (11,5) |
1 (3,8) |
4 (15,4) |
1 (3,8) |
3 (11,5) |
14 (53,8) |
|
10 (38,5) |
4 (15,3) |
||||||
|
II группа (АХТ) n=34 |
3 (8,8) |
5 (14,7) |
3 (8,8) |
5 (14,7) |
2 (5,9) |
3 (8,8) |
21 (61,7)* |
|
16 (47)* |
5 (14,7) |
||||||
Примечание: * – различия между группами статистически значимы (p<0,05).
Таблица 3
Характеристика рецидивов рака мочевого пузыря у больных исследуемых групп, абс.ч. (%)
|
Характеристика рецидивов |
I группа (НАХТ) |
II группа (АХТ) |
|
Всего рецидивов |
14 (53,8) |
21 (61,7) * |
|
Продолженный рост опухоли |
1 (7,1) |
2 (9,5) |
|
Единичный рецидив |
10 (71,4) |
14 (66,7) |
|
Множественный рецидив |
4 (28,6) |
7 (33,3) |
|
Поверхностный рецидив |
9 (64,3) |
13 (61,9) |
|
Инвазивный рецидив |
5 (35,7) |
8 (38,1) |
|
Среднее время появления рецидивов (мес) |
10,5 ± 0,5 |
7,8 ± 0,5 * |
Примечание: * – различия между группами статистически значимы (p<0,05).
Частота и сроки выявления рецидивов в исследуемых группах, абс.ч. (%)
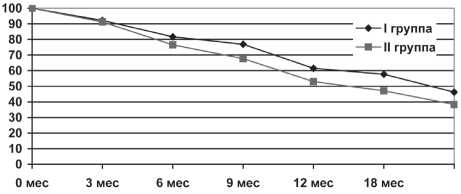
Рис. 1. Показатели 2-летней безрецидивной выживаемости у больных исследуемых группах продолжить лекарственное лечение, и в этом случае можно ожидать увеличение степени повреждения опухолевых клеток.
При анализе результатов лечения мышечноинвазивного РМП одним из наиболее значимых моментов является оценка частоты и сроков появления местных рецидивов опухоли. По нашим данным, за 2-летний период наблюдения рецидивы РМП возникли у 53,8 % пациентов, получавших химиотерапию в предоперационном режиме, в контрольной группе этот показатель был значимо выше и составил 61,7 % (p<0,05) (табл. 2).
В обеих группах пациентов, независимо от режима проведения химиотерапии, большая часть рецидивов опухоли определялась уже на первом году наблюдения. Тем не менее у больных, получивших НАХТ, местные рецидивы выявлялись реже по сравнению с пациентами, которым проводилась адъювантная химиотерапия (АХТ), – в 38,5 % и 47 % наблюдений соответственно (p<0,05). Среднее время появления рецидива в исследуемой группе составило 10,5 ± 0,5 мес, в контрольной группе – 7,8 ± 0,5 мес (p<0,05) (табл. 3). При изучении клинических особенностей роста рецидивных опухолей в зависимости от вида лечения каких-либо значимых различий отмечено не было. Так, у больных обеих групп преимущественно выявлялись единичные опухолевые узлы, которые характеризовались поверхностным характером роста новообразования.
Анализ отдаленных результатов показал, что 2-летняя безрецидивная выживаемость у больных с предоперационной химиотерапией составила 46,2 %, тогда как в группе с АХТ она была достоверно ниже – 38,3 % (p<0,05)
(рис. 1). Поскольку все пациенты после проведенного лечения были живы и ни в одном клиническом наблюдении не было выявлено отдаленных метастазов, показатели общей и безметастатической 2-летней выживаемости составили 100 %.
Больным с рецидивирующим течением заболевания проводились повторные ТУРы с последующими курсами внутрипузырной или системной (в зависимости от степени инвазии опухоли) химиотерапии. Однако у ряда пациентов в связи с частым возникновением повторных рецидивов и значительным укорочением сроков между их выявлением были определены показания к выполнению радикальной цистэктомии. В итоге органоуносящей операции подверглись 5 (14,7 %) больных II группы, что более чем в 2 раза превысило количество подобных операций в I группе – 2 (7,7 %) (р<0,05).
Заключение
Таким образом, проведение системной химиотерапии у больных мышечно-инвазивным раком мочевого пузыря в предоперационном режиме способствует снижению количества рецидивов опухоли, позволяет отодвинуть сроки их появления, соответственно, увеличить продолжительность жизни без признаков местного проявления опухолевого роста и уменьшить количество выполняемых органоуносящих операций.


