Непосредственные результаты модифицированной операции Росса
Автор: Чернов И.И., Козьмин Д.Ю., Макеев С.А., Демецкая В.В., Тарасов Д.Г.
Журнал: Патология кровообращения и кардиохирургия @journal-meshalkin
Рубрика: Приобретенные пороки сердца
Статья в выпуске: 1 т.20, 2016 года.
Бесплатный доступ
Цель. Оценка непосредственных результатов модифицированной операции Росса у взрослых пациентов с различной патологией аортального клапана. Материал и методы. В ретроспективное одноцентровое исследование включили 21 взрослого пациента (средний возраст 41±10,1 года), которому выполнили модифицированную операцию Росса по поводу порока аортального клапана различной этиологии. Пациентов не разделяли на группы в зависимости от типа модификации процедуры Росса (собственная аорта или синтетический протез). В 42,9% случаев выполнили комбинированные вмешательства при сопутствующей патологии. Проанализировали результаты хирургического лечения в течение госпитального периода. Результаты. Случаев госпитальной летальности не было. Во время операции выявили три случая острой сердечной недостаточности вследствие деформации устьев коронарных артерий, что потребовало коронарного шунтирования. В послеоперационном периоде отмечены один случай периоперационного инфаркта миокарда, одно острое нарушение мозгового кровообращения и одно кровотечение, потребовавшее рестернотомии. У двух пациентов развилась полиорганная недостаточность, разрешившаяся в результате лечения. Среднее время пребывания в отделении анестезиологии, реанимации и интенсивной терапии составило 42,0±47,7 (от 16 до 181) ч. Во всех случаях при контрольном ультразвуковом исследовании сердца перед выпиской ауто- и гомографты демонстрировали хорошие гемодинамические показатели. Заключение. Модификации операции Росса, направленные на профилактику развития недостаточности клапана легочного аутографта вследствие дилатации «неоартального корня», являются воспроизводимыми и безопасными методиками. Для определения эффективности этих модификаций необходима оценка средне- и долгосрочных результатов.
Аортальный порок, процедура росса, модифицированная операция росса, дилатация корня аорты
Короткий адрес: https://sciup.org/142140723
IDR: 142140723
Immediate results of modified Ross procedure
Objective. The study aims to assess immediate results of modified Ross procedure in adults with aortic valve pathology of various etiology. Methods. This retrospective study included 21 adult patients (mean age 41 years), who underwent modified Ross procedure for aortic valve disease of various etiology. Patients were not divided into groups according to the used type of modification (use was made of a patient's aorta or synthetic prosthesis). In 42.9% of cases combined operations were performed in case of concurrent valve pathology. The immediate operative results during hospital stay were analyzed. Results. There was no hospital mortality. There were 3 cases of coronary ostia kinking during the procedure resulting in acute heart failure, which required bypass grafting. Postoperative complications included 1 case of perioperative AMI, 1 case of stroke and 1 case of bleeding that necessitated resternotomy. Multiorgan failure occurred in 2 patients. Mean time of ICU stay was 42 (16-181) hours. Good hemodynamic results of both homo- and autografts were confirmed by echocardiography before discharge in all cases. Conclusion. Modifications of the Ross procedure used in our study to prevent neoaortic root dilatation leading to aortic regurgitation are reproducible and safe in experienced hands. Middle and long term follow-up is needed to determine their safety and efficacy.
Текст научной статьи Непосредственные результаты модифицированной операции Росса
Citation: Chernov II, Kozmin DYu, Makeev SA, Demetskaya VV, Tarasov DG. Immediate results of modified Ross procedure. Patologiya krovoobrashcheniya i kardiokhirurgiya [Circulation Pathology and Cardiac Surgery]. 2016;20(1):12-18. (In Russ.).
Ряд авторов предлагают имплантировать легочный аутографт в синтетический сосудистый протез, считая, что такая методика технически проще и не требует дополнительного времени. Данный способ укрепления неокорня аорты демонстрирует положительные отдаленные результаты [11–14].
Материал и методы
С 2014 по 2015 гг. в Федеральном центре сердечно-сосудистой хирургии (Астрахань) выполнили 21 модифицированную операцию Росса взрослым пациентам. Исследование является одноцентровым и ретроспективным. В группу включили больных старше 18 лет с пороком аортального клапана, которым
провели процедуру Росса в модифицированном виде. Общая характеристика пациентов представлена ниже.
Интраоперационная чреспищеводная эхокардиография (ЭхоКГ) – стандарт при кардиохирургических вмешательствах в Федеральном центре сердечно-сосудистой хирургии (Астрахань). До операции оценивали состояние желудочков и клапанов сердца, уточняли характер поражения аортального клапана, измеряли размеры аорты и фиброзных колец аортального клапана и клапана легочной артерии. Все операции выполняли через полную срединную стернотомию в условиях искусственного кровообращения, умеренной гипотермической перфузией (32–34 °С) и фармакохолодовой кристаллоидной кардиоплегии. Подключали аппарат искусственного кровообращения по схеме «восходящая аорта – полые вены». В качестве кардиоплегического раствора во всех случаях использовали
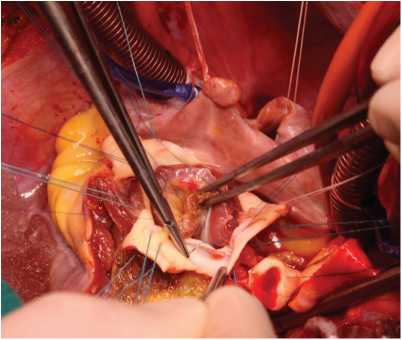
Рис. 1. Имплантация легочного аутографта непрерывным швом
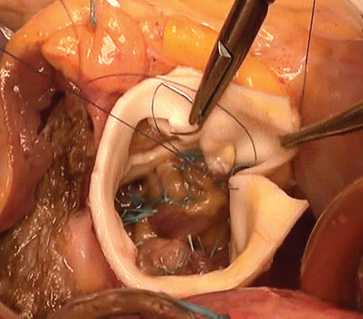
Рис. 2. Имплантация легочного аутографта: а – интрааортально; б – сосудистый протез
б
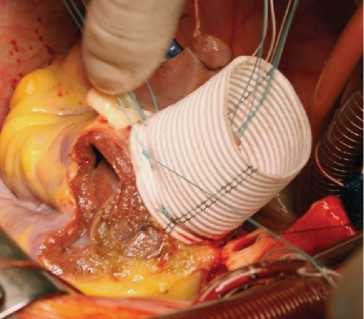
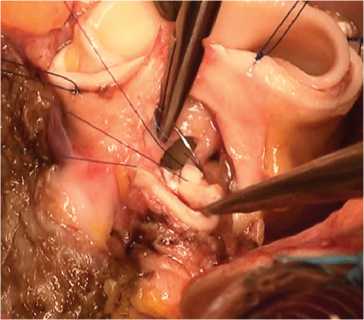
Рис. 3. Имплантация устья левой коронарной артерии в аутографт: а – интрааортально; б – сосудистый протез
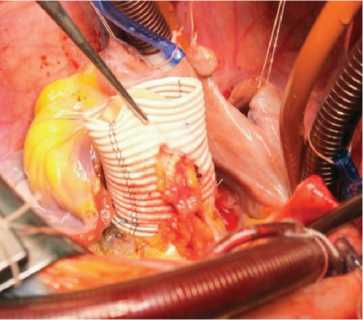
а
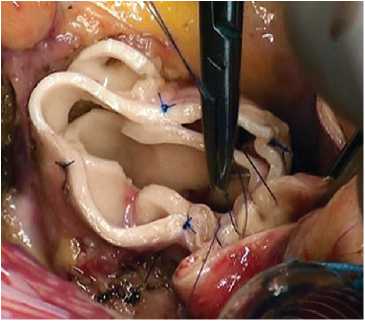
Рис. 4. Формирование дистального анастомоза с аортой: а – интрааортально; б – сосудистый протез
б
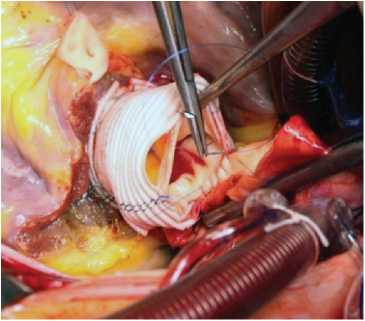
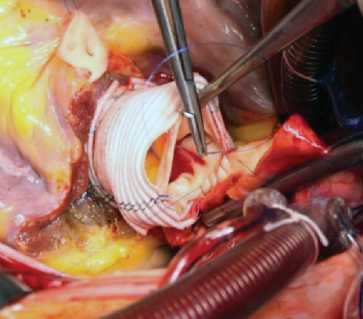
раствор «Кустодиол», доставляемый антеградно через устья коронарных артерий однократно в объеме 3 000 мл. Дополнительно применяли локальную гипотермию миокарда ледяной крошкой. После иссечения пораженного аортального клапана проводили декальцинацию с промыванием полости левого желудочка и обрабатывали фиброзное кольцо аортального клапана раствором антисептика. При значительном расширении фиброзного кольца выполняли редукционную аннулопластику. Во всех случаях использовали полное замещение корня аорты (total root replacement). Проксимальный анастомоз легочного аутографта накладывали с использованием непрерывного (15 случаев) или отдельных узловых (6 случаев) швов (рис. 1). Для профилактики дилатации аутографта в отдаленном периоде имплантировали аутографт в собственный корень аорты или синтетический протез (рис. 2). Устья коронарных артерий имплан- тировали в аутографт по методике «кнопок» (рис. 3). Дистальный анастомоз укрепленного аутографта с восходящей аортой по типу «сэндвича» накладывали однорядным швом (рис. 4). Для реконструкции выводного тракта правого желудочка использовали свежеприготовленный легочный гомографт 26–30 мм (Санкт-Петербургский банк гомографтов, Санкт-Петербург, Россия).
В табл. 1 представлены интраоперационные данные в зависимости от вида модификации процедуры Росса (рис. 5).
После окончания искусственного кровообращения проводили контрольное чреспищеводное ультразвуковое исследование для оценки функции миокарда и клапанов, гемодинамики на аутографте в аортальной позиции и гомографте в выводном отделе правого желудочка. Всем пациентам выполняли трансторакальное ультразвуковое исследование сердца перед выпиской.
Таблица 1 Интраоперационные данные
|
Интрааортальная методика, n = 12 |
Сосудистый протез, n = 9 |
|
|
Изолированная процедура Росса, n (%) |
8 (66,7) |
4 (44,4) |
|
Время окклюзии аорты, мин |
111,6±16,3 |
118,5±12,9 |
|
Время искусственного кровообращения, мин |
139,6±33,9 |
143,0±21,0 |
|
Комбинированные вмешательства, n (%) Коронарное шунтирование, n (%) |
4 (33,3) |
5 (55,6) |
|
плановое |
2 (16,7) |
|
|
экстренное |
1 (8,3) |
2 (22,2) |
|
Пластика митрального клапана, n (%) Протезирование восходящего отдела и дуги аорты, n (%) |
1 (8,3) |
1 (11,1) |
|
Коррекция неполной формы атриовентрикулярного канала, n (%) |
1 (11,1) |
|
|
Общее время окклюзии аорты, мин |
117,5±15,8 |
154,4±26,0 |
|
Общее время искусственного кровообращения, мин |
157±35,4 |
203,8±40,8 |
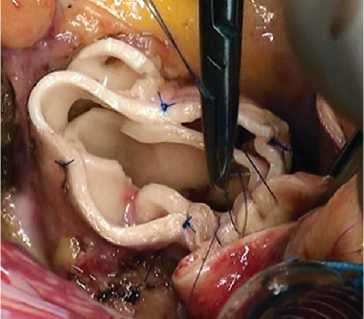
Рис. 5. Окончательный вид операции: а – интрааортально; б – сосудистый протез
б
Статистическую обработку данных (расчет средних, минимальных и максимальных значений величин, стандартных отклонений) осуществляли в программе Microsoft Excel 2013.
Результаты
В госпитальном периоде отметили ряд нефатальных осложнений (представлены ниже). Рецидивов инфекционного эндокардита и летальных случаев не отмечено.
Интраоперационные осложнения, n (%)
|
Кровотечение, потребовавшее повторной окклюзии аорты |
3 (14,3) |
|
Острое нарушение коронарного кровотока, потребовавшее |
3 (14,3) |
|
экстренного коронарного шунтирования Дисфункция неоаортального |
1 (4,8) |
|
клапана вследствие технических причин |
Послеоперационные осложнения, n (%)
|
Периоперационный инфаркт миокарда |
1 (4,8) |
|
Острое нарушение мозгового кровообращения |
1 (4,8) |
|
Кровотечение, потребовавшее рестернотомии |
1 (4,8) |
|
Острая почечная недостаточность, потребовавшая диализа |
3 (14,3) |
|
Нарушения ритма сердца |
2 (9,5) |
|
Полиорганная недостаточность |
2 (9,5) |
У 3 больных после снятия зажима с аорты возникли признаки острой сердечной недостаточности вследствие нарушения коронарного кровоснабжения в системе правой (2 случая) и левой (1 случай) коронарных артерий, потребовавшие шунтирования соответствующих бассейнов. При этом периопера-ционный инфаркт миокарда развился лишь у одного больного. Гемодиафильтрация понадобилась 3 больным, причем у одного пациента острая почечная дисфункция возникла на фоне предшествующей хронической почечной недостаточности.
Среднее время пребывания в отделении анестезиологии, реанимации и интенсивной терапии составило 42,0±47,7 (от 16 до 181) ч, для 2 больных – более 6 сут. В качестве проявлений постперикардиотом-ного синдрома зарегистрировано по одному случаю гидроторакса и гидроперикарда, потребовавшие дренирования.
При контрольной трансторакальной ЭхоКГ, выполненной перед выпиской пациентов, отмечена хорошая сократимость и признаки нормализации объемов полости левого желудочка (табл. 2).
Во всех случаях при контрольной эхокардиографии ауто- и гомографты демонстрировали положительные гемодинамические показатели (представлены ниже).
Аутографт
|
Максимальный градиент, мм рт. ст. Регургитация, n (%) |
9,1±5,3 |
|
отсутствует |
2 (9,5) |
|
0–1 степень |
19 (90,5) |
|
Гомографт Максимальный градиент, мм рт. ст. Регургитация, n (%) |
4,2±1,5 |
|
отсутствует |
9 (42,9) |
|
0–1 степень |
12 (57,1) |
Таблица 2 Динамика данных ЭхоКГ в госпитальном периоде
|
Показатель |
До операции |
При выписке |
|
Фракция выброса левого желудочка, % |
59,0±8,0 |
53,5±8,6 |
|
Конечный диастолический объем левого желудочка, мл |
168,6±62,8 |
142,1±51,1 |
|
Индекс конечного диастолического объема, мл/м2 |
87,0±30,9 |
73,0±23,4 |
|
Конечный систолический объем левого желудочка, мл |
70,0±31,0 |
69±35,9 |
|
Индекс конечного систолического объема, мл/м2 |
35,9±14,4 |
35,1±16,7 |
|
Расчетное давление в легочной артерии |
31,7±11,0 |
32,4±6,3 |
|
Диаметр фиброзного кольца аортального клапана |
24,0±3,1 |
21,3±1,6 |
|
Диаметр аорты на уровне |
||
|
синусов Вальсальвы |
37,2±5,1 |
30,5±3,4 |
|
восходящего отдела |
39,2±8,7 |
31,8±3,8 |
Средний послеоперационный койко-день составил 7,9±2,6 дня. Всех больных выписали из стационара в удовлетворительном состоянии.
Обсуждение
Операция Росса у отдельной категории взрослых пациентов является альтернативой традиционному протезированию аортального клапана. Обладая рядом преимуществ (оптимальные гемодинамические характеристики аутографта, устойчивость к инфекции, отсутствие пожизненного приема антикоагулянтов, минимальный риск тромбоэмболических осложнений), процедура Росса технически трудновыполнимая операция для большинства хирургов. Основная проблема отдаленного периода – дилатация неокорня аорты с формированием недостаточности клапана и необходимость повторной операции [7–9].
Описанные в литературе методики укрепления легочного аутографта при операции Росса позволяют сохранить правильную геометрию и нормальную функцию легочного аутографта в течение длительного времени и, следовательно, избежать повторной операции [8, 10].
К 2016 г. в Федеральном центре сердечно-сосудистой хирургии (Астрахань) выполнили около 170 «классических» операций Росса взрослым пациентам с пороками аортального клапана [15]. С 2014 г. с целью профилактики дилатации корня неоаорты используют методики укрепления аутографта с применением синтетического сосудистого протеза и собственной аорты пациента. Полученные непосредственные результаты 21 операции позволяют проводить данные вмешательства с приемлемым уровнем безопасности и эффективности. В дальнейшем планируем изучение отдаленных результатов этих методик.
Нерешенными остаются вопросы о состоянии стенки аорты, которой укреплен аутографт, к моменту повторной операции. Насколько выражен спаечный про- цесс между аутографтом и стенкой аорты? Будет ли возможно выполнить операцию Дэвида на неоаорталь-ном клапане в отдаленном периоде наблюдения [11]?
Заключение
В представленном исследовании показаны выполнимость и безопасность модификаций операции Росса, а также вероятность улучшения отдаленных результатов. Возможно минимизировать количество интра- и послеоперационных осложнений при дальнейшем накоплении опыта. Ввиду небольшой численности исследуемой группы провести сравнение двух описанных методик невозможно. Для определения эффективности этих модификаций необходима оценка отдаленных результатов.
Список литературы Непосредственные результаты модифицированной операции Росса
- Ross D.N. Replacement of aortic and mitral valves with a pulmonary autograft//Lancet. 1967. Vol. 2 (7523). P. 956-958.
- Караськов А.М., Железнев С.И., Богачев-Прокофьев А.В., Демин И.И., Кулумбегов О.И. Процедура Росса как этап сочетанного вмешательства при комбинированной патологии сердца//Кардиология и сердечно-сосудистая хирургия. 2010. Т. 3. № 3. С. 64-67.
- Elkins R.C., Thompson D.M., Lane M.M., Elkins C.C., Peyton M.D. The Ross operation: 16-year experience//J. Thorac. Cardiovasc. Surg. 2008. Vol. 136 (3). P. 623-630, 630.e1-5. doi: 10.1016/j. jtcvs.2008.02.080.
- Frigiola A., Ranucci M., Carlucci C., Giamberti A., Abella R., Di donato M. The Ross procedure in Adults: Long-Term Follow-Up and Echocardiographic Changes Leading to Pulmonary Autograft Reoperation//Ann. Thorac. Surg. 2008. Vol. 86 (2). P. 482-489 DOI: 10.1016/j.athoracsur.2008.04.001
- Kouchoukos N.T. Aortic allografts and pulmonary autograft for replacement of the aortic valve and aortic root//Ann. Thorac. Surg. 1999. Vol. 67 (6). P. 1846-1848.
- Караськов А.М., Шарифулин Р.М., Богачев-Прокофьев А.В., Демин И.И., Железнев С.И., Опен А.Б. Коррекция аортальных пороков в сочетании с расширением восходящей аорты у взрослых пациентов: сравнение процедуры Росса и операции Бенталла-Де Боно//Патология кровообращения и кардиохирургия. 2015. Т. 19. № 3. С. 50-57.
- David T.E., David C., Woo A., Manlhoit C. The Ross procedure: outcomes at 20 years//J. Thorac. Cardiovasc. Surg. 2014. Vol. 147 (1). P. 85-93 DOI: 10.1016/j.jtcvs.2013.08.007
- Skillington P.D., Mokhles M.M., Takkenberg J.J., O'Keefe M., Grigg L., Wilson W., Larobina M., Tatoulis J. Twenty-year analysis of autologous support of the pulmonary autograft in the Ross procedure//Ann. Thorac. Surg. 2013. Vol. 96 (3). P. 823-829 DOI: 10.1016/j.athoracsur.2013.04.019
- Takkenberg J.J., Klieverik L.M., Schoof P.H., van Herwerden L.A., Zondervan P.E., Roos-Hesselink J.W., Eijkemans M.J., Yacoub M.H., Bogers A.J. The Ross procedure: a systematic review and meta-analysis//Circulation. 2009. Vol. 119 (2). P. 222-228.
- Skillington P.D., Mokhles M.M., Takkenberg J.J., Larobina M., O'Keefe M., Wynne R., Tatoulis J. The Ross procedure using autologous support of the pulmonary autograft: techniques and late results//J. Thorac. Cardiovasc. Surg. 2015. Vol. 149 (2 Suppl). P. S46-52 DOI: 10.1016/j.jtcvs.2014.08.068
- Carrel T. The autograft inclusion: An obligatory step to avoid late failure following the Ross procedure?//J. Thorac. Cardiovasc. Surg. 2015. Vol. 149 (2 Suppl). P. S53-54. doi: 10.1016/j. jtcvs.2014.09.023.
- Carrel T., Schwerzmann M., Eckstein F., Aymard T., Kadner A. Preliminary results following reinforcement of the pulmonary autograft to prevent dilatation after the Ross procedure//J. Thorac. Cardiovasc. Surg. 2008. Vol. 136 (2). P. 47275 DOI: 10.1016/j.jtcvs.2008.02.004
- Carrel T., Schonhoff F., Aymard T., Kadner A. Reinforcement of the pulmonary autograft with a prosthtic graft to prevent dilatation after the Ross procedure//Oper. Tech. Thorac. Cardiovasc. Surg. 2012. Vol. 17 (1). P. 41-43 DOI: 10.1053/j.optechstcvs.2011.02.001
- Juthier F., Banfi C., Vincentelli A., Ennezat P.V., Le Tourneau T., Pincon C., Prat A. Modified Ross operation with reinforcement of the pulmonary autograft: six-year results//J. Thorac. Cardiovasc. Surg. 2010. Vol. 139 (6). P. 1420-1423 DOI: 10.1016/j.jtcvs.2010.01.032
- Чернов И.И., Козьмин Д.Ю., Уртаев Р.А., Тунгусов Д.С., Макеев С.А., Демецкая В.В., Козлова К.А., Тарасов Д.Г. Результаты операции Росса у больных с пороками аортального клапана//Кардиология и сердечно-сосудистая хирургия. 2013. Т. 6. № 1. С. 72-75.


