Низкочастотные колебания микрососудов кожи: динамика, синхронизация и соответствие изменениям сосудистого тонуса в ходе тилт-теста
Автор: Миронов С.А., Киселев А.Р., Симонян М.А., Шварц В.А., Караваев А.С., Боровкова Е.И., Ишбулатов Ю.М., Попова Ю.В., Посненкова О.М., Гриднев В.И.
Журнал: Саратовский научно-медицинский журнал @ssmj
Рубрика: Кардиология
Статья в выпуске: 3 т.15, 2019 года.
Бесплатный доступ
Цель: изучить динамику низкочастотных колебаний (LF; основная частота около 0,1 Гц) в спектрах пальцевых фотоплетизмограмм (ФПГ), их синхронизацию с подобным LF-ритмом в кардиоинтервалограмме (КИГ) и соответствие изменениям сосудистого тонуса в течение тилт-теста у здоровых добровольцев. Материал и методы. Проанализированы синхронные записи КИГ, дыхания, реовазографии левого плеча и ФПГ с ладонных поверхностей дистальных фаланг безымянных пальцев, а также данные центральной гемодинамики методом импедансной реокардиографии у 30 здоровых добровольцев в течение тилт-теста. Изучена динамика LF- колебаний в сигналах ФПГ, их связь (в т.ч. синхронизация) с аналогичными колебаниями в КИГ и показателями сосудистого тонуса. Результаты. На этапах тилт-теста значения мощности LF- колебаний в спектрах ФПГ не имели статистически значимых отличий. В период ортостаза индекс синхронизации LF-колебаний увеличивался (р
Вариабельность ритма сердца, вегетативная регуляция, периферический сосудистый тонус, фотоплетизмограмма
Короткий адрес: https://sciup.org/149135390
IDR: 149135390 | УДК: 537.86
Low-frequency skin microvascular oscillations: dynamics, synchronization and compliance with changes in vascular tone during the tilt test
The purpose is to study the dynamics of low-frequency oscillations (LF; basic frequency of about 0.1 Hz) in the spectra of fingerprint photoplethysmograms (PPG), their synchronization with a similar LF-rhythm in cardiointervalogram (CIG) and compliance with changes in vascular tone during the tilt test in healthy volunteers. Material and Methods. Synchronous cardiointerval recording, breathing recording, left shoulder rheovasography and PPG records from the palm surfaces of distal phalanges of anonymous fingers were analyzed, as well as central hemodynamics data by impedance rheocardiography in 30 healthy volunteers during the tilt test. Dynamics of LF-oscillations in PPG signals, their interaction (including synchronization) with similar oscillations in CIG and vascular tone parameters were studied. Results. At the stages of tilt test the values of LF-oscillations power in the spectra of PPG had no statistically significant differences. During the tilt test the index of synchronization of LF-oscillations increased (p
Текст научной статьи Низкочастотные колебания микрососудов кожи: динамика, синхронизация и соответствие изменениям сосудистого тонуса в ходе тилт-теста
Однако интерпретация подобных колебаний в периферическом кровотоке, в частности в сигнале фотопле-тизмограмм (ФПГ), остается дискуссионным вопросом.
Фотоплетизмография — один из часто используемых методов для оценки периферического кровотока [11]. Регистрация сигнала ФПГ может выполняться на разных участках тела человека, однако наиболее типичным местом регистрации являются пальцы рук. Сигнал ФПГ характеризует кровенаполнение значительного объема тканей пальца с расположенными в них сосудами различного диаметра и физиологического предназначения (пальцевые артерии, артериолы, капилляры, венулы и вены) [12]. Колебания тока крови в этих сосудах определяют спектральную плотность компонентов сигнала ФПГ. Ранее было показано, что LF-колебания в ритме сердца и в дистальном сосудистом русле, оцениваемом по сигналу ФПГ, периодически синхронизируются друг с другом, обеспечивая функциональное взаимодействие между механизмами вегетативной регуляции в этих отделах ССС [4, 5]. Для удобства оценки степени синхронизации нами предложена мера — индекс S, который показал свое потенциально важное клиническое значение [5].
Традиционно LF-колебания рассматривают в качестве маркера симпатической активности на уровне сердца, АД и микроциркуляторного русла [13].
Цель: изучить динамику LF-колебаний, выделенных из пальцевых фотоплетизмограмм, их синхронизацию с подобным (0,1 Гц) ритмом в кардиоинтер-валограмме и соответствие изменениям сосудистого тонуса в период проведения пассивной ортостатической пробы (тилт-теста) у здоровых добровольцев.
Решение поставленной цели имеет значение для развития диагностических методов в кардиологии.
Материал и методы. В исследование включено 30 здоровых волонтеров (26 мужчин и 4 женщины) в возрасте 26,5 (25,0; 29,0) года, с индексом массы тела 24,0 (22,0; 25,7) кг/м2 (данные представлены в виде медианы и квартильного диапазона), без пред- и обморочных состояний в анамнезе. Все испытуемые дали информированное добровольное согласие на участие в исследовании.
Всем добровольцам при спонтанном дыхании проведен тилт-тест с углом наклона стола 70º. Выполнялась синхронная регистрация электрокардиограммы (ЭКГ), дыхания (при помощи респираторного пояса), реокардиографии, реовазографии (РВГ) левого плеча и ФПГ с ладонных поверхностей дистальных фаланг безымянных пальцев. Указанные биологические сигналы регистрировались при помощи реографа-полианализатора РГПА-6/12 «Реан-Поли» (модификация 04) (Медиком МТД, Россия).
Перед началом пробы испытуемый находился в положении лёжа в расслабленном бодрствовании не менее 10 минут. Синхронную регистрацию сигналов производили через 3 минуты от начала каждого этапа функциональной пробы (положение «лёжа»/по-ложение «стоя») продолжительностью по 10 минут (данные использовались для оценки нервной регуляции). С 11-й минуты, в течение 60±10 секунд, рассчитывались показатели центральной гемодинамики (в анализ включали 10 последовательных сердечных сокращений) и частота дыхания. В целом тилт-тест продолжался около 35–40 минут. Все исследования проводились в одно и то же время суток (13.00–17.00). Для дальнейшего анализа отбирались записи сигналов, не содержащие помех, экстрасистол, заметного линейного тренда и переходных процессов.
При анализе ВСР оценивались следующие показатели [1]: средняя частота сердечных сокращений (ЧСС), мощности высокочастотного (high frequency — HF 0,15–0,4 Гц) и низкочастотного (low frequency — LF 0,04–0,15 Гц) диапазонов спектра, выраженные в нормализованных единицах (далее по тексту обозначены как HF, n. u. и LF, n. u. соответственно), а также показатель LF/HF Аналогичные показатели вычислены и для сигналов ФПГ. Также вычислялось значение индекса синхронизации ( S )
для LF-колебаний, выделенных из ВСР и ФПГ, согласно ранее описанной нами методике [5].
Методом тетраполярной грудной реографии по В. Г. Кубичеку рассчитывали ударный объем крови, оценивали факторы, определяющие величину сердечного выброса. Для нивелирования индивидуальных антропометрических особенностей изучаемые показатели приводили к площади поверхности тела, определяемой по формуле Дюбуа.
С помощью двух идентичных рефлектометриче-ских ФПГ-датчиков определяли амплитуду систолической волны (АСВ), характеризующую пульсовое кровенаполнение сосудов. Конструктивно ФПГ-датчики были интегрированные, расстояние между светодиодом (950 нм) и фотоприёмником 1,8 мм, что предполагает максимум восприятия на глубине до 1,0 мм.
Используя РВГ и ФПГ, оценивали время распространения пульсовой волны (время от зубца R синхронно записанной ЭКГ до начало очередной рео-графической или фотоплетизмографической волны), характеризующее суммарное состояние артерий, расположенных выше исследуемого участка, главным образом их упругоэластические свойства и тонус [14, 15]. Далее рассчитывали скорость распространения пульсовой волны (СРПВ, м/с), по смыслу показатель аналогичен предыдущему, но учитывает расстояние, пройденное пульсовой вольной, т. е. нивелирует антропометрические отличия участвующих в исследовании добровольцев. Определяли комбинированную СРПВ (аортопальцевой сегмент), отдельно на уровне артерий эластического (аортоподмышечный сегмент, СРПВ э) и мышечного типов (плечепальцевой сегмент, СРПВ м), а также отношение СРПВ м/э.
Контроль уровня артериального давления осуществлялся с помощью автоматического тонометра на плечо Omron i-C10.
Статистические расчеты выполнялись при помощи программного пакета Statistica 6.1. Исходно все данные проверены на соответствие закону нормального распределения на основе критерия Шапиро — Уилка. Выявлено, что структура некоторых параметров не описывается законом нормального распределения, поэтому дальнейшие исследования зависимостей производились методами непараметрической статистики. Анализ показателей в динамике проводился с помощью критерия Уилкоксона для связанных выборок и с помощью метода Манна — Уитни для несвязанных выборок. Данные представлены в виде медианы и значений квартильного диапазона Ме (25%; 75%). Для исследования корреляционных связей применяли непараметрический критерий Спирмена. Надежность используемых статистических оценок принималась не менее 95%.
Результаты. Тилт-тест не спровоцировал синкопе ни у одного из добровольцев. Изменения частоты дыхания и показателей центральной гемодинамики в ходе функциональной пробы представлены в табл. 1. В положении «стоя» регистрировались
Таблица 1
Изменение показателей центральной гемодинамики в ходе тилт-теста у здоровых лиц
|
Показатель |
Этапы функциональной пробы |
р |
∆, % |
|
|
Положение «лёжа», n=30 |
Положение «стоя», n=30 |
|||
|
Средняя ЧД, кол/мин |
15,8 (14,3; 18,1) |
16,2 (14,5; 19,3) |
0,903 |
|
|
Средняя ЧСС, уд/мин |
60,0 (55,0; 63,0) |
80,5 (74,0; 90,0) |
<0,001 |
35,0 (28,2; 44,6) |
|
СД, мм рт. ст. |
117,0 (110,0; 125,0) |
116 (108,0; 128,0) |
0,751 |
–2,7 (–9,0; 1,8) |
|
Показатель |
Этапы функциональной пробы |
р |
∆, % |
|
|
Положение «лёжа», n=30 |
Положение «стоя», n=30 |
|||
|
ДД, мм рт. ст. |
70,0 (69,0; 75,0) |
84,0 (78,0; 88,0) |
<0,001 |
18,8 (12,5; 23,9) |
|
ПД, мм рт. ст. |
45,0 (40,0; 50,0) |
32,0 (26,0; 39,0) |
<0,001 |
–34,0 (–43,1; –26,6) |
|
САД, мм рт. ст. |
91,0 (87,0; 95,0) |
97,0 (92,0; 105,0) |
0,013 |
6,3 (2,1; 10,9) |
|
КДДЛЖ, мм рт. ст. |
11,8 (11,1; 12,5) |
10,0 (8,9; 10,7) |
<0,001 |
–14,9 (–23,7; –9,5) |
|
УИ, мл/м2 |
50,2 (42,4; 61,5) |
27,5 (20,6; 33,0) |
<0,001 |
–47,2 (–56,7; –34,5) |
|
СИ, л/(мин*м2) |
3,0 (2,6; 3,5) |
2,2 (1,8; 2,5) |
<0,001 |
–29,1 (–37,1; –13,0) |
|
DO2I, мл/мин/м2 |
558,0 (485,4; 654,7) |
416,6 (334,8; 465,0) |
<0,001 |
–29,1 (–37,1; –13,0) |
|
ИОПСС, дин*с/см-5/м2 |
2411,6 (2020,2; 2683,6) |
3818,4 (3085,1; 4509,4) |
<0,001 |
62,4 (43,3; 82,1) |
Примечание: данные представлены в виде медианы и квартильного диапазона Ме (25%; 75%); ЧД — частота дыхания; ЧСС — частота сердечных сокращений; СД — систолическое артериальное давление; ДД — диастолическое артериальное давление; ПД — пульсовое давление; САД — среднее артериальное давление; КДДЛЖ — конечное диастолическое давление в полости левого желудочка; УИ — ударный индекс; СИ — сердечный индекс; DO2I — индекс доставки кислорода; ИОПСС — индекс общего периферического сосудистого сопротивления.
Таблица 2
Изменение пульсового кровенаполнения по данным фотоплетизмографии в ходе тилт-теста у здоровых лиц
|
Показатель |
Положение «лёжа», n=30 |
Положение «стоя», n=30 |
р |
∆, % |
|
АСВ-R, pm |
3,7 (1,0; 4,4) |
0,8 (0,5; 1,5) |
<0,001 |
–58,9 (–81,4; –30,0) |
|
АСВ-L, pm |
4,3 (2,0; 5,8) |
1,2 (0,7; 2,2) |
<0,001 |
–59,6 (–77,7; –37,1) |
Примечание: данные представлены в виде медианы и квартильного диапазона Ме (25%; 75%); АСВ — амплитуда систолической волны на уровне дистальной фаланги безымянного пальца; R — правая рука; L — левая рука.
Таблица 3
|
Сегмент |
Этапы функциональной пробы |
р |
∆,% |
|
|
Положение «лёжа», n=30 |
Положение «стоя», n=30 |
|||
|
Аортопальцевой (R), м/с |
6,5 (6,2; 6,9) |
6,36 (6,0; 6,6) |
0,211 |
|
|
Аортопальцевой (L), м/с |
6,7 (6,4; 7,1) |
6,31 (5,82; 6,6) |
<0,001 |
|
|
Аортоподмышеч. (L), м/с |
3,6 (3,4; 3,9) |
3,0 (2,8; 3,3) |
<0,001 |
|
|
Плечепальцевой (L), м/с |
13,6 (12,2; 16,9) |
18,6 (14,3; 21,6) |
0,002 |
18,3 (–0,8; 49,2) |
|
СРПВ м/э (L) |
3,5 (3,2; 4,5) |
5,8 (4,2; 7,3) |
0,001 |
39,2 (10,1; 81,0) |
Примечание: данные представлены в виде медианы и квартильного диапазона Ме (25%; 75%); СРПВ м/э — тонус сосудистой стенки; R — правая сторона; L — левая сторона.
Динамика скорости распространения пульсовой волны в ходе тилт-теста у здоровых лиц
достоверные изменения показателей пред-, постнагрузки и насосной функции сердца, а также снижение транспорта кислорода к тканям (DO 2 I) на ~30%.
В табл. 2 показано снижение пульсового кровенаполнения от исходных значений (∆АСВ) в симметричных отведениях. При этом корреляционные связи между АСВ и спектральными индексами ФПГ (LF, n. u.; LF/HF) на этапах тилт-теста отсутствовали.
Визуально колебания периферического кровотока, наблюдаемые в симметричных областях кожи в течение времени, демонстрировали стабильную синхронность в положении как «лёжа», так и «стоя» (рис. 1).
В табл. 3 представлена динамика СРПВ в различных сегментах сосудистого русла. Все изменения статистически значимые. Обращает на себя внимание увеличение СРПВ на уровне артерий мышечного типа вследствие повышения нейрогенного сосудистого тонуса (ДСРПВ м/э: 39,2%). Показатель тонуса сосудов и LF-колебания ФПГ-спектров (СРПВ м/э — LF, n. u.) на этапах тилт-теста не коррелировали.
В табл. 4 показана динамика сердечных сокращений, частоты дыхания и показателей вегетативной регуляции ССС на этапах тилт-теста. В положении «лёжа» ЧСС и ЧД соответствовали состоянию покоя.
В положении «лёжа» доля HF-колебаний в спектре ВСР значимо превышала соответствующий показатель в пальцевых ФПГ-спектрах (р<0,001). Пальцевые ФПГ-спектры имели сопоставимые значения по этому показателю (р>0,05), коэффициент корреляции r=0,47 (р < 0,01).
В положении «стоя» наблюдалась разнонаправленная динамика HF-колебаний в изучаемых спектрах. Так, в ВСР она понижалась (р<0,001), а в ФПГ повышалась, причем в отведении слева изменения имели статистическую значимость (р<0,01). Пальцевые ФПГ-спектры, как и в положении «лёжа», не имели достоверных отличий в HF-диапазонах (рис. 2). Коэффициент корреляции показателей (HF, n. u.) увеличился до умеренной силы связи (r=0,67, р < 0,001).
В положении «лёжа» доля LF-колебаний в спектре ВСР значимо отличалась в меньшую сторону от соот-
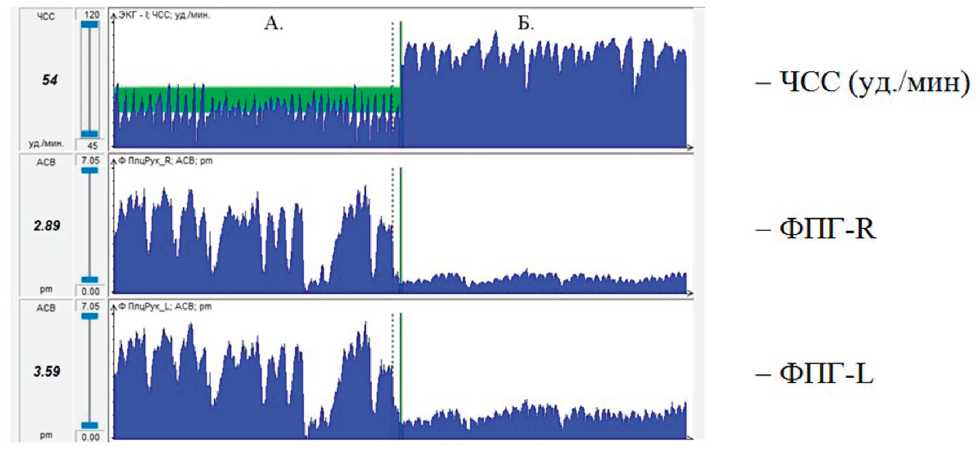
Рис. 1. Одновременная регистрация сердечных сокращений и периферического кровотока в правом (R) и левом (L) безымянных пальцах одного здорового добровольца. Обращает на себя внимание сходство симметричных ФПГ. ФПГ-сигналы показывают синхронное присутствие медленных (в диапазоне 0,1 Гц) колебаний
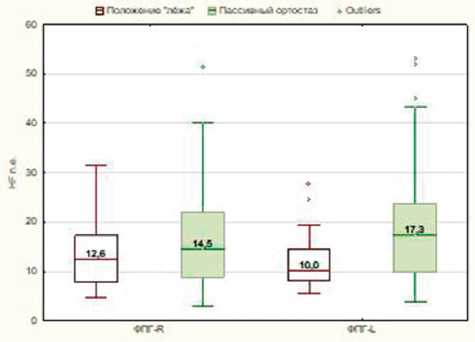
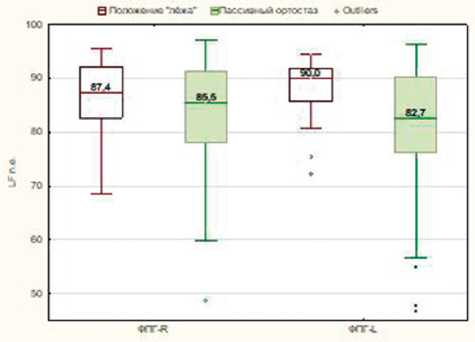
Рис. 2. Динамика HF- и LF-колебаний ФПГ-спектров на этапах тилт-теста. Показано отсутствие достоверной разницы в HF-и LF-диапазонах ФПГ-спектров, выраженных в нормализованных единицах, в положении как «лёжа», так и «стоя»
Таблица 4
Динамика частоты дыхания и показателей вегетативной регуляции сердечно-сосудистой системы в ходе тилт-теста у здоровых лиц
|
Показатель |
Этапы функциональной пробы |
р |
∆, % |
|
|
Положение «лёжа», n=30 |
Пассивный ортостаз, n=30 |
|||
|
Средняя ЧД, кол/мин |
17,4 (15,1; 18,1) |
17,2 (15,4; 19,8) |
0,424 |
|
|
Средняя ЧСС, уд/мин |
60,0 (56,0; 65,0) |
80,0 (75,0; 89,0) |
<0,001 |
|
|
HF, n. u. в спектре ВСР |
55,1 (42,0; 65,8) |
24,9 (13,5; 35,7) |
<0,001 |
|
|
HF, n. u. в спектре ФПГ-R |
12,5 (7,8; 17,3) |
14,5 (8,8; 22,0) |
0,216 |
5,9 (–44,1; 162,0) |
|
HF, n. u. в спектре ФПГ-L |
10,0 (8,2; 14,3) |
17,3 (9,7; 23,7) |
0,007 |
48,9 (2,7; 150,9) |
|
LF, n. u. в спектре ВСР |
44,8 (34,1; 57,9) |
75,0 (64,2; 86,4) |
<0,001 |
48,9 (27,8; 121,5) |
|
LF, n. u. в спектре ФПГ-R |
87,4 (82,6; 92,1) |
85,4 (77,9; 91,1) |
0,612 |
–0,8 (–17,6; 5,8) |
|
LF, n. u. в спектре ФПГ-L |
89,9 (85,6; 91,7) |
82,6 (76,2; 90,2) |
0,008 |
–5,4 (–17,1; –0,2) |
|
LF/HF в спектре ВСР |
0,8 (0,5; 1,3) |
3,0 (1,7; 6,3) |
<0,001 |
|
|
LF/HF в спектре ФПГ-R |
6,9 (4,7; 11,7) |
5,8 (3,5; 10,3) |
0,325 |
|
|
LF/HF в спектре ФПГ-L |
9,0 (5,9; 11,1) |
4,7 (3,2; 9,2) |
0,047 |
|
|
Показатель |
Этапы функциональной пробы |
р |
∆, % |
|
|
Положение «лёжа», n=30 |
Пассивный ортостаз, n=30 |
|||
|
S (ВСР-ФПГ-R), % |
38,1 (30,3; 44,2) |
46,7 (36,4; 58,5) |
0,007 |
27,7 (4,7; 59,7) |
|
S (ВСР-ФПГ-L), % |
36,6 (30,8; 45,2) |
51,3 (39,3; 57,2) |
0,008 |
25,8 (4,9; 48,0) |
Примечание: данные представлены в виде медианы и квартильного диапазона Ме (25%; 75%); ЧСС — частота сердечных сокращений; ЧД — частота дыхания; ВСР — вариабельность сердечного ритма; ФПГ-R (L) — спектр вариабельности фотоплетизмографической волны, зарегистрированный с дистальной фаланги безымянного пальца правой (R) или левой (L) руки; S — индекс синхронизации LF-колебаний в ВСР и ФПГ. Спектральные оценки ВСР и ФПГ оценивались с 1-й по 5-ю минуту включительно в течение каждого этапа функциональной пробы. ЧСС, ЧД и индекс S оценивались в течение 10 минут на каждом этапе функциональной пробы.
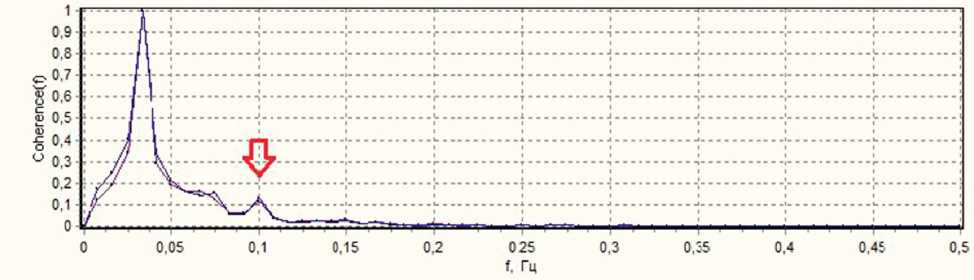
Рис. 3. Спектральная плотность мощности в диапазоне 0,005–0,5 Гц ФПГ-сигналов. Обращает на себя внимание сходство спектрального состава обоих ФПГ-сигналов, имеется четкий пик около 0,1 Гц-частоты (низкочастотные колебания, LF)
ветствующего показателя обеих ФПГ (р<0,001). Пальцевые ФПГ-спектры имели сопоставимые значения в LF-диапазонах (р>0,05). Коэффициент корреляции показателей (LF, n. u.) имел слабую силу связи (r=0,47, р < 0,01).
В положении «стоя» наблюдалась разнонаправленная динамика LF-колебаний в изучаемых сигналах. Так, в ВСР она повышалась (р<0,001), а в обеих ФПГ снижалась, причем в отведении слева изменения имели статистическую значимость (р<0,01). Пальцевые ФПГ-спектры, как и в положении «лёжа», не имели достоверных отличий в LF-диапазонах (р>0,05), коэффициент корреляции показателей (LF, n. u.) увеличился до r=0,67 (р<0,001).
Выявлена слабая корреляционная зависимость LF-колебаний, полученных из различных сигналов. Так, для пары (ВСР — ФПГ-R) в положении «лёжа» r=0,31 (р=0,09, близкое к достоверному), в положении «стоя» r=0,41 (р<0,05); для пары (ВСР — ФПГ-L) в положении «лёжа» r=0,39 (р<0,05), в положении «стоя» r=0,21 (р=0,25, статистически не значимо).
На рис. 3 показаны ФПГ-спектры, полученные по тем же данным, что и на рис. 1. Спектры из двух симметричных областей очень похожи, что подтверждается визуальным впечатлением от подобных волн, присутствующих в этих двух сигналах.
В период тилт-теста регистрировалось повышение показателя LF/HF в ВСР и его снижение в пальцевых ФПГ При этом повышение уровня LF/HF в ВСР обусловлено значимым увеличением мощности LF-колебаний на фоне снижения мощности HF-колебаний. Снижение показателя LF/HF в пальцевых ФПГ происходило в результате увеличения общей мощности колебаний в этих спектрах преимущественно за счет HF-диапазона. Важно отметить, что доля колебаний в LF-диапазоне в изучаемых ФПГ-спектрах значительно превышала долю колебаний в HF-диапазоне на всех этапах наблюдения, что и объясняет высокие значения показателя LF/HF в этих сигналах.
На этапах тилт-теста показатель LF/HF в пальцевых ФПГ имел схожие значения (р>0,05).
Индекс S между 0,1 Гц-колебаниями ВСР и каждой ФПГ на этапах тилт-теста был схожим (р>0,05). Переход в вертикальное положение сопровождался достоверным увеличением синхронизованности 0,1 Гц-ритмов для каждой изучаемой пары колебаний (р<0,01).
Обсуждение. Тилт-тест у здоровых испытуемых вызывает стремительный отток венозной крови из органов грудной клетки в регионы, расположенные ниже диафрагмы. Основная масса венозной крови смещается в первые 10 секунд и почти полностью завершается к 3–5-й минуте ортостатического стресса. Дополнительный венозный объем в органы брюшной полости, таза и нижних конечностях может составлять 0,5–1,0 л. Кроме этого, снижение объема циркулирующей крови происходит и из-за снижения объема плазмы за счет транскапиллярной фильтрации в интерстиций. Подсчитано, что через 5 минут объем плазмы уменьшается на 10% (500 мл), а через и 10 минут на 15-20% (700 мл) [16]. Снижение предна-грузки на правое сердце вызывает падение ударного объема левого желудочка и, как результат, уменьшение сердечного выброса приблизительно на 20%. Для поддержания достаточного гемодинамического ответа в условиях пониженного сердечного выброса активируется целая группа рефлексов, направленных на повышение тонуса симпатического звена вегетативной нервной системы. Увеличивается ЧСС, сократимость миокарда, повышается тонус резистивных и емкостных сосудов. За счет подобных компенсаторных реакций, направленных на предупреждение церебральной гипоперфузии, в представленном исследовании у здоровых лиц среднее артериальное давление поддерживалось на оптимальном для данной нагрузки уровне (АСАД 6,3%, p<0,05).
В период пассивного ортостаза в исследуемой группе добровольцев производительность сердца (АСИ) упала на 29,1% (р<0,001), а периферический кровоток (ААСВ) на ~б0% (р<0,0о1). Среднее артериальное давление поддерживалось за счет увеличения сердечных сокращений (АЧСС 35,0%, р<0,001) и периферического сосудистого сопротивления (АИоПсС 62,4%, р<0,001). Другие функции сердечно-сосудистой системы (преднагрузка, сократимость миокарда, тонус емкостных сосудов и др.) в данной работе не анализировались.
Уменьшение пульсового кровенаполнения (АСВ) в течение пассивного ортостаза обусловлено в том числе снижением ударного объема крови и увеличением сосудистого тонуса. В качестве показателя, характеризующего тонус сосудистой стенки, мы использовали отношение скорости распространения пульсовой волны по сосудам мышечного типа к таковой по сосудам эластического типа (СРПВ м/э). В нашей работе динамика этого показателя совпадала с динамикой общего периферического сосудистого сопротивления. В положении «стоя» коэффициент корреляции в этой паре показателей (СРПВ м/э — ИОПСС) имел умеренную силу связи (r=0,60, p<0,05). Считается, что косвенные изменения в нейрогенном тонусе средних и крупных сосудах отражает СРПВ, а в резистивных — общее периферическое сосудистое сопротивление.
ЧСС как показатель хронотропной функции сердца определяется активностью симпатической нервной системы. По нашим данным, увеличение относительной мощности LF-колебаний в спектре ВСР в период вертикализации привело к росту ЧСС на 35% (см. табл. 4). Физиологическая связь между LF-колебаниями в ВСР и ЧСС вполне очевидна. Подобную зависимость мы ожидали увидеть и между LF-колебаниями в микрососудах кожи с упомянутыми показателями сосудистого тонуса. Полагали, что вариабельность ФПГ-волны в основном определяется тонусом артериол дермального слоя кожи. Однако воздействие ортостатического стресса не привело к достоверным изменениям в LF-диапазонах ФПГ-спектров. Динамика данных колебаний, выраженных в нормализованных единицах, была достаточно скромной и в сравнении со спектром ВСР имела обратную направленность. Мы не нашли также достоверных корреляций между уровнем относительной мощности (LF, n. u.) LF-колебаний и величиной сосудистого тонуса по показателям ИОПСС и СРПВ м/э. Таким образом, объяснить почему в период пассивного ортостаза среднее артериальное давление оставалось на уровне, обеспечивающем нормальную перфузию тканей, пока затруднительно.
Ранее нами показана высокая когерентность в пальцевых ФПГ-спектрах (диапазон 0,005–0,5 Гц) у большинства исследованных здоровых добровольцев в положении «лёжа» и у меньшего числа в положении «стоя» [17]. Тот факт, что LF-колебания синхронно изменяются в симметричных участках (дистальные фаланги безымянных пальцев), подтверждает наличие центральных вегетативных механизмов, модулирующих периферический кровоток. В исследовании [18] выдвинута гипотеза об автоколебательной природе и функциональной автономности подсистемы вегетативной регуляции, участвующей в регуляции кожного кровотока на частоте, близкой к 0,1 Гц. Синхронизация LF-колебаний, выделенных из различ- ных сигналов ССС, — это еще одно подтверждение в пользу вегетативного происхождения низкочастотных колебаний в микрососудах кожи. Взаимодействие двух контуров регуляции («сердечный ритм — дистальный кровоток») позволяет судить о качестве вегетативного управления ССС и ее адаптационных возможностей. Например, наблюдается значительное снижение индекса S у пациентов с острым инфарктом миокарда по сравнению с контрольной группой, не имеющей признаков сердечной патологии [5].
Все здоровые добровольцы нашего исследования имели отрицательный результат тилт-теста (отсутствие предсинкопе или синкопе). Этот факт позволяет говорить о состоятельности механизмов вегетативной регуляции ССС, обладающих необходимым функциональным резервом. Подтверждением тому была динамика индекса S . В целом по группе этот показатель достоверно увеличивался (ВСР-ФПГ-R на 27,7%; ВСР-ФПГ-L на 25,8%), характеризуя таким образом «плотность» взаимодействия двух подсистем вегетативной регуляции в меняющихся условиях функционирования системы «сердце — сосуды».
Остается открытым вопрос о структурах микро-сосудистого русла кожи, определяющих колебания кровотока, а следовательно, изменения объемов DC-и AC-компонент в ФПГ-сигнале. Одни авторы [19] считают, что в основе лежит тонус артериол, другие [20] придерживаются мнения, что ФПГ-волна есть результат открытых артериовенозных анастомозов. Допустим, что элементы дистального русла, через которые происходит модуляция кровотока с частотой около 0,1 Гц, уже известны. Тогда с учетом полученных данных можно заключить следующее: а) независимо от положения тела в пространстве относительная мощность LF-колебаний в ФПГ-спектрах с симметричных отведений имеет сопоставимые значения (р>0,05); б) в период пассивного ортостаза происходит незначительное перераспределение спектральной плотности в ФПГ-сигналах в пользу HF-колебаний. Напомним, что HF-колебания являются отражением пассивного влияния вдоха и выдоха на периферическое кровообращение.
Главным ограничением метода ФПГ является отсутствие возможности измерять колебания кровотока в абсолютных единицах. Кроме этого, информация в ФПГ-сигнале получена с достаточно большого объема зондируемой ткани, содержащей огромное количество микрососудов с различными диаметрами, физиологическим предназначением и свойственными флуктуациями. Поэтому говорить о какой-то конкретной части микрососудистого русла дермального слоя кожи, являющейся потенциальным источником LF-колебаний, пока преждевременно. Мы анализировали ФПГ-сигналы с дистальных фаланг пальцев, которые богаты артериовенозными анастомозами (до 500 на 1 см2). Возможно, исследовав кожу с другой части тела, мы получим иную спектральную плотность колебаний в периферическом кровотоке.
Измерение артериального давления нами проводилось дискретно. Отсутствие возможности непрерывно (beat-to-beat) отслеживать колебания артериального давления в ситуациях, когда режим кровообращения быстро изменяется (например, тилт-тест), неизбежно сказывается на точности получаемых данных. Применительно к нашему исследованию ошибочные данные о среднем артериальном давлении искажают величину общего периферического сосудистого сопротивления. Вероятно, с этим ограничением связано отсутствие зависимости между сосудистым сопротивлением и относительной мощностью LF-колебаний в ФПГ-спектрах.
Заключение. Следует подчеркнуть, что, оценивая мощность LF-колебаний (ФПГ-сигнал) в относительных единицах, мы до конца не знаем, как в действительности меняется их динамика. Группе здоровых добровольцев мы провели пробу с пассивным ортостазом, которая не выявила достоверных отличий в значениях мощности LF-колебаний (LF, n. u.) в микрососудах кожи. Подобная динамика показателя (LF, n. u.) совсем не соответствовала изменениям сосудистого тонуса на уровне крупных/средних и резистивных сосудов. Допустим, что управлению кожного кровотока присущи индивидуальные отличия (с учетом одинаковых условий для участников), направленные на достижение какой-то «главной» цели. Тогда характерные для каждого индивида отличия в вегетативной регуляции могут нивелироваться в общей группе. Это предположение будет результатом наших дополнительных исследований.
В ходе исследования показано, что у здоровых добровольцев в период пассивного ортостаза происходит усиление взаимодействия подсистем вегетативной регуляции («сердечный ритм — дистальный кровоток»). Индекс S достоверно увеличивался в обеих парах исследуемых сигналов (ВСР-ФПГ-R, ВСР-ФПГ-L), подчеркивая функциональную целостность системы вегетативного управления ССС.
Список литературы Низкочастотные колебания микрососудов кожи: динамика, синхронизация и соответствие изменениям сосудистого тонуса в ходе тилт-теста
- Heart rate variability: Standards of measurement, physiological interpretation, and clinical use/Task Force of the European Society of Cardiology and The North American Society of Pacing and Electrophysiology. European Heart Journal 1996; 17:354-81.
- Parati G, Saul JP, Di Rienzo M, et al. Spectral analysis of blood pressure and heart rate variability in evaluating cardiovascular regulation: A critical appraisal. Hypertension 1995; 25: 1276-86.
- Liao F, Jan Y-K. Enhanced phase synchronization of blood flow oscillations between heated and adjacent non-heated sacral skin. Med Biol Eng Comput2012; 50 (10): 1059-70.
- Karavaev AS, Prokhorov MD, Ponomarenko VI, et al. Synchronization of low-frequency oscillations in the human cardiovascular system. Chaos 2009; 19 (3): 1-7.
- Kiselev AR, Karavaev AS, Gridnev VI, et al. Method of estimation of synchronization strength between low- frequency oscillations in heart rate variability and photoplethysmographic waveform variability. Russ Open Med J 2016; 5: e0101.
- Nollo G, Faes L, Porta A, et al. Exploring directionality in spontaneous heart period and systolic pressure variability interactions in humans: Implications in the evaluation of baroreflex gain. Am J Physiol Heart Circ Physiol 2005; 288: 1777-85.
- Julien C, Malpas SC, Stauss HM. Sympathetic modulation of blood pressure variability. J Hypertens 2001; 19 (10): 1707-12.
- Wray DW, Fadel PJ, Keller DM, et al. Dynamic carotid baroreflex control of the peripheral circulation during exercise in humans. Journal of Physiology 2004; 559 (2): 675-84.
- Cooley RL, Montano N, Cogliati C, et al. Evidence for a central origin of the low-frequency oscillation in RR- interval variability. Circulation 1998; 98 (6): 556-61.
- DeBoerRW, Karemaker JM, Strackee J. Hemodynamic fluctuations and baroreflex sensitivity in humans: A beat-to-beat model. Am J Physiol Heart Circ Physiol 1987; 253 (3): 680-89.
- Allen J. Photoplethysmographyanditsapplication in clinical physiological measurement. physiological measurement 2007; 28(3): 1-39.
- Higgins JL, Fronek A. Photoplethysmographic evaluation of the relationship between skin reflectance and skin blood volume. Journal of Biomedical Engineering 1986; 8 (2): 130-6.
- Bernardi L. Synchronous and baroceptor-sensitive oscillations in skin microcirculation: Evidence for central autonomic control. Am J Physiol Heart Circ Physiol 1997; 273 (442-4): 1867-78.
- Зенков Л.Р, Ронкин M.A. Функциональная диагностика нервных болезней: рук-во для врачей. 5-е изд. М.: МЕДпресс-информ, 2013; 488 с.
- Иванов Л. Б., Макаров В.А. Лекции по клинической реографии. М.: АОЗТ "Антидор", 2000; 320 с.
- Smit AAJ, Halliwill JR, Low PA, Wieling W. Pathophysiological basis of orthostatic hypotension in autonomic failure. Journal of Physiology 1999; 519 (1): 1-10.
- Kiselev AR, Mironov SA, Karavaev AS, et al. A comprehensive assessment of cardiovascular autonomic control using photoplethysmograms recorded from the earlobe and fingers. Physiological Measurement 2016; 37 (4): 580-95.
- Karavaev AS, Kiselev AR, Gridnev VI, et al. Phase and frequency locking of 0.1-Hz oscillations in heart rate and baroreflex control of blood pressure by breathing of linearly varying frequency as determined in healthy subjects. Human Physiology 2013; 39 (4): 416-25.
- Spigulis J. Optical noninvasive monitoring of skin blood pulsations. Applied Optics 2005; 44 (10): 1850-57.
- Kim JM, Arakawa K, Benson KT, et al. Pulse oximetry and circulatory kinetics associated with pulse volume amplitude measured by photoelectric plethysmography. Anesthesia and Analgesia 1986; 65 (12): 1333-9.


