Новая технология моделирования безаллергенного пространства в период сна у больных атопической бронхиальной астмой
Автор: Аверьянов Александр Вячеславович, Ильина Наталья Ивановна, Сокуренко Сергей Иванович, Шартанова Наталья Владимировна, Борисова Татьяна Вадимовна, Третьяк А.А.
Журнал: Клиническая практика @clinpractice
Рубрика: Оригинальные исследования
Статья в выпуске: 1 (13), 2013 года.
Бесплатный доступ
Представлены результаты клинического исследования эффективности нового метода очистки воздуха в зоне дыхания пациента при включении его в схему лечения обострения бронхиальной астмы. Показано, что у больных, получавших дополнительную терапию исследуемой технологией Protexo®, достоверно раньше уменьшалась потребность в бронхолитиках и быстрее редуцировалось ощущение одышки. Значимого влияния на параметры внешнего дыхания установлено не было.
Бронхиальная астма, очистка воздуха, безаллергенное пространство, аsthma
Короткий адрес: https://sciup.org/14338442
IDR: 14338442
New method for non allergic space modelling during sleep in patients with atopic asthma
The results of the clinical trial of a new air cleaning method in the breathing zone of the patient with asthma exacerbation are presented. It is shown that in patients treated with additional tech- nology Protexo®, the bronchodilators usage and dispnoe score significantly reduced. Significant effects on respiratory parameters has not been established.
Текст научной статьи Новая технология моделирования безаллергенного пространства в период сна у больных атопической бронхиальной астмой
Создание безаллергенной среды является важнейшим условием успешного лечения пациентов, страдающих гетерогенными формами аллергических заболеваний верхних и нижних дыхательных путей. Существующие формы элиминации аллергенов из воздушного пространства, окружающего больного, сводятся либо к удалению (изолированию) потенциальных источников и резервуаров аллергенов, либо к очистке воздуха различными способами. Одно из последних крупных исследований, включавшее 3727 взрослых пациентов, оценивало эффективность профилактики обострений атопической астмы в зависимости от разных мер контроля окружающей среды [1].
Авторы пришли к выводу, что для предотв- ращения симптомов заболевания необходимо соблюдать минимум 5 из 8 проанализированных условий. При этом градация эффективности рекомендаций распределилась следующим образом: отсутствие контакта с табачным дымом (80%), отсутствие животных в доме (53,9%), стирка простыней в горячей воде (43,2%), использование очистителей воздуха (27,4%), применение чехлов для подушек (23,7%) и матрасов (23,4%), удаление ковров (14,5%), использование увлажнителей воздуха (13,8%). Как видно, среди технических приспособлений для профилактики астмы наиболее значимыми признаны очистители воздуха. Фильтрационные устройства, способные задерживать взвешенные в воздухе частицы, в том числе аллергены, в настоящее время весьма широко представлены на рынке медицинской и бытовой техники. Разумеется, врачи информируют пациентов о потенциальной пользе таких приборов. Однако, очень часто подобные рекомендации основаны не на строгой доказательной базе, а на информации производителя, позиционирующего свою продукцию как средство для профилактики проявлений респираторной аллергии. Между тем, эффективность большинства бытовых очистителей воздуха или систем кондиционирования зависит не только от степени фильтрации, но и от уровня загрязненности воздушной среды, особенностей вентиляции и объема помещения и своевременной замены фильтров. Известно, что загрязненные фильтры сами контаминированы аллергенами и могут быть колонизированы инфекционными патогенами, особенно спорами грибков, превращаясь со временем в потенциально опасный источник аллергенов [2, 3].
Бытовые воздухоочистители не проходят медицинских испытаний и поэтому их возможная польза для пациентов обоснована лишь теоретически. Однако даже в отношении тех фильтрационных систем, которые участвовали в клинических исследованиях, не слишком много доказательств их реального вклада в результаты комплексного лечения и профилактики бронхиальной астмы.
В 2002 г. Е. McDonald и соавт. опубликовали мета-анализ 10 рандомизированных контролированных исследований эффективности очистителей воздуха у больных астмой. Авторы выявили минимальное улучшение симптоматики и качества сна при использовании данных приборов [4]. Более подробный анализ 18 исследований в 2010 г. представили JL Sublett и соавт. [5]. Вывод оказался следующим: положительный эффект на течение астмы оказывают приборы, оснащенные специальными фильтрами тонкой очистки (НЕРА-фильтр), и в том случае, если они находятся рядом с зоной дыхания пациента во время сна. Действительно, период сна имеет особенно важное значение для больных астмой, когда из-за физиологических биоритмов нервной и эндокринной систем, а также эффекта накопления аллергенов в зоне дыхания часто наблюдается усиление симптомов респираторной аллергии.
Оригинальное решение по уменьшению концентрации аэроаллергенов вокруг головы пациента было предложено шведскими учеными, ре- зультатом которого стало создание нового прибора Protexo® Airsonett, создающего вертикальный нисходящий, слегка охлажденный поток предварительно очищенного воздуха, направленный в зону дыхания больного.
В силу некоторой разницы температур и ламинарного движения потока на границе с воздухом помещения создается барьер, препятствующий проникновению внешних аллергенов (рис. 1, 2) Своеобразный безаллергенный воздушный «зонтик» вокруг головы пациента должен снижать антигенную нагрузку и уменьшать проявления респираторной аллергии.
Целью нашего исследования была оценка эффективности и переносимости применения прибора Protexo® Airsonett (Швеция) у больных с атопической бронхиальной астмой неконтролируемого течения, при включении в комплексную схему лечения.
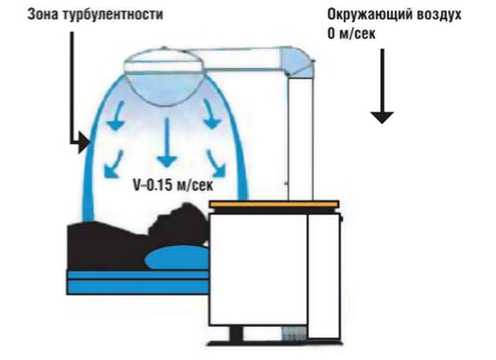
Рис. 1. Принцип работы прибора Protexo ® Airsonett
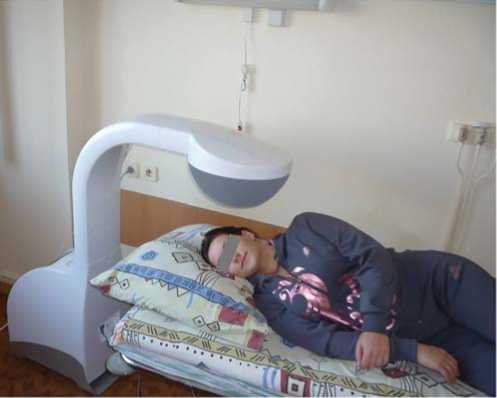
Рис. 2. Внешний вид головной части прибора Protexo ® Airsonett
Критерии включения пациентов в исследование:
-
1. Мужчины и женщины 18-50 лет
-
2. Подтвержденный диагноз атопической бронхиальной астмы (АБА)
-
3. Возможность проведения методики Protexo у пациента.
-
4. Фаза неконтролируемого течения заболевания
-
5. 80%>ОФВ1> 40 % от должных величин
-
6. Стандартная терапия заболевания
-
7. Наличие письменного информированного согласия на участие в исследовании.
Критерии исключения пациентов из исследования:
-
1. Фаза контролируемого течения заболевания
-
2. Неатопическая бронхиальная астма
-
3. Беременность, кормление грудью
-
4. Дополнительная к стандартной терапия БА
-
5. Пациенты с тяжелой сопутствующей патологией: иммунодефицит, диабет, декомпенсированная печеночная и почечная недостаточность, злокачественные опухоли любой локализации.
Дизайн исследования. Рандомизированное сравнительное плацебо-контролированное исследование. Все пациенты были рандомизированы в две группы. Пациенты группы 1 (n=18) получали стандартную терапию + сеансы Protexo в течение всего периода сна, пациенты группы 2 (n=19) – стандартную терапию + плацебо-имитацию метода Protexo без включения активного режима.
Оценка течения заболевания проводилась на 1, 3, 5, 7, 10 сутки от начала терапии по следующим симптомам: кашель, одышка, дополнительная потребность в ингаляторах, качество сна по дневнику самоконтроля, заполняемого пациентом.
Кашель, одышка, дополнительная потребность в ингаляторах оценивались по 4-балльной шкале, где за 0 баллов принималось отсутствие симптома, а за 3 балла – максимальная выраженность симптома.
Оценка качества сна проводилась по 3-балльной шкале:
-
1 балл – качество сна неудовлетворительное
-
2 балла – качество сна удовлетворительное
-
3 балла – качество сна хорошее.
Кроме того, в первые сутки лечения проводился замер числа частиц в зоне дыхания пациента (рядом с краем подушки) портативным счетчиком частиц GT-01, производства Met One Instruments Inc, США ( количество частиц размером 2 мкм в 1 кубическом футе) в начале сеанса очистки воздуха и перед его окончанием через 8 часов работы.
Спирометрия проводилась в день включения в исследование и через 10 сеансов применения технологии Protexo.
Все пациенты, участвовавшие в исследовании, получали стандартную терапию, включающую в себя в/в введение кортикостероидов (преднизолон 90 мг/сут или его эквивалентные аналоги); ИГКС 400-800 мкг беклометазо-на/сутки; β -2 агонисты короткого действия (сальбутамол 400 мкг/сутки).
Статистическая обработка результатов исследования производилась при помощи пакета прикладных программ "Statistica for Windows StatSoft Inc. Версия 6.0". Данные описательной статистики представлены как выборочное среднее ± стандартное отклонение. Достоверность различий между группами в динамике оцениваемых параметров рассчитывалась тестом Уилкоксона. Различия считались статистически достоверными при p<0,05.
Результаты:
В обеих группах наблюдалась редукция клинических симптомов заболевания (табл. 1, 2) У пациентов, получавших в комплексном лечении дополнительную очистку воздуха технологией Protexo, имелась тенденция к более быстрой динамике анализируемых параметров уже с 3 дня исследования. Тем не менее, достоверные отличия были выявлены лишь в отношении более редкого использования бронхолитиков на 3-й, 5-й и 7-й день наблюдения и меньшего ощущения одышки на 5-й день в основной группе. В более поздние сроки, на фоне практически полного исчезновения симптомов, обе группы уже не отличались по данным параметрам (рис. 3).
Статистически значимых отличий между пациентами по выраженности кашля и качеству сна ни в одной из контрольных точек получено не было. То же самое касалось и показателя ОФВ1 – он возрастал в обеих группах практически симметрично к 10-му дню наблюдения.
Примечательны данные по изменению числа
Таблица 1
|
Кашель |
||
|
Группа Protexo |
Группа плацебо |
|
|
Исходно |
1,67 + 0,59 |
1,63 + 0,68 |
|
3-й день |
1,17 + 0,78 |
1,39 + 0,69 |
|
5-й день |
0,56 + 0,7 |
0,88 + 0,67 |
|
7-й день |
0,11 + 0,32 |
0,32 + 0,58 |
|
10-й день |
0,04 + 0,18 |
0,16 + 0,68 |
|
Одышка |
||
|
Группа Protexo |
Группа плацебо |
|
|
Исходно |
1,22 + 0,8 |
1,21 + 0,79 |
|
3-й день |
0,83 + 0,71 |
1,0 + 0,74 |
|
5-й день |
0,44 + 0,62* |
0,74 + 0,73 |
|
7-й день |
0,22 + 0,55 |
0,26 + 0,56 |
|
10-й день |
0 |
0 |
*р<0,05 в сравнении различий в динамике показателей
Таблица 2
Динамика потребности в бронхолитиках и качества сна в исследуемых группах (баллы)
|
Дополнительная потребность в бронхолитиках |
||
|
Группа Protexo |
Группа плацебо |
|
|
Исходно |
1,11 + 0,58 |
1,37 + 0,68 |
|
3-й день |
0,5 + 0,51* |
1,0 + 0,67 |
|
5-й день |
0,11 + 0,32* |
0,57 + 0,69 |
|
7-й день |
0* |
0,36 + 0,68 |
|
10-й день |
0 |
0,16 + 0,510 |
|
Качество сна |
||
|
Группа Protexo |
Группа плацебо |
|
|
Исходно |
1,66 + 0,76 |
1,89 + 0,81 |
|
3-й день |
2,1 + 0,54 |
2,1 + 0,74 |
|
5-й день |
2,72 + 0,46 |
2,79 + 0,42 |
|
7-й день |
2,94 + 0,23 |
2,89 + 0,45 |
|
10-й день |
3,0 + 0,0 |
2,94 + 0,23 |
*р<0,05 в сравнении различий в динамике показателей
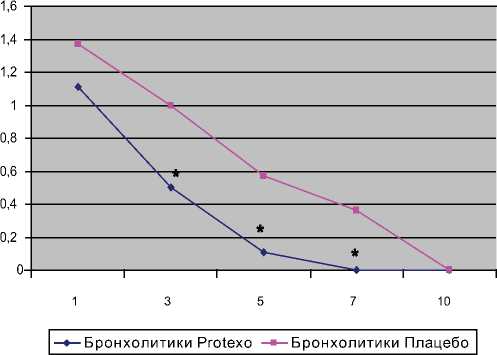
Рис. 3. Диаграмма снижения дополнительной потребности в бронхолитиках в сравниваемых группах.
взвешенных частиц в зоне дыхания пациента. Проведенный анализ показал, что через 8 часов работы исследуемого прибора эта цифра уменьшалась на порядок: с 177278 + 55522 до 18741 + 22202 частиц в кубическом футе (табл. 3).
Переносимость применения технологии Protexo у всех пациентов была высоком уровне. Единственный больной, предъявивший жалобы на слишком холодный поток воздуха из прибора, получал лечение в режиме плацебо.
Обсуждение
Результаты проведенного нами исследования в целом подтверждают дополнительный терапевтический эффект очистки воздуха даже у пациентов, находящихся в фазе неконтролируемого течения бронхиальной астмы и получаю-
Таблица 3
Динамика ОФВ1 (% от должного) и количества частиц в зоне дыхания пациентов в исследуемых группах
|
ОФВ1 |
||
|
Группа Protexo |
Группа плацебо |
|
|
Исходно |
70,86 + 9,89 |
69,42 + 12,31 |
|
10-й день |
92,52 + 14,03 |
92,36 + 14,4 |
|
3 Количество частиц (размер 2 мкм) в 1 футе |
||
|
Группа Protexo |
Группа плацебо |
|
|
Исходно |
177278 + 55522 |
188217 + 94483 |
|
Через 8 часов |
18741 + 22202*** |
161109 + 96513 |
***р<0,001 в сравнении различий в динамике показателей
Динамика кашля и одышки в исследуемых группах (баллы)
щих активное лечение. Нужно отметить, что исследования по оценке эффективности тех или иных фильтрующих воздух систем проводятся, как правило, в домашних условиях и в длительном периоде наблюдения. Особенностью нашей работы была попытка оценить возможный вклад нового устройства, очищающего воздух от взвешенных частиц в зоне дыхания, в доста- точно короткое время пребывания больного в стационаре. В отношении минимальных необходимых сроков пребывания в гипоаллергенной среде для клинической реализации эффекта элиминации аллергенов консенсуса до настоящего времени не достигнуто.
J Hedman и соавт., на когорте из 32 детей, больных астмой, показали, что даже 40-минут- ное пребывание в галапалате 5 дней в неделю достоверно снижает бронхиальную гиперреактивность к концу 2-й недели лечения [6].
В нашей работе уже к 3-му дню лечения у пациентов в группе Protexo отмечено более значимое уменьшение потребности в ингаляционных бронхолитиках, чем у получавших плацебо режим. По-видимому, это объясняется уменьшением гиперреактивности бронхов в ответ на снижение антигенной нагрузки.
Многие предшествующие исследования показали, что именно снижение гиперреактивности лежит в основе позитивных эффектов различных методов элиминации аллергенов – от пребывания на высокогорье до погружения в соляные шахты [7, 8]. При этом весьма примечательно, что уменьшение бронхиальной гиперреактивности не всегда сопровождается значимым приростом традиционных функциональных показателей [9]. Мы также не получили существенного увеличения ОФВ1 в группе Protexo, однако исходно трудно было предположить такую возможность у больных, получающих высокие дозы бронходилататоров. Несколько неожиданным для нас стало отсутствие значимого влияния исследуемой технологии на качество сна. Мы предполагаем, что в данном случае имела место методологическая недоработка. Субъективная оценка сна эффективна только при его существенных нарушениях, а нашими пациентами в большинстве случаев начальная характеристика сна была дана как «удовлетворительная». В этой ситуации больному очень трудно провести грань между «удовлетворительным» и «хорошим» сном. Возможно, стоило применить многоступенчатую шкалу субъективной оценки, либо использовать современные методы объективизации, такие как полисомнография. Безусловно, определенные ограничения на результаты исследования накладывает его краткосрочность и ограниченное число включенных больных.
Если говорить о других исследованиях технологии Protexo, то на сегодняшний день доступны всего 2 журнальные публикации. Первое рандомизированное 10-недельное исследо- вание провели C. Pedroletti и соавт. [10]. На небольшой группе пациентов с атопической астмой они показали достоверное снижение уровня оксида азота в выдыхаемом воздухе и улучшение качества жизни при неизменных характеристиках функции внешнего дыхания в сравнении с плацебо-эффектом.
Результаты второго крупного исследования у 312 больных от 7 до 70 лет с бронхиальной астмой с недостаточным уровнем контроля опубликованы в январе 2012 г. [11]. Пациенты в домашних условиях каждую ночь в течение 12 месяцев проводили либо с работающим прибором в активном режиме, либо в режиме плацебо. Было выявлено достоверное улучшение качества жизни по опроснику AQLQ, особенно ярко выраженное у пациентов с плохим контролем астмы и высокой интенсивностью лечения (GINA4). В группе лечения также достоверно снижался уровень выдыхаемого NO, особенно заметный у тех пациентов, которые изначально имели более высокие показатели. Авторы исследования не выявили достоверного влияния на такие показатели спирометрии как FEV1, PEF и FEF50.
Подобные эффекты могут быть достигнуты лишь при высокой степени очистки воздуха в зоне дыхания пациента. Действительно, проведенные нами измерения свидетельствуют о присутствии в воздухе палат специализированных стационаров достаточно большого числа взвешенных частиц, концентрация которых уменьшается на порядок в ходе применения технологии Protexo.
Заключение
Включение в схему лечения больных атопической бронхиальной астмой неконтролируемого течения метода создания безаллергенной среды в период сна прибором Protexo® Airsonett приводит к более быстрому уменьшению симптомов заболевания, снижению потребности в бронходилататорах при отсутствии неблагоприятных эффектов и может быть рекомендовано к применению в клинической практике в качестве дополнительного метода.
Список литературы Новая технология моделирования безаллергенного пространства в период сна у больных атопической бронхиальной астмой
- Roy A, Wisnivesky JP. Comprehensive use of environmental control practices among adults with asthma. Allergy Asthma Proc. 2010;31(5):72-7.
- Simmons RB, Crow SA. Fungal colonization of air filters for use in heating, ventilating, and air conditioning (HVAC) systems. J Ind Microbiol. 1995;14(1):41-5.
- Hanssen SO. HVAC -the importance of clean in Клиническая практика №1, 2013 http://clinpractice.ru 17 Оригинальные исследования take section and dry air filter in cold climate. Indoor Air. 2004;14(Suppl 7):195-201.
- McDonald E, et al. Effect of air filtration systems on asthma: a systematic review of randomized trials. Chest. 2002;122(5):1535-42.
- Sublett JL, Seltzer J, Burkhead R, et al. Air filters and air cleaners: rostrum by the American Academy of Allergy, Asthma & Immunology Indoor Allergen Committee. J Allergy Clin Immunol. 2010; 125(1):32-8.
- Hedman J, Hugg T, Sandell J. The effect of salt chamber treatment on bronchial hyperresponsiveness in asthmatics. Allergy 2006;61(5): 605-10.
- Peroni DG, Boner AL, Vallone G, et al. Effective allergen avoidance at high altitude reduces allergen-induced bronchial hyperresponsiveness. Am J Respir Crit Care Med 1994;149:1442-6.
- van der Heide S, van Aalderen WM, Kauffman HF. Clinical effects of air cleaners in homes of asthmatic children sensitized to pet allergens. J Allergy Clin Immunol. 1999 Aug;104(2 Pt 1):447-51.
- Sulser C, et al. Can the use of HEPA cleaners in homes of asthmatic children and adolescents sensitized to cat and dog allergens decrease bronchial hyperresponsiveness and allergen contents in solid dust? Int Arch Allergy Immunol. 2009;148(1):23-30.
- Pedroletti C, Millinger E, DahlJn B. Clinical effects of purified air administered to the breathing zone in allergic asthma: A double-blind randomized cross-over trial. Respir Med. 2009 Sep;103(9):1313-9.
- Boyle RJ, Pedroletti C, Wickman M. Nocturnal temperature controlled laminar airflow for treating atopic asthma: a randomised controlled trial. Thorax. 2012 Jan 16. [Epub ahead of print].


