Новые рекомендации по диагностике и лечению больных с впервые диагностированной множественной миеломой
Автор: Бессмельцев С.С.
Журнал: Вестник гематологии @bulletin-of-hematology
Рубрика: Передовая статья
Статья в выпуске: 1 т.22, 2026 года.
Бесплатный доступ
Выживаемость пациентов с множественной миеломой значительно улучшилась в последние годы благодаря внедрению различных классов новых препаратов, таких как ингибиторы протеасом, иммуномодулирующие агенты и моноклональные антитела. Однако у подавляющего большинства больных множественной миеломой наблюдается рецидив с более агрессивным течением заболевания из-за приобретения дальнейших генетических мутаций, которые могут вызывать устойчивость к текущим методам терапии. С момента публикации в 2021 году рекомендаций Европейской гематологической ассоциации (EHA) для лечения пациентов с множественной миеломой (MM), созданных в сотрудничестве с Европейским обществом медицинской онкологии, была разработана новая международная система стратификации (R2-ISS), одобрены EMA и/или FDA 14 новых схем для лечения пациентов с ММ. В настоящей статье представлены обновленные рекомендации Европейской гематологической ассоциации и Европейской сети миеломы (EMN) для повседневной клинической практики по диагностике и лечению больных с впервые диагностированной множественной миеломой.
Множественная миелома, рекомендации, диагностические критерии, терапия, минимальная остаточная болезнь, выживаемость
Короткий адрес: https://sciup.org/170211662
IDR: 170211662
New recommendations for diagnostics and treatment of patients with newly diagnostic multiple myeloma
Although the survival rate of patients with multiple myeloma has significantly improved in the last years thanks to the introduction of various classes of new drugs, such as proteasome inhibitors, immunomodulatory agents, and monoclonal antibodies, the vast majority of these subjects’ relapse with a more aggressive disease due to the acquisition of further genetic mutations that may cause resistance to current salvage therapies. Since the publication of the European Hematology Association (EHA) guidelines for the treatment of patients with multiple myeloma (MM) in 2021, developed in collaboration with the European Society of Medical Oncology, a new international stratification system (R2-ISS) has been developed, and 14 new regimens have been approved by the EMA and/or FDA for the treatment of patients with MM. This article presents the updated recommendations of the European Hematology Association (EHA) and the European Myeloma Network (EMN) for the daily clinical practice of diagnosing and treating patients with newly diagnosed multiple myeloma.
Текст научной статьи Новые рекомендации по диагностике и лечению больных с впервые диагностированной множественной миеломой
Введение . Множественная миелома ( ММ ) – это гетерогенное заболевание , определяемое клональ ной пролиферацией плазматических клеток , гема тологическая опухоль , которая составляет 1,0-1,8% среди всех видов онкологических заболеваний и 10-15% среди гематологических злокачественных новообразований [1]. Чаще всего ММ диагностиру ется в возрасте 65-70 лет , распространенность за болевания среди населения моложе 40 лет не пре вышает 2% [2]. В Европе ММ является второй по распространенности гематологической опухолью , с заболеваемостью 4,5-6,0/100 000 человек в год . В
Oncology, a new international stratification system (R2-ISS) has been developed, and 14 new regimens have been approved by the EMA and/or FDA for the treatment of patients with MM. This article presents the updated recommendations of the European Hematology Association (EHA) and the European Myeloma Network (EMN) for the daily clinical practice of diagnosing and treating patients with newly diagnosed multiple myeloma.
США в 2023 году [3] на MM приходилось почти 22% всех смертей , связанных с онкогематологическими заболеваниями .
За последние 20 лет показатели выживаемости у пациентов с ММ значительно улучшились: среди тех, кто участвовал в клинических испытаниях, почти 60% пациентов, получивших аутологичную трансплантацию гемопоэтических стволовых клеток (АутоТГСК), оставались живы в течении 10 лет [4]. По оценкам Соединенных Штатов, относительная 5-летняя выживаемость в период с 2014 по 2020 год составила 61,1%. Однако, несмотря на не вызы- вающие сомнений успехи, только 10-15% пациентов достигают выживаемости, сопоставимой с соответствующей общей популяцией [5]. И хотя в последнее время появилась концепция функционального излечения, т.е. устойчивого отсутствия измеряемой болезни в течение 5 лет и более после прекращения противоопухолевой терапии [6], заболевание на сегодняшний день остается неизлечимым. Течение ММ характеризуется серией ремиссий и рецидивов, с развитием в итоге рефрактерного рецидива [7,8].
В 2021 году Европейская гематологическая ассо циация (EHA) и Европейское общество медицинской онкологии (ESMO) совместно разработали рекомен дации для клинической практики по лечению па циентов с MM [9]. За прошедшие годы Европейским агентством по лекарственным средствам (EMA) и Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) были одобрены несколько новых схем для лечения пациентов с впервые диагностированной множе ственной миеломой ( ВД MM). Кроме того , были раз работаны новые факторы прогноза для определе ния высокого риска , новая система стратификации больных ММ , а оценка минимальной остаточной бо лезни ( МОБ ) стала очень важным показателем глу бины противоопухолевого ответа .
Новые рекомендации по лечению пациентов с ВДММ опубликованы в 2025 году . Они включают подходы к диагностике , лечению и мониторингу со стояния больных [10]. Для разработки рекоменда ций от EHA и Европейской сети миеломы (EMN) была предложена междисциплинарная группа экспертов по ММ из различных учреждений и стран Европы , которые рассмотрели всю соответствующую лите ратуру , включая результаты рандомизированных клинических исследований , метаанализы , система тические обзоры , руководящие принципы , наблю дательные исследования , серии случаев и отчеты о случаях , связанных с диагностикой и лечением ММ . Для разработки рекомендаций были использованы уровни доказательств и оценки , адаптированные из системы оценки Службы общественного здравоох ранения США .
Цель настоящей работы . Представить читателю обновленные клинические рекомендации по веде нию пациентов с впервые диагностированной мно жественной миеломой , а также тлеющей миеломой , включая диагностику , прогноз и использование ле карственных средств , доказавших свою эффектив ность в клинических исследованиях последних лет .
Материалы и методы. Для достижения поставленной цели нами проанализированы основные научные публикации, посвященные тлеющей и симптоматической множественной миеломе, основная литература, включая результаты рандомизированных клинических исследований, метаанализы, наблюдательные исследования, связанные с диагностикой и лечением ММ, которые послужили базой для разработки новых клинических рекомендаций экспертами EHA–EMN. Для изучения отобраны 68 работ, опубликованных в преобладающем большинстве в течение последние 5 лет. Включение более ранних работ допускалось в связи с высокоинформативными материалами либо, если это были первоисточники.
Результаты
Диагностика и стадии множественной миеломы
Диагностические критерии симптоматической MM и тлеющей миеломы ( ТММ ), определенные в руководящих принципах EHA в 2021 году , остаются неизменными [9]. В соответствии с Международ ной системой стадирования (ISS), предложенной в 2005 году , опухолевая нагрузка при ММ оценива ется по таким показателям , как концентрация β 2- микроглобулина и альбумина в сыворотке крови [11]. Однако последующие исследования показали , что анализ хромосомных нарушений позволяет бо лее надежно стратифицировать больных на группы риска . Поэтому в 2015 г . IMWG представила обнов ленную классификацию R-ISS, в которой учитывают ся показатели ISS и неблагоприятные хромосомные аномалии ( ХА ), а также высокая активность ЛДГ , коррелирующая с общей массой опухолевых кле ток и являющаяся независимым фактором прогноза [12]. В новой модели стратификации нашли отраже ние делеция 17p, транслокации t(4;14) и t(14;16).
Но в последующем было выяснено , что не менее значимыми для прогноза являются транслокация t(14;20) и , особенно , амплификация 1q, а также ген p53 – ген - супрессор опухолевого роста , который ло кализован на коротком плече 17- й хромосомы ( ло кус 17 р 13)
В 2022 г., уже после публикации Европейских рекомендаций по диагностике и лечению ММ, модель стратификации R1-ISS подвергнута пересмотру (R2-ISS), была добавлена хромосома +1q21, как самая частая вторичная поломка и очевидный фактор неблагоприятного прогноза [13]. Эта система ста-дирования основана на четырех прогностических маркерах, включающих сывороточные биомаркеры и хромосомные аномалии, которым присваиваются баллы для определения группы риска. Каждому признаку риска было присвоено значение в соответствии с их влиянием на ОВ (ISS II – 1; ISS III – 1,5; del(17p) – 1; t(4;14) – 1; +1q21 – 0,5; ЛДГ > верхней границы нормы (ВГН) – 1). Пациенты были разделены на четыре группы риска в соответствии с общим суммарным баллом: низкий (второй пересмотр Международной системы стадирования [R2-ISS]-I, 19,2%, 0 баллов), низкий-промежуточный (II, 30,8%, 0,5-1 балл), высокий-промежуточный (III, 41,2%, 1,5-2,5 балла), высокий (IV, 8,8%, 3-5 баллов) риск. Установлено, что при использовании стандартных протоколов лечения больные ММ в этих группах риска имели разные медианы ОВ (не достигнута, 109, 2 месяца, 68,5 месяцев и 37,9 месяцев соответствен- но группам риска) и ВБП (68 месяцев, 45,5 месяцев, 30,2 месяца и 19,9 месяцев) [13]. Вторая редакция Международной системы стадирования (R2-ISS) существенно улучшила стратификацию рисков пациентов с впервые выявленной ММ промежуточного риска.
Множественная миелома , как известно , характе ризуется выраженной геномной гетерогенностью , обусловленной сложной комбинацией численных и структурных изменений хромосом , которые игра ют ключевую роль в онкогенезе , приводя к измене нию структуры и функции генов - мишеней , генному дисбалансу и , как следствие , нарушению регуляции клеточного цикла [1]. С помощью FISH- анализа пер вичные хромосомные изменения выявляются у 90% пациентов с ВДММ . Выявление одновременно как минимум двух аномалий высокого риска или толь ко делеции 17p, но с пороговым значением в кло нальной фракции опухоли = 0,55, а также мутации гена TP53 свидетельствует об очень высоком риске . В связи с этим появились такие понятия : миелома «Double Hit» ( две любые генетические аномалии вы сокого риска ) и миелома «Triple Hit» ( три и более ге нетических аномалии высокого риска ) [7].
Новые прогностические критерии
В 2025 году Международное общество по из учению миеломы (IMS) совместно с Международ ной рабочей группой по изучению миеломы (IMWG) созвали экспертную группу с целью пересмотреть определение высокого риска и сформулировать консенсусное определение , учитывающее новые данные молекулярных / геномных исследований , обновлённые клинические данные и современные концепции стратификации риска [14]. В результате была разработана и предложена для клинического применения согласованная геномная стратифика ция (CGS) высокого риска , который определяется выявлением одной из следующих аномалий :
-
(1) del (17p) с клональной долей >20% и / или мутацией TP53;
-
(2) t(4;14), t(14;16) или t(14;20) вместе с 1q+ и / или del (1p32);
-
(3) моноаллельная del (1p32) наряду с 1q+ или биаллельная del (1p32);
-
(4) β 2- микроглобулин ≥ 5,5 мг / дл при нормаль ном уровне креатинина (<1,2 мг / дл ).
Кроме того, предлагается еще несколько иных показателей высокого риска, которые включают оценку циркулирующих плазматических клеток, уровень сывороточного M-белка, определенного с помощью масс-спектрометрии, и профилирование экспрессии генов. Так, несколько исследовательских групп сообщили о прогностической ценности выявления циркулирующих плазматических клеток [15-17]. Было установлено, что оценка количества циркулирующих плазматических клеток с учетом критериев ISS, может более четко выделить больных ММ с худшим прогнозом. Выживаемость без прогрессирования (ВБП) и общая выживаемость (ОВ) больных с каждым логарифмическим увеличением циркулирующих плазматических клеток постепенно ухудшалась. И наоборот, пациенты с ВДММ без циркулирующих плазматических клеток, показали беспрецедентные результаты, а именно, 5-летняя ВБП и ОВ 83% и 97% соответственно с присутствием и без плазматических клеток в кровотоке больных [17].
Количество циркулирующих плазматических клеток , определенное с помощью проточной цито метрии следующего поколения (NGF), также может быть использовано для более точной диагностики плазмоклеточного лейкоза [18, 19]. Плазмоклеточ ный лейкоз – редкое лимфопролиферативное за болевание , характеризующееся злокачественной пролиферацией плазматических клеток в костном мозге и сопутствующим поражением перифериче ской крови , который в настоящее время определя ется как ≥ 5% плазматических клеток в мазках пери ферической крови [20].
Количественный метод иммунопреципитации с использованием масс - спектрометрии более чув ствительный , чем иммунофиксационный электро форез для обнаружения M- белка у пациентов с ММ , как при первичной диагностике , так и во время лечения , и имеет большее прогностическое значе ние . В последние годы внимание исследователей привлекает такой показатель как профилирование экспрессии генов (GEP), имеющих независимую про гностическую значимость , особенно у пациентов с ВДММ [21].
Представленные результаты подчеркивают мо лекулярное разнообразие MM и , в частности , демон стрируют , что комбинированный GEP и хромосомное профилирование при постановке диагноза может предсказать клинический исход со значительной точностью . Пациенты с ММ со статусом double-hit или GEP высокого риска вряд ли выиграют от те кущих подходов к лечению , включая поддержива ющую терапию леналидомидом . У таких пациентов может быть полезной интенсивная постоянная те рапия комбинированными агентами . К сожалению , профилирование экспрессии генов мало доступно в обычных клинических условиях .
Оценка результатов терапии
Критерии оценки ответа на лечение, предложенные в 2016 году IMWG, не изменились [22]. В эти критерии был введен новый показатель для использования – минимальная остаточная (резидуальная) болезнь (МОБ), то есть, выявление опухолевых плазматических клеток на субклиническом уровне после проведения успешной противоопухолевой терапии. Определение МОБ является важной задачей, позволяющей более глубоко оценить эффективность терапии, дает значимую независимую прогностическую информацию в отношении общей и беспро-грессивной выживаемости больных ММ и является определяющим критерием степени эрадикации опухолевого клона. Для определения МОБ используют молекулярные и визуализирующие методы. Выбор методики зависит от характеристик: применимости, высокой чувствительности и специфичности, распространённости, доказанной клинической ценности и экономичности [7].
Молекулярные методы обнаружения МОБ бы стро развивались , их чувствительность и примени мость значительно расширились . Для повышения чувствительности детекции миеломных клеток были разработаны новые высокопроизводитель ные методы оценки аспиратов костного мозга ( КМ ), включая многопараметрическую проточную цитометрию ( МПЦ ), МПЦ нового поколения (Nextgeneration flow – NGF), аллель - специфичную олиго - нуклеотидную качественную полимеразную цепную реакцию ( АСО - ПЦР ) и секвенирование нового поко ления (NGS). Эти методы дают возможность прово дить быстрое исследование от нескольких тысяч до миллиона клеток КМ или соответствующего коли чества ДНК за один тест и позволяют выполнять ко личественную оценку остаточных опухолевых кле ток в КМ . В критериях 2016 года МОБ - негативность костного мозга определяется как отсутствие злока чественных плазматических клеток в 100 000 ядер - ных клетках костного мозга ( порог чувствительно сти составляет <10 - 5). Тем не менее , новые данные свидетельствуют о том , что более низкие значения ( например , 10 - 6) обеспечивают лучший прогноз , чем стандартное определение , хотя этой чувствительно сти труднее достичь [23].
К визуализирующим методам относятся магнит но - резонансная томография ( МРТ ) и позитронно эмиссионная томография , совмещенная с рентге новской компьютерной томографией ( ПЭТ / КТ ). Эти методы исследования позволяют оценить степень поражения всего скелета одномоментно , что важ но из - за диффузно - очагового характера поражения костного мозга при ММ [1]. Вне костного мозга ПЭТ / КТ может помочь выявить гиперметаболические об ласти у ~15–20% пациентов с МОБ - негативностью КМ и считается одним из лучших доступных визу ализирующих методов в настоящее время . Диффу зионно - взвешенная МРТ ( ДВИ , DWI) — метод маг нитно - резонансной томографии , основанный на измерении случайного ( броуновского ) движения молекул воды в тканях . Интенсивность сигнала на диффузионно - взвешенном изображении ( ДВИ ) от ражает диффузионную способность молекул воды в вокселе ( трёхмерном пикселе ) исследуемого объ екта . Крупный метаанализ показал , что ДВИ МРТ значительно более чувствительна , чем ПЭТ - КТ при выявлении аномальных участков в костном мозге пациентов с MM [24].
Разрабатываются новые иммуно-ПЭТ-подходы — это методы визуализации, основанные на использовании моноклональных антител и других связанных молекул, меченных позитронно-радиоактивными нуклидами. Такие подходы позволяют неинвазивно оценивать экспрессию и распределение мишеней in vivo, что помогает в диагностике, прогнозе, выборе терапии и мониторинге лечения многих заболеваний. Иммуно-позитронно-эмиссионная томография (иммуно-ПЭТ), нацеленная на CD38, позволяет обнаруживать и визуализировать клетки миеломы, экспрессирующие CD38, в организме человека. Например, по данным Ulaner G. A. et al., иммуно-ПЭТ позволила обнаружить >100 очагов миеломы у пациента с биохимическим прогрессированием, но с отрицательными результатами ПЭТ/ КТ [25]. Авторы сообщили о 76-летнем мужчине с множественной миеломой, у которого наблюдалась биохимическая прогрессия после трансплантации стволовых клеток. По результатам биопсии костного мозга плазматических клеток не обнаружено. ПЭТ/КТ изменений не выявила. И только иммуноПЭТ позволила верифицировать прогрессию ММ и инициировать системную терапию даратумумабом, леналидомидом и дексаметазоном.
Устойчивый МОБ - негативный статус в течение ≥ 12 месяцев сильно коррелирует с ВБП и общей вы живаемостью ( ОВ ) у пациентов с ВД MM. Использо вание МОБ для принятия решений о смене лечения и его продолжительности продолжает изучаться . На сегодняшний день не ясно , следует ли прекра тить поддерживающую или непрерывную терапию у пациентов с отрицательным МОБ - статусом , следу ет ли изменить лечебные подходы при втором или последующем рецидиве у пациентов с положитель ным результатом МОБ ( особенно при MM высоко го риска ). В то же время доказано , что у пациентов с ММ стандартного риска , получивших АутоТГСК , при устойчивом МОБ - негативном статусе , возможно прекращение поддерживающей терапии леналидо мидом после 3 лет применения [26].
Обсуждается необходимость и значимость использование иммунофиксации образцов мочи для оценки ответа, для чего требуется сдача образцов мочи, собранных в течение 24 часов. Иммунофиксация мочи — это тест, который выявляет аномальные белки в моче, в частности М-белок. Однако было показано, что оценка сывороточных свободных легких цепей (СЛЦ) превосходит прогностическое значение иммунофиксации мочи при ММ [27]. В настоящее время определение сывороточных κ и λ СЛЦ стало частью рутинных клинических анализов, в особенности, для диагностики и наблюдения за пациентами с несекретирующей и олигосекретирующей миеломой, миеломой легких цепей и AL-амилоидозом. Соотношение СЛЦ при постановке диагноза является независимым прогностическим фактором течения ММ и включено в критерии оценки ответа. В то же время взгляды на значимость СЛЦ остаются противоречивыми, поскольку в некоторых исследованиях приводятся противоположные результаты, свидетельствующие о том, что СЛЦ нельзя расценивать как достоверный метод оценки МОБ при миеломе [7].
Рекомендации [10]
-
• Как ПЭТ - КТ , так и ДВИ МРТ считаются дополни тельными к МОБ костного мозга при оценке статуса минимальной остаточной болезни [ консенсус V, B].
-
• Иммунофиксация мочи не является обязатель ным тестом для оценки ответа , но должна прово диться при постановке диагноза и во время каждого рецидива , чтобы исключить другие патологии ( та кие как AL- амилоидоз или болезнь отложения лег ких цепей ) [III, C].
Тлеющая множественная миелома
Тлеющая ММ ( ТММ ) – это бессимптомное со стояние , соответствующее временному промежут ку между моноклональной гаммапатией неопре деленного значения (MGUS) и симптоматической MM. Тлеющая ММ не является биологической про межуточной стадией между MGUS и MM, а скорее представляет собой гетерогенное клинически определенное состояние , при котором некоторые пациенты ( примерно две трети ) имеют MGUS ( пред - злокачественную опухоль ), а другие ( примерно одна треть ) имеют MM ( злокачественную опухоль ) [28]. К сожалению , ни одна патологическая или молекуляр ная особенность не может достоверно различить эти две группы пациентов . Для практических и кли нических целей , для выявления пациентов с ТММ , у которых , вероятно , уже произошла злокачественная трансформация ( ТММ высокого риска ), используют ся конкретные факторы риска [7].
Распространенность ТММ в общей популяции составляет 0,53% у лиц в возрасте ≥ 40 лет . Между народная рабочая группа по миеломе (IMWG) опре делила Т MM как клональное расстройство плазма тических клеток с ≥ 10% плазматических клеток в КМ и / или уровнем парапротеина в сыворотке ≥ 3 г / дл ( или уровнем парапротеина в моче ≥ 500 мг /24 ч при отсутствии сывороточного моноклонального белка (M- белка )) без гиперкальциемии , почечной недостаточности , анемии или поражений костей скелета , или признаков амилоидоза легких цепей (CRAB- критерии ). Несекретирующая миелома харак теризуется отсутствием M- белка в сыворотке крови и моче , плазмоцитозом костного мозга . Одиночная плазмоцитома кости , экстрамедуллярная плазмоци тома и множественные одиночные плазмоцитомы (+/- рецидивирующие ) также определяются как от дельные образования . Симптоматическая миелома требует признаков повреждения органов и тканей [29].
Разработаны различные классификационные модели для оценки риска прогрессирования ТММ до симптоматической ММ. Одной из таких моделей является IMWG модель «2-20-20»/«20-20-20» (зависит от единиц измерения М-белка), которая используется для классификации пациентов подгруп- пы с низким, промежуточным или высоким риском прогрессирования. Эту модель обычно называют трехфакторной моделью, потому что она включает три фактора риска: уровень сывороточного M-белка (2 г/дл или 20 г/л), отношение вовлеченных и не-вовлеченных свободных легких цепей сыворотки (sFLC – > 20) и инфильтрацию костного мозга плазматическими клетками (20% и более) [30]. Добавление цитогенетических аномалий (t(4;14), t(14;16), 1q+, del13q и моносомия 13) в эту модель сделало ее четырехфакторной, которая выделяет четыре группы риска [30]. При использовании трехфакторной модели 2-летний риск прогрессирования ТММ: 6% для низкого риска (38%; без факторов риска); 18% для промежуточного риска (33%; 1 фактор) и 44% для высокого риска (29%; 2-3 фактора). Добавление цитогенетических аномалий позволило выделить 4 группы (низкий риск – 0 факторов, низкий промежуточный риск – 1 фактор, промежуточный риск – 2 и высокий риск ≥3 факторов) с прогрессированием через 2 года с частотой 6%, 23%, 46% и 63% соответственно. Модель стратификации риска 2/20/20 может быть легко реализована для выявления ТMM высокого риска для клинических исследований и обычной практики.
В настоящее время подход « наблюдай и жди » яв ляется стандартной стратегией управления , реко мендованной для всех пациентов с Т MM [7, 31]. Тем не менее , два независимых исследования III фазы показали , что пациенты с ТММ высокого риска ( на момент начала исследования ), которые получали леналидомид плюс дексаметазон или только лена лидомид , имели более длительную продолжитель ность ВБП ( и ОВ в случае применения Rd), чем в группе наблюдения [32, 33].
В первом исследовании [32] при медиане наблю дения 12,5 лет , медиана времени до прогрессии в MM в группе пациентов , получивших девять 4- недель ных индукционных циклов Rd, с последующей под держкой леналидомидом в течение 2 лет , составила 9,5 лет , а в группе в наблюдения 2,1 года (HR: 0,28, 95% CI: 0,18-0,44, p = 0,0001). Медиана ОВ составила 8,5 лет в группе наблюдения и не была достигнута в группе Rd (HR: 0,57, 95% CI: 0,34-0,95, p = 0,032).
Во втором исследовании [33] при медиане наблю дения 35 месяцев при приеме только леналидомида ВБП была более длительной , чем в группе наблюде ния ( Р = 0,002). Выживаемость без прогрессирова ния в течение одного , 2 и 3 лет составила 98%, 93% и 91% для группы с леналидомидом по сравнению с 89%, 76% и 66% для группы наблюдения соответ ственно . Негематологические побочные эффекты 3- й или 4- й степени тяжести наблюдались у 28% па циентов , получавших леналидомид .
Представленные результаты были обусловлены главным образом группой больных тлеющей миеломой высокого риска. К сожалению, эти ключевые исследования не были регистрационными, и, следова- тельно, ни один из подходов не одобрен для лечения ТMM ни EMA, ни FDA. Эти испытания, однако, привели к инициированию нескольких дальнейших исследований с участием пациентов с ТММ высокого риска, основной целью которых были две стратегии: 1) задержка прогрессирования до ММ и 2) лечение.
Задержка прогрессирования ТММ до симпто матической MM
С целью задержки прогрессии тлеющей миеломы в симптоматическую было проведено исследование CENTAURUS (II фаза ), в котором в качестве лечения использовали анти -CD38 моноклональное анти тело « Даратумумаб » [34, 35]. В общей сложности в исследование были включены 123 пациента в воз расте ≥ 18 лет с подтвержденным диагнозом ТММ высокого риска или промежуточного риска в тече ние <5 лет , которые были рандомизированы для лечения даратумумабом . ТММ высокого риска или промежуточного риска была диагностирована при количестве плазматических клеток в костного моз га ≥ 10% до <60% и , по крайней мере , при выявлении одного из следующих показателей : сывороточный M- белок ≥ 3 г / дл (IgA ≥ 2 г / дл ), M- белок мочи >500 мг /24 ч , аномальное соотношение FLC (<0,126 или >8) с сывороточным M- белком <3 г / дл , но ≥ 1 г / дл . Пациенты были случайным образом распределены (1:1:1) для получения одного из трех режимов до зирования даратумумаба : расширенный интенсив ный ( интенсивный ), расширенный промежуточный ( промежуточный ) и короткий режим . Даратумумаб 16 мг / кг вводили внутривенно в 8- недельных ци клах . В интенсивной группе пациенты получали да - ратумумаб еженедельно в цикле 1, каждые 2 недели в циклах 2 и 3, каждые 4 недели в циклах 4–7 и каж дые 8 недель в циклах 8–20. В промежуточной груп пе пациенты получали даратумумаб еженедельно в цикле 1 и каждые 8 недель в циклах 2-20. В группе с коротким режимом дозирования пациенты получа ли даратумумаб еженедельно в течение только од ного цикла . При периоде наблюдения 85,2 месяца , в группах интенсивного , промежуточного и короткого режимов дозирования даратумумаба , полный ответ или лучше составили 4,9%, 9,8% и 0%; частота обще го ответа – 58,5%, 53,7% и 37,5%; медиана ВБП не была достигнута , 84,4 мес . и 74,1 мес . соответствен но . Количество пациентов , прекративших лечение из - за нежелательных явлений ( НЯ ), было одинако во низким во всех группах лечения . Большинство случаев прогрессирования было установлено на ос новании критериев SLiM и лишь у 2 пациентов про грессирование было связано с формированием оча гов остеолизиса . При медиане наблюдения ∼ 7 лет эти данные свидетельствуют о том , что , во - первых , длительное применение даратумумаба переносится вполне удовлетворительно и во - вторых , обосновы вают его роль в качестве раннего вмешательства при ТММ с промежуточным и высоким риском с це лью задержки ее прогрессирования .
Полученные результаты явились основание для инициации III фазы исследования AQUILA, в которое вошло 390 пациентов с ТММ высокого риска для по лучения подкожного даратумумаба в фиксирован ной дозе 1800 мг в течение 3 лет (39 циклов ) или до прогрессирования (194 больных , 1 группа ), либо для активного наблюдения (196 больных , 2 группа ) [36]. Следует отметить , что при наборе пациентов в иссле дование AQUILA соблюдался ряд важных условий , в частности анамнез ТММ не должен превышать 5 лет . Прогрессирование определялось в соответствии с критериями SLiM-CRAB. Основной конечной точкой была выживаемость без прогрессирования . По итогу исследования пятилетняя ВБП составила 63,1% про тив 40,8% в группах пациентов , получавших дарату - мумаб против только наблюдавшихся (HR 0,49, 95% CI 0,36-0,67; P <0,001), а ОВ – 93,0% против 86,9% (HR 0,52, 95% CI 0,27-0,98). Важно отметить , что ста тистически значимое улучшение ВБП отмечалось только у пациентов 1 группы с высоким риском (HR 0,36; 95% CI 0,23–0,58), что позволяет рассматри вать эту категорию больных в качестве целевой для подобной терапии . При анализе этого исследо вания обращает на себя внимание очень значимый аргумент в пользу даратумумаба . Исследователи рассчитали ВБП 2 ( время от даты рандомизации до даты прогрессирования или летального исхода во время следующей линии терапии ), которая также оказалась выше у пациентов , получавших даратуму - маб в первой линии , что указывает на то , что раннее вмешательство , не оказывает негативного влияния на последующее лечение в случае прогрессирова ния заболевания . Что касается переносимости дли тельной терапии даратумумабом , то самым частым вариантом нежелательных явлений 3–4 степени тя жести была артериальная гипертензия . Лишь у 5,7% пациентов неблагоприятные события привели к прекращению лечения даратумумабом , но никаких новых проблем безопасности не было выявлено .
Таким образом , среди пациентов с ТММ и высо ким риском подкожная монотерапия даратумума - бом сопровождалась значительно более низким риском прогрессирования до активной множествен ной миеломы или смерти и более высокой общей выживаемостью , чем среди пациентов с активным мониторингом .
Надо ли лечить тлеющую миелому ?
К настоящему времени проведено 3 исследова ния второй и одно – третьей фазы , в которых обо сновывались подходы к лечению ТММ с намерения ми ее излечения . Было показано , что раннее лечение тлеющей миеломы высокого риска задерживает прогрессирование до множественной миеломы . Под тверждением стали результаты исследований , в ко торых изучались опции интенсивной терапии ТММ высокого риска , ориентированных на достижение МОБ - отрицательного ответа .
В одном нерандомизированном контролируемом исследовании II фазы [37] 54 пациента с ТММ высокого риска получили восемь 4-недельных циклов KRd [карфилзомиб 36 мг/м2 (первые 2 дозы по 20 мг/м2), дексаметазон (20 мг, циклы 1-4; 10 мг, циклы 5-8 два раза в неделю)], с последующим назначением 28-дневных циклов поддержки леналидомидом (25 мг дни 1-21). АутоТГСК не выполнялась. В результате 70,4% больных достигли МОБ-отрицательного ПО (95% CI 56,4%-82,0%) с медианой устойчивости в течение 5,5 лет. Через 8 лет ВБП составила 91,2%, не зарегистрировано ни одной смерти, связанной с MM. Негематологические побочные эффекты 3-й степени наблюдались у 21 пациента (38,9%) и включали тромбоэмболию, сыпь и легочную инфекцию, при этом 4-й степени побочных эффектов не было. Результаты этого исследования позволяют предположить, что лечение тлеющей миеломы высокого риска новыми триплетами, такими как KRd, и поддерживающая терапия леналидомидом, может изменить естественное течение тлеющей миеломы, значительно задерживая развитие заболевания. Для подтверждения этого соотношения пользы и риска необходимы рандомизированные клинические исследования.
Еще в одном исследовании фазы II ASCENT [38] 87 пациентов с ТММ высокого риска ( определяемой в соответствии с трехфакторной моделью IMWG или системой подсчета баллов IMWG) получили квадри - плет DaraKRd в качестве индукции и консолидации ( всего 12 циклов ) с уменьшением частоты введения даратумумаба и снижением дозы дексаметазона , а затем 12 циклов DaraR в качестве поддерживающей терапии ( в целом лечение продолжалось 2 года ). Ча стота общего ответа составила 97%, включая 38% строгих полных ответа ( сПО ) и 92% ≥ ОхЧО . Так же , как и в предыдущем исследовании , авторы сооб щают о достижении устойчивого МОБ - негативного статуса (84%, 10–5), медиана ВБП не достигнута , а 3- летняя ВБП равнялась 89,9%. Зарегистрированы лишь 3 случая биохимического прогрессирования и у 1 пациента выявлен плазмоклеточный лейкоз . Гематологическая токсичность 3 степени и выше за регистрирована у 18% пациентов , негематологиче ская – у 61%.
Наконец , Mateos M.V. et al. в 2024 году опублико вали результаты крупного исследования CESAR, в котором был использован подход к лечению ТММ , применяемый для впервые диагностированных па циентов с ММ [39]. В исследование вошли 90 паци ентов с тлеющей миеломой высокого риска (>50% риска прогрессирования через 2 года ), кандидатов на трансплантацию гемопоэтических стволовых клеток . Пациенты были в возрасте от 18 до 70 лет и имели право на АутоТГСК со статусом ECOG 0-1. Все получили индукционную терапию карфилзо - мибом , леналидомидом и дексаметазоном ( схема KRd), шесть циклов , а затем высокие дозы мелфала - на (200 мг / м 2), АутоТГСК , два цикла консолидации
KRd и далее поддерживающая терапия Rd в течение 2 лет . Первичной конечной точкой был показатель МОБ - негативности , оцениваемый по NGF. После медианы наблюдения 70 месяцев и 3 месяца после АутоТГСК , у 62% пациентов установлен полный МОБ - отрицательный ответ , а у 31% больных он со хранялся в течение 4 лет . Только у пяти пациентов наблюдалась прогрессия в ММ . Причем наличие лю бого из критериев SLiM или CRAB предсказывало прогрессирование ТММ до симптоматической ММ ( у четырех из пяти пациентов ; отношение рисков 0,12; 95% CI 0,14-1,13; Р = 0,03). В целом частота прогрес сирования в течение 70 мес . составила 94%. У трид цати шести пациентов наблюдалось биохимическое прогрессирование . 70- месячная выживаемость рав нялась 92%. Нейтропения и инфекции были наи более частыми НЯ во время лечения больных , ко торые привели к одной смерти . Авторы сообщили также о трех новых первичных злокачественных новообразованиях . Такой лечебный подход , безус ловно , обнадеживает , поскольку у 31% пациентов после ВДХТ - АутоТГСК через 4 года сохранялся МОБ - отрицательный ответ и лишь умеренный уровень смертности .
Таким образом , мы рассмотрели 3 исследования . Исходя из результатов приведенных исследований , следует констатировать , что оптимальный подход к пациентам с тлеющей миеломой высокого риска все еще изучается . Проведенные исследования по казали , что раннее лечение снижает риск прогрес сирования до активной ММ и улучшает общую вы живаемость по сравнению с одним наблюдением . Особенно интересен лечебный подход к ТММ высо кого риска , сопоставимый с тем , который исполь зуется при ВДММ . У трети пациентов с ТММ в тече ние 4 лет поддерживался МОБ - негативный статус . Возможно , что интенсивная терапия на этом этапе может потенциально искоренить злокачественный клон и привести к долгосрочным ремиссиям или даже излечению . Тем не менее , текущих данных пока недостаточно для принятия какой - либо конкретной позиции в отношении терапии тлеющей миеломы . Необходимы новые клинические исследования и бо лее длительные сроки наблюдения , чтобы показать истинное излечение .
Группа экспертов EHA и EMN рекомендует [10]:
-
• Пациенты с ТММ низкого риска или средне го риска должны обследоваться каждые 6 месяцев или каждые 3-6 месяцев соответственно , для оцен ки риска прогрессирования до ММ [I, B]; оценка ри ска должна проводиться с использованием моделей классификации IMWG.
-
• Окончательного решения по лечению тлеющей миеломы нет , но монотерапия даратумумабом в те чение 3 лет может быть рассмотрена у пациентов с ТММ высокого риска [I, A].
Лечение пациентов с впервые диагностиро ванной множественной миеломой , являющихся кандидатами на проведение АутоТГСК
Современный алгоритм лечения множественной миеломы ( ММ ) предполагает на этапе диагности ки опухоли обязательную стратификацию больных на группы риска с решением вопроса о возможно сти выполнения трансплантации аутологичных гемопоэтических стволовых клеток ( АутоТГСК ). Трансплантация аутологичных гемопоэтических стволовых клеток , несмотря на регистрацию но вых лекарственных препаратов и внедрение новых медицинских технологий , признана стандартом и остается базовой составляющей алгоритма лечения больных множественной миеломой в возрасте до 70 лет без сопутствующих заболеваний . Такой под ход позволяет у пациентов с минимальным коли чеством сопутствующих заболеваний и сохранным соматическим статусом выбрать соответствующую схему лечения , спланировать длительность индук ционной терапии , определить возможные сроки проведения АутоТГСК в качестве консолидирующе го этапа и инициировать в последующем поддержи вающую терапию . Обычно до процедуры мобили зации и сбора гемопоэтических стволовых клеток проводят 3–4 цикла индукционной терапии для максимально возможного уменьшения опухолевой массы , нормализации состояния больного и купиро вания симптомов [1,7].
В 2021 году EHA-ESMO опубликовали рекомендации по лечению пациентов с ВДММ, имеющих право на трансплантацию, с индукционными режимами, включающими ингибитор протеасомы бортезомиб плюс Rd (VRd) или даратумумаб в сочетании с борте-зомибом, иммуномодулирующим препаратом талидомидом и дексаметазон (DaraVTd), с последующей высокодозовой терапией, АутоТГСК и поддерживающей терапией леналидомидом или талидомидом [9]. Именно эти 2 схемы считалась стандартным лечебным подходом при впервые диагностированной множественной миеломе у пациентов, подходящим для трансплантации гемопоэтических стволовых клеток. При невозможности использования одного из этих индукционных режимов, можно использовать резервные схемы – VTD (бортезомиб / талидомид / дексаметазон) или VCD (бортезомиб / циклофосфамид / дексаметазон), но их эффективность ниже.
Однако за годы , прошедшие после публикации текущих рекомендаций по терапии ММ , стало по нятным , что необходимы новые стратегии для увеличения глубины ответа и предотвращения ре цидива , новые опции , которые способны привести к наиболее полной эрадикации всего пула опухоле вых клеток и достичь долгосрочного контроля забо левания .
В новые рекомендации по лечению ММ [10] включены все схемы , которые одобрены EMA и / или FDA или были исследованы в регистрационных ис следованиях ( рисунок 1).
Схемы , которые показали пользу в испытаниях III фазы , но не были протестированы в регистрацион -
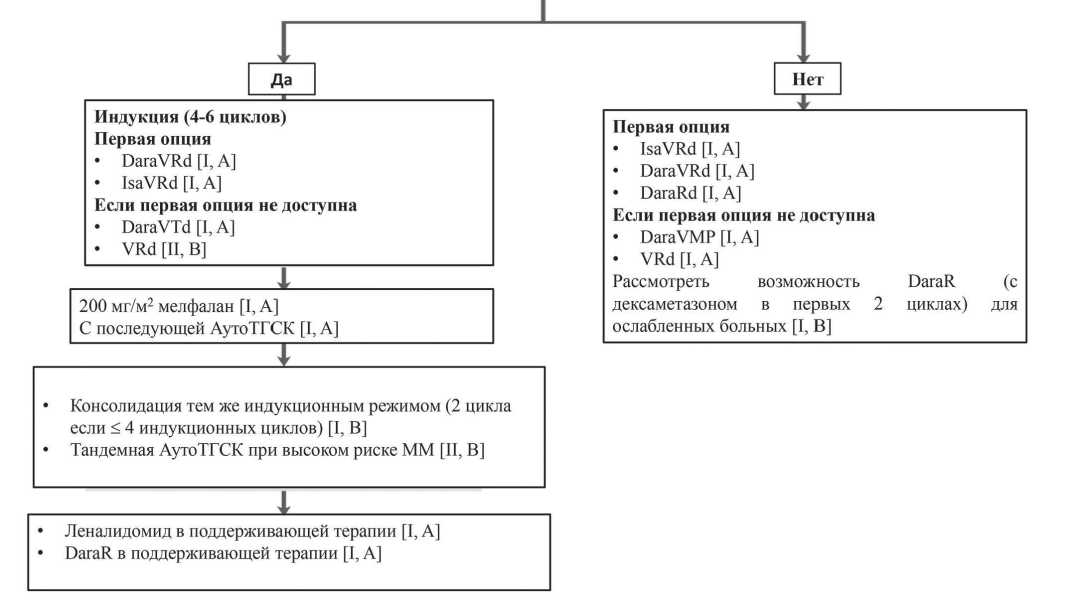
Рисунок 1. Первая линия терапии пациентов с впервые диагностированной ММ, подходящих для АутоТГСК (цит. по [10])
ных исследованиях , обсуждаются , но пока не вклю чены в рекомендации .
В 2024 году были опубликованы результаты ран домизированного исследования III фазы PERSEUS [40], которые предоставили доказательства высо кой эффективности новой схемы терапии – дарату - мумаб в сочетании с VRd ( квадриплет DaraVRd). В исследование в общей сложности были рандомизи рованы (1:1) 709 пациентов . У 22,4% и 22% больных соответственно в группе DaraVRd и VRd, выявлен высокий цитогенетический риск , у 15,5% и 14,2% -ISS-III.
Больным, вошедшим в исследование, в качестве индукции было назначено подкожное введение даратумумаба в сочетании с VRd (4 цикла) с последующей АутоТГСК и 2 циклами консолидирующей терапии VRd. Далее больные переводились на поддерживающую терапию DaraR (группа DaraVRd). Вторая группа (группа VRd) получала индукцию VRd (4 цикла), АутоТГСК и консолидацию VRd с последующей поддержкой леналидомидом. Пациенты в группе DaraVRd при достижении и сохранении устойчивого МОБ-негативного статуса в течение 12 месяцев (порог чувствительности 10-5 или ниже), получали поддержку DaraR в течение 2 лет, а затем переводились на леналидомид до прогрессирования заболевания или неприемлемой токсичности; все остальные пациенты в этой группе получали DaraR до прогрессирования заболевания или неприемлемой токсичности. Пациенты возобновляли терапию даратумумабом, если у них была подтверждена потеря полного ответа без прогрессирования заболевания (повторное появление M-белка сыворотки или мочи при иммунофиксации или электрофорезе или наличие ≥5% плазматических клеток в костном мозге) или рецидив МОБ (наличие злокачественных клеток при пороге чувствительности 10-4 или выше). В группе VRd больные получали только леналидомид и тоже до прогрессирования. При медиане наблюдения 48 месяцев прогрессирование заболевания или смерть произошли у 50 из 355 пациентов (14,1%) в группе Dara-VRd и 103 из 354 пациентов (29,1%) в группе VRd. 4-летняя ВБП составила 84,3% против 67,7% в группах DaraVRd и VRd (HR 0,42, 95% CI 0,30-0,59; P <0,001) соответственно. Коэффициент риска прогрессирования заболевания или смерти в группе Dara-VRd по сравнению с группой VRd составил 0,42 (95% CI, от 0,30 до 0,59; P <0,001) (Рисунок 2). Общая выживаемость была сходной в обеих группах.
Процент пациентов с полным ответом или луч ше был выше в группе Dara-VRd, чем в группе VRd (87,9% против 70,1%, P <0,001), как и процент паци ентов с МОБ - отрицательным статусом (10 –5) (75,2% против 47,5%, P<0,001). МОБ - отрицательный ответ при пороге чувствительности 10–6 составил 65,1 и 32,2% (p <0,0001), устойчивый МОБ - отрицательный ответ ≥ 12 мес . (10–5) — 64,8 и 29,7% (p <0,0001) со ответственно . Нежелательные явления 3 или 4 сте пени выявлены у большинства пациентов в обеих группах ; наиболее распространенными были ней тропения (62,1% с Dara-VRd и 51,0% с VRd) и тром боцитопения (29,1% и 17,3% соответственно ). Се рьезные побочные эффекты наблюдались у 57,0% пациентов в группе Dara-VRd и 49,3% пациентов в группе VRd.
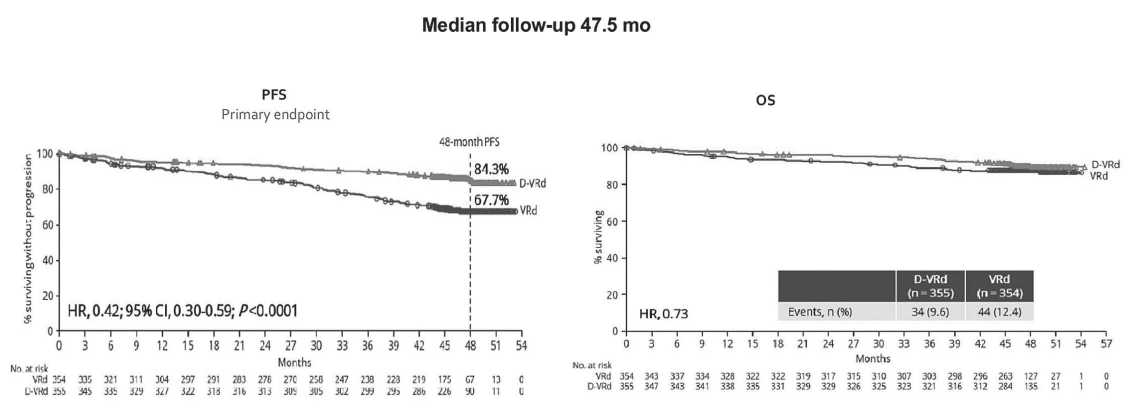
Рисунок 2. PERSEUS: выживаемость без прогрессирования (PFS) и общая выживаемость (OS) в группах пациентов с ММ, получавших D-VRd или VRd (цит. по [40])
Примечание. PFS – выживаемость без прогрессирования; OS – общая выживаемость; Primary endpoint – первичная конечная точка; VRd – даратумумаб, бортезомиб, леналидомид, дексаметазон – нижняя кривая; D-VRd - бортезомиб, леналидомид, дексаметазон – верхняя кривая; HR – отношение рисков; CI – конфиденциальный интервал
В отличие от предыдущих исследований , в PERSEUS не было второй рандомизации для поддер живающей терапии . Этот аспект дизайна исследо вания PERSEUS позволяет более четко интерпрети ровать преимущества добавления даратумумаба по всему режиму лечения , от индукционной терапии VRd до поддерживающей терапии леналидомидом , которая является стандартом для этой популяции пациентов . В то же время , это может усложнить определение вклада каждого компонента лечения в эффективность каждой фазы лечения .
Между тем , публикация результатов рандомизи рованного активно - контролируемого исследования III фазы AURIGA [41] усилила позицию DaraR в каче стве поддерживающей терапии . В это исследование были включены пациенты с ВД MM, достигшие очень хорошего частичного ответа ( ОхЧО ) или лучше , со храняющегося в течение 6 мес . после выполненной АутоТГСК , МОБ - положительные и ранее не получав шие анти -CD38 моноклональные антитела . Рандо мизация была произведена с учетом цитогенетиче ского риска ( стандартный риск / неизвестный риск или высокий риск ). Высокий риск определялся как наличие ≥ 1 из следующих цитогенетических анома лий : del(17p), t(4;14) и t(14;16).
Пациенты были случайным образом распреде лены в соотношении 1:1 для получения поддержи вающей терапии Dara-R или R ( леналидомид ). Одна группа пациентов (n = 101) получала R по 10 мг в сутки , начиная с 1- го по 28- й день каждого 28- днев ного цикла ; после 3- х циклов доза могла быть уве личена до 15 мг в зависимости от переносимости и по усмотрению исследователя . Пациенты во вто рой группе (Dara-R, n = 99) одновременно получа ли подкожно даратумумаб (1800 мг в сочетании с рекомбинантной гиалуронидазой человека PH20 (2000 ед / мл ) еженедельно в течение 1 и 2 циклов , каждые 2 недели в течение 3-6- го циклов и каждые 4 недели , начиная с 7- го цикла ( все 28- дневные ци клы ). Исследуемое лечение продолжалось в течение максимального периода , равного 36 циклам , или до прогрессирования заболевания , появления непри емлемой токсичности или отмены согласия пациен та .
Согласно представленным результатам , МОБ - негативный статус через 12 месяцев от начала под держивающей терапии был выше в группе Dara-R (50,5% против 18,8%; P <0,0001). При медиане на блюдения 32 месяца терапия Dara-R улучшила ВБП (82,7% против 66,4% только с леналидомидом через 30 месяцев ). Частота устойчивого МОБ - негативного статуса , продолжающегося ≥ 6 месяцев для группы с Dara-R, была в ~2,5 раза выше , чем у группы с R (35,4% (P = 0,0005). Более высокие показатели МОБ - отрицательного статуса (10–5) к 12 месяцам также наблюдались в группе Dara-R, чем в группе R (56,8% против 23,2% соответственно ).
Таким образом, среди пациентов с вновь выявлен- ной ММ, кандидатов на трансплантацию, которые не получали анти-CD38 антитела и имели ≥охЧО, а также были МОБ-положительными после АутоТГСК, назначение Dara-R значительно чаще меняло статус МОБ с положительного на отрицательный по сравнению с группой пациентов, получавших поддержку только леналидомидом. Это исследование продемонстрировало возможность применения дарату-мумаба не только в индукции/консолидации, но и в поддерживающей терапии в качестве стандарта. Связанные с лечением НЯ любой степени были зарегистрированы у 99,0% пациентов в обеих группах лечения. НЯ степени 3/4 наблюдались у 74,0% пациентов в группе Dara-R и 67,3% пациентов в группе R.
Весьма примечательны результаты исследова ния III фазы GMMG-HD7, которое включало пациен тов с ВДММ , являющихся кандидатами на АутоТГСК , и состояло из двух частей ( две последовательные рандомизации ) [42]. В этом исследовании применя лось другое анти -CD38 моноклональное антитело – Изатуксимаб (Isa).
В части 1 пациенты рандомизированы в соотно шении 1:1. В качестве индукционной терапии одна группа пациентов (n = 329) получила три 6- недель ных цикла стандартной схемы RVd. Пациентам груп пы Isa-RVd (n = 331) дополнительно был назначен изатуксимаб по 10 мг / кг внутривенно один раз в день на 1- й , 8- й , 15- й , 22- й и 29- й дни 1- го цикла и на 1- й , 15- й и 29- й дни 2- го и 3- го циклов . После за вершения индукционной терапии выполнена моби лизация аутологичных гемопоэтических стволовых клеток и проведена одна или две АутоТГСК . Тандем ная АутоТГСК была рекомендована тем пациентам , которые достигли < полного ответа ( ПО ) или имели заболевание высокого риска . В части 2 (2 рандоми зация ) пациентам назначена поддерживающая те рапия леналидомидом в монорежиме или в комби нации с изатуксимабом (Isa-R).
В результате пациенты группы Isa-RVd получили неоспоримые преимущества по частоте достижения ПО и МОБ - статуса перед группой больных , нахо дившихся на RVd. Так , полный ответ зарегистриро ван у 43,5% и 34,0% больных , а МОБ - негативность – у 66,2% и 47,7%; P <0,0001) после выполненной трансплантации в этих группах больных . Индукци онная терапия квадриплетом Isa-RVd значительно продлила выживаемость без прогрессирования по сравнению с триплетом RVd, причем независимо от вида поддерживающей терапии (HR 0,70 [95% CI от 0,52 до 0,95]; P = 0,0184).
Анализ результатов лечения после индукции по казал значительно более длительную ВБП у пациен тов , достигших МОБ - негативности , по сравнению с МОБ - положительными пациентами . Выживаемость без прогрессирования от старта поддерживающей терапии была значительно выше среди пациен тов с MRD- негативностью по сравнению с МОБ - положительными (HR 0,41, 95% CI 0,25 - 0,65; P
<0,001). Однако пациенты в обеих группах с МОБ - негативным статусом имели аналогичную ВБП (P = 0,77).
При анализе этого исследования обращают на себя внимания некоторые ограничения , в част ности , одно из них связано с тандемной АутоТГСК . Меньше пациентов на Isa-RVd по сравнению с RVd получили тандемную АутоТГСК , что частично объ ясняется более высокой долей пациентов на Isa-RVd, достигающих ПО . Несмотря на большее количество тандемных трансплантаций в контрольной группе , наблюдалось последовательное улучшение пока зателей МОБ - негативности и ПО после трансплан тации в пользу Isa-RVd. В окончательном анализе части 1 ( первая рандомизация ), терапия Isa-RVd продемонстрировала увеличение ВБП и более вы сокие значения МОБ - негативного статуса по срав нению с RVd в клинически значимых подгруппах , за исключением пациентов с PS WHO >1, R-ISS стадии III и цитогенетикой высокого риска .
Таким образом , 18- недельная индукционная те рапия по схеме Isa-RVd с последующей трансплан тацией привела к более высоким показателям МОБ - отрицательного (10–5) ответа , что увеличивает ВБП по сравнению с RVd независимо от поддерживаю щей терапии у пациентов с ВДММ . Эти результаты подтверждают важность использования квадрипле - тов , включающих изатуксимаб , в качестве текущего стандарта терапии пациентов с ВДММ . Как уже ука зывалось выше , в исследовании PERSEUS III фазы [40] добавление даратумумаба (Dara) к индукции RVd, консолидации RVd и в последующем поддер живающей терапии привело к значительному улуч шению ВБП . Сравнение результатов исследований PERSEUS и GMMG-HD7 ограничено из - за различий в дизайне исследования ( интенсивность дозы , про должительность индукции , использование консо лидации и случайное распределение для поддержи вающей терапии ), это может объяснить различия в группах высокого риска , хотя в обоих исследованиях были продемонстрированы преимущества квадри - плетов перед триплетом .
Еще одна рекомендуемая схема лечения, доказавшая свою эффективность по результатам долгосрочного наблюдения – исследование III фазы CASSIOPEIA [43]. В этом исследовании режим DaraVTd (даратумумаб, бортезомиб, талидомид, дексаметазон; группа 1) или VTd (группа 2) был назначен в качестве режима индукции перед АутоТГСК и консолидации с последующим применением дара-тумумаба в качестве поддерживающей терапии у пациентов с ВДММ, планируемых на трансплантацию. 1085 пациентов были рандомизированы (1:1) для получения DaraVTd или VTd для индукции (по 4 цикла), далее АутоТГСК и по 2 цикла консолидации теми же программами (первая рандомизация). Затем тем больным, у которых был достигнут частичный ответ или лучше (2 рандомизация), была назначена поддерживающая терапия даратумума-бом 16 мг/кг каждые 8 недель (1 группа, n=442) до 2 лет или пациенты только наблюдались (2 группа, n=444) (1:1).
Через 100 дней после АутоТГСК число строгих пол ных ответов ( сПО ), в том числе с МОБ - негативным статусом , было значительно выше среди больных из группы Dara-VTD против VTD. Оценка ВБП на 18 ме сяцев наблюдения показала превосходство DaraVTD над VTD (92,7% против 84,6%, P <0,0001). На дату окончания клинических исследований , 1 сентября 2023 г ., медиана наблюдения составила 80,1 месяцев с момента первой рандомизации и 70,6 месяцев со времени второй рандомизации . Выживаемость без прогрессирования после повторной рандомизации была значительно выше в группе с поддерживаю щей терапией даратумумабом , чем в группе , где про водилось только наблюдение ( медиана не достигну та [95% CI 79,9- не поддается оценке ] по сравнению с 45,8 месяцами [95% CI 0,40-0,59; P <0,0001]; оче видное преимущество наблюдалось в группе Dara-VTd на фоне поддерживающего лечения даратуму - мабом по сравнению с Dara-VTd на фоне наблюдения ( медиана не достигнута против 72,1 мес ; p=0,048) и в группе VTD на фоне лечения даратумумабом по сравнению с VTD при наблюдении ( медиана не до стигнута против 32,7 месяцев ; P <0,0001).
Таким образом , результаты исследования CASSIOPEIA показали , что включение даратумумаба в схемы индукции , консолидации и поддерживаю щей терапии приводит к превосходным результатам выживаемости без прогрессирования . Несмотря на то , что на этапе поддержки сравнивали монотера пию даратумумабом с наблюдением , такие резуль таты являются основанием считать , что Dara-VTd является стандартным методом индукционной те рапии перед АутоТГСК с последующей поддержива ющей монотерапией даратумумабом у пациентов с впервые диагностированной множественной мие ломой .
Помимо описанных выше , существуют другие схемы , которые могут оказаться приоритетными в клинической практике . Так , замена бортезомиба на карфилзомиб в квадриплетах привела к отличным показателям МОБ - статуса , особенно у пациентов с ММ высокого риска . Например , в исследовании III фазы IsKia [44] 302 пациента были рандомизирова ны на 2 группы (1:1) для получения четырех циклов квадриплета IsaKRd ( изатуксимаб , карфилзомиб , ле налидомид , дексаметазон ) или триплета KRd, с по следующим применением высоких доз мелфалана и АутоТГСК и далее консолидацией четырьмя цикла ми IsaKRd или KRd. Показатель МОБ - негативности (10 - 5) после завершения консолидации составил 77% в группе с IsaKRd против 67% в группе с KRd (HR 1,67; P = 0,049), а при МОБ 10–6 - 67% против 48% (HR 2,29; P <0,001). У пациентов с ММ высокого риска по казатель МОБ - негативности 10–6 с IsaKRd составил
72% и 67% у пациентов с стандартным риском . При чем у пациентов с double-hit миеломой показатель МОБ - негативности при использовании IsaKRd был сопоставим с таковым в подгруппе пациентов стан дартного риска (76% и 79% соответственно ).
Частота отрицательных результатов МОБ после индукции ( первая ключевая вторичная конечная точка ) также была значительно выше при IsaKRd по сравнению с KRd (10-5: 45% против 26%, P <0,001); 10-6: 27% vs 14%, P = 0,004). После индукции уровень негативности МОБ (10-5) у пациентов с высоким ри ском и double-hit, получавших IsaKRd, составил 60% и 54%, а при МОБ 10-6 – 40% и 31% соответственно . Показатели негативности МОБ после АутоТГСК так же были значительно выше при IsaKRd по сравне нию с KRd (10-5: 64% против 49%; 10-6: 52% против 27%, P <0,001), с постоянным преимуществом во всех подгруппах . При текущем наблюдении ( меди ана 20 месяцев ) не было выявлено различий в по казателях ВБП . Прекращение лечения из - за токсич ности составило 6% в группе IsaKRd по сравнению с 5% в группе KRd; связанные с лечением случаи смер ти составили 4 при IsaKRd (2 COVID, 1 пневмония , 1 тромбоэмболия легочной артерии ) и 1 при KRd ( сеп тический шок ).
Таким образом , у пациентов с ВДММ добавление изатуксимаба к KRd в индукции перед АутоТГСК и в период консолидации значительно увеличило ча стоту МОБ - негативных ответов на каждом этапе лечения по сравнению с KRd без каких - либо новых проблем с безопасностью . Важно подчеркнуть , что это преимущество сохранилось у пациентов с высо ким риском .
Такие обнадеживающие результаты, спустя 2 года, были подтверждены в исследовании III фазы MIDAS [45], в которое вошло 791 пациентов с ВДММ, кандидатов на трансплантацию. Медиана возраста составила 59 лет; у 13% была III стадия по ISS, у 5% – III стадия по R-ISS и у 8% – высокий цитогенетический риск. Все получили шесть 28-дневных индукционных циклов IsaKRd (изатуксимаб, карфил-зомиб, леналидомид, дексаметазон). В целом 96% пациентов завершили индукцию. Медиана выхода клеток CD34+ составила 7×106/кг, при этом 94% пациентам выполнена тандемная трансплантация. Уровень объективного ответа составил 95%, при этом после индукции 91% пациентов достигли ОхЧО или лучше. Уровень МОБ-негативности составил 63% при пороге чувствительности 10-5 (47% при пороге 10–6). Во время индукции у 7 пациентов наблюдалось прогрессирование заболевания; 5 умерли из-за прогрессирования заболевания (n = 1), сердечных осложнений (n = 2) или других причин (n = 2). Наиболее частыми побочными эффектами 3/4 степени тяжести были нейтропения (25%), тромбоцитопения (5%) и инфекции (7%); только 13% пациентов сообщили о периферической нейропатии любой степени тяжести. В заключении авторы делают вывод о том, что индукция IsaKRD привела к качественному ответу и высокому уровню МОБ-негативности, обеспечив успешный сбор стволовых клеток без каких-либо новых сигналов о безопасности.
В исследовании фазы II IFM 2018-04 также проде монстрирована эффективность , тандемной транс плантации при высоком цитогенетическом риске . В данном исследовании на каждом этапе , начиная с индукции и завершая поддерживающей терапией , использовался даратумумаб [46]. В исследование вошли 50 больных с ВДММ в возрасте <65 лет ( ме диана 57 лет ), с высоким цитогенетическим риском - t(4;14), del 17p и / или t(14;16)). Всем пациентам в качестве индукции проведено 6 циклов Dara-KRd ( даратумумаб / карфилзомиб / леналидомид / дек саметазон ), далее сбор гемопоэтических стволовых клеток , АутоТГСК -1, консолидация 4 циклами Dara-KRd, АутоТГСК -2, поддерживающая терапия дара - тумумабом ( каждые 8 недель ) или леналидомидом ( по 10 мг 28- дневные циклы ) в течение 2 лет . Не благоприятными событиями 3-4 степени , связан ными с лечением (>5% пациентов ), были нейтропе ния (38%), анемия (14%), тромбоцитопения (8%), инфекция (6%), почечная недостаточность (6%) и тромбоз глубоких вен (6%). Результаты исследо вания : частота общего ответа составила 100%, из них ПО – 81%. Показатель МОБ - негативности (10-6) составил 94%. После медианы наблюдения в 33 месяца , 30- месячная выживаемость без прогресси рования и общая выживаемость составили 80% и 91% соответственно [46]. Наряду с этим было про анализировано прогностическое влияние исходных параметров , включая цитогенетическую подгруппу (t(4;14), t(14;16), del(17p), увеличение (1q), del(1p). Ни один из этих параметров не был достоверно свя зан с ухудшением ВБП .
Исходя из полученных результатов , можно с уве ренностью констатировать , что лечебная стратегия , включающая Dara-KRd в индукции до АутоТГСК , и в консолидации , дополненной АутоТГСК -2 с последу ющей поддерживающей терапией даратумумабом или леналидомидом , безопасна и обеспечивает глу бокие ответы у пациентов с ВДММ в возрасте < 65 лет с цитогенетическим профилем высокого риска .
Что касается поддерживающего лечения, ряд рандомизированных исследований, во-первых, продемонстрировали преимущество бортезомиба над талидомидом, особенно у пациентов с ММ высокого риска, а во-вторых, результативность иксазомиба в сочетании с леналидомидом по сравнению с активным наблюдением за больными [47]. Так, в исследовании L. Rosinol et al. [48] больные после индукционной терапии схемой VRD с последующей АутоТГСК и консолидации VRD, были рандомизированы на 2 группы: в одной из них назначена поддерживающая терапия леналидомидом и дексаметазоном (RD), а в другой RD плюс иксазомиб (IRD). RD включала леналидомид в дозе 15 мг/сут с 1 по 21 день плюс дек- саметазон в дозе 20 мг/сут с 1 по 4 день и с 9 по 12 день с интервалом в 4 недели, тогда как в группе IRD добавлялся пероральный иксазомиб в дозе 4 мг в 1, 8 и 15 дни. При достижении МОБ-отрицательного статуса после 24 циклов поддержка прекращалась, в то время как пациенты с МОБ-положительным результатом теста оставались на поддерживающей терапии RD еще в течение 36 циклов. Исследование показало, что после медианы наблюдения, равной 69 месяцев с момента начала поддерживающей терапии, ВБП была сходной в обеих группах больных, с 6-летней ВБП 61,3% и 55,6% для RD и IRD соответственно (HR 1,136; 95% CI 0,809-1,603) [48]. После 2 лет поддерживающей терапии лечение было прекращено у 163 пациентов с отрицательным МОБ статусом, в то время как 63 пациента с положительным тестом на МОБ продолжали терапию RD. Прекращение лечения у пациентов с отрицательным результатом теста на МОБ привело к низкой частоте прогрессирования (17,2% за 4 года), даже у пациентов с критериями высокого риска. Таким образом, представленные результаты показывают эффективность поддержания RD и подтверждают безопасность прекращения поддерживающей терапии у пациентов с отрицательным МОБ статусом через 2 года.
На сегодняшний день , АутоТГСК является пред почтительным методом лечения больных с ВДММ . Дискуссия о необходимости двойной АутоТГСК про должается . Поэтому вопрос о необходимости ее про ведения необходимо решать в трансплантационном центре с учетом результатов контрольного обсле дования больного . Однако данные накапливаются , несмотря на неоднозначный характер опублико ванных результатов исследования ( что можно объ яснить и различием в дизайне исследований ), тан демная АутоТГСК является эффективной лечебной опцией для пациентов с ММ высокого риска ( Рису нок 1).
Наряду с АутоТГСК, предлагается аллогенная трансплантация стволовых клеток (АллоТГСК), которая, по мнению ряда исследователей, может быть реальным методом излечения больных ММ. В то же время проведение АллоТГСК, как известно, сопровождается развитием тяжелых осложнений (острая и хроническая реакция «трансплантат против хозяина», инфекционные осложнения и др.) и высокой летальностью, частота которой в течение 100 дней после трансплантации у больных ММ колеблется от 10% до 56% в разных сериях исследований. Поэтому аллогенная ТГСК на сегодняшний день не является рекомендуемой лечебной опцией при ММ. Однако молодые пациенты, у которых наступает рецидив после второй аутологичной трансплантации, при наличии HLA-идентичного донора, могут быть кандидатами на аллогенную трансплантацию. Тем не менее, аллогенная трансплантация гемопоэтических стволовых клеток (АллоТГСК) имеет очень ограниченное значение у пациентов с MM. В последние годы появились работы по использованию аутологичной трансплантации, а в последующем – аллогенной (ауто-аллоТГСК) с использованием режимов кондиционирования сниженной интенсивности. Однако результаты исследования III фазы показали, что ее эффективность не превышает таковую тандемный АутоТГСК у пациентов со стандартным риском MM [49]. В рамках одного исследования 3-й фазы были включены пациенты (моложе 70 лет) с адекватной функцией органов, которые прошли не менее трех циклов системной антимиеломной терапии в течение последних 10 месяцев, имели право на включение в исследование. Пациентам была назначена аутологичная ТГСК с последующей аллогенной ТГСК (группа ауто-алло) или тандемную аутологичную ТГСК (группа ауто-ауто). Пациенты из группы "ауто-ауто" впоследствии были случайным образом распределены (1:1) на поддерживающую терапию (талидомид плюс дексаметазон) или наблюдение.
По результатам исследования показатели ВБП и общей выживаемости не отличались между груп пами больных , получивших ауто - ауто или ауто - ал - ло . По оценке методом Каплана - Мейера 3- летняя выживаемость составила 43% в группе ауто - алло и 46% в группе ауто - ауто ( р =0,671); общая выживае мость также не отличалась через 3 года (77% против 80%; Р = 0,191). У 46% пациентов в группе ауто - алло выявлены нежелательные явления 3-5 степени тя жести , как и у 42% в группе ауто - ауто . Нежелатель ными явлениями , которые в наибольшей степени различались между группами , были гипербилиру бинемия (11% пациент в группе ауто - алло против 3% в группе ауто - ауто ) и периферическая нейропа тия (6% в группе ауто - алло против 12% в группе ау - то - ауто ) [49].
Аналогичные результаты были сообщены Kroger N. et al. по результатам исследования II фазы [50]. Это открытое многоцентровое клиническое иссле дование в параллельных группах для сравнения АутоТГСК / АллоТГСК с аутологичной тандемной трансплантацией , после выполнения которых в течение 2 лет проводилась поддерживающая те рапия талидомидом (100 мг / сут ). Пациенты могли пройти максимум восемь циклов индукции , а после АллоТСКТ были разрешены дополнительные про филактические вливания донорских лимфоцитов . Медиана возраста больных в обеих группах состави ла 51 год . В общей сложности 178 пациентам была проведена повторная трансплантация (132 аллоген ных и 46 аутологичных ). Период наблюдения в ходе исследования составил 48 месяцев , считая со второй ТГСК . Долгосрочное наблюдение за состоянием здо ровья и выживаемостью пациентов продолжалось в течение 10 лет со медианой наблюдения 82 месяца .
ВБП через 4 года после второй трансплантации составила 47% при аллотрансплантации и 35% при аутотрансплантации. Через 8 лет эта разница уве- личилась до 22% (Р = 0,10). Совокупная частота без-рецидивной смертности и рецидива через 4 года составила 13% (95% CI 8-20%) и 2% (95% CI 0,3-2%) (Р = 0,044), а также 40% (95% CI 33-50%) и 63% (95% CI 50-79%) (Р=0,04) для АллоТГСК и АутоТГСК соответственно. Разница в отношении рецидива/прогрес-сирования увеличилась до 33% (АллоТГСК: 44%. АутоТГСК: 77%) при медиане наблюдения 82 месяца (Р = 0,002). Четырехлетняя общая выживаемость составила 66% (95% CI 57-73%) при АллоТГСК и 66% (95% CI 50-78%) при АутоТГСК (Р=0,91), а 8-летняя общая выживаемость – 52% и 50% (Р = 0,87) соответственно. Авторы резюмируют, что АллоТГСК с последующей поддерживающей терапией талидомидом снизила частоту рецидивов или прогрессирования на 23% при периоде наблюдения 4 года и на 33% при периоде наблюдения 8 лет. За этот же период АллоТГСК привела к снижению смертности, связанной с заболеванием, примерно на треть, с 30% до 21%. Однако преимущество в показателях ВБП после АллоТГСК не достигло статистической значимости.
То есть , АллоТГСК , вероятно , может обеспечить ограниченную пользу в конкретной подгруппе па циентов с MM высокого риска , однако эта польза су щественно ниже в случае применения DaraR в каче стве поддерживающей терапии после выполненной АутоТГСК . Для совершенствования подхода к алло генной ТГСК , вероятно , необходима работа по даль нейшему усилению эффекта " трансплантат против миеломы ", что и приведет к снижению смертности , связанной с трансплантацией .
Лечение пациентов, не являющихся кандидата- ми на проведение АутоТГСК
Проведение АутоТГСК у пожилых и ослабленных пациентов сопряжено с риском существенной ток сичности и ранней летальности . Основываясь на ре зультатах актуальных клинических исследований III фазы по лечению пациентов с ВДММ , не подходящих для АутоТГСК , стандартными схемами были призна ны DaraRd, DaraVMP и VRd [51-53], рекомендован ные EHA [9]. В последние годы были опубликованы результаты лечения пожилых пациентов , показав шие целесообразность использования три - или ква - дриплетов , содержащих моноклональные антитела ( МКА ). Действительно включение анти -CD38 МКА ( даратумумаб , изатуксимаб ) в схемы первой линии терапии ВДММ существенно улучшило результаты лечения пожилых пациентов .
В 2024 г . были опубликованы результаты срав нительного исследования III фазы IMROZ (Isa-VRd vs VRd) у пациентов с ВДММ , не подходящих для АутоТГСК [54]. 446 пациентов в возрасте 18-80 лет были случайным образом распределены (3:2) для получения IsaVRd против VRd в качестве индукции , а затем IsaRd и Rd ( группа контроля ) соответствен но , в качестве поддерживающей терапии достигну той ремиссии . При медиане наблюдения 59,7 меся цев Isa-VRd, а в поддерживающей терапии Isa-Rd, существенно снизился риск прогрессии или смерти ( на 40,4%). Медиана ВБП в группе терапии с изатук - симабом не была достигнута vs 54,3 мес . (P <0,0001) в группе контроля . 5- летняя ВБП составила 63,2% в группе Isa-VRd против 45,2% в группе VRd (HR 0,60, 98,5% CI 0,41-0,88; P <0,001) ( Рисунок 3).
Процент пациентов с полным ответом или лучше
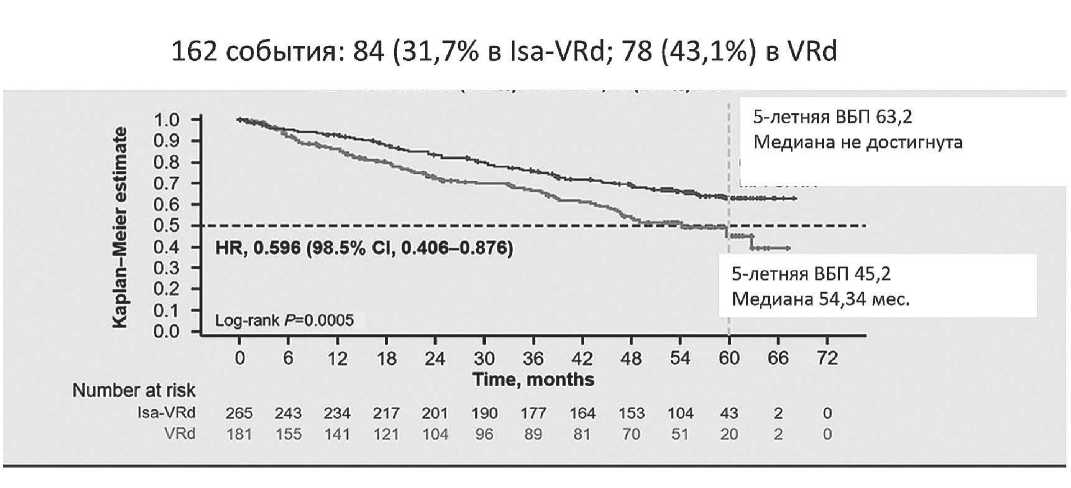
Рисунок 3. - IMROZ: Выживаемость без прогрессирования (цит. по [54]).
Примечание. Isa-VRd – верхняя кривая; VRd – нижняя кривая
в группе Isa-VRd превысил таковой в группе боль ных , находящихся на терапии VRd (74,7% против 64,1%, P = 0,01), как и процент пациентов с МОБ - отрицательным статусом (10–5) и полным ответом (55,5% против 40,9%, P = 0,003). Никаких новых сиг налов безопасности при приеме Isa-VRd не наблю далось . Частота серьезных побочных эффектов во время лечения и частота побочных эффектов , при водящих к прекращению лечения , были одинаковы ми в двух группах больных .
Значение Isa-VRd дополнительно подтвердили результаты исследования III фазы BENEFIT [55], проведенного Intergroupe Francophone du Myeloma (IFM). В этом исследовании 270 пациентов , не под лежащих трансплантации , с ВДММ в возрасте 65-79 лет были распределены (1:1) для получения ква - дриплета Isa-VRd против триплета Isa-Rd. По полу ченным результатам , МОБ - негативность (10-5) через 18 месяцев после рандомизации была гораздо выше среди пациентов , получавших Isa-VRd (53% против 26%; HR 3,16, 95% CI 1,89-5,28; P <0,0001). Более вы сокие показатели негативности МОБ при Isa-VRd также наблюдались через 12 месяцев как при пороге чувствительности 10-5, так и при 10-6. 24- месячные показатели ВБП и ОО составили 80,0% и 91,5 для Isa-Rd, и 85,2% и 91,1% для Isa-VRd соответственно . Доля пациентов с полным ответом или улучшением состояния через 18 месяцев была выше при Isa-VRd (58% против 33%; P <0,0001), как и доля пациен тов с отрицательным результатом МОБ и полным ответом или улучшением состояния (37% против 17%; P = 0,0003). Еженедельный прием бортезоми - ба существенно не повлиял на относительную ин тенсивность приема Isa-Rd. Было зарегистрировано 271 расстройство нервной системы , из которых 163 (60%) – нейропатия , развившаяся у 38 (28%) паци ентов в группе Isa-Rd и у 70 (52%) пациентов в груп пе Isa-VRd. Периферическая нейропатия ≥ 2 степени наблюдалась у 13 (10%) пациентов ( у 1 пациента была нейропатия 3 степени ) в группе Isa-Rd и у 37 (27%) пациентов ( у 4 пациентов была нейропатия 3 степени ) в группе Isa-VRd. Таким образом , профиль безопасности как препаратов Isa-Rd, так и Isa-VRd соответствовал известным профилям безопасно сти при Dara-Rd, и , кроме того , случаи прекраще ния лечения и смерти из - за НЯ в группе Isa-VRd со ответствовали количеству пациентов , получавших Isa-Rd. В целом результаты исследования BENEFIT продемонстрировали значимое преимущество ква - дриплета изатуксимаб плюс VRd по сравнению с триплетом Isa-Rd. Эти данные , по мнению авторов , подтверждают , что Isa-VRd является новым методом стандартной терапии пациентов с ВДММ в возрасте от 65 до 79 лет .
В начале 2025 г. опубликованы результаты сходного по дизайну с IMROZ исследования III фазы CEPHEUS с даратумумабом (Dara-VRd vs VRd). В исследовании CEPHEUS больные получили 8 циклов квадриплета Dara-VRd или триплета VRd с последующим переводом на длительную поддерживающую терапию Dara-Rd или Rd до прогрессирования или неприемлемой токсичности (даратумумаб вводился подкожно) [56] У 28,1% была выявлена III стадия заболевания по ISS, а у 13,2% – высокий цитогенетический риск (t(4;14), t(14;16) или del(17p)); ECOG = 2 выявлен у 11,7% для Dara-VRd против 7,1% для VRd, а 36,0% и 42,4% соответственно имели ECOG, равный 0.
При медиане наблюдения 58,7 месяцев , общий показатель МОБ - негативности при пороге чувстви тельности 10 - 5, составил 60,9% в группе Dara-VRd против 39,4% в группе VRd (HR 2,37, 95% CI 1,58– 3,55; P <0,0001) ( Рисунок 4).
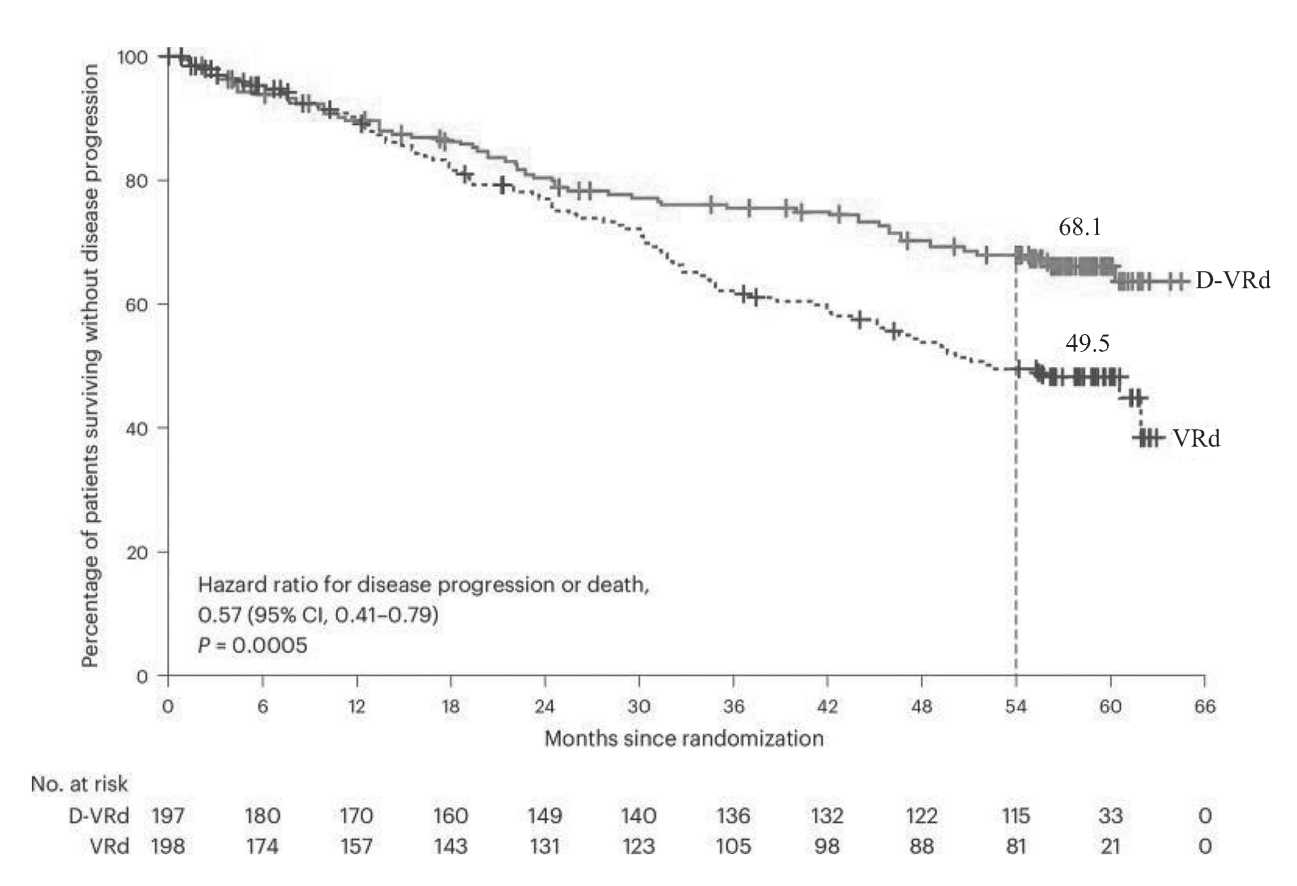
Частота отрицательных результатов МОБ при 10-6 также была выше при применении Dara-VRd по сравнению с VRd (46,2% против 27,3%; HR 2,24; 95% CI 1,48-3,40; P = 0,0001. Устойчивый показатель МОБ - негативности ( ≥ 12 месяцев ) в группе Dara-VRd значительно превысил таковой в группе VRd (48,7% против 26,3%; HR 2,63; 95% CI, 1,73–4,00; P <0,0001). Прогрессирование заболевания или смерть про изошли у 32,0% пациентов в группе Dara-VRd и у 46,0% в группе VRd. Применение D-VRd значитель но улучшало ВБП по сравнению с VRd, с коэффи циентом риска 0,57 (95% CI 0,41–0,79; P = 0,000), а медиана ВБП не была достигнута по сравнению с 52,6 мес . соответственно (HR 0,57, 95% CI 0,41-0,79; P = 0,0005); 54- месячный показатель ВБП составил 68,1% против 49,5% ( Рисунок 5).
Результаты CEPHEUS показали , что сочетание даратумумаба с VRd значительно улучшило кли нические результаты , включая МОБ - статус и ВБП , по сравнению с VRd у пациентов с ВДММ , не подхо дящих для трансплантации , и это еще один метод стандартной терапии у этой категории больных .
Еще одна схема терапии у пациентов пожилого возраста – D-VMP ( даратумумаб , бортезомиб , мел - фалан , преднизолон , которая перешла из преды дущих клинических рекомендаций . Ее назначение обосновано результатами рандомизированного ис следования III фазы ALCYONE, в котором приняли участие 706 пациентов с ВДММ , не являющиеся кан дидатами на проведение АутоТГСК ( возраст ≥ 65 лет или наличие существенных сопутствующих забо леваний ) [57]. В этом исследовании больные были рандомизированы на 2 группы . Пациенты 1 группы ( контрольная ) получали до девяти 6- недельных ци клов VMP ( подкожно бортезомиб 1,3 мг / м 2 1, 4, 8, 11, 22, 25, 29 и 32 дни первого цикла , а со второго по девятый циклы – 1, 8, 22 и 29 дни ; мелфалан 9 мг / м 2 и преднизолон 60 мг / м 2 внутрь с 1 по 4 день каждого цикла ) и далее больные переходили в ста тус наблюдения . Лечение пациентов 2 группы было дополнено даратумумабом ( схема D-VMP), который назначался внутривенно (16 мг / кг один раз в неде лю в течение первого цикла , 1 раз в 3 недели со вто -
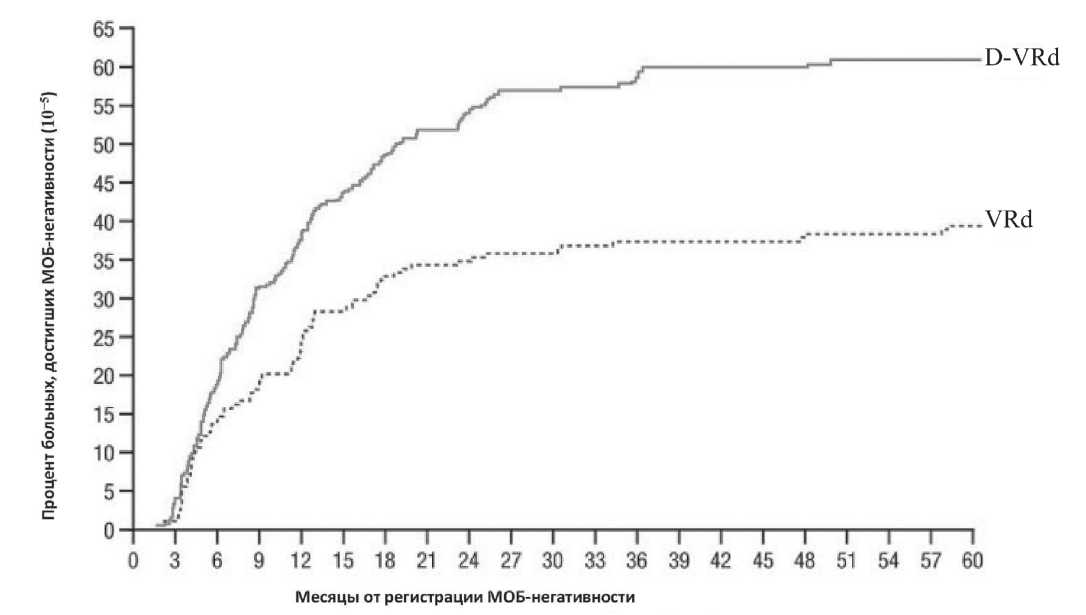
Рисунок 4. Частота МОБ-негативных результатов (порог чувствительности 10 -5 ) (Цит. по [56]).
Примечание. D-VRd - подкожное введение даратумумаба плюс бортезомиб/леналидомид/ дексаметазон; МОБ -минимальная остаточная болезнь; VRd, бортезомиб/леналидомид/дексаметазон.
68.1
D-VRd
49.5
VRd
80 -
60 -
40 -
20 -
No. at risk
D-VRd
VRd
Hazard ratio for disease progression or death, 0.57 (95% Cl, 0.41-0.79)
P = 0.0005
1 i
24 30 36 42
Months since randomization
Рисунок 5. Выживаемость без прогрессирования, рассчитанная по методу Каплана-Мейера, среди пациентов, получавших D-VRd или VRd (цит. по [56]).
рого по девятый циклы , а затем 1 раз в 4 недели до прогрессирования заболевания или неприемлемой токсичности ). При медиане наблюдения 40 мес . ме диана ВБП составляла 36,4 мес . для D-VMP и 19,3 мес . – VMP, а 36- месячная общая выживаемость – 78% и 68% соответственно . Зарегистрировано снижение риска смерти пациентов , получавших D-VMP, на 40%.
Окончательный анализ исследования ALCYONE опубликован Mateos M. V. et al. в 2025 году . Представ лены убедительные существенные преимущества D-VMP перед VMP при долгосрочном наблюдении [58], а именно , при медиане наблюдения 86,7 ме сяцев комбинация D-VMP обеспечила отчетливое увеличение ОВ , которая составила 83 месяца про тив 53,6 месяцев в группе больных с VMP (HR 0,65, 95% CI 0,53-0,80; P <0,0001). Наиболее распростра ненными НЯ 3 или 4 степени тяжести были нейтро пения (40% в группе D-VMP против 39% в группе VMP), тромбоцитопения (35% против 38%) и ане мия (18% против 20%). Смерти из - за побочных эф фектов , связанных с лечением , наблюдались у пяти (1%) из 346 пациентов в группе D-VMP ( пневмония , острый инфаркт миокарда , нейроэндокринная опу холь , синдром лизиса опухоли и острая дыхательная недостаточность ) и у трех (1%) из 354 пациентов в группе VMP ( острый миелоидный лейкоз , легочная эмболия и бактериальная пневмония ).
Таким образом , после более чем 7- летнего на блюдения D-VMP продолжала демонстрировать клинические преимущества в сравнении с VMP у пациентов с впервые выявленной множественной миеломой , которые не могли получить АутоТГСК , поддерживая в течение этих лет эффективность и безопасность терапии на основе даратумумаба .
На серьезные преимущества D-VMP перед VMP обращается внимание и в исследовании III фазы OCTANS [59]. В исследовании при сроке наблюдения за больными >3 лет медиана выживаемости без прогрессирования составила 38,7 мес. против 19,2 мес.; медиана времени до следующего лечения – 46,8 мес. против 20,6 мес.; частота МОБ-негативности – 40,4% против 10,8%, устойчивый негативный МОБ статус в течение ≥12 месяцев – 24,7% против 1,4%, ≥18 месяцев – 15,1% против 1,4% [59]. Медиана выживаемости без прогрессирования была выше у пациентов, у которых был достигнут отрицательный результат МОБ, и у пациентов с устойчивым отрицательным результатом МОБ. Преимущество в выживаемости без прогрессирования, наблюдаемое при применении D-VMP, сохранялось в большинстве клинически значимых подгрупп, включая пациентов с цитогенетическими факторами высокого риска. При длительном наблюдении никаких новых проблем с безопасностью выявлено не было. Окончательный анализ OCTANS продолжает демонстрировать клиническое преимущество D-VMP по сравнению с VMP у пациентов с ВДММ, не подлежащих трансплантации, что согласуется с результатами глобального исследования ALCYONE и поддерживает использование комбинаций даратумумаба в этой популяции пациентов.
Еще один триплет (D-Rd), также как и D-VMP со хранили свою роль в терапии пожилых пациентов . Его эффективность и относительная безопасность показана в проспективном сравнительном исследо вании III фазы MAIA [60], в котором было отмечено значительное улучшение выживаемости без про грессирования заболевания при применении три плета D-Rd по сравнению с дуплетом Rd у пациентов с впервые диагностированной множественной мие ломой , не имеющих права на трансплантацию (D-Rd vs Rd).
Пациенты были рандомизированы (1:1) для по лучения 28- дневных циклов внутривенного введе ния даратумумаба (16 мг / кг один раз в неделю в те чение циклов 1-2, один раз в 2 недели в циклах 3-6 и один раз в 4 недели после этого ) плюс пероральный прием леналидомида (25 мг в 1-21- й дни каждого цикла ) и дексаметазона (40 мг в 1, 8, 15 и 22- й дни каждого цикла ; группа даратумумаба ) или только леналидомида и дексаметазона ( контрольная груп па ).
При медиане наблюдения 56,2 мес ., медиана ВБП не достигнута в группе D-Rd против 34,4 мес . в кон трольной группе . Медиана ОВ не достигнута в обеих группах больных , но преимущество на 60 месяцев наблюдения , отчетливое – 66,3% в группе DaraRd и 53,1% – Rd (P = 0,0013 [60]. Наиболее частыми (>5%) побочными эффектами 3- й степени или выше были нейтропения (54% пациентов в группе даратуму - маба против 37% в контрольной группе ), пневмо ния (19% против 11%), анемия (17% против 22%) и лимфопения (16% против 11%). Летальные исходы , связанные с лечением , произошли у 4% пациентов в группе даратумумаба и у 3% пациентов в контроль ной группе .
Долгосрочные результаты еще более убедитель ны [61]. Так , при медиане наблюдения 89,3 мес . ме диана ВБП составила 61,9 vs 34,4 мес . (P <0,0001), ме диана ОВ — 90,3 vs 64,1 мес . (P <0,0001) для 2 групп рандомизации соответственно [61]. Улучшение ОВ отмечалось у всех пациентов , достигших МОБ - отрицательного статуса , при этом частота достиже ния МОБ - негативности была в 3 раза выше в группе D-Rd, чем в группе Rd.
Представленные данные свидетельствуют, что показатели достижения качественного и МОБ-отрицательного ответа, выживаемости без прогрессирования при терапии Isa-VRd или D-VRd гораздо выше, чем при применении триплета VRd, а D-VMP D-Rd выше, чем VMP и Rd. Результаты клинических исследований триплетов и квадриплетов, включавших анти-CD38 МКА, у пациентов с ВДMM, не подходящих для АутоТГСК, действительно продемонстрировали беспрецедентные результаты достижения MОБ-негативных ответов при пороге чувствитель- ности 10-5 и 10-6 и существенный прирост показателей выживаемости. Обращает на себя внимание лишь увеличение токсичности новых режимов, что указывает на необходимость адекватного отбора пожилых пациентов с приемлемым физическим статусом.
Ослабленные пациенты
Слабость — это субъективное ощущение сниже ния физической или психической энергии , при ко тором человек чувствует нехватку сил для привыч ных действий , нарушение концентрации внимания , невозможность выполнять обычные повседневные нагрузки , уязвимость к стрессовым ситуациям и вы сокому риску состояний , связанных со здоровьем ( таких как нарушения обмена веществ , инфекции или рак ), что приводит к увеличению заболеваемо сти и смертности [62]. Установлено , что по крайней мере две трети пациентов с ММ в той или иной сте пени имеют слабость . Например , в одном когортном популяционном исследовании около 40% пациентов с ММ имели тяжелую слабость [63]. Возраст , сопут ствующие заболевания в сочетании с ослабленно - стью имеют значительное влияние на эффектив ность и переносимость специфической терапии у пациентов с ММ , что требует тщательного внимания к выбору терапевтических средств , дозы и терапии сопровождения у данной группы больных , с целью обеспечения оптимальных результатов лечения . Па циенты со слабостью не всегда могут иметь доступ к развивающемуся спектру методов лечения , которые улучшают результаты у большинства пациентов с ММ младшего возраста и / или более благоприятно го состояния работоспособности . Поэтому эта груп па пациентов , определяемая как хрупкие , является неудовлетворенной клинической потребностью .
Выявление пациентов, подверженных риску слабости, является ключом к улучшению общих результатов лечения пациентов. С этой целью IMWG FS была разработана адаптированная к MM система гериатрической оценки, которая включает в себя не только функциональные, но и клинические показатели и считается золотым стандартом в этой области [64]. Система гериатрической оценки состоит из 3 инструментов: Katz Activity of Daily Living (ADL), Lawton Instrumental Activity of Daily Living (IADL) и Charlson Comorbidity Index (CCI). Шкалы ADL и IADL были приняты для оценки деятельности по уходу за собой, выполнения домашних задач (управление домашним хозяйством) и статуса независимости от других людей [65]. CCI оценивает количество и тяжесть сопутствующих заболеваний [66]. CCI был разработан под руководством Мэри Чарлсон в 1987 году для оценки отдаленного прогноза коморбид-ных больных. Была проанализирована смертность пациентов в течение одного года в зависимости от наличия различных сопутствующих заболеваний, в результате был создан список из 19 сопутствующих заболеваний, взвешенных от 1 до 6 баллов, в соот- ветствии с их относительным риском смерти. При расчете этого индекса суммируются баллы, соответствующие сопутствующим заболеваниям, а также добавляется один балл на каждые десять лет жизни при превышении пациентом сорокалетнего возраста (то есть 50 лет – 1 балл, 60 лет – 2 балла и т. д.), рассчитывается общая оценка (от 0 до 40 баллов). Возраст является единственным неустранимым предиктором частоты коморбидной отягощенности. Под коморбидностью чаще всего подразумевается сосуществование двух и/или более заболеваний у одного пациента, патогенетически взаимосвязанных между собой. Важнейшую роль в формировании коморбидности играют универсальные патофизиологические механизмы и развивающиеся общепатологические процессы (хроническое воспаление, дистрофия, нарушения крово- и лимфообращения и др.)
Главным отличием индекса Charlson считается возможность оценки возраста пациента и опреде ления летальности , которая при отсутствии комор - бидности составляет 12%, при 1–2 баллах – 26%, при 3–4 баллах – 52%, а при сумме более 5 баллов – 85%. Данный индекс очень часто используется в клини ческой практике и входит в критерии включения пациентов в некоторые клинические исследования . Однако эта шкала никогда не используется у паци ентов в возрасте <55 лет .
Для мониторинга динамики заболевания и выбора оптимальной тактики лечения широко используется шкала ECOG (Eastern Cooperative Oncology Group /World Health Organization Performance Status (ECOG/WHO PS), которая описывает уровень функционального состояния пациента в рамках способности заботиться о себе, повседневной деятельности и физической активности (0-4 балла). Высокий FS (≥2) может предсказать низкую переносимость лечения, более низкую реакцию на лечение, а также плохие результаты выживаемости и качества жизни не только в клинических исследованиях, но и в реальных популяциях. В 1991 г. M.D. Miller опубликовал модифицированную шкалу CIRS для пожилых пациентов – CIRS-G (Cumulative Illness Rating Scale for Geriatrics). В шкале оценивается состояние каждой из систем органов, при этом «0» соответствует отсутствию заболеваний выбранной системы, «1» – легким отклонениям от нормы или перенесенным в прошлом заболеваниям, «2» – болезни, нуждающейся в назначении медикаментозной терапии, «3» – заболеванию, ставшему причиной инвалидности, а «4» – тяжелой органной недостаточности, требующей проведения неотложной терапии. Сумма баллов может варьировать от 0 до 56. Пациенты высокого риска (имеющие 6 и более баллов согласно данным литературы), не являются кандидатами для интенсивной терапии. Основным недостатком индекса CIRS-G является его относительная сложность и избыточность. Недостаточная валидация порогового значения балла, разделяющего пациентов на про- гностические группы, приводят к тому, что она редко используется вне клинических исследований.
Несмотря на доказательства , демонстрирую щие прогностический потенциал этих клинически основанных систем оценки , доступны лишь огра ниченные данные для подтверждения их прогно стической ценности , что снижает их применение в клинической практике .
Как уже представлено выше , D-Rd в настоящее время считается стандартным режимом лечения по жилых пациентов с ВДММ , в том числе с IMWG FS ≥ 2, о чем свидетельствуют результаты исследования III фазы MAIA, опубликованные Facon T., Cook G., Usmani S.G. et al. в 2022 году . В исследовании представлен анализ подгрупп по статусу слабости . Оценка сла бости проводилась ретроспективно с использова нием возраста , индекса сопутствующей патологии Чарльсона и базового показателя ECOG. Пациенты были классифицированы как сохранные , промежу точный уровень сохранности (fit + intermediate) или ослабленные / хрупкие . Из рандомизированных па циентов (D-Rd, n = 368; Rd, n = 369) 396 пациентов имели промежуточный уровень сохранности (D-Rd, 196 [53,3%]; Rd, 200 [54,2%]), а 341 пациент были ос лабленными (172 [46,7%]; 169 [45,8%]).
Установлено , что D-Rd превосходит Rd как с точ ки зрения ВБП , так и ОВ в подгруппе пациентов с IMWG FS ≥ 2 [67]. После 36,4- месячного наблюдения преимущество D-Rd по сравнению с Rd сохранялось во всех подгруппах слабости : сохранные ( медиана не достигнута против 41,7 месяцев ); промежуточ ный уровень сохранности ( медиана не достигнута в обеих когортах ); ослабленные / хрупкие ( медиана не достигнута против 30,4 месяца ; P = 0,003). Во всех подгруппах наблюдались более высокие показатели полного и МОБ - негативного (10-5) ответа в группе пациентов , получавших D-Rd. Наиболее частым по бочным эффектом 3/4 степени , возникающим в ре зультате лечения , у пациентов с промежуточным уровнем сохранности и ослабленных пациентов была нейтропения ( промежуточный уровень со хранности D-Rd – 45,4% и Rd – 37,2% соответствен но ; ослабленные – 57,7% и 33,1% соответственно ). Полученные результаты , хотя и основаны на ре троспективной оценке слабости , подтверждают клиническую пользу D-Rd у пациентов с ВДММ , не подходящих для трансплантации , независимо от со стояния слабости .
В проспективном открытом рандомизированном исследовании III фазы IFM2017-03 [68] лечение ле налидомидом плюс даратумумабом с дексаметазо ном , было ограничено двумя циклами , что снизило риск прогрессирования или смерти по сравнению с Rd, у пожилых пациентов и / или с IMWG FS ≥ 2, т . е . этот подход ограничивает лечение дексаметазоном . Пациенты в возрасте 65 лет и старше ( медиана воз раста 81 год ) с ВДММ и соматическим статусом ≥ 2 были распределены 2:1 для получения D-R против
Rd ( даратумумаб (1800 мг подкожно ) плюс перо ральный леналидомид (25 мг в день в течение 21 дня 28- дневного цикла ) и дексаметазон (20 мг в неделю только в течение двух циклов ; группа ща дящей стратегии ) или леналидомид (25 мг в день ) и пероральный дексаметазон (20 мг в неделю ; кон трольная группа )). Медиана наблюдения составила 46,3 месяца . Медиана ВБП составила 53,4 месяца против 22,5 месяцев в группе контроля (P <0,0001), а медиана ОВ не была достигнута по сравнению с 47,2 месяцами (P = 0,0001). Хотя медиана продолжитель ность лечения была больше в группе D-R (31,6 ме сяца против 14,3 месяцев с Rd), частота возникнове ния инфекций степени ≥ 3 была аналогичной (19% против 21%).
Таким образом , в исследовании IFM2017-03 ис пользование леналидомида плюс даратумумаба , с дексаметазоном , ограниченным 2 циклами лече ния , снизило риск прогрессирования или смерти по сравнению с леналидомидом плюс дексаметазон без дополнительных опасений по поводу безопасности . Леналидомид плюс даратумумаб можно рассматри вать в качестве варианта лечения для пожилых па циентов со слабостью , с IMWG FS ≥ 2 и недавно диа гностированной множественной миеломой .
Рекомендации [10]
-
• У пациентов в возрасте <70 лет без сопутству ющих заболеваний рекомендуется индукционная терапия с последующей высокодозовой терапией и АутоТГСК [I, A].
-
• Что касается индукционной терапии до Ау - тоТГСК , то D-VRd и Isa-VRd на сегодняшний день являются наиболее эффективными и безопасными среди квадриплетов и рекомендуются в качестве но вых схем стандартной терапии [I, A].
DaraVTd - еще один действенный вариант стан дартной терапии [I, A], хотя он не сравнивался на прямую с D-VRd. Если вышеуказанные схемы недо ступны , можно использовать VRd [II, B]. Для всех индукционных схем рекомендуется от четырех до шести циклов ( Рисунок 1).
-
• Сбор гемопоэтических стволовых клеток дол жен проводиться после трех или четырех индукци онных циклов [I, A].
-
• Высокодозовая терапия мелфаланом 200 мг / м 2 – это рекомендуемый режим кондиционирования перед АутоТГСК [I, A].
-
• На сегодняшний день консолидирующая те рапия после АутоТГСК не является стандартным подходом . Однако у пациентов , которые получили только четыре цикла индукции D-VRd, следует рас смотреть необходимость применения двух циклов консолидации DaraVRd [I, B].
-
• Тандемная АутоТГСК может быть показана па циентам с ММ высокого цитогенетического риска [II, B] или всем пациентам , которые получили ин дукцию триплетом VCD [I, A].
-
• Леналидомид считался стандартным методом
поддерживающей терапии после АутоТГСК у всех пациентов с MM [I, A]. На основе результатов иссле дования PERSEUS, согласно которого добавление даратумумаба к леналидомиду увеличило выжива емость без прогрессирования , этот дуплет является новым стандартом поддерживающей терапии [I, A].
-
• Пациенты , которым не показана АутоТГСК , но имеющие IMWG FS <2 и возраст <80 лет , могут полу чать два новых режима : Isa-VRd и D-VRd [I, A].
Триплет D-Rd всем пациентам , не являющихся кандидатами на трансплантацию , особенно с IMWG FS ≥ 1 [I, A]. Щадящая стратегия дексаметазона (D-R) должна быть рассмотрена у пациентов с IMWG FS ≥ 2 [I, B]. Если ни один из вышеупомянутых вариантов недоступен , можно использовать D-VMP или VRd [I, A].
Таким образом, в нашей статье представлены обновленные рекомендации Европейской гематологической ассоциации (EHA) и Европейской сети миеломы (EMN) для повседневной клинической практики по диагностике и лечению больных с впервые диагностированной множественной миеломой, новые прогностические критерии. Приведены результаты рандомизированных клинических исследований, послужившие базой для разработки новых клинических рекомендаций. Рассмотрены также резуль- таты исследований по лечению больных с тлеющей миеломой, в первую очередь с высоким цитогенетическим риском. Однако на сегодняшний день оптимальный подход к пациентам с тлеющей миеломой высокого риска все еще изучается.
Мы считаем , что эти рекомендации являются по лезным ресурсом для врачей , лечащих пациентов с MM. Несмотря на то , что за годы , прошедшие после издания предыдущих клинических рекомендаций , результаты лечения больных улучшились , больные живут с ММ дольше , благодаря внедрению различ ных классов новых лекарственных препаратов , тем не менее у подавляющего большинства больных на блюдается рецидив , зачастую с более агрессивным течением заболевания . Поэтому смена концепции терапии ММ в сторону использования новых под ходов , новых лекарственных препаратов у зна чительной части пациентов является очевидной . Убедительно продемонстрированы преимущества использования квадриплетов над триплетами в первой линии терапии . Адекватное использование новых препаратов будет способствовать более диф ференцированной терапии ММ с учетом как сопут ствующей патологии у пациентов , так и различной токсичности лекарственных средств .


