Новые ультразвуковые технологии в клинической практике
Автор: Карпов Ростислав Сергеевич, Павлюкова Елена Николаевна, Бощенко Алла Александровна, Врублевский Александр Васильевич, Терешенкова Екатерина Константиновна
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: Клинические исследования
Статья в выпуске: 2 т.30, 2015 года.
Бесплатный доступ
В данной статье приводятся результаты использования новых ультразвуковых технологий в клинической практике. Применение технологии “след пятна” (Speckle Tracking Imaging) позволило провести оценку контрактильной функции левого желудочка (ЛЖ), диагностировать ранние субклинические признаки поражения сердца при нормальной систолической и диастолической функции ЛЖ у больных артериальной гипертонией (АГ) без гипертрофии ЛЖ (ГЛЖ). Изучена деформация эндокардиального и эпикардиального слоя ЛЖ в зависимости от формы ГЛЖ и суточного профиля артериального давления (АД). Показана связь показателей механики сердца с суточным профилем АД в зависимости от наличия или отсутствия ГЛЖ. Выявлен феномен ригидной ротации ЛЖ у больных хронической сердечной недостаточностью (ХСН) с узким комплексом QRS. Трансторакальная визуализация магистральных коронарных артерий (КА) является адекватным методом визуализации ствола левой КА (ЛКА), передней нисходящей (ПНА) и правой КА (ПКА). Метод может быть полезен для неинвазивной однократной или серийной диагностики стенозов ствола ЛКА и ПНА, хронических окклюзий ПНА и ПКА. Показана связь величины коронарного резерва (КР) с суточным профилем АД при АГ.
Технология "след пятна" (speckle tracking imaging), механика сердца, деформация левого желудочка, ротация левого желудочка, ригидная ротация левого желудочка, скручивание левого желудочка, ишемическая болезнь сердца, хроническая сердечная недостаточность, артериальная гипертония, гипертрофия левого желудочка, типы постинфарктного ремоделирования левого желудочка, трансторакальная визуализация коронарный артерий, коронарный резерв, суточный профиль артериального давления
Короткий адрес: https://sciup.org/14920024
IDR: 14920024 | УДК: 616.12-008.1-172.7
New ultrasonic technologies in clinical practice
This article presents results of implementation of new ultrasound technologies in clinical practice. The use of speckle tracking imaging allowed for evaluation of contractile function of the left ventricle and diagnosis of early subclinical signs of cardiac injury in the presence of normal systolic and diastolic function of the left ventricle in patients with arterial hypertension without left ventricular hypertrophy (LVH). Deformations of endocardial and epicardial layers of the left ventricle were studied in regard to the form of LVH and 24-hour profile of arterial blood pressure. Associations of indicators of cardiac mechanics with 24-hour arterial blood pressure profile were demonstrated depending on the presence orabsence of LVH. Phenomenon of rigid left ventricular rotation in patients with chronic heart failure with the narrow QRS complex was discovered. Transthoracic imaging of large coronary arteries is an adequate method of visualization of the left main coronary artery, left anterior descending artery, and right coronary artery. The method may be useful for noninvasive one-time and serial diagnosis of stenosis of the left main coronary artery and the left anterior descending artery as well as of chronic occlusions of the left anterior descending artery and the right coronary artery. The study showed relationship between the coronary reserve values and 24-hour arterial blood pressure profile in patients with arterial hypertension.
Текст научной статьи Новые ультразвуковые технологии в клинической практике
Фракция выброса (ФВ) ЛЖ как наиболее часто применяемый показатель систолической функции ЛЖ имеет ограничение, поскольку само измерение подвергается ошибке при очертании границ эндокарда. Кроме того, ФВ ЛЖ в большей степени описывает изменения полости ЛЖ и не всегда является отражением миокардиальной контрактильности. В настоящее время с позиции контрактильности рассматривают деформацию миокарда, ротацию и скручивание ЛЖ [1–3].
Спиральная ориентация миофибрилл ЛЖ является структурной основой вращательного движения ЛЖ, при котором верхушка сердца идет против часовой стрелки, а основание – по часовой стрелке [4–6]. Ротация верхушки по отношению к основанию по часовой стрелке в систолу приводит к скручиванию. Ротационная функция ЛЖ играет важную роль в ФВ и наполнении ЛЖ [7–10], и эта функция более чувствительна к изменениям регионарной и глобальной функции ЛЖ [9, 11–13]. Тем не менее состояние деформационных свойств, ротации ЛЖ в зависимости от типа постинфарктного ремоделирования ЛЖ, а также формы гипертрофии ЛЖ и уровня АД остается недостаточно изученными в отечественной и зарубежной литературе.
До настоящего времени сономикрометрия и магнитно-резонансная томография (МРТ) были единственными методами оценки ротации и поворота по оси ЛЖ [11, 14]. Сономикрометрия является агрессивным методом исследования, может использоваться только в эксперименте у животных, находящихся под анестезией. Использование МРТ в рутинной практике ограничено стоимостью, длительностью исследования, технической сложностью анализа данных.
Новая ультразвуковая технология Speckle Tracking Imaging (2D Strain) позволяет оценить деформацию ЛЖ не только в продольном, радиальном или поперечном направлениях или по окружности, но и дает возможность отдельно определить деформацию эндокардиального, среднего и эпикардиального слоев ЛЖ. Кроме того, эта технология позволяет оценить ротацию (Rotation) базальных, средних и верхушечных сегментов и определить вращение сердца по оси (Torsion) [1, 3].
С другой стороны, хорошо известно, что клинические симптомы и прогноз у больных ишемической болезнью сердца (ИБС) более тесно взаимосвязаны с функциональным состоянием коронарного русла, а не с анатомической выраженностью атеросклеротического поражения. До недавнего времени прямая количественная оценка кровотока в магистральных коронарных артериях (МКА) была возможна только с помощью инвазивных интракоронарных методов диагностики, сопряженных с большими временными и финансовыми затратами, высоким риском осложнений и лучевой нагрузкой на больного. Усовершенствование технологий изображения, в частности, появление новых типов мультичастотных датчиков, современных эхоконтрастных препаратов и технологии второй тканевой гармоники, позволило рассматривать неинвазивные ультразвуковые методы исследования, в частности, трансторакальную эхокардиографию (ТТЭхоКГ), в качестве потенциально пригодных для серийной оценки коронарной гемодинамики. Сообщалось, что успешная визуализация дистальных отделов (д/3) ПНА и спектр коронарного кровотока в сосуде хорошего качества при ТТЭхоКГ могут быть получены в 83–100% случаев, а определение КР как показателя кумулятивной функции артерии может быть выполнено у 76–100% больных. В последние годы по мере накопления визуализа-ционного опыта появились работы об успешной ультразвуковой детекции д/3 ПКА и отдельные сообщения, касающиеся визуализации других сегментов ПНА, ПКА и первых попыток обнаружения огибающей артерии (ОА).
Цель данного сообщения: оценка механики сердца в зависимости от типа постинфарктного ремоделирования ЛЖ, формы ГЛЖ и уровня АД, изучение диагностических возможностей ТТЭхоКГ, выполненной с помощью широкополосных датчиков и технологии второй тканевой гармоники, для оценки структуры и функции МКА у больных с сердечно-сосудистой патологией.
Материал и методы
Анализ механики ЛЖ в зависимости от типа постинфарктного ремоделирования, формы ГЛЖ и уровня АД был выполнен у 137 больных в возрасте от 18 до 75 лет. При этом выделяли пациентов с ишемическим генезом и неишемическим генезом ХСН и функциональным классом (ФК) СН по NYHA III–IV. Всем пациентам была выполнена диагностическая коронарная ангиография (КАГ).
Объектом исследования для ТТЭхоКГ служили 498 человек, из которых 331 были больны ИБС, 132 – АГ и 35 – здоровые добровольцы. В группу пациентов с ИБС включали лиц в возрасте 18–70 лет с болью в левой половине грудной клетке по типу определенной или вероятной стенокардии, или безболевой ишемии миокарда, с регулярным синусовым ритмом, которым на ближайшую неделю было запланировано проведение КАГ.
Группу здоровых добровольцев составили лица в возрасте от 20 до 60 лет, не имеющие заболеваний сердца, в том числе нарушений ритма и проводимости (кроме неполной блокады правой ножки пучка Гиса), факторов риска ИБС, ожирения >I степени и атеросклеротическо- го поражения периферических артерий.
Трансторакальное ультразвуковое исследование МКА и стресс-эхокардиографическое исследование (стресс-ЭхоКГ) с оценкой КР проводили на ультразвуковых диагностических системах Vivid 7 и Vivid 7 Dimension (GE Healthcare, США) с помощью широкополосных секторных матричных датчиков M3S (1,7–3,4 МГц) и M4S (1,5– 4,3 МГц) и режима второй тканевой гармоники без эхоконтрастного усиления сигнала, КАГ – на ангиографических комплексах Coroskop Plus и Cardoskop U (Siemens, Германия).
Двухмерные изображения ЛЖ, зарегистрированные из парастернальной позиции на уровне базальных и верхушечных сегментов в серошкальном изображении при частоте кадров (frame rate) 36 и более в секунду, автоматически “замораживались” в конце систолы. Затем, используя soft-программы (Echopac PC, GE Healthcare), проводилось оконтурирование границ эндокарда, и “автоматически” были получены изогнутый М-режим и кривые ротации каждого из шести сегментов ЛЖ на уровне базальных сегментов и верхушки. По кривым, полученным из парастернальной позиции по короткой оси ЛЖ на уровне базальных сегментов и верхушки, рассчитывали ротацию (Rotation) ЛЖ в конце систолы на базальном (RotMV) и верхушечном уровнях (Rotapex) и скорость ротации (град/с–1) на базальном (RotRMV) и верхушечном уровнях (RotRapex). Поскольку верхушка в систолу движется против часовой стрелки, а базальные сегменты – по часовой стрелке, то кривая ротации верхушки в норме имеет положительное значение, а кривая ротации на базальном уровне в конце систолы – отрицательное значение [15]. Скручивание ЛЖ в конце систолы оценивали по кривой, полученной “автоматически” или количественно: ротация в конце систолы на уровне верхушки минус ротация в конце систолы на уровне базальных сегментов [15]. Поворот по оси ЛЖ рассчитывали количественно по формуле: скручивание ЛЖ / на длинник ЛЖ, оцениваемый из апикальной позиции на уровне 4 камер в конце диастолы.
По кривым, полученным из апикальной позиции на уровне 4 и 2 камер и подлинной оси, рассчитывали глобальную деформацию в продольном направлении (Global Longitudinal Strain/Strain Rate), a по кривым, полученным из парастернальной позиции на уровне ФК митрального клапана, папиллярных мышц и верхушечных сегментов, – глобальную деформацию по окружности (Global Circumferential Strain/Strain Rate).
Результаты и обсуждение
Анализ зависимости типов постинфарктного ремоделирования и ротации ЛЖ на уровне верхушки показал, что аномалия апикальной ротации ЛЖ (движение верхушки по часовой стрелке) зарегистрирована у 47,83% больных с III типом ремоделирования ЛЖ. У пациентов с I и II типом постинфарктного ремоделирования ЛЖ этот феномен выявлен у 8,11 и 16,83% пациентов соответственно [15].
Феномен “ригидной ротации”, т.е. уменьшение скручивания ЛЖ вплоть до его отсутствия, регистрируется у большинства больных ХСН, имевших расширенный комплекс QRS [16–19]. Следует отметить, что феномен “ригидной ротации” ЛЖ был впервые зарегистрирован нами у больных ХСН, имевших узкий комплекс QRS. Не было выявлено различий в частоте регистрации движения верхушки по часовой стрелке между пациентами с ишемическим и неишемическим генезом ХСН [20, 21]. Индексы сферичности и конусности ЛЖ взаимосвязаны с Rotapex у пациентов с перенесенным передним инфарктом миокарда и низкой ФВ ЛЖ, независимо от типа постинфарктного ремоделирования ЛЖ [15]. Было показано, что скорость ротации ЛЖ на уровне базальных сегментов (RotRMV) связана с индексом сферичности (r=0,66; p=0,014) у лиц с ишемическим генезом ХСН.
Скручивание ЛЖ в систолу зависит от направления движения верхушки в систолу, независимо от генеза ХСН, и оно было в большей степени сниженным у пациентов с направлением верхушки в систолу по часовой стрелке. Поворот по оси ЛЖ в систолу был ниже (Zadj=–2,023; p=0,042) у больных с неишемическим генезом ХСН (0,19б±0,082 ° /см vs 0,324±0,259 ° /см). У пациентов с ХСН поворот по оси ЛЖ был взаимосвязан с индексом сферичности ЛЖ (линейный регрессионный анализ: ХСН неишемического генеза – beta 0,971; R=0,970; R2=0,942; F=115,008; df=1,7; p=0,00001; ХСН ишемического генеза – beta 0,846; R=0,845; R2=0,715; F=30,199; df=1,12; p=0,000001). Это является логичным, поскольку значение индекса сферичности ЛЖ взаимосвязано с ориентацией мышечных волокон и величиной угла, который они образуют в спираль [22]. Следовательно, увеличение угла спирали сопровождается увеличением индекса сферичности ЛЖ и уменьшением скручивания [23].
Исследование механики ЛЖ при АГ показало, что при концентрической ГЛЖ снижена глобальная деформация ЛЖ в продольном направлении в систолу, что свидетельствовало о субклинической систолической дисфункции ЛЖ у пациентов с нормальными значениями ФВ ЛЖ. Следует отметить, что у 11 (37,93%) из 29 больных АГ без ГЛЖ было выявлено снижение Global Longitudinal StrainAvg при ненарушенной диастолической функции ЛЖ.
Анализ деформации эндокардиального и эпикардиального слоев ЛЖ в продольном направлении и по окружности у больных с АГ в зависимости от наличия или отсутствия ГЛЖ, формы ГЛЖ показал, что глобальная деформация эндокардиального слоя ЛЖ в продольном направлении и по окружности выше глобальной деформации эпикардиального слоя как у практически здоровых лиц, так и у больных с ГЛЖ, независимо от ее формы, и у пациентов с гипертрофической кардиомиопатией. При концентрической ГЛЖ глобальная деформация эпикардиального слоя по окружности на уровне верхушки коррелирует со скручиванием ЛЖ (r=–0,82; р=0,003) и раскручиванием ЛЖ (r=0,65; р=0,04), а эндокардиального слоя – с раскручиванием ЛЖ (r=0,65; р=0,03). Нами выявлены различия в корреляционных связях показателей суточного профиля АД с деформацией эндокардиального и эпикардиального слоев у больных с АГ без ГЛЖ и концентрической ГЛЖ. Если у пациентов с АГ без ГЛЖ (n=29) деформация эпикардиального слоя по окружности на уровне базальных сегментов и деформация эндо- кардиального слоя ЛЖ по окружности на уровне верхушечных сегментов коррелировали с интегральными показателями систолического АД (r=0,89–0,91), то при концентрической ГЛЖ деформация эндокардиального слоя в продольном направлении коррелировала с интегральными показателями САД и диастолического АД – ДАД (для САД r=0,56–0,61; для ДАД r=–0,56–0,67).
Следует отметить, что Rotapex (r=0,61–0,69), RotRapex (r=0,66–0,82) коррелировали с уровнем ДАД и его интегральными показателями только у пациентов с АГ без ГЛЖ.
Таким образом, использование новой технологии “след пятна” позволяет по-новому взглянуть на механику сердца в зависимости от сердечно-сосудистой патологии. Это дает основание для дальнейшего изучения данного вопроса.
Установлено, что основным принципом исследования МКА при ТТЭхоКГ является не оценка анатомии коронарного русла и характеристик стенки сосудов, а изучение направления и скоростей коронарного кровотока. Частота успешной визуализации в режиме цветного допплеровского картирования и регистрации допплеровского спектра кровотока оказалась высокой для сегментов, имеющих четкую привязку к анатомическим ориентирам, в частности, ствола ЛКА (75% случаев успеха), всех сегментов ПНА (84–93% успеха) и д/3 ПКА, представленной задней межжелудочковой артерией (ЗМЖА; 90% успеха) [24].
У здоровых добровольцев линейные скорости кровотока во всех сегментах МКА были невысокими и в 95% случаев находились в диапазоне от 16 до 42 см/с. Стенозирование МКА приводило к турбулентности кровотока и увеличению систолических и диастолических скоростных параметров кровотока пропорционально выраженности сужения. Мы разработали несколько качественных, полуколичественных и количественных допплерографических критериев диагностики стенозов МКА >50%, чувствительность, специфичность и диагностическая точность которых представлена в таблице 1 [24]. Первыми, простыми в использовании, но наименее чувствительными признаками служили локальное изменение цветовой картограммы потока (alising-феномен) и повышение пиковой диастолической скорости кровотока (Vpd) более 60 см/с. Более корректно выявлять стенозы МКА >50% позволяло сравнение пиковых диастолических скоростей или их интегралов (VTId) в престенотическом и сте-
Таблица 1
Возможности ТТЭхоКГ для диагностики стенозов и хронических окклюзий МКА при условии хорошей визуализации сосудов
|
Критерии |
Ч |
Сп |
ДТ |
|
Стенозы МКА |
|||
|
Аliasing-феномен |
45% |
94% |
87% |
|
Vpd>60 см/с |
52% |
94% |
88% |
|
Vpdв зоне стеноза /Vpdв престенотической зоне >2,0 |
70% |
96% |
93% |
|
(1 – VTId в престенотической зоне / VTId в зоне стеноза) Ч 100% >50% |
77% |
97% |
95% |
|
Хронические коронарные окклюзии |
|||
|
Инверсия кровотока в д/3 ПНА или СВ ПНА как критерий для ПНА |
92% |
98% |
94% |
|
Инверсия кровотока в ЗМЖА или СВ ПКА как критерий для ПКА |
90% |
96% |
94% |
|
Инверсия кровотока в ветви тупого края как критерий для ОА |
75% |
100% |
98% |
Примечание: Ч – чувствительность критерия; Сп – специфичность; ДТ – диагностическая точность.
нотическом участках. Статистический анализ, выполненный для отдельных МКА, показал, что ТТЭхоКГ демонстрирует высокую специфичность при диагностике стенозов всех сосудов, однако ее чувствительность для ОА и ПКА является низкой из-за дефектов визуализации, поэтому метод может быть рекомендован только для скринингового выявления стенозирования ствола ЛКА и ПНА.
Хронические коронарные окклюзии (ХКО) МКА при ТТЭхоКГ сопровождались изменением направления кровотока на ретроградное или ретроантероградное дистальнее поражения. Так, появление инвертированного кровотока в д/3 ПНА и/или септальных ветвях (СВ) ПНА, расцениваемое как эпикардиальное и интрамиокардиальное коллатеральное заполнение, соответственно, служило признаком ХКО ПНА. Инвертированный поток в ЗМЖА и/или СВ ПКА был критерием ХКО ПКА и расценивался как эпикардиальное и интрамиокардиальное коллатеральное заполнение соответственно. Ретроградный кровоток в ветви тупого края (ВТК) служил критерием ХКО ОА. Чувствительность и специфичность разработанных критериев при трансторакальной диагностике ХКО представлены в таблице 1 [25].
Изучение дипиридамол-опосредованного КР в д/3 ПНА было возможно в 94% случаев, в д/3 ПКА (ЗМЖА) – в 88%, в двух артериях одновременно – в 85%, тогда как в д/3 ОА – только в 31% случаев [26].
У здоровых добровольцев среднего возраста уровень КР в ПНА и ПКА составил 3,10±0,98 и 2,92±0,80, в большинстве случаев находясь в диапазоне от 2 до 4. Стенозирование ПНА и ПКА сопровождалось снижением КР дистальнее зоны стеноза, а выраженность снижения зависела от степени стенозирования сосудов. Подтверждением этого была обратная взаимосвязь между максимальным процентом стенозирования сосуда и КР в нем, составившая для ПНА –0,65, для ПКА –0,54. При стресс-ЭхоКГ с дипиридамолом у лиц с неясным генезом боли в груди КР со значением <2,0 был более чувствительным предиктором стенозов ПНА и ПКА>50%, чем появление зон с нарушенной локальной сократимостью – НЛС (86 и 63% соответственно; p<0,001), но несколько менее специфичным (80 и 88% соответственно; p=NS), и диагностическая точность двух методов не имела статистически значимых различий – 80 и 82% для НЛС и КР соответственно. Очень хорошие результаты показало комбинирование двух методик. Дополнение стандартной стресс-ЭхоКГ оценкой КР в ПНА уже повышало чувствительность теста с 63 до 73%, а определение КР в двух артериях (и ПНА, и ПКА) приводило к приросту чувствительности до 91%, сопровождаясь лишь небольшой утратой специфичности. Повышение чувствительности комбинированного теста происходило за счет улучшения диагностики умеренных (50–70%) стенозов и однососудистого поражения, при которых стандартный тест с оценкой НЛС часто был отрицательным.
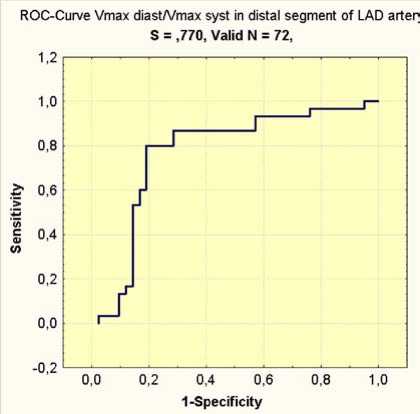
Рис. 2. Кривая ROC-анализа для показателя отношения Vmax diast/Vmax syst <2,0 и >2,0 в дистальном сегменте ПНА
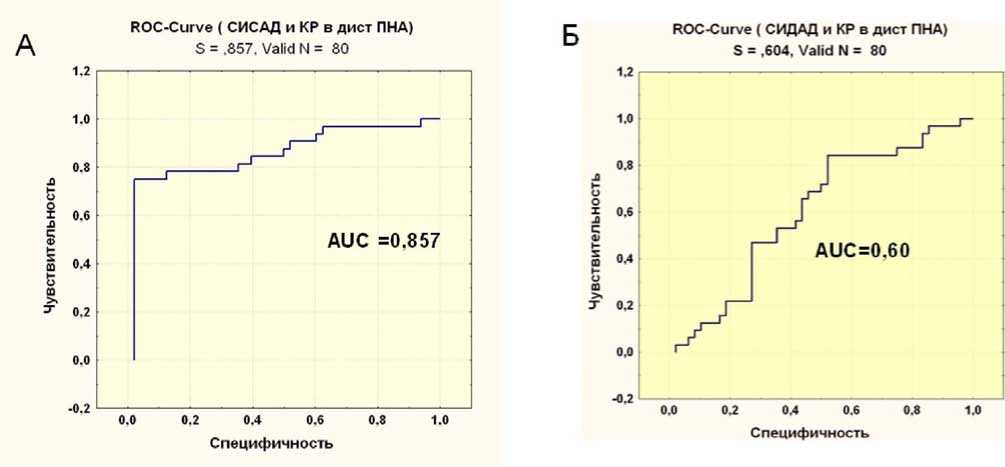
Рис. 1. Roc-кривая значения КР в дистальном сегменте ПНА в зависимости от степени снижения САД (А) и ДАД (Б) в ночное время у больных АГ с концентрической ГЛЖ и ангиографически не измененными коронарными артериями
Анализ взаимосвязей значений КР с суточным профилем АД у больных АГ показал, что только у больных с концентрической ГЛЖ была выявлена взаимосвязь между степенью снижения САД в ночное время и величиной КР в дистальном сегменте ПНА и отсутствие данной связи между КР и степенью снижения ДАД в ночное время. Так, у пациентов, относившихся к подгруппе лиц “nondippers” по САД, у 48 (85,7%) из 56 пациентов значения КР в дистальном сегменте ПНА были менее 2,0, в то время как в подгруппе “dippers” КР менее 2 наблюдался только в одном случае (4,34%) из 23 пациентов. Сравнительный анализ суточного индекса по ДАД показал, что КР менее
2,0 в дистальном сегменте ПНА был зарегистрирован у 23 (71,8%) из 32 пациентов “non-dippers” и у 26 (54,16%) из 48 “dippers”. Полученные данные свидетельствуют о том, что у пациентов с АГ и концентрической ГЛЖ, относящихся к подгруппе “non-dippers” по степени снижения САД, КР снижен. В подтверждение вышесказанного нами был проведен ROC-анализ. Площадь под кривой была равной 0,857 для степени снижения САД в ночное время и 0,60 – для степени снижения ДАД (рис. 1) [27].
Оценка максимальной скорости потока в период диастолы и систолы в дистальном сегменте ПНА у пациентов с ХСН позволила дифференцировать больных ИБС с тяжелой левожелудочковой дисфункцией и пациентов с ХСН неишемического генеза по значению показателя Vmax diast/Vmax syst более 2,0. Чувствительность, специфичность и диагностическая точность составили 83,33; 76,66 и 80,5% соответственно, а точность положительного и отрицательного предсказания отнесения пациента в группу лиц с неишемическим генезом ХСН составила 83,3 и 76,6% соответственно. Площадь под кривой ROC-анализа – 0,77 (рис. 2) [28].
Таким образом, ТТЭхоКГ с использованием широкополосных датчиков и технологии второй тканевой гармоники является адекватным методом визуализации ствола ЛКА, ПНА на всем протяжении и дистальных отделов ПКА. Метод может быть полезен для неинвазивной однократной или серийной диагностики стенозов ствола ЛКА и ПНА, хронических окклюзий ПНА и ПКА, оценки кумулятивной функции ПНА и ПКА на основании исследования КР, а также исследований коронарной артериальной гемодинамики в покое и при нагрузке.
Список литературы Новые ультразвуковые технологии в клинической практике
- Amundsen B.H., Helle-Valle T., Edvardsen T. et al. Noninvasive myocardial strain measurement by speckle tracking echocardiography. Validation against sonomicrometry and tagged magnetic resonance imaging//J. Am. Coll. Cardiol. -2006. -Vol. 47. -P. 789-793
- Geyer H., Caracciolo G., Abe H. et al. Assessment of myocardial mechanics using speckle tracking echocardiography: fundamentals and clinical applications//J. Am. Soc. Echocardiogr. -2010. -Vol. 23. -P. 351-369.
- Leitman M., Lysyansky P., Sidenko S. et al. Two dimension strain -a novel software for real-time quantitative echocardiographic assessement of myocardial function//J. Am. Soc. Echocardiogr. -2004. -Vol. 17. -P. 1021-1029.
- Henson R.E., Song S.K., Pastorek J.S. et al. Left ventricular torsion is equal in mice and human//Am. J. Physiol. Heart Circ. Physiol. -2000. -Vol. 278. -P. H1117-H1123.
- Opdahl A., Helle-Valle T., Remme E.W. et al. Apical rotation by speckle tracking echocardiography: a simplified bedside index of left ventricular twist//J. Am. Soc. Echocardiogr. -2008. -Vol. 21. -P. 1121-1128.
- Torrent-Guasp F., Buckberg G.D., Clemente C. et al. The structure and function of the helical heart and its buttress wrapping. I. The normal macroscopic structure of the heart//Thoracic and Cardiovascular Surgery. -2001. -Vol. 13 (4). -P. 301-319.
- Gibbons Kroeker C.A., Ter Keurs H.E., Knudtson M.L. et al. An optical device to measure the dynamics of apex rotation of the left ventricle//Am. J. Physiol. Heart Circ. Physiol. -1993. -Vol. 265. -P. H1444-H1449.
- McDonald I.G. The shape and movements of the human left ventricle during systole: a study by cineangiography and by cineradiography of epicardial markers//Am. J. Cardiol. -1970. -Vol. 26. -P. 221-230.
- Moon M.R., Ingels N.B. Jr, Daughters G.T. et al. Alterations in left ventricular twist mechanics with inotropic stimulation and volume loading in human subjects//Circulation. -1994. -Vol. 89. -P. 142-150.
- Rademakers F.E., Buchalter M.B., Rogers W.J. et al. Dissociation between left ventricular untwisting and filling: accentuation by catecholamines//Circulation. -1992. -Vol. 85. -P. 15721581.
- Buchalter M.B., Rademakers F.E., Weiss J.L. et al. Rotational deformation of the canine left ventricle measured by magnetic resonance tagging: effects of catecholamines, ischemia, and pacing//Cardiovasc. Res. -1994. -Vol. 28. -P. 629-635.
- Hansen D.E., Daughters G.T., Alderman E.L. et al. Effect of volume loading, pressure loading, and inotropic stimulation on left ventricular torsion in humans//Circulation. -1991. -Vol. 83. -P. 1315-1326.
- Kroeker C.A., Tyberg J.V., Beyar R. Effects of on left ventricular apical rotation: an experimental study in anesthetized dogs//Circulation. -1995. -Vol. 92. -P. 3539-3548.
- Sandstede J.J.W., Johnson T., Harre K. et al. Cardiac systolic rotation and contraction before and after valve replacement for aortic stenosis: a myocardial tagging study using MR imaging//Am.J. Roentgenol. -2002. -Vol. 178. -P. 953-958.
- Карпов Р.С., Павлюкова Е.Н. Глобальная деформация, ротация и скручивание левого желудочка у больных ишемической болезнью сердца с тяжелой левожелудочковой дисфункцией//Центрально-азиатский медицинский журнал. -2012. -№ 1. -С. 19-27.
- Kanzaki H., Nakatani S., Yamada N. et al. Impaired systolic torsion in dilated cardiomyopathy: reversal of apical rotation at midsystole characterized with magnetic resonance tagging method//Basic Res. Cardiol. -2006. -Vol. 101. -P. 465-470.
- Van Dalen B.M., Caliskan K., Soliman O.I.I. et al. Left ventricular solid body rotation in non-compaction cardiomyopathy: a potential new objective and quantitative functional diagnostic criterion?//Eur. J. Heart Failure. -2008. -Vol. 10. -P. 10881093.
- Popescu B.A., Beladan C.C., Calin A. et al. Left Ventricular remodeling and torsional dynamics in dilated cardiomyopathy: reversed apical rotation as a marker of disease severity//Eur. J. Heart Failure. -2009. -Vol. 11. -P. 945-951.
- Russel I.K., Gotte M.J.W. New insights in LV torsion for the selection of cardiac resynchronization therapy candidates//Neth. Heart. -2011. -Vol. 19. -P. 386-391.
- Павлюкова Е.Н., Трубина Е.В., Карпов Р.С. Ротация, скручивание и поворот по оси левого желудочка у больных ишемической и дилатационной кардиомиопатией//Ультразвуковая и функциональная диагностика. -2013. -№ 1. -С. 44-53.
- Павлюкова Е.Н., Карпов Р.С. Деформация, ротация и поворот по оси левого желудочка у больных ишемической болезнью сердца с тяжелой левожелудочковой дисфункцией//Терапевтический архив. -2012. -№ 9. -С. 11-16.
- Taber L.A., Yang M., Podszus W.W. Mechanics of ventricular torsion//J. Biomechanics. -1996. -Vol. 29, No. 6. -Р. 745-752.
- Sengupta P.P., Tajik J., Chandrasekaran K., Khandheria B.K. Twist mechanics of the left ventricle//JACC: Cardiovascular Imaging. -2008. -Vol. 1, No. 3. -Р. 366-376.
- Карпов Р.С., Бощенко А.А., Врублевский А.В. Трансторакальное ультразвуковое исследование магистральных коронарных артерий//Доктор. Ру. -2013. -Т. 80, № 2. -С. 16-25.
- Boshchenko A.A., Vrublevsky A.V., Karpov R.S. Transthoracic echocardiography in the detection of chronic total coronary artery occlusion//Eur. J. Echocardiography. -2009. -Vol. 10, No. 1. -Р. 62-68.
- Бощенко А.А., Врублевский А.В., Карпов Р.С. Роль коронарного резерва в диагностике гемодинамически значимых стенозов передней нисходящей и правой коронарных артерий: трансторакальное ультразвуковое исследование//Кардиология. -2011. -№ 8. -С. 4-14.
- Павлюкова Е.Н., Аксенова А.А., Терешенкова Е.К. и др. Коронарный резерв и суточный профиль артериального давления у больных с артериальной гипертонией//Медицинский алфавит. “Кардиология”. -2014. -№ 2. -С. 38-42.
- Трубина Е.В. Коронарный кровоток, деформация, ротация и скручивание левого желудочка у больных ишемической и дилатационной кардиомиопатиями: автореф. дис.. канд. мед. наук. -Томск, 2012. -27 с.


