Новый объемобразующий препарат для лечения стрессового недержания мочи на основе частиц поли--капролактона
Автор: Исмаилова А.М., Макаров А.В., Туховская Е.А., Белоус Г.И., Аполихина И.А., Саидова А.С., Богородский С.Э., Арутюнян И.В., Ельчанинов А.В., Лохонина А.В., Никитина М.П., Попов В.К., Бичерова И.А., Фатхудинов Т.Х.
Журнал: Экспериментальная и клиническая урология @ecuro
Рубрика: Экспериментальная урология
Статья в выпуске: 1, 2019 года.
Бесплатный доступ
Разработка новых методов и малоинвазивных технологий лечения стрессового недержания мочи у женщин является одной из актуальных проблем современной гинекологии. Перспективным подходом снижения частоты интра- и постоперационных осложнений и обеспечения максимально эффективной реабилитации больных является использование периуретрального введения объемообразующих средств, создающих в области трансплантации дополнительный объем. Предложен объемобразующий препарат на основе мелкодисперсных (характерный размер 100÷200 мкм) частиц поли-ε-капролактона, полученных методом сверхкритической флюидной пластификации с последующим криоизмельчением. На модели стрессового недержания мочи у самок крыс SD проведено сравнение разработанного препарата с уже зарегистрированным в России препаратом SUI Urodex®. Анализ полученных результатов показал, что препарат на основе частиц поли-ε-капролактона обладает высокой эффективностью при лечении недержания мочи. Уродинамический показатель LPP (давление вытекания первой капли мочи) при введении нового объемобразующего препарата на основе частиц поликапролактона сопоставим с таковым для зарегистрированного средства SUI Urodex®...
Стрессовое недержание мочи, объемобразующий препарат, поликапролактон, уродинамическое исследование, экспериментальная модель
Короткий адрес: https://sciup.org/142220503
IDR: 142220503 | DOI: 10.29188/2222-8543-2019-11-1-18-23
New volume-forming drug for the treatment of stress urinary incontinence based on poly--caprolactone particles
The development of new methods and minimally invasive technologies for treating stress urinary incontinence in women is one of the most urgent problems of modern gynecology. The promising approaches is the use of periurethral administration of bulking agents that create additional volume in the field of transplantation and aimed at achieving an equilibrium pressure between the bladder and urethra. Thus bulking agents are capable for reducing the frequency of intra-and post-operative complications, as well as ensuring the most effective rehabilitation of patients. Bulking agent based on polycaprolactone particles obtained by the supercritical fluid method is proposed. This agent was compared with SUI Urodex® in an experimental model of stress urinary incontinence in in female SD rats. The analysis of the results showed that the bulking agent based on polycaprolactone particles has the same high efficiency in the treatment of urinary incontinence. The urodynamic index of LPP of a new bulking agent based on polycaprolactone particles is comparable to that for SUI Urodex®. Bulking agent based on polycaprolactone particles presumably has several advantages: such as a longer therapeutic effect (about 3 years) due to slow biodegradation in the body, lower cost pharmacological market due to production in Russia. Authors declare lack of the possible conflicts of interests.
Текст научной статьи Новый объемобразующий препарат для лечения стрессового недержания мочи на основе частиц поли--капролактона
трессовое недержание мочи (СНМ) у женщин является актуальной проблемой урогинекологии, не угрожающей жизни пациенток, но ощутимо ухудшающей ее качество, зачастую приводя щей к социальной дезадаптации [1,2]. По данным эпидемиологических исследований, распространен- ность недержания мочи у женщин весьма значительна: до 25% молодых женщин, от 44 до 57% женщин в постменопаузе и до 75% женщин старшей возрастной группы испытывают проблемы с удержанием мочи [3]. Патофизиология СНМ сложна: оно может быть связано с анатомическими нарушениями в области уретры (гипермобильность) или на- рушениями функции сфинктера уретры, связанными с потерей эластичности и нарушениями смыкания (недостаточность сфинктера уретры). Несмотря на значительное количество существующих в настоящий момент терапевтических и хирургических методов лечения, постоянно ведутся исследования по их модификации и поиску новых [4-7].
Перспективным хирургическим подходом, способным обеспечить эффективное лечение и снизить частоту интра- и постоперационных осложнений, является введение объемообразующих средств в подслизистый слой уретры [2,8], создающих в области трансплантации дополнительный объем соединительной ткани (дополнительный неконтролируемый сфинктер) и направленных на создание градиентного давления между мочевым пузырем и уретрой [9]. На сегодняшний день существуют десятки разнообразных объемообразующих средств, однако их общим недостатком является короткая продолжительность терапевтического эффекта за счет довольно быстрой биодеградации (около 12 месяцев) и высокая цена на фармакологическом рынке.
В качестве объемообразующих средств в клинике используются био-резорбируемые синтетические материалы на основе полимеров и сополимеров молочной и гликолевой кислот, а также алифатических полиэфиров [10]. Биодеградация этих материалов в организме человека может проходить в течение довольно длительного времени (трех и более лет) и их конечными продуктами являются водорастворимые и нетоксичные продукты нормального метаболизма, которые либо выводятся из организма естественным путем, либо претерпевают дальнейшую цепочку химических превращений вплоть до углекислого газа и воды [11].
Сверхкритическая флюидная (СКФ) обработка алифатических полиэфиров с помощью диоксида углерода позволяет модифицировать структуру как поверхности, так и внутреннего объема полимерного материала с одновременным удалением из него растворимых в сверхкритическом диоксиде углерода (ск-CО2) токсичных компонентов (низкомолекулярные олигомеры, технологические примеси и др.). Это дает возможность формирования более эффективных препаратов для лечения СНМ по сравнению с существующими объемообразующими трансплантатами, как за счет их более продолжительной биодеградации в организме, так и за счет их повышенной биосовместимости.
Рассмотрев различные варианты микроносителей на основе алифатических полиэфиров, нами были выбраны частицы поли-ε-капролактона (ПКЛ), как наиболее подходящие, на наш взгляд, структуры для решения поставленной задачи [12]. В ходе наших предыдущих исследований показано, что они характеризуются оптимальной, морфологией, стабильностью, не обладают цитотоксическим эффектом, а также имеют выраженные адгезивные свойства [13].
Целью данной работы является изучение эффективности нового объемообразующего средства на основе поли-ε-капролактона в сравнении с зарегистрированным препаратом SUI Urodex® на модели стрессового недержания мочи у самок крыс SD.
МАТЕРИАЛЫ и МЕТОДЫ
Получение частиц ПКЛ
В качестве биорезорбируемого полимера для формирования объемообразующих частиц мы использовали низкомолекулярный поли-ε-капролак-тон (“SIGMA-ALDRICH” № 440752, M w ≈14000). Для его СКФ пластификации в наших экспериментах применялся диоксид углерода (ОСЧ, ГОСТ 805085) производства Балашихинского кислородного завода (г. Балашиха, Московская обл.) без какой-либо дополнительной очистки.
Для формирования частиц ПКЛ использовалась оригинальная (разработанная и изготовленная в ФНИЦ

Рис. 1. Микрофотография частиц ПКЛ полученных методом СКФ пластификации с последующим криоизмельчением
"Кристаллография и фотоника" РАН) установка для получения мелкодисперсных полимерных порошков методом СКФ пластификации с последующим криоизмельчением.
На рисунке 1 представлено характерное изображение сканирующей электронной микроскопии частиц ПКЛ со средним размером порядка 100 мкм.
Экспериментальные группы
В эксперименте использовали самок крыс Sprague Dawley 190-220 г. Животные были разделены на три группы: 1 группа – контрольная, получавшая в качестве лечения физиологический раствор, 2 группа (сравнения) – Urodex, получавшая в качестве лечения зарегистрированный имплантант SUI Urodex®, 3 группа – Поликапролактон, получавшая в качестве лечения новое объемобразующее средство Поликапролактон. В каждой группе было по 10 животных.
Моделирование СНМ
В качестве модели СНМ была выбрана методика, основанная на повреждении полового (срамного) нерва (nervus pudendus) с помощью электрокоагулятора [14]. Перед операцией животных наркотизировали смесью Золетил® 100 и Рометар в объеме 200 и 600 мкл/кг, соответственно, путем внутримышечного введения. Далее у этого животного удаляли шерсть в области живота (около 3 см2), смачивали участок кожи и помещали животное на специальную пластину, обеспечивающую увеличение электропроводности при использовании ножа коагулятора. В эксперименте использовался электрохирургический коагулятор «Surtron 120» (производитель LED SpA, Италия). В ходе операции доступ к половому нерву осуществляли с двух сторон, делая надрезы над большой ягодичной мышцей, препарировали ягодичную мышцу до подвздошно-крестцовой ямки, обеспечивая доступ к нервным отросткам, отходящим от седалищного нерва. Затем вводили нож коагулятора в рану на задней поверхности туловища в подвздошно-крестцовую ямку при мощности 50 ЕД, экспериментальная и клиническая урология № 1 2 0 19 коагулировали в течение 3-5 секунд нервные окончания, выходящие из позвоночного столба, среди которых находится и половой нерв.
После выполнения всех хирургических процедур раны ушивали с использованием стерильных саморас-сасывающихся хирургических ниток и вводили антибиотик Байтрил внутримышечно в объеме 0,1 мл.
Измерение уродинамического показателя LPP
Перед моделированием СНМ, через 7 дней (перед введением веществ), через 14 и 28 дней после моделирования СНМ у животных регистрировали LPP (leak point pressure – давление вытекания первой капли мочи) – уродинамический показатель демонстрирующий эффективность работы сфинктера. Этот параметр является объективным показателем наличия СНМ. Регистрация данного параметра осуществлялась с помощью датчика давления (MLT0670, ADInstruments, США), системы регистрации давления PowerLab PL3504 и мостикового усилителя FE224 (ADInstruments, США). Единицами измерения являются мм. рт. ст.
Для процедуры измерения LPP животных предварительно наркотизировали описанным выше способом. Далее выполняли катетеризацию мочевого пузыря через уретру с использованием полиэтиленового катетера РЕ 50. Объем мочевого пузыря измеряли как максимальный объем воды, вводимый в мочевой пузырь, при котором происходила утечка мочи через уретру. Данный показатель необходим для определения объема жидкости, вводимой в мочевой пузырь при измерении LPP, что соответствует половине от полного объема. LPP измеряли следующим образом: в мочевой пузырь вводили половину емкости мочевого пузыря, а затем осторожно надавливали на переднюю брюшную стенку. Регистрировали давление, которое было достигнуто при появлении первой капли мочи в устье уретры. Проводили последовательно 5 измерений LPP.
Введение объемобразующих препаратов в стенку уретры
Через 7 дней после выполнения операции по моделированию СНМ животным проводили введение исследуемых препаратов в стенку уретры. Предварительно животных наркотизировали. Для доступа к уретре осуществляли срединную лапаратомию в нижней трети живота, раздвигали абдоминальные мышцы и жир, вскрывали брюшину. Затем осторожно с помощью пинцета подтягивали мочевой пузырь кверху чтобы получить доступ к верхней трети уретры, тупым способом освобождали среднюю треть уретры. После осуществлялось введение исследуемых веществ (физиологический раствор, SUI Urodex® или Поликапролактон) через иглу G27 в стенку уретры с обеих сторон в 6 точек, т.е. на трех уровнях, в объеме 10-20 мкл на точку.
Перед введением трансплантата их исходные вещества разводили стерильным физиологическим раствором в соотношении 6/1 (300 мкл SUI Urodex® или Поликапролактона разбавляли 50 мкл физраствора).
Вывод животных из эксперимента
Экспериментальные животные подверглись эвтаназии в CO 2 -камере сразу после завершения эксперимента (28 день эксперимента).
Гистологический морфометрический анализ уретры
У всех животных после эвтаназии извлекали уретру и фиксировали в 4% растворе формалина, обезвоживали, затем готовили парафиновые блоки и делали серийные поперечные срезы толщиной 4-6 мкм на 15 уровнях от дистального конца уретры до шейки мочевого пузыря. Анализировали толщину слизистого слоя и просвет уретры, как описано ранее [15]. Препараты окрашивали гематоксилином и эозином. Для обсчета просвета уретры выделяли область препарата, взятую из верхней трети уретры, куда осуществляли введение исследуемых препаратов или физраствора. Эти препараты сканировали при увеличении х35. Обсчет гистологических срезов проводился с помощью программы «Adobe Photoshop CS5». Измерялась площадь просвета уретры инструментом «Magic Wand», а также толщина слизистой оболочки с помощью «Ruler Tool» – выводилось среднее значение из пяти замеров на срезе.
Статистический анализ данных
Для всех количественных данных была применена описательная статистика: считали среднее значение и стандартное отклонение. Для определения достоверности межгрупповых различий данные статистически обрабатывали с использованием программного обеспечения Statistica 7.1. Группы сравнивали между собой в каждой временной точке эксперимента. Применялся непараметрический метод Kruskal Wallis. Различия между группами считали статистически значимыми при p≤0,05.
РЕЗУЛЬТАТЫ
После обработки полученных данных в программном обеспечении Microsoft Office Excel 2007 и Sta-tistica 7.1 были получены следующие результаты.
По результатам оценки показателя LPP было показано, что после выполнения операции по моделированию СНМ давление в мочевом пузыре, необходимое для истечения первой капли мочи из устья уретры, резко снижается. На рисунке 2 представлена гистограмма, на которой
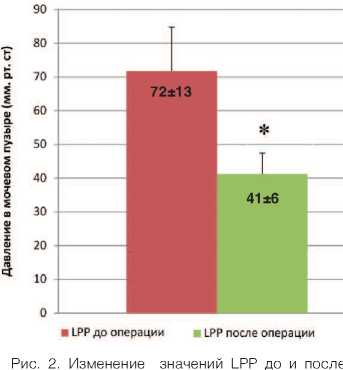
операции
* р ≤0,05 относительно группы «До операции» согласно непараметрическому тесту Kruskal Wallis.
приведены значения LPP (давление в мочевом пузыре), полученные до и после (спустя 7 дней) выполнения двусторонней электрокоагуляции полового нерва (моделирования СНМ).
Спустя 7 дней после введения тестируемых веществ в стенку уретры наблюдалось достоверное повышение значений LPP, как для животных, получавших Поликапролактон, так и для животных, получавших SUI Urodex®. Значения LPP выросли практически до исходных (до операции) и были достоверно выше значений в контрольной группе (рис. 3).
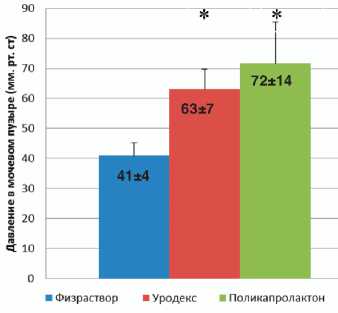
Рис. 3. Значения LPP на 7-й день исследования. * р ≤0,05 относительно группы «Контроль» согласно непараметрическому тесту Kruskal Wallis.
На 14-й день после введения препаратов сохранялись высокие значения LPP при введении обоих препаратов (рис. 4).
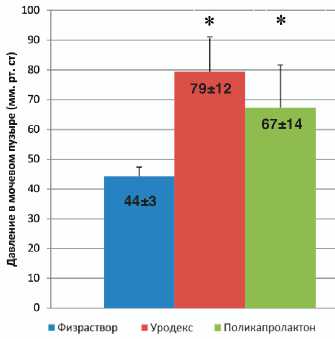
Рис. 4. Значения LPP на 14-й день исследования. * р ≤0,05 относительно группы «Контроль» согласно непараметрическому тесту Kruskal Wallis
На 28-й день после введения препаратов значения LPP для обоих препаратов были на уровне до операции, тогда как в группе, получавшей физраствор, значения оставались на преж- нем послеоперационном уровне (рис. 5).
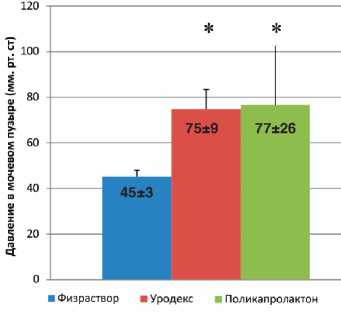
Рис. 5. Значения LPP на 28-ой день исследования. * р ≤0,05 относительно группы «Контроль» согласно непараметрическому тесту Kruskal Wallis
Таким образом, на 14, 21 и 28 день исследования в группах, где вводили Поликароплактон или Уродекс, значения давления в мочевом пузыре, необходимого для истечения первой капли из устья уретры, повышались и на поздних сроках наблюдения возвращались к исходным данным (до выполнения моделирования СНМ), при этом в группе, где вводился только физиологический раствор давление сохранялось на уровне послеоперационного.
На рисунке 6 представлены показательные образцы гистологических препаратов срезов уретры из каждой экспериментальной группы.
ОБСУЖДЕНИЕ
Эффективность в лечении СНМ показали оба исследуемых вещества (SUI Urodex® и Поликапролактон). Уже через неделю после введения исследуемых веществ в стенку уретры наблюдалось достоверное увеличение значений LPP, при этом в группе «Контроль», где вводился только физиологический раствор, давление сохранилось на уровне послеоперационного. Эффект исследуемых препаратов сохранялся до последнего дня эксперимента, о чем свидетельствует достоверное отличие значений LPP в опытных группах от группы «Контроль».
При морфологическом исследовании было показано, что после выполнения двусторонней коагуляции полового нерва происходило увеличение просвета уретры за счет нарушения мышечного тонуса, возникшего вследствие нарушения иннервации. Описанные изменения приводили к постепенной деградации мышечной прослойки стенки уретры. За счет дисфункции мышц сфинктера (вследствие нарушения иннервации) и увеличивался просвет уретры, нарушался нормальный процесс мочеиспускания.
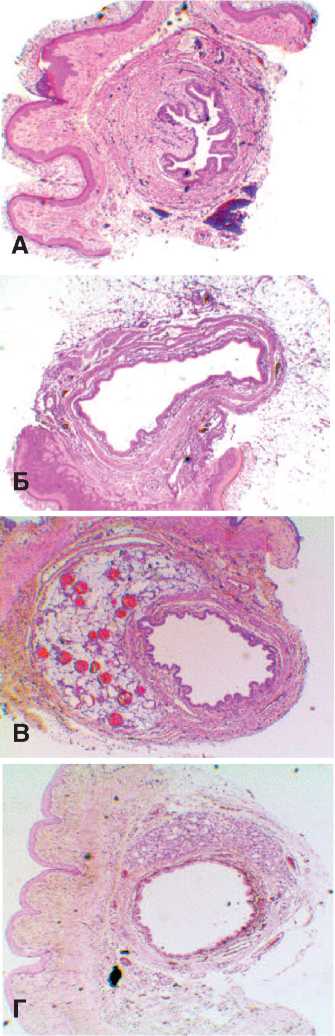
Рис. 6. Гистологические препараты уретры: интактное животное (А); с моделированным недержанием при введении физиологического раствора (Б), при введении SUI Urodex® (В), при введении Поликапролактона (Г). Препараты окрашены гема-токсилин-эозином. Увеличение 3,5Х6.
экспериментальная и клиническая урология № 1 2 0 19
Также было показано наличие частиц трансплантатов Поликапролактона и SUI Urodex® в области введения, однако просвет уретры на гистологических срезах не уменьшался в опытных группах. Введение препарата не приводило к фактическому сужению уретры, однако происходило ее механическое сдавливание частицами объемобразующих препаратов за счет образующейся прокладки между стенками уретры и прилежащими тканями. За счет образования подобного механического «корсета» вокруг уретры восстанавливалась ее барьерная функция и, как следствие, значения уродинамиче-ского показателя LPP восстанавливались до исходных значений (до выполнения моделирования СНМ).
ЗАКЛЮЧЕНИЕ
Проведенный анализ полученных результатов показал, что препарат на основе частиц Поликапролактона обладает высокой эффективностью при лечении недержания мочи, как и препарат сравнения SUI Urodex®. Уродинамический показатель LPP нового объемобразующего препарата на основе частиц полика- пролактона сопоставим с таковым для зарегистрированного средства SUI Urodex®, но при этом предположительно обладает рядом преимуществ: более длительный терапевтический эффект (около 3 лет) за счет медленной биодеградации в организме, более низкая стоимость на фармакологическом рынке за счет производства на территории России [16,17]. Все это указывает на необходимость дальнейшего изучения препарата на основе частиц поликапролактона, как нового эффективного малоинвазивного средства для коррекции стрессового недержания мочи.
Работа выполнена в рамках Государственного Задания по КБК 0908 0130290059 611 на 2018 – 2019 гг. по теме «Создание полностью резорбируемого хирургического протеза для пластики дефектов полостей тела и укрепления мягких тканей».
Список литературы Новый объемобразующий препарат для лечения стрессового недержания мочи на основе частиц поли--капролактона
- Nidhi S, Sudakshina C. Clinical evaluation of urinary incontinence. J Midlife Health 2018; 9(2): 55-64 DOI: 10.4103/jmh.JMH_122_17
- Rautenberg O, Zivanovic I, Kociszewski J, Kuszka A, Münst J, Eisele L, et al. Current treatment concepts for stress urinary incontinence. Praxis (Bern 1994) 2017;106(15):829e-836e. a002843 DOI: 10.1024/1661-8157/
- Button BM, Holland AE, Sherburn MS, Chase J, Wilson JW, Burge AT. Prevalence, impact and specialised treatment of urinary incontinence in women with chronic lung disease. Physiotherapy 2018 pii: S0031-9406(18)30155-X DOI: 10.1016/j.physio.2018.07.006
- Casteleijn FM, Zwolsman SE, Kowalik CR, Roovers JPWR. Patients' perspectives on urethral bulk injection therapy and mid-urethral sling surgery for stress urinary incontinence. Int Urogynecol J 2018;29(9):1249-1257 DOI: 10.1007/s00192-018-3644-0
- Kawaguchi S, Narimoto K, Urata S, Takeyama M, Kadono Y, Mizokami A. Predictors of persistent stress urinary incontinence after transvaginal mesh repair. BMC Womens Health 2018;18(1):174. doi: 10.1186/s12905-018-0667-0.
- Oliveira LM, Dias MM, Martins SB, Haddad JM, Giräo MJBC, Castro RA. Surgical treatment for stress urinary incontinence in women: a systematic review and meta-analysis. Rev Bras Ginecol Obstet 2018;40(8):477-490
- DOI: 10.1055/s-0038-1667184
- Radziminska A, Weber-Rajek M, Str^czynska A, Podhorecka M, Kozakiewicz M, Kçdziora-Kornatowska K, Goch A. The impact of pelvic floor muscle training on the myostatin concentration and severity of urinary incontinence in elderly women with stress urinary incontinence -a pilot study Clin Interv Aging 2018;13:1893-1898
- DOI: 10.2147/CIA.S177730
- Mamut A, Carlson KV. Periurethral bulking agents for female stress urinary incontinence in Canada. Can Urol Assoc J 2017;11(6Suppl2):S152-4
- DOI: 10.5489/cuaj.4612
- Sender H. Current use of injectable agents for female stress urinary incontinence. Rev Urol 2005;7(suppl 1):S12-S21.
- Kotb AF, Campeau L, Corcos J. Urethral bulking agents: techniques and outcomes. Curr Urol Rep. 2009;10(5):396-400.
- Li Y, Chu Z, Li X, Ding X, Guo M, Zhao H, et al. The effect of mechanical loads on the degradation of aliphatic biodegradable polyesters. Regen Biomater 2017;4(3):179-190
- DOI: 10.1093/rb/rbx009
- Арутюнян И.В., Тенчурин Т.Х., Кананыхина Е.Ю., Черников В.П., Васюкова О.А., Ельчанинов А.В., и др. Нетканые материалы на основе поликапролактона для тканевой инженерии: выбор структуры и способа заселения. Гены и клетки 2017;12(1):62-71.
- Фатхудинов Т.Х., Попов В.К., Арутюнян И.В., Богородский С.Э., Кротова Л.И., Макаров А.В., и др. Микрочастицы алифатических полиэфиров, полученные с помощью сверхкритического диоксида углерода, как объемообразующее средство для лечения стрессового недержания. Акушерство и гинекология 2015;(1):85-92.
- Макаров А.В., Фатхудинов Т.Х., Туховская Е.А., Аполихина И.А., Арутюнян И.В., Исмаилова А.М., и др. Экспериментальные модели стрессового недержания мочи. Урология 2015;(4):24-28.
- Lim SH, Wang T, Tseng G, Lee YF, Huang Y, Chen J, Cheng C. The distribution of muscles fibers and their types in the female rat urethra: cytoarchitecture and three-dimensional reconstruction. Anat Rec 2013; 296(10):1640-1649
- DOI: 10.1002/ar.22740
- Sun H, Mei L, Song C, Cui X, Wang P. The in vivo degradation, absorption and excretion of PCL-based implant Biomaterials. 2006;27(9):1735-40.
- Abedalwafa M, Wang F, Wang L, Li C. Biodegradable poly-epsilon-caprolactone (PCL) for tissue engineering applications: a review. Rev Adv Mater Sci 2013;34:123-140


