Новый способ синтеза 1-нафталинсульфоната тетрафенилвисмута
Автор: Рыбакова Анастасия Владимировна
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Химия элементоорганических соединений
Статья в выпуске: 1 т.14, 2022 года.
Бесплатный доступ
Взаимодействием пентафенилвисмута с бис (1 - нафталинсульфонатом) трифенилсурьмы в бензоле синтезирован с выходом 38 % 1 - нафталинсульфонат тетрафенилвисмута, который после перекристаллизации из воды идентифицирован как гидрат Ph4BiOSO2C10H7 × H2O (1). Cтроение 1 (бесцветные кристаллы c т. пл. 178 °С) определено методом рентгеноструктурного анализа (РСА) на автоматическом четырехкружном дифрактометре D8 Quest Bruker (Мо Кα -излучение, λ = 0,71073 Å, графитовый монохроматор) при 293 К. Размер кристалла 0,27 × 0,25 × 0,09 мм, P- 1, a = 9,542(5), b = 12,595(5), c = 13,998(5) Å, a = 74,228(15), β = 80,06(2), g = 68,758(15) град., V = 1503,7(12) Å3, Z = 2. Область сбора данных по 2q 5,72-77,8°, интервалы индексов отражений -16 ≤ h ≤ 16, -22 ≤ k ≤ 22, -24 ≤ l ≤ 24; измерено всего 102981 отражений, 17181 независимых отражений, переменных уточнения 364, μ = 5,968 мм-1; GOOF 0,987, окончательные значения факторов расходимости R 1 = 0,0534 и wR 2 = 0,0941 (по рефлексам F 2> 2s( F 2), R 1 = 0,1619 и wR 2 = 0,1163 (по всем рефлексам), остаточная электронная плотность 2,65/-1,05 e/Å3. Атом висмута в молекуле 1 имеет сильно искаженную тригонально-бипирамидальную координацию с аренсульфонатным заместителем в аксиальном положении. Валентные углы СBiС составляют 100,52(8)-119,28(7)°, расстояния Bi-C и Bi-О равны 2,179(2)-2,212(2) и 2,915(1) Å соответственно. Две молекулы 1 объединены в димеры посредством водородных связей между атомами водорода двух молекул воды и атомами кислорода двух нафталинсульфонатных групп.
Синтез, строение, гидрат 1-нафталинсульфоната тетрафенилвисмута, рентгеноструктурный анализ
Короткий адрес: https://sciup.org/147236621
IDR: 147236621 | УДК: 546.87+546.865+547-305.2+548+548.3+548.312.5 | DOI: 10.14529/chem220104
A new method for the synthesis of tetraphenylbismuth 1-naphthalenesulfonate
The reaction of pentaphenylbismuth with triphenylantimony bis (1-naphthalenesulfonate) in benzene led to tetraphenylbismuth 1-naphthalenesulfonate, yielding 38%, which after recrystallization from water was identified as Ph4BiOSO2C10H7 × H2O hydrate (1). Structure 1 (colorless crystals with mp 178 °C) was determined by X-ray diffraction analysis (XRD) on an automatic four-circle D8 Quest Bruker diffractometer (Мо Кα radiation, λ = 0.71073 Å, graphite monochromator) at 293 K. Crystal size 0.27 × 0.25 × 0.09 mm, P- 1, a = 9.542 (5), b = 12.595 (5), c = 13.998 (5) Å, a = 74.228 (15), β = 80.06 (2), g= 68.758 (15) deg., V = 1503.7 (12) Å3, Z = 2. Data collection area for 2q equaled 5.72-77.8°, reflection index intervals were -16 ≤ h ≤ 16, -22 ≤ k ≤ 22, -24 ≤ l ≤ 24; a total of 102981 reflections were measured, 17181 independent reflections, refinement variables 364, μ = 5.968 mm-1; GOOF 0.987, the final values of the divergence factors R1 = 0.0534 and wR 2 = 0.0941 (for reflexes F2> 2s (F2), R1 = 0.1619 and wR 2 = 0.1163 (for all reflections), residual electron density 2.65 /-1.05 e/Å3. The bismuth atom in molecule 1 has a strongly distorted trigonal-bipyramidal coordination with the arenesulfonate substituent in the axial position. The СBiС bond angles are 100.52 (8) -119.28 (7)°, the Bi-C and Bi-O distances are 2.179 (2) -2.212 (2) and 2.915 (1) Å, respectively. Two molecules 1 are combined into dimers through hydrogen bonds between the hydrogen atoms of two water molecules and the oxygen atoms of two naphthalenesulfonate groups.
Текст научной статьи Новый способ синтеза 1-нафталинсульфоната тетрафенилвисмута
Установлено, что фенильные соединения висмута (III, V) селективно окисляют либо эффективно О- , С- , N - фенилируют различные органические субстраты [1]. С помощью висмуторганических соединений синтезируют многие биологически активные вещества, например аналоги природных алкалоидов, производные индола, 4-гидроксикумарина, хроман-4-она, метилгидрогоната, хининона, гин-гколидов и макролидов. Однако в настоящее время в органический синтез вовлечено крайне ограниченное число производных висмута: трифенилвисмут, пентафенилвисмут, тозилат и трифторацетат тетрафенилвисмута, карбонат, дихлорид, диацетат трифенилвисмута и µ-оксо бис (хлоротрифенил-висмут). Это обусловлено, прежде всего, тем, что ряд известных устойчивых висмуторганических соединений действительно немногочислен. Относительно устойчивыми производными пятивалентного висмута являются аренсульфонаты тетрафенилвисмута, которые получают дефенилированием пентафенилвисмута аренсульфоновыми кислотами либо по реакции перераспределения лигандов из пентафенилвисмута и бис (аренсульфоната) трифенилвисмута [2 - 6]. Следует отметить также метод синтеза аренсульфонатов тетраарилвисмута, основанный на реакции внедрения оксида серы по связи Bi - C в пентаарилвисмуте [7].
В продолжение изучения синтеза аренсульфонатов тетрафенилвисмута в настоящей работе исследовано взаимодействие пентафенилвисмута с бис (1-нафталинсульфонатом) трифенил-сурьмы.
Экспериментальная часть
Синтез пентафенилвисмута осуществляли по методике, описанной в [8].
Бис (1-нафталинсульфонат) трифенилсурьмы. К смеси 0,50 г (1,42 ммоль) трифенилсурьмы, 0,69 г (2,83 ммоль) кристаллогидрата 1-нафталинсульфокислоты в 20 мл этилового эфира добавляли
0,18 г 70%-ного раствора трет -бутилгидропероксида. Реакцию проводили при комнатной температуре в течение 12 ч. После удаления растворителя остаток перекристаллизовывали из толуола. Получили 0,50 г (50 %) бесцветных кристаллов с т. пл. 221 ° С. ИК-спектр, ( v /см-1): 1270 оч. с., 1115 оч. с. (SO 2 ), 1080 с. (SO). Найдено, %: С 58,88; H 3,86. С 38 Н 29 O 6 S 2 Sb. Вычислено, %: С 59,45; H 3,78.
Взаимодействие пентафенилвисмута с бис (1-нафталинсульфонатом) трифенилсурьмы . К раствору 0,44 г (0,57 ммоль) бис (1-нафталинсульфоната) трифенилсурьмы в 60 мл бензола при перемешивании медленно прибавляли при 20 ° С 0,34 г (0,57 ммоль) пентафенилвисмута до исчезновения окраски, характерной для его растворов. После удаления растворителя твердый остаток промывали петролейным эфиром и перекристаллизовывали из воды. Получили 0,16 г (38 %) гидрата 1-нафталинсульфоната тетрафенилвисмута с водой ( 1 ) с т. разл. 113 ° С. Найдено, %: С 54,91; Н 3,90. C 34 H 29 BiO 4 S. Вычислено, %: С 54,65; Н 3,99.
Дифференциальную сканирующую калориметрию проводили с помощью комплекса синхронного термического анализа Netzsch 449C Jupiter, ИК-спектры записывали на ИК-Фурье спектрометре Shimadzu IRAffinity-1S; образцы готовили таблетированием с KBr (область поглощения 4000 - 400 см - 1).
Рентгеноструктурный анализ кристалла соединения 1 проводили на дифрактометре D8 Quest фирмы Bruker (Mo K „ -излучение, X 0,71073 А, графитовый монохроматор) при 293 К. Сбор, редактирование данных и уточнение параметров элементарной ячейки, а также учет поглощения проведены по программам SMART и SAINT- Plus [9]. Все расчеты по определению и уточнению структуры выполнены по программам SHELXL/PC [10] и OLEX2 [11]. Структура определена прямым методом и уточнена методом наименьших квадратов в анизотропном приближении для неводородных атомов. Основные кристаллографические данные и результаты уточнения структуры 1 приведены в табл. 1, основные длины связей и валентные углы - в табл. 2.
Полные таблицы координат атомов, длин связей и валентных углов депонированы в Кембриджском банке структурных данных (№ 2063135 (1); ; .
Обсуждение результатов
Известно, что пентаарилсурьма реагирует с производными сурьмы общей формулы Ar 3 SbX 2 (X – электроноакцепторный заместитель) с образованием производных сурьмы Ar 4 SbX [12–25], однако реакции пентафенилвисмута c фенильными соединениями сурьмы Ph3SbX2 (X = F, Cl, Br, NO3 изучены на немногих примерах [26].
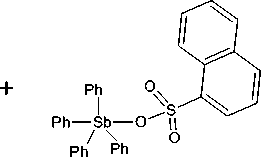
В настоящей работе изучено взаимодействие пентафенилвисмута с бис (1 - нафталинсульфонатом) трифенилсурьмы в бензоле. Бис (1 - нафталинсульфонат) трифенилсурьмы получали из трифенилсурь-мы, 1-нафталинсульфоновой кислоты и трет- бутилгидропероксида по реакции окислительного присоединения.
Ph Sb
+
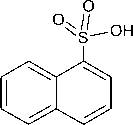
t -BuOOH
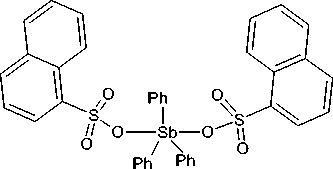
+ t -BuOH + h o
Показано, что при добавлении пентафенилвисмута к раствору бис (1 - нафталинсульфоната) трифенилсурьмы в бензоле пурпурный цвет раствора пентафенилвисмута исчезает и появляется бесцветный осадок, перекристаллизация которого из воды приводит к образованию гидрата 1 - нафталинсульфоната тетрафенилвисмута Ph4BiOSO2C10H7 • H2O ( 1 ), выделенного из реакционной смеси с выходом 38 %.
Химия элементоорганических соединений
p h b i +
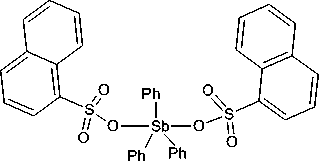
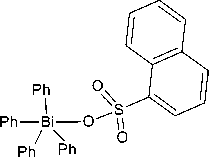
В ИК-спектре гидрата 1 наблюдаются полосы в области валентных колебаний SO2-группы (1182 и 1236 см–1). Полоса очень сильной интенсивности при 1050 см-1 может быть отнесена к колебаниям SO. Известно, что наиболее характерными признаками водородной связи в колебательном спектре считаются низкочастотный сдвиг, увеличение интенсивности и значительное уширение полосы валентных колебаний гидроксильных групп. Действительно, в ИК спектре соединения 1 наблюдается интенсивная полоса при 3559 см–1, которую можно отнести к колебаниям гидроксильной группы молекул воды.
По данным РСА, атом висмута в молекуле 1 имеет сильно искаженную тригонально-бипирамидальную координацию с аренсульфонатным заместителем в аксиальном положении (рис. 1). Аксиальный угол составляет 173,20°, сумма углов в псевдоэкваториальной плоскости равна 347,67°, выход атома висмута из экваториальной плоскости к аксиальному атому углерода составляет 0,451 А. Значения углов ОBiCэкв (71,78-83,74°) меньше 90°, а СаксBiCэкв больше 90° (100,52-103,46°) и приближаются к тетраэдрическому углу. Расстояние Bi-O (2,915 А) значи- тельно превышают сумму ковалентных радиусов атомов висмута и кислорода, что указывает на координационный характер связи. Две молекулы 1 объединены в димер посредством водородных связей между атомами водорода двух молекул воды и атомов кислорода двух нафталинсульфонатных групп.
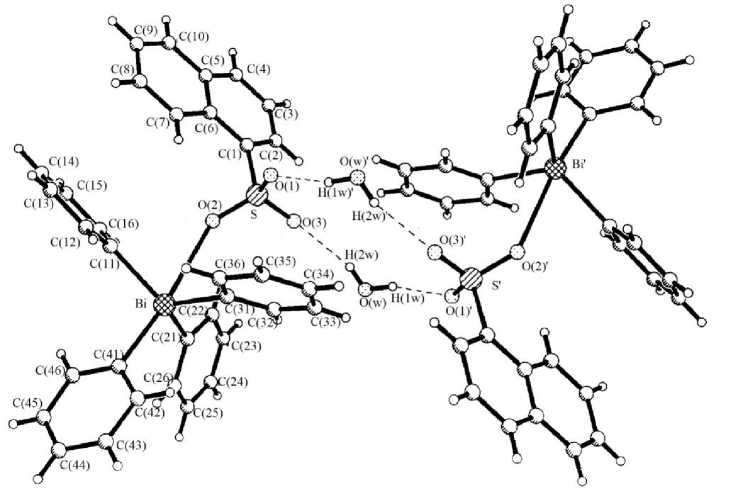
Рис. 1. Строение кристаллогидрата 1-нафталинсульфоната тетрафенилвисмута Ph 4 BiOSO 2 C™H 7 - H 2 O (1)
Таблица 1
Кристаллографические данные, параметры эксперимента и уточнения структуры соединения 1
|
Параметр |
Значение |
|
М |
742,61 |
|
Сингония |
Триклинная |
|
Пр. гр. |
P -1 |
|
a , Å |
9,542(5) |
|
b , Å |
12,595(5) |
|
c, Å |
13,998(5) |
|
α , град. |
74,228(15) |
|
β, град. |
80,06(2) |
|
γ , град. |
68,758(15) |
|
V , Å3 |
1503,7(12) |
|
Z |
2 |
|
ρ (выч.), г/см3 |
1,640 |
|
µ , мм–1 |
5,968 |
|
F (000) |
728,0 |
|
Форма кристалла (размер, мм) |
0,27 × 0,25 × 0,09 |
|
Область сбора данных по 2 θ , град |
5,72 - 77,8 |
|
Интервалы индексов отражений |
–16 ≤ h ≤ 16, –22 ≤ k ≤ 22, –24 ≤ l ≤ 24 |
|
Измерено отражений |
102981 |
|
Независимых отражений |
17181 ( R int = 0,1080) |
|
Число отражений с F 2 > 2 σ ( F 2) |
7955 |
|
Переменных уточнения |
364 |
|
GOOF |
0,987 |
|
R -факторы по F 2 > 2 σ ( F 2) |
R 1 = 0,0534, wR 2 = 0,0941 |
|
R -факторы по всем отражениям |
R 1 = 0,1619, wR 2 = 0,1163 |
|
Остаточная электронная плотность (max/min), e/A3 |
2,65/–1,05 |
Taблица 2
Основные длины связей и валентные углы в структуре 1
|
Связь |
d , Å |
Связь |
d , Å |
||
|
Bi-C(31) |
2,179(2) |
S-O(3) |
1,441(2) |
||
|
Bi-C(11) |
2,194(2) |
S-O(1) |
1,442(2) |
||
|
Bi-C(41) |
2,204(2) |
S-O(2) |
1,450(2) |
||
|
Bi-C(21) |
2,212(2) |
S-C(1) |
1,789(2) |
||
|
Bi-O(2)' |
2,915(1) |
||||
|
Угол |
ω , град. |
Угол |
ω , град. |
||
|
C(31)BiC(11) |
119,28(7) |
O(3)SO(1) |
113,7(1) |
||
|
C(31)BiC(41) |
103,46(8) |
O(3)SO(2) |
112,6(1) |
||
|
C(11)BiC(41) |
101,50(7) |
O(1)SO(2) |
113,7(1) |
||
|
C(31)BiC(21) |
112,12(8) |
O(3)SC(1) |
105,2(1) |
||
|
C(11)BiC(21) |
116,27(7) |
O(1)SC(1) |
105,6(1) |
||
|
C(41)BiC(21) |
100,52(8) |
O(2)SC(1) |
105,1(1) |
||
|
C(31)BiO(2) |
79,55(6) |
C(2)C(1)C(6) |
120,8(2) |
||
|
C(11)BiO(2) |
71,78(5) |
C(21)BiO(2) |
83,74(6) |
||
|
C(41)BiO(2) |
173,20(7) |
C(2)C(1)S |
117,5(2) |
||
|
Водородные связи в структуре |
|||||
|
Связь |
Расстояния, Å |
Угол OНO, град. |
|||
|
O-Н |
Н∙∙∙O |
O∙∙∙O |
|||
|
Ow-H(1w)…O(1) |
0,92(3) |
2,01(3) |
2,904(3) |
165(3) |
|
|
Ow-H(2w)…O(3) |
0,83(3) |
2,04(3) |
2,843(3) |
163(3) |
|
Химия элементоорганических соединений
Выводы
В настоящей работе из пентафенилвисмута и бис (1-нафталинсульфоната) трифенилсурьмы получен с выходом 38 % гидрат 1-нафталинсульфоната тетрафенилвисмута, строение которого доказано методом РСА.
Выражаю благодарность проф. В.В. Шарутину за проведенные рентгеноструктурные исследования.
Список литературы Новый способ синтеза 1-нафталинсульфоната тетрафенилвисмута
- Шарутин, В.В. Синтез, строение и применение арильных соединений висмута / В.В. Шару-тин, Т.В. Мосунова // Вестник ЮУрГУ. Серия «Химия». – 2020. – Т. 12, № 3. – С. 7–66. DOI: 10.14529/chem200301
- Синтез и строение сурьма- и висмуторганических производных 4-сульфофенола и 2,4-дисульфофенола / В.В. Шарутин, И.В. Егорова, А.П. Пакусина и др. // Коорд. химия. – 2007. – Т. 33, № 3. – С. 176–183.
- Синтез и кристаллическая структура гидрата бензолсульфоната и 3,4-диметилбензолсульфоната тетрафенилвисмута / В.В. Шарутин, И.В. Егорова, Т.К. Иваненко и др. // Коорд. химия. – 2003. – Т. 29, № 7. – С. 502–507.
- Синтез и строение 2,4-диметилбензолсульфоната тетрафенилвисмута / В.В. Шарутин, И.В. Егорова, Т.К. Иваненко и др. // Коорд. химия. – 2003. – Т. 29, № 5. – С. 341–345.
- Синтез и строение аренсульфонатов тетрафенилвисмута / В.В. Шарутин, О.К. Шарутина, И.В. Егорова и др. // Журн. общ. химии. – 1999. – Т. 69, вып. 9. – С. 1470–1473.
- Шарутин, В.В. Аренсульфонаты тетра- и триарилвисмута. Синтез и строение / В.В. Шару-тин, О.К. Шарутина, И.В. Егорова и др. // Изв. АН. Серия химическая. – 1999, № 12. – С. 2350–2354.
- Шарутин, В.В. Внедрение оксида серы SO3 по связи Bi-C в пентафенилвисмуте / В.В. Ша-рутин, И.В. Егорова, Т.К. Иваненко // Журн. общ. химии. – 2002. – Т. 72, вып. 1. – С. 162.
- Кочешков, К.А. Методы элементоорганической химии. Сурьма, висмут / К.А. Кочешков, А.П. Сколдинов, Н.Н. Землянский. – М.: Наука, 1976. – 483 с.
- Bruker. SMART and SAINT-Plus. Versions 5.0. Data Collection and Processing Software for the SMART System. Bruker AXS Inc., Madison, Wisconsin, USA, 1998.
- Bruker. SHELXTL/PC. Versions 5.10. An Integrated System for Solving, Refining and Display-ing Crystal Structures from Diffraction Data. Bruker AXS Inc., Madison, Wisconsin, USA, 1998.
- OLEX2: a Complete Structure Solution, Refinement and Analysis Program / O.V. Dolomanov, L.J. Bourhis, R.J. Gildea et al. // J. Appl. Cryst. – 2009. – V. 42. – P. 339–341. DOI: 10.1107/S0021889808042726.
- Способ получения солей тетрафенилстибония общей формулы Ph4SbX [X=Cl, Br, OC(O)Ph, SCN] / В.В. Шарутин, В.С. Сенчурин, О.К. Шарутина и др. // Журн. общ. хим. – 1996. – Т. 66. – Вып. 10. – С. 1755–1756.
- Синтез и строение 2,4-диметилбензолсульфоната тетрафенилсурьмы / В.В. Шарутин, О.К. Шарутина, Т.А. Тарасова и др. // Журн. общ. хим. – 2000. – Т. 70, Вып. 8. – С. 1311–1314.
- Взаимодействие пентафенилсурьмы с диацилатами трифенилвисмута / В.В. Шарутин, О.К. Шарутина, И.В. Егорова и др. // Журн. общ. хим. – 2000. – Т. 70, Вып. 6. – С. 937–939.
- Синтез и строение пентафторбензоата тетрафенилсурьмы и нитрата тетра-п-толилсурьмы / В.В. Шарутин, О.К. Шарутина, Е.А. Бондарь и др. // Коорд. химия. – 2001. – Т. 27, № 6. – С. 423–427.
- Синтез фторбензоатов тетра- и триарилсурьмы / В.В. Шарутин, О.К. Шарутина, Е.А. Бондарь и др. // ЖОХ. – 2002. – Т. 72, вып. 3. – С. 419–420.
- Синтез и строение фторбензоатов тетра- и триарилсурьмы / В.В. Шарутин, О.К. Шарути-на, Е.А. Бондарь и др. // Коорд. химия. – 2002. – Т. 28, № 5. – С. 356–363.
- Синтез и строение 2-фуроината и бензоата тетрафенилсурьмы / В.В. Шарутин, А.П. Па-кусина, Т.П. Платонова и др. // Коорд. химия. – 2002. – Т. 28, № 11. – С. 803–808.
- Сурьмаорганические производные 2,4,6-трибромфенола / В.В. Шарутин, А.П. Пакусина, М.А. Пушилин и др. // ЖОХ. – 2003. – Т. 73, вып. 4. – С. 573–577.
- Синтез и строение 4-метилбензолсульфоната тетра-п-толилсурьмы / В.В. Шарутин, А.П. Пакусина, И.В. Егорова и др. // Коорд. химия. – 2003. – Т. 29, № 5. – С. 336–340.
- Особенности строения дикарбоксилатов триорганилсурьмы R3Sb[OC(O)R’)]2 / В.В. Шарутин, О.К. Шарутина, А.П. Пакусина и др. // Коорд. химия. – 2003. – Т. 29, № 11. – С. 843–851.
- Синтез и строение ниацината тетрафенилсурьмы / В.В. Шарутин, А.П. Пакусина, Т.П. Платонова и др. // ЖОХ. – 2003. – Т. 73, вып. 2. – С. 234–237.
- Синтез и строение дикарбоксилатов триарилсурьмы Ar3Sb[OC(O)R]2 (Ar = Ph, n-Tol; R = 2-C4H3O, 3-C5H4N / В.В. Шарутин, О.К. Шарутина, А.П. Пакусина и др. // Коорд. химия. – 2003. – Т. 29, № 10. – С. 750–759.
- Синтез и строение органосульфонатов тетра- и трифенилсурьмы / В.В. Шарутин, О.К. Шарутина, А.П. Пакусина и др. // Коорд. химия. – 2004. – Т. 30, № 1. – С. 15–24.
- Шарутин, В.В. Синтез, реакции и строение арильных соединений пятивалентной сурьмы / В.В. Шарутин, А.И. Поддельский, О.К. Шарутина // Коорд. химия. – 2020. – Т. 46, № 10. – С. 579-648. DOI: 10.31857/S0132344X20100011
- Реакции пентафенилвисмута и -сурьмы с элементоорганическими соединениями Ph3EX2 (E = Sb, Bi; X = F, Cl, Br, NO3 / В.В. Шарутин, О.К. Шарутина, И.В. Егорова, Л.П. Панова // Журн. общ. химии. – 1998. – Т. 68, вып. 2. – С. 345–346.


