Новый вариант неоадьювантной термохимиолучевой терапии в лечении больных местно-распространенным нерезектабельным раком прямой кишки
Автор: Гордеев С.С., Барсуков Ю.А., Ткачев С.И., Павлова А.М.
Журнал: Московский хирургический журнал @mossj
Рубрика: Клинические исследования
Статья в выпуске: 6 (28), 2012 года.
Бесплатный доступ
В статье представлены результаты проспективного нерандомизированного клинического исследования II фазы, в котором оценивается безопасность и эффективность нового режима терморадиохимиотерапии в лечении больных местно-распространенным нерезектабельным раком прямой кишки (Т4NxM0). В исследование включено 64 пациента, которым проводилась комбинированная химиолучевая терапия СОД 40 Гр с использованием капецитабина, оксалиплатина, локальной гипертермии и метронидазола в составе полимерной композиции. Применение созданной программы лечения позволило выполнить R0 резекцию у 92,2% пациентов, при этом токсичность оставалась на приемлемом уровне (токсичность III-IV степени отмечена у 20,3% пациентов). Общая 2-летняя выживаемость составила 94,3%, безрецидивная - 80,0%. Тридцати пяти пациентам (54.7%) выполнены сфинктеросохраняющие операции, обоснована безопасность сфинктерсохраняющего лечения у данной категории пациентов. Созданный вариант комплексного лечения позволяет повысить число R0 резекций, обладает умеренной токсичностью и требует дальнейшего изучения.
Местно-распространенный рак прямой кишки, нерезектабельный, комплексное лечение, химиолучевая терапия
Короткий адрес: https://sciup.org/142211059
IDR: 142211059 | УДК: 616.351-006.6-085
Текст научной статьи Новый вариант неоадьювантной термохимиолучевой терапии в лечении больных местно-распространенным нерезектабельным раком прямой кишки
Выбор тактики лечения больных нерезектабельным местно-распространенным раком прямой кишки представляет собой одну из нерешенных проблем современной онкологии. Техническая трудность выполнения хирургических вмешательств, часто требующих резекции одного или нескольких смежных органов, у данной группы пациентов часто является причиной отказа в оказании медицинской помощи или ограничения ее паллиативным лечением. Проблема осложняется тем, что такие формы заболевания крайне редко рассматриваются отдельно в исследованиях, и в отношении их лечения отсутствуют какие-либо принятые стандарты или рекомендации.
Сам термин «местно-распространенный рак прямой кишки» не имеет единого определения в медицинской литературе. Некоторые авторы относят к нему любые формы заболевания с наличием поражения параректальных лимфоузлов, другие – только опухоли, распространяющиеся на соседние органы [1, 2]. Резектабельность, или операбельность, по определению является относительным понятием, и его использование в большинстве случаев делает критерии выбора пациентов невоспроизводимыми в различных клинических центрах. Отсутствие единого определения ведет к затруднению анализа доступных данных по эффективности различных лечебных методик.
В ограниченном количестве доступных исследований, где отдельно анализировалась группа пациентов с местнораспространенным неоперабельным раком прямой кишки, методом выбора была предоперационная мелкофракционная лучевая терапия СОД 50–60 Гр с одновременным использованием фторпиримидинов [3, 4, 5, 6, 7, 8]. Также возможно применение режима лучевой терапии с гипофракционированием с эквивалентными суммарными дозами облучения [9]. Данный подход имеет преимущества в виде снижения общего времени лечения, повышения его экономической эффективности, а также увеличения временного промежутка между сеансами облучения для лучшей реоксигенации опухолевых клеток и их перераспределения по фазам клеточного цикла.
Стратегия развития программ комбинированного лечения местно-распространенного рака прямой кишки лежит в поиске путей селективного повышения лучевого повреждения опухоли путем применения различных радиомодифицирующих и хемомодифицирующих агентов.
Изучение эффективности программы полирадиомодификации в лечении локализованного рака прямой кишки показали безопасность и эффективность применения электроноакцепторного соединения метронидазола в составе полимерной композиции для эндоректального применения [10, 11]. Его действие усиливается при совместном использовании с локальной гипертермией. Более того, локальная гипертермия обладает самостоятельным радиомодифицирующим действием, эффективна в отношении радиорези-стентных гипоксических клеток опухоли, хотя до сих пор мало изучалась в клинических исследованиях [12].
Целью данного исследования явилось улучшение результатов лечения больных местно-распространенным неоперабельным раком прямой кишки за счет создания нового варианта комплексного лечения, позволяющего повысить резектабельность опухоли и расширить показания к проведению сфинктеросохраняющих хирургических вмешательств.
Пациенты и методы. Пациенты. В исследование включались пациенты с первично-неоперабельным местнораспространенным раком прямой кишки Т4NxM0. Под неоперабельным местнораспространенным раком мы подразумеваем абсолютно иммобильные опухоли, инфильтрирующие стенки таза, крестец или магистральные сосуды. Другими критериями включения были общий статус по шкале Карновского 80 и выше, отсутствие отдаленных метастазов и метахронных злокачественных новообразований. Всем больным лечение проводилось в отделении проктологии РОНЦ имени Н.Н. Блохина в период с сентября 2007 года по январь 2011 года.
В обязательную программу обследования входило проведение пальцевого ректального исследования, колоноскопии, ирригографии, ТРУЗИ, КТ органов грудной и брюшной полости с внутривенным контрастированием, КТ или МРТ органов малого таза, рентгенографии легких, определения уровней маркеров РЭА и СА 19.9. Все исследования за исключением КТ органов грудной и брюшной полости с внутривенным контрастированием, колоноскопии и рентгенографии легких повторялись перед оперативным вмешательством.
В исследуемую группу были включены 64 пациента в возрасте от 24 до 79 лет (средний возраст – 55,5 лет), среди них 40 (62,5%) мужчин и 24 (37,5%) женщины. Общие данные об исследуемой группе представлены в таблице 1.
Схема лечения. В основу создания программы комплексного лечения (рис. 1) положено усиление канцеро-цидного действия лучевой терапии на фоне аддитивных и синегрических эффектов при использовании разнонаправленных радиосенсибилизаторов: локальной гипертермии,
Таблица 1
Общие данные об исследуемой группе пациентов
|
Характеристика |
Количество |
% |
|
Кол-во пациентов |
64 |
|
|
Пол |
||
|
Муж. |
40 |
62,5 |
|
Жен. |
24 |
37,5 |
|
Средний возраст, лет |
57 (24-79) |
|
|
Морфологическое строение |
||
|
Высокодифференцированная а/к |
9 |
14 |
|
Умереннодифференцированная а/к |
34 |
53,1 |
|
Низкодифференцированная а/к |
5 |
7,8 |
|
Недифференцированная а/к |
1 |
1,6 |
|
Слизеобразующая а/к |
14 |
21,9 |
|
Перстневидноклеточный рак |
1 |
1,6 |
|
Расстояние от переходной складки |
||
|
<3 cм |
3 |
4,7 |
|
3–6 cм |
33 |
51,6 |
|
6,1–9 cм |
23 |
36,1 |
|
9,1–12 cм |
5 |
7,8 |
|
Размер опухоли |
||
|
Средний размер опухоли, cм |
9,5 (4,0–20,0) |
|
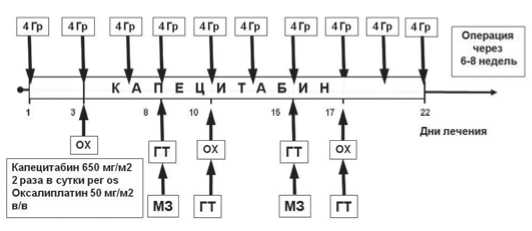
Схема лечения больных местнораспространенным нерезектабель-ным раком прямой кишки (патент РФ № 2414936): Гр – Грей, Ox – оксалиплатин, ГТ – локальная гипертермия, МЗ - метронидазол метронидазола в составе полимерной композиции для локального применения, химиотерапии капецитабином и оксалиплатином.
Лучевая терапия. Дистанционная лучевая терапия проводилась с использованием 3D-планирования на линейных укорителях фотонами энергией 6 мB. Клинический объем облучения включал первичную опухоль и все регионарные лимфатические узлы таза – параректальные, внутренние, наружные и общие подвздошные лимфатические узлы, обтураторные лимфатические узлы. Лучевое воздействие проводилось 3 раза в неделю с РОД 4 Гр до СОД 40 Гр.
Радиомодификаторы. Пациенты получали капеци-табин в дозе 650 мг/м2 2 раза в день per os в течение всего курса лучевой терапии. На 3, 10, 17 дни лечения проводилась внутривенная инфузия оксалиплатина в дозе 50 мг/м2. В качестве премедикации использовался ондансентрон 8 мг внутривенно и дексаметазон 8 мг внутривенно.
Локальная гипертермия выполнялась после достижения суммарной дозы 16 Гр после сеанса лучевой терапии в течение 60 минут при температуре 41–45°С на аппарате «Яхта-4» или «Ягель». Температура в опухоли во время сеанса локальной гипертермии оценивалась при помощи термодатчика, находящегося на верхушке гибкого зонда диаметром 1 мм.
Метронидазол в составе полимерной композиции в концентрации 10 мг/м2 вводился внутриректально во время первого и третьего сеансов локальной гипертермии с экспозицией 5 часов перед сеансом лучевой терапии.
Хирургическое лечение. Хирургическое лечение проводилось через 6–8 недель после окончания курса лучевой терапии. После лапаротомии выполняли ревизию органов брюшной полости. Выбор объема операции оставался за хирургом. Стандартными операциями были чрезбрюшная резекция прямой кишки, брюшно-анальная резекция с низведением сигмовидной кишки и брюшно-промежностная экстирпация. При вовлечении соседних органов и тканей они резецировались «en block» с первичной опухолью.
Статистическая обработка информации проводилась при помощи программы Statistica Software (Statsoft, Tulsa, OK), версии 7.1. Основным критерием оценки эффективности было число R0 резекций, дополнительными - общая и без-рецидивная 2-летняя выживаемость, токсичность по шкале NCI-CTC v.3.0, частота достижения лечебного патоморфоза III-IV степени (по шкале Dworak O./Лавниковой Г.А.), частота выполнения сфинктеросохраняющих операций.
Для демонстрации 20% повышения числа R0-резекций (Н0=70%, Н1=90%) с α=0,05 и β= 80% в исследование необходимо было включить не менее 62 пациентов.
Безрецидивная выживаемость считалась от момента включения в исследование до диагностики рецидива заболевания или смерти пациента. Общая выживаемость считалась от момента включения пациента в исследования до его смерти. Общая и безрецидивная выживаемость анализировались по методу Kaplan–Meier. Для определения достоверности различий в выживаемости использовался «log-rank test». Токсичность лечения определялась от момента начала лечения до дня хирургического лечения.
Результаты
Неоадьювантное лечение. Все кроме 2 пациентов прошли лечение в запланированном объеме. 1 пациентке лечение было прекращено на дозе 16 Гр из-за развития диареи III степени, другому пациенту лечение было прекращено при достижении СОД 32 Гр также из-за развития диареи III степени. Несмотря на это, в последующем обоим пациентам удалось выполнить оперативное вмешательство в объеме R0. Медиана времени до хирургического лечения в исследуемой группе составила 51,4 дня.
Токсичность лечения. Побочные эффекты лечения отмечались у 35 из 64 пациентов (54,7%). Распределение по степеням токсичности было следующее: у 21 (32,8%) пациентов – 1 степени, у 18 (28,1%) – 2 степени, у 12 (18,7%) – III степени, у 1 (1,6%) пациентки – IV степени (рис. 2). Таким образом, только у 13 (20,3%) из 64 пациентов побочные эффекты лечения требовали активного наблюдения и медикаментозной коррекции и только у 1 (1,6%) пациентки потребовали лечения в стационарных условиях и значительной (117 дней) отсрочки хирургического этапа лечения. В структуре осложнений преобладали: диарея – у 22 (34,4%) пациентов, рвота – у 12 (18,9%) пациентов, кожные реакции – у 11 (17,2%) пациентов, цистит – у 10 (15,6%) пациентов, ректит – у 10 (15,6%) пациентов, лейкопения – у 7 (10,9%) пациентов.
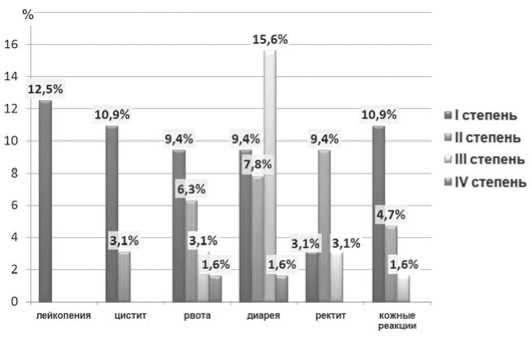
Рис. 2. Побочные эффекты лечения (NCI-CTC v.3.0)
Хирургическое лечение. Интра- и послеоперационные осложнения . 59 (92,2%) пациентам удалось выполнить удаление опухоли. У 5 (7,8%) пациентов операция закончилась эксплоративной лапаротомией из-за врастания опухоли в крестец (у 3 пациентов), в подвздошные сосуды (у 1 пациента), в крестец и мочевой пузырь (у 1 пациента). Тридцати шести пациентам выполнены сфинктеросохраняющие операции, что составило 61% от всех пациентов, которым хирургическое лечение было проведено с удалением опухоли.
Интраоперационные осложнения отмечены у 2 пациентов: у 1 пациента была травма уретры и у 1 пациента вскрыт опухолевый абсцесс в полости малого таза. Различного рода послеоперационные осложнения наблюдались у 19 (29,7%) пациентов. У 9 (14,7%) пациентов осложнения развились после брюшно-промежностной экстирпации прямой кишки: у 3 пациентов отмечено нагноение раны промежности, у 3 пациентов – формирование пузырно-промежностного свища, у 1 пациента – атония мочевого пузыря, у 2 пациентов - цистит. У 10 (15.6%) пациентов осложнения развились после брюшно-анальной резекции прямой кишки: у 2 па- циентов – несостоятельность колоанального анастомоза, у 2 пациентов – формирование пресакральной гематомы, у 2 пациентов – атония мочевого пузыря, у 1 пациента – тромбоз глубокой вены бедра, у 1 пациента – стриктура колоа-нального анастомоза, у 1 пациента – желудочно-кишечное кровотечение (на фоне сопутствующей язвенной болезни желудка), у 1 пациента – инфаркт миокарда.
Патоморфологическое исследование. У всех пациентов, прошедших хирургическое лечение в радикальном объеме, края резекции были без признаков опухолевой инвазии (R0) – 92,2%. У 7 пациентов (10,9%) отмечена полная регрессия опухоли, у 30 (46,9%) – III степень лечебного патоморфоза. У 18 (28,1%) пациентов была 2 степень лечебного патомор-фоза. У 4 (6,2%) пациентов отмечена только 1 степень лечебного патоморфоза (рис. 3). У 5 (7,8%) пациентов лечебный патоморфоз не был оценен, так как опухоль не была удалена во время операции.
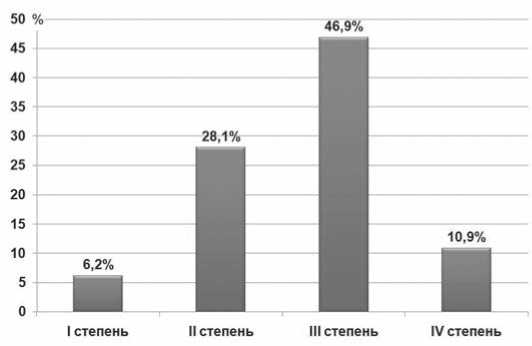
Рис. 3. Лечебный патоморфоз(Dworak O.)
У 14 (21,9%) пациентов было обнаружено поражение регионарных лимфатических узлов, из них у 5 (7,8%) было поражено 3 и более лимфатических узла. Низкая частота выявления метастатического поражения регионарных лимфатических узлов пациентов с такими распространенными формами рака прямой кишки может объясняться большим числом пациентов с III–IV степенью лечебного патоморфоза.
Отдаленные результаты лечения. Медиана наблюдения составила 24,9 месяцев. У 8 (12,5%) пациентов развился локорегионарный рецидив заболевания и у 10 (15,6%) – отдаленные метастазы. У 6 пациентов развились метастазы в печень, у 1 – в печень и легкие, у 1 – только в легкие, у 1 – в забрюшинные лимфатические узлы и у 1 пациента – в кости. Среднее время до развития метастазов варьировало от 7,4 месяцев до 63,9 месяцев (в среднем – 25.8 месяцев). Среди 10 пациентов с метастазами 3 погибли через 5, 7 и 11 месяцев соответственно. Остальные 7 пациентов наблюдаются в течение 4–14 месяцев.
У 7 пациентов рецидив располагался внекишечно и у 1 пациента – в области внутренних подвздошных лимфатических узлов. Время до развития рецидива составило от 5,5 месяцев до 37,6 месяцев (в среднем – 16,1 месяцев). У 5 пациентов одновременно отмечено развитие рецидива и метастазов рака прямой кишки. Среди 7 пациентов с рецидивом рака прямой кишки 4 погибли в сроки от 7 до 11 месяцев после его выявления. Трое пациентов наблюдаются в течение 1, 5 и 13 месяцев соответственно. Общая 2-летняя выживаемость составила 91% (рис. 4), безрецидивная – 83,0% (рис. 5).
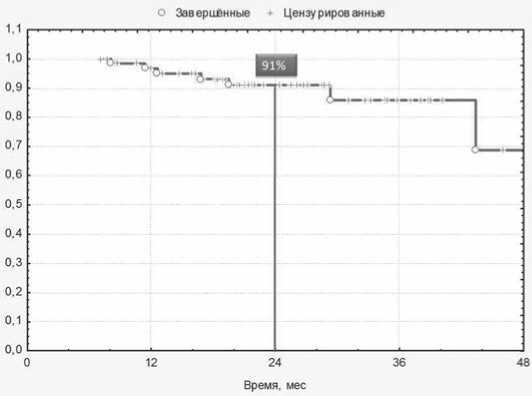
Рис. 4. Общая 2-летняя выживаемость в исследуемой группе (Kaplan-Meier)
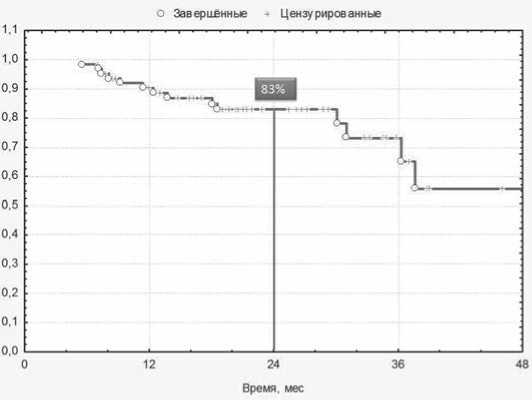
Рис. 5. Безрецидивная 2-летняя выживаемость в исследуемой группе (Kaplan-Meier)
Ни общая (рис. 6), ни безрецидивная (рис. 7) выживаемость достоверно не различались в зависимости от вида хирургического лечения. В группах пациентов, которым были выполнены брюшно-промежностные экстирпации прямой кишки и сфинктеросохраняющие операции, 2-летняя общая выживаемость составила 93,2% и 85,6%, 2-летняя без-рецидивная выживаемость – 88% и 71,9% соответственно. Отмечалась тенденция к лучшим результатам в группе сфинктеросохраняющего лечения.
Обсуждение
Созданная программа неоадьювантной химиолучевой терапии в нашем исследовании продемонстрировала высокую эффективность и умеренную токсичность. По данным лите-
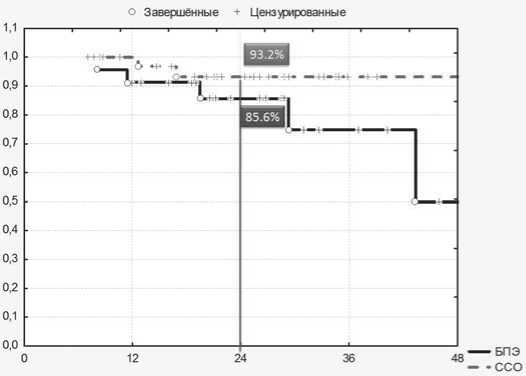
Время, мес
Рис. 6. Общая 2-летняя выживаемость в зависимости от метода хирургического лечения. Log rank test p=0,157
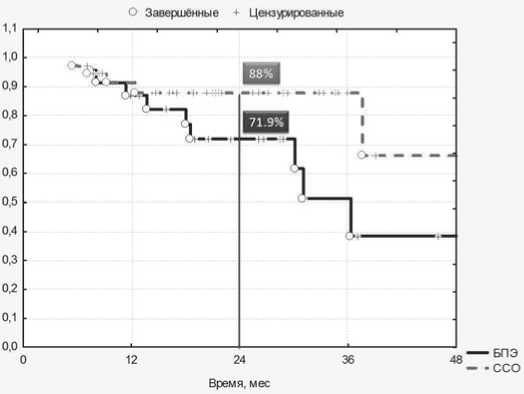
Рис. 7. Безрецидивная 2-летняя выживаемость в зависимости от метода хирургического лечения. Log rank test p=0,064
ратуры, в исследованиях II–III фазы частота R0-резекций в сопоставимых группах пациентов варьировала от 57,7 до 87%, но в большинстве исследований не превышала 70% [3, 4, 5, 6, 7, 8, 13]. Однако терминологические различия и особенности проводимого в различных клиниках хирургического лечения вносят значительный субъективный фактор в результаты этих исследований, и не позволяют проводить непосредственных сравнений. В нашей работе было успешно продемонстрировано 20% повышение числа R0 резекций для местнораспространенного неоперабельного рака прямой кишки относительно 70%, взятых в качестве нулевой гипотезы.
Токсичность является основным фактором, лимитирующим применение современных схем многокомпонентного лечения. В нашем исследовании была показана удовлетворительная переносимость неоадьювантной терморадиохимиотерапии. Ни один пациент не погиб от осложнений проведенного лечения. Суммарная доля токсичности III–IV степени составила 20,3%. По данным литературы, токсичность III–IV степени после проведения химиолучевой терапии больным местно-распространенным раком прямой кишки отмечается в 7,7% [7] – 43% случаев [14], однако в большинстве работ, как и в нашей, этот показатель находится на уровне 20% [3, 4, 5, 6, 13]. Таким образом, несмотря на использование 4 активных радиомодификаторов (капе-цитабин, оксалиплатин, локальная гипертермия, метронидазол), нам удалось сохранить общую переносимость разработанной схемы лечения на приемлемом уровне. Таких результатов удалось добиться за счет тщательного наблюдения пациентов, своевременного назначения сопутствующей терапии при развитии осложнений I–II степени, качественного планирования лучевой терапии. Преимуществом использования гипертермии также является отсутствие побочных эффектов при условии качественного термоконтроля и применения адекватных систем охлаждения.
Частота развития полных регрессий опухоли в нашем исследовании ниже, чем во многих аналогичных работах. В первую очередь это объясняется исходно большими размерами опухолей (средний размер – 9,6 см), а также высоким качеством проводимого морфологического исследования. Различие III и IV степени лечебного патоморфоза по классификации Dworak заключается только в обнаружении единичных жизнеспособных клеток опухоли. Возможность их обнаружения напрямую зависит от количества взятых блоков и тщательности микроскопического исследования. Так, суммарная доля лечебного патоморфоза III–IV степени в нашем исследовании (57,8%) выше, чем в ряде исследований других авторов, в которых была показана большая доля полных регрессий опухоли [15, 16]. В прогностическом плане достижение лечебного патоморфоза как III, так и IV степени является одинаково благоприятным для пациента [17, 18]. Весь курс неоадьювантного лечения с учетом перерыва между окончанием лучевой терапии и операции составлял в среднем 9–12 недель, и ни у одного пациента за это время не отмечено прогрессирования заболевания и роста опухоли. Высокую чувствительность к проводимому лечению мы объясняем использованием многокомпонентной схемы лечения, включающей разнонаправленные радиомодификаторы, влияющие в свою очередь на различные механизмы опухолевой резистентности.
Анализ отдаленных результатов показал, что лишь у 8 (12,5%) пациентов развился рецидив заболевания, несмотря на значительное местное распространение опухолевого процесса. В сравнимых исследованиях данный показатель составляет от 5% до 44% [3, 19], что отражает значительную гетерогенность в группах больных местнораспространенным раком прямой кишки и различное качество хирургического лечения. Проведение сфинктеросохраняющего лечения в нашем исследовании не ухудшало отдаленных результатов, что оправдывает их выполнение у данной тяжелой категории пациентов.
Выводы
Таким образом, представленная схема является безопасной, способствует высокой частоте выполнений хирургических вмешательств в радикальном объеме у больных местно-распространенным раком прямой кишки и требует дальнейшего изучения. Проведение сфинктеросохраняющего лечения у больных местно-распространенным неоперабельным раком прямой кишки безопасно в условиях комбинированного лечения.
Список литературы Новый вариант неоадьювантной термохимиолучевой терапии в лечении больных местно-распространенным нерезектабельным раком прямой кишки
- Capirci C. Rubello D., Pasini F. et al. The role of dual-time combined 18-fluorodeoxyglucose positron emission tomography and computed tomography in the staging and restaging workup of locally advanced rectal cancer, treated with preoperative chemoradiation therapy and radical surgery//Int. J. Radiat. Oncol. Biol. Phys. 2009. Vol. 74, № 5. P. 1461-1469.
- Horisberger K., Treschl A., Mai S. et al. Cetuximab in combination with capecitabine, irinotecan, and radiotherapy for patients with locally advanced rectal cancer: results of a Phase II MARGIT trial//Int. J. Radiat. Oncol. Biol. Phys. 2009. Vol. 74, № 5. P. 1487-1493.
- Braendengen M., Tveit K.M., Berglund A. et al. Randomized phase III study comparing preoperative radiotherapy with chemoradiotherapy in nonresectable rectal cancer//J. Clin. Oncol. 2008. Vol. 26, № 22. P. 3687-3694.
- Bulow S., Jensen L.H., Altaf R. et al. A national cohort study of long-course preoperative radiotherapy in primary fixed rectal cancer in Denmark//Colorectal Dis. 2010. Vol. 12, № 7 Online. P. e18-23.
- Kim N.K., Baik S.H., Seong J.S. et al. Oncologic outcomes after neoadjuvant chemoradiation followed by curative resection with tumor-specific mesorectal excision for fixed locally advanced rectal cancer: Impact of postirradiated pathologic downstaging on local recurrence and survival//Ann. Surg. 2006. Vol. 244, № 6. P. 1024-1030.
- Mathis K.L., Nelson H., Pemberton J.H. et al. Unresectable colorectal cancer can be cured with multimodality therapy//Ann. Surg. 2008. Vol. 248, № 4. P. 592-598.
- Vestermark L.W., Jacobsen A., Qvortrup C. et al. Long-term results of a phase II trial of high-dose radiotherapy (60 Gy) and UFT/lleucovorin in patients with non-resectable locally advanced rectal cancer (LARC)//Act. Oncol. 2008. Vol. 47, № 3. P. 428-433.
- Vestermark L.W., Jensen H.A., Pfeiffer P. High-dose radiotherapy (60 Gy) with oral UFT/folinic acid and escalating doses of oxaliplatin in patients with non-resectable locally advanced rectal cancer (LARC): a phase I trial//Act. Oncol. 2012. Vol. 51, № 3. P. 311-317.
- Koukourakis M.I., Simopoulos C., Pitiakoudis M. et al. Hypofractionated accelerated radiotherapy, cytoprotection and capecitabine in the treatment of rectal cancer: a feasibility study//Anticancer Res. 2008. Vol. 28, № 5B. P. 3035-3040.
- Барсуков Ю.А., Ткачев С.И., Кныш В.И. и др. Комбинированное лечение рака прямой кишки с использованием полирадиомодификации//Вопр. онк. 2008. Т. 54, № 3. P. 350-353.
- Барсуков Ю.А., Ткачев С.И., Кныш В.И. и др. Лечение рака прямой кишки с использованием нескольких радиомодификаторов при предоперационной лучевой терапии//Мед. радиол. 2008. № 2. P. 25-30.
- De Haas-Kock D.F., Buijsen J., Pijls-Johannesma M. et al. Concomitant hyperthermia and radiation therapy for treating locally advanced rectal cancer//Cochrane Database Syst. Rev. 2009. № 3. P. CD006269.
- Levine E.L., Collins S., Susnerwala S. Phase II study of radiotherapy plus concurrent irinotecan (CPT-11) and infusional 5-fluorouracil (5FU) in the treatment of T3-T4 locally advanced inoperable rectal cancer//J. Clin. Oncol. (Meeting Abstracts). 2004. Vol. 22, № 14. P. 3612.
- Chau I., Brown C., Cunningham D.et al. Neoadjuvant capecitabine and oxaliplatin followed by synchronous chemoradiation and total mesorectal excision in magnetic resonance imaging-defined poor-risk rectal cancer//J. Clin. Oncol. 2006. Vol. 24, № 4. P. 668-674.
- Cerard J.P., Chapet O., Nemoz C. et al. Preoperative concurrent chemoradiotherapy in locally advanced rectal cancer with high-dose radiation and oxaliplatin-containing regimen: the Lyon R0-04 phase II trial//J. Clin. Oncol. 2003. Vol. 21, № 6. P. 1119-1124.
- Kim J.S., Cho M.J., Song K.S.et al. Preoperative chemoradiation using oral capecitabine in locally advanced rectal cancer//Int J Radiat Oncol Biol Phys. -2002. -Vol. 54. № 2. -P. 403-8.
- Losi L., Luppi C., Cavioli M. et al. Prognostic value of Dworak grade of regression (GR) in patients with rectal carcinoma treated with preoperative radiochemotherapy//Int. J. Colorectal Dis. 2006. Vol. 21, № 7. P. 645-651.
- Suarez J., Vera R., Balen E. et al. Pathologic response assessed by Mandard grade is a better prognostic factor than down staging for disease-free survival after preoperative radiochemotherapy for advanced rectal cancer//Colorectal Dis. 2008. Vol. 10, № 6. P. 563-568.
- Frykholm C.J., Pahlman L., Climelius B. Combined chemo-and radiotherapy vs. radiotherapy alone in the treatment of primary, nonresectable adenocarcinoma of the rectum//Int. J. Radiat. Oncol. Biol. Phys. 2001. Vol. 50, № 2. P. 427-434.


