О генoтоксичности модифицированных нуклеозидов
Автор: Селезнева Е.С., Белоусова З.П., Макарова Т.В.
Журнал: Известия Самарского научного центра Российской академии наук @izvestiya-ssc
Рубрика: Проблемы прикладной экологии
Статья в выпуске: 2 т.2, 2000 года.
Бесплатный доступ
Анализировали генотоксичность синтезированных модифиц ированных аналогов нуклеозидов: 1-b -D-рибофуранозилбензотриазол(I), 1-b-D-рибофуранозилбензоимидазол(II), 1-b-D-эритрофуранозилбензоимидазол (III). Обнаружили, что все синтезированные соединения индуцируют рецессивные и доминантные летальные мутации у Drosophila melanogaster, ингибируют бласттрансформацию ядер лимфоцитов периферической крови человека и понижают фертильность самок и самцов Drosophila melanogaster. Обсуждается возможность влияния синтезированных соединений на клеточное деление.
Короткий адрес: https://sciup.org/148197611
IDR: 148197611
About genotoxicity of modified nuclosides
It was analysed the genotoxicity of synthetic modified analogs of the nucleosides: 1-b-Dribofuranozilbenzotriazol (I), 1-b-D-ribofuranozilbenzoimidazol (II), 1-b-D-eritrofuranozilbenzoimidazol (III). It was founded that all synthetic compounds induce the recessive and dominant lethal mutations of Drosophila melanogaster, inhibit the blasttransfomation of lymphocyte nucleoses in the periferic human blood, decrease the fertility of females and males of Drosophila melanogaster. The possibility of the influencing of synthetic compounds on the cell division is discussed.
Текст научной статьи О генoтоксичности модифицированных нуклеозидов
-
1 Самарский государственный университет
-
2 Самарский муниципальный университет Наяновой
Анализировали генотоксичность синтезированных модифицированных аналогов нуклеозидов: 1- в -D-рибофуранозилбензотриазол(I), 1- в -В-рибофуранозилбензоимидазол(П), 1- в -D-эритрофурано-зилбензоимидазол (III). Обнаружили, что все синтезированные соединения индуцируют рецессивные и доминантные летальные мутации у Drosophila melanogaster, ингибируют бласттрансформа-цию ядер лимфоцитов периферической крови человека и понижают фертильность самок и самцов Drosophila melanogaster. Обсуждается возможность влияния синтезированных соединений на клеточное деление.
В медицине широко используются модифицированные нуклеозиды как антибактериальные и антивирусные препараты [3,8]. Между тем давно известно, что многие из них проявляют генотоксичность так как представляют собой модифицированные предшественники ДНК. Так 4,6-ами-ноурацил индуцирует хромосомные аберрации у Vicia faba; 8-азагуанин и 8-азатимин являются сильными метастатиками для животных клеток; 5-бромурацил - специфический мутаген для прокариот [9]. Аналоги пурина - кофеин, ксантин, ксантозин индуцируют гетероплоидию [7].
Высокая потребность в новых фармакологических препаратах побуждает синтезировать новые модифицированные нуклеозиды, которые необходимо подвергнуть генетическому мониторингу.
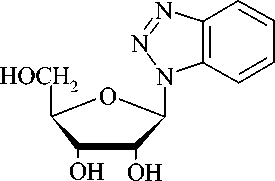
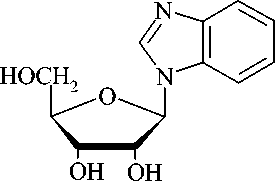
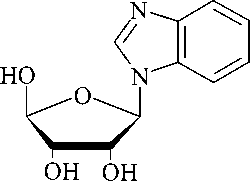
Были синтезированы аналоги нуклеозидов: 1- P -D-рибофуранозилбензотриазол (I), 1 - P -D-рибофуранозилбензоимидазол
(II), 1- P -D-эритрофуранозилбензоимидазол (III), структурные формулы которых приведены на рисунке 1.
Мы предположили, что структурное сходство синтезированных соединений (I,II, III) с природными пуринами послужит причиной появления у них генотоксичных свойств.
Мутагенную активность определяли по способности веществ индуцировать рецессивные и доминантные летальные мутации у дрозофилы [2,4], а также индуцировать хромосомные аберрации в лимфоцитах периферической крови человека [5]. Токсичность веществ определяли по ингибированию бла-сттрансформации лимфоцитов периферической крови человека, стимулированные к клеточному делению ФГА, а также по способности веществ снижать фертильность Drosophila melanogaster.
При анализе мутагенной активности I -III использовали в дозеLD50, которая была
-
(I) (II) (III)
Рис.1. Структурные формулы синтезированных веществ
Таблица 1. Способность веществ индуцировать доминантные летали у имаго Drosophila melanogaster
Для анализа способности I - III индуцировать доминантные летали растворами синтезированных соединений воздействовали либо на самок (900 штук), либо на самцов (900 штук), которых затем скрещивали с интактными особями противоположного пола. Число доминантных летальных мутаций (ДЛМ) оценивали по количеству яиц из которых не вылуплялись личинки. Кладки яиц собирались в течение суток каждые 5 часов.
Результаты эксперимента суммированы в таблице 1.
Статистический анализ с использованием критериев Стьюдента и Фишера показал, что все синтезированные соединения достоверно (для P>99%) индуцируют доминантные летали в опыте по сравнению с контролем. Мы не обнаружили достоверных отличий в действии веществ на самок и самцов, кроме того все веществ индуцировали приблизительно одинаковое количество доминантных летальных мутаций.
Способность I - III вызывать рецессивные летальные мутации в Х-хромосомах самцов Drosophila melanogaster определяли стан дартными методом "Меллер-5". Результатом исследования представлены в таблице 2.
Проведенный статистический анализ не выявил отличий между действием веществ, но показал что все вещества достоверно индуцируют рецессивные летальные мутации у самцов Drosophila melanogaster для P>99%.
Анализ способности веществ индуцировать хромосомные аберрации в лимфоцитах периферической крови человека, показал что в концентрации, не вызывающей гемолиз эритроцитов - 0,001%, соединения не проявляют мутагенный эффект. Было проанализировано 200 препаратов. Ни в одной из проанализированных нами мета-фазных пластинок мы не обнаружили хромосомных перестроек.
Отсутствие мутагенного ответа на уровне клеточной культуры не говорит о специфичности действия данных веществ, так как на уровне целого организма многие вещества, не проявившие мутагенную активность, проходят дополнительную активацию и становятся мутагенами. Ферментативные системы Drosophila melanogaster обладают такими свойствами, и поэтому рекомендованы для генетического мониторинга. Кроме того, они обладают ферментативной активностью, сходной с таковой у микросомальной фракции ферментов печени млекопитающих, где и про-
Таблица 2. Способность аналогов нуклеозидов индуцировать рецессивные летали в Х-хромосомах самцов Drosophila melanogaster
|
Вещества |
Число проанализированных хромосом |
Процент рецессивных леталей |
|
I |
1200 |
3,06 ± 0,99 |
|
II |
1009 |
2,85 ± 0,39 |
|
III |
1100 |
2,87 ± 0,36 |
|
контроль |
1150 |
0,16 ± 0,28 |
Таблица 3. Способность модифицированных нуклеозидов подавлять бласттрансформацию ядер лимфоцитов периферической крови человека
При анализе числа бласттрансформиро-ванных ядер мы обнаружили цитостатический эффект действия исследуемых аналогов нуклеозидов (табл.3). Результаты анализа цитотоксичности представлены в таблице 3.
Все вещества ингибируют бласттрансформацию ядер (различия между опытом и контролем достоверны для P>99%). Разведение в 10 раз не снижает цитотоксического эффекта, кроме того соединения проявляют равное ингибирующее действие.
Так как полученные нами результаты говорят о наличии у I - III генотоксических свойств, то мы предположили, что могут ингибировать и фертильность у тест-объек-та. Для этого 1600 самок и самцов, подвергнутых воздействию токсикантов, скрещивали с интактными особями противоположно-
Изменение количества отложенных яиц при воздействии токсикантами на имаго дрозофилы
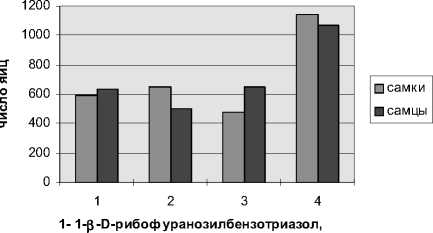
2- 1- в -D-рибофуранозилбензоимидазол,
3- 1— в -D-зритрофуранозилбензоимидазол, 4-контроль
Рис.1. Результаты анализа влияния веществ на фертильность дрозофилы го пола. Каждые 5 часов подсчитывали число отложенных яиц. Мы обнаружили, что у самок и самцов Drosophila melanogaster снижается количество отложенных яиц (рис.1).
Статистический анализ показал, что вещества достоверно снижают фертильность Drosophila melanogaster, причем если I равнотоксичен как для самок, так и для самцов, у которых в равной степени падала фертильность, то II сильнее подавлял фертильность у самцов, а III - у самок (P>95%). Снижение фертильности по нашему мнению является косвенным показателем эмбриотоксичности исследуемых веществ.
Проведенное исследование показало, что все изученные аналоги нуклеозидов обнаружили генотоксичность и это позволяет предположить, что причиной генотоксичности служит нарушение процессов клеточного деления. В пользу этого предположения говорят данные полученные другими авторами [1, 6], показавшими, что аналоги предшественников ДНК нарушают нормальную репликацию и таким образом подавляют или изменяют отдельные стадии клеточного деления.


