Об использовании флоридзина при микроразмножении садовых растений
Автор: Упадышев М.Т., Дроздовский Э.М.
Журнал: Сельскохозяйственная биология @agrobiology
Рубрика: Регуляторы роста растений
Статья в выпуске: 1 т.38, 2003 года.
Бесплатный доступ
Изучали влияние флоридзина на ризогенез микропобегов груши (Pyrus communis L.), рябины (Sorbus aucuparia L.), малины красной (Rubus idaeus L.) ремонтантного типа, ежевики (Rubus sp.), малино-ежевичных гибридов (Rubus sp.) и жимолости съедобной (Lonicera edulis Tursz.).
Короткий адрес: https://sciup.org/142132859
IDR: 142132859 | УДК: 634.1:581.143.6
Micropropagation of garden plants in vitro under the influence of growth regulator floridzine
The effect of floridzine on rhyzogenesis of micropropagule of Pyrus communis L., Sorbus aucuparia L., Rubus idaeus L. of remontant type, Rubus sp., and Lonisera edulis Tursz. was studied. It was shown, that employment of floridzin as separately as together with indolyl butyric acid stimulates the forming of roots in micropropagule of fruit and berry crops. Stimulatory action of floridzin depends on special and varietal peculiarities of plants and also on their ability for taking root.
Текст научной статьи Об использовании флоридзина при микроразмножении садовых растений
Целью настоящей работы было исследование раздельного и совместного действия флоридзина и индолилмасляной кислоты на ризогенез различных ягодных и плодовых культур in vitro.
Методика. В опытах использовали побеги груши ( Pyrus communis L.) сорта Лада, рябины ( Sorbus aucuparia L.) сортов Алая крупная и Титан, малины красной ( Ru-bus idaeus L.) сорта Калашник, ежевики ( Rubus sp.) сортов Торнфри и Смутстем, малино-ежевичных ( Rubus sp.) гибридов сортов Логанберри, Санберри, Краснодарская, жимолости съедобной ( Lonicera edulis Tursz.) сорта МОВИР.
Для культивирования пробирочных растений применяли модифицированную среду Мурасиге и Скуга с добавлением сахарозы (15 г/л), тиамина и никотиновой кислоты (по 0,5 мг/л), агар-агара (7 г/л), рН 5,7-5,8. Микропобеги длиной 20-25 мм укореняли на питательной среде с включением индолилмасляной кислоты (ИМК) в концентрации 0,75 мг/л и флоридзина в концентрациях 1, 10 и 100 мг/л. Испытывали три препарата флоридзина: Ф-1 (фирма «Carlo Erbu», Италия), Ф-2 (Всероссийский селекционно-технологический институт садоводства и питомниководства, Москва) (11) и Ф-3 (фирма «Karl Roth», Германия). Культивирование проводили при освещенности 2000 лк, температуре 23-25 о С и 16-часовом фотопериоде. Повторность каждого варианта опыта 15-кратная. Укореняемость (% от общего числа высаженных побегов), число и длину корней, высоту побега, диаметр каллуса у основания экспланта определяли через 2 и 4 нед после высадки микропобегов. Статистическую обработку данных проводили по Доспехову (12).
Результаты. Внесение в питательную среду флоридзина, как отдельно, так и совместно с ИМК у большинства изученных нами культур существенно стимулировало процесс образования корней. При совместном применении ИМК и флоридзина укоре-няемость трудноукореняемых микропобегов груши возрастала в 2 раза по сравнению с вариантом, в котором использовали только ИМК (рис. а). При этом максимальная укореняемость (40 %) была отмечена при внесении препарата Ф-1 в концентрации 10
мг/л уже через 2 нед культивирования, а Ф-2 — через 4 нед (концентрация 10 и 100 мг/л).
Включение в состав питательной среды для культивирования микропобегов груши флоридзина в концентрации 1 мг/л оказалось малоэффективным. Добавление флоридзина в питательную среду, не содержавшую ИМК, способствовало повышению укореняемости побегов груши на 20 %, стимулировало интенсивный
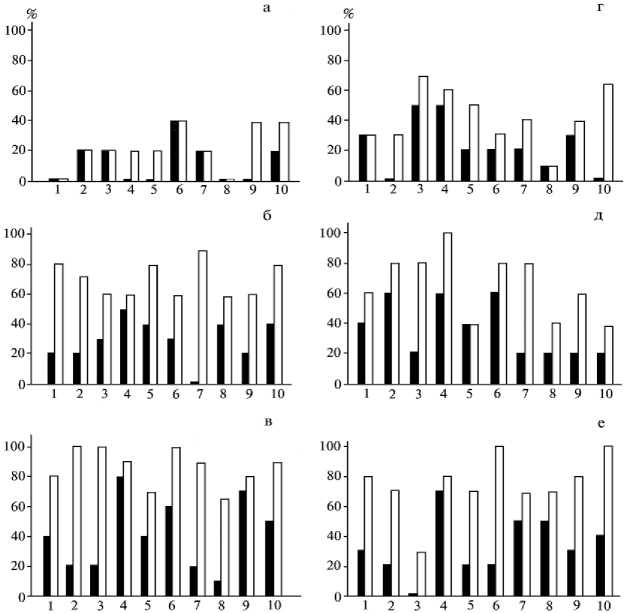
Доля укоренившихся побегов (%) груши сорта Лада (а) , рябины сорта Алая крупная (б) , ежевики сорта Торнфри (в) , малино-ежевичных гибридов сортов Логанберри (г) и Краснодарская (д) , жимолости съедобной сорта МОВИР (е) по вариантам опыта: 1 — контроль (без регуляторов роста); 2 — ИМК (0,75 мг/л); 3 — Ф-1 (10 мг/л); 4 — Ф-2 (10 мг/л); 5 — ИМК + Ф-1 (0,75+1 мг/л); 6 — ИМК + Ф-1 (0,75+10 мг/л); 7 — ИМК + Ф-1 (0,75+100 мг/л); 8 — ИМК + Ф-2 (0,75+1 мг/л); 9 — ИМК + Ф-2 (0,75+10 мг/л); 10 — ИМК + Ф-2 (0,75+100 мг/л); ■ и □ — продолжительность культивирования соответственно 14 и 30 сут.
рост корней в длину, что проявлялось через 1 мес культивирования. Однако число корней в вариантах при внесении в среду культивирования только флоридзина было небольшим (табл. 1). В случае использования флоридзина в концентрации 100 мг/л в смеси с ИМК наблюдалось сильное разрастание каллусных тканей в основании экспланта: диаметр каллуса был в 1,5 раза больше, чем при использовании ИМК. В литературе имеются сведения об аналогичном влиянии флоридзина на рост каллусной ткани яблони in vitro (13). Однако явного торможения процессов дифференциации корней и роста побегов в длину нами не отмечено.
При увеличении концентрации флоридзина питательная среда приобретала светло-зеленоватый оттенок, что, вероятно, обусловлено окислением и разложением флоридзина с образованием родственных ему продуктов и вызвано автоклавированием среды при высоких температурах. Нельзя не учитывать, что продукты окисления флоридзина при культивировании растений in vitro обладают иной, возможно, и более высокой активностью в отношении ризогенеза, чем флоридзин, как это было показано ранее на растениях яблони в питомнике (14).
Микропобеги рябины красной характеризовались сортовой специфичностью на введение в состав питательной среды флоридзина. Так, укореняемость побегов сорта Алая крупная составляла 50 % уже через 2 нед при добавлении в среду препарата Ф-2 в концентрации 10 мг/л, тогда как в контроле число укоренившихся побегов было в 2,5 раза ниже (рис. б). При совместном применении ИМК и Ф-1 по мере увеличения концентрации последнего на начальном этапе культивирования наблюдалось ингибирование ризогенеза. Однако через 1 мес максимальное укоренение (90 %) отмечено при концентрации Ф-1 100 мг/л. Совместное применение Ф-2 (100 мг/л) и ИМК через 1 мес культивирования также обеспечивало высокую укореняемость. Наибольшее число корней формировалось при
-
1. Число корней микропобегов различных плодовых и ягодных культур в зависимости от концентрации флоридзина (Ф) и индолилмасляной кислоты (ИМК) в среде культивирования (шт/раст.)
Сорт
Продолжительность
Вариант опыта
культивирования, сут
Контроль
ИМК,
Ф-1,
Ф-2,
ИМК + Ф-1, мг/л
ИМК + Ф-2, мг/л
0,75 мг/л
10 мг/л
10 мг/л
0,75+1 0,75+10 —1 0,75+100
0,75+1 0,75+10 0,75+100
Г р у ш а
Лада
14
0
0,6*
0,2
0
0 0,8* 0,6*
0 0 0,2
30
0
0,6*
0,2
0,2
0,8* 0,8* 0,6*
0 0,8* 0,6*
Р я б и н а
Алая крупная
14
0,2
0,2
0,8*
1,5*
0,7* 0,5 0
2,0* 0,4 0,6*
30
3,3
2,1
2,0
2,4
1,7 1,8* 2,7
2,6 1,4* 1,8
Титан
14
0
0,2
0
0,3
0,3 1,1* 0,4
0,8* 1,2* 0,6*
30
0,8
1,5*
0,1
0,7
0,5 1,1 0,4
1,2* 1,2* 0,6
Е ж е в и к а
Торнфри
14
0,6
0,6
0,6
1,6
0,4 0,8 0,3
0,1 1,3* 0,8
30
7,0
7,2
4,6
2,9*
4,7 4,0* 3,1*
5,4 7,9 5,6
М
а л и н о - е ж е в и ч н ы й г и б р и д
Логанберри
14
0,6
0
0,5
0,9*
0,5 0,5 0,2
0,2 0,5 0
30
1,3
0,5
3,2*
2,5*
1,4 0,6 1,4
0,3 0,9 0,9
Санберри
14
0,6
0,1*
0,7
0,2
0,1* 0,1* 0,1*
1,1* 0* 0*
30
3,4
1,9
2,5
2,3
0,7* 0,7* 0,9*
1,1* 0,2* 1,8*
Краснодарская
14
0,8
0,8
0,2* 1,8*
0,4*
0,6
0,2*
0,2*
0,4*
0,6
30
1,8
3,4*
1,2 3,0*
0,4*
1,6
3,0*
1,2
0,8*
0,6*
Ж и м о л о с т ь
МОВИР
14
0,4
0,3
0 1,1*
0,7
0,2
1,1*
1,2*
0,6
0,9*
30
2,0
5,6*
0,6* 4,2*
4,5*
8,1*
5,8*
3,7
5,9*
4,3*
-
2. Длина корней микропобегов различных плодовых и ягодных культур в зависимости от концентрации флоридзина (Ф) и индолилмасляной кислоты (ИМК) в среде культивирования (мм)
Сорт
Продолжительность
культивирования, сут
Вариант опыта
Контроль
ИМК,
Ф-1,
Ф-2,
ИМК + Ф-1, мг/л
ИМК + Ф-2, мг/л
0,75 мг/л
10 мг/л
10 мг/л
0,75+1 0,75+10 0,75+100
0,75+1
0,75+10 0,75+100
* Р < 0,05.
П р и м е ч а н и е. Описание вариантов опыта и препаратов см. в разделе «Методика».
00 CD
CD О
Г р у ш а
|
Лада |
14 |
0 |
0,4* |
0,1 |
0 |
0 |
0,6* |
0,6* |
0 |
0 |
0,4* |
|
30 |
0 |
0,4 |
13,0* |
14,0* |
0,8* |
0,6 |
0,6 |
0 |
1,2* |
0,6 |
|
|
Р я б и н а |
|||||||||||
|
Алая крупная |
14 |
0,2 |
0,2 |
1,0* |
3,9* |
1,5* |
0,5 |
0 |
7,1* |
0,2 |
0,3 |
|
30 |
39,9 |
12,2* |
41,4 |
60,0* |
11,2* |
11,5* |
7,4* |
22,0 |
4,0* |
12,8* |
|
|
Титан |
14 |
0 |
0,1 |
0 |
0,1 |
0,2 |
0,6* |
0,2 |
0,3 |
0,5* |
0,2 |
|
30 |
13,0 |
7,6 |
2,7* |
14,5 |
2,0* |
1,9* |
0,8* |
1,0* |
0,6* |
0,2* |
|
|
Е ж е в и к а |
|||||||||||
|
Торнфри |
14 |
3,8 |
0,6* |
3,4 |
5,9* |
1,0* |
2,1 |
0,2* |
0,1* |
3,1 |
1,8* |
|
30 |
65,0 |
48,6 |
45,6 |
23,0* |
25,5* |
24,0* |
14,6* |
18,5* |
41,4 |
23,5* |
|
|
М а л и н о |
- е ж е в и ч н ы й |
г и б р и д |
|||||||||
|
Логанберри |
14 |
1,4 |
0* |
2,3* |
3,7* |
0,4* |
0,3* |
0,4 |
0,1* |
0,5* |
0* |
|
30 |
14,6 |
2,3* |
25,6* |
29,2* |
5,7* |
1,3* |
5,5* |
1,4* |
1,9* |
2,3* |
|
|
Санберри |
14 |
2,7 |
0,6* |
3,4 |
0,9* |
0,1* |
0,1* |
0,2* |
4,2* |
0* |
0* |
|
30 |
36,7 |
13,5* |
29,0 |
19,5 |
4,8* |
3,1* |
5,0* |
4,2* |
2,0* |
8,3* |
|
|
Краснодарская |
14 |
2,6 |
1,0* |
0,4* |
6,8* |
1,4 |
1,6 |
0,2* |
0,2* |
0,6* |
0,2* |
|
30 |
16,8 |
6,2* |
8,2* |
32,6* |
1,4* |
2,4* |
8,2* |
1,0* |
2,8* |
0,4* |
|
|
Ж и м о л о с т ь |
|||||||||||
|
МОВИР |
14 |
1,0 |
0,3* |
0* |
2,0* |
0,3* |
0,3* |
0,8 |
0,8 |
0,3* |
1,2 |
|
30 |
17,8 |
37,5* |
10,8 |
37,8* |
29,9* |
52,3* |
33,6* |
23,7 |
30,3* |
31,3* |
* Р < 0,05.
П р и м е ч а н и е. То же, что в таблице 1.
введении в среду ИМК и Ф-2 (1 мг/л) через 2 нед культивирования, без регуляторов роста — через 4 нед (см. табл. 1). Интенсивному росту корней в длину способствовало культивирование микропобегов в течение 1 мес на среде с препаратом Ф-2, который превосходил ИМК по эффективности почти в 5 раз (табл. 2).
У рябины сорта Титан в отличие от сорта Алая крупная в течение всего периода укоренения положительный результат выявлен при использовании смеси ИМК и Ф-2 (1 мг/л). При увеличении концентрации последнего наблюдалась тенденция к ослаблению ризогенной активности. Наибольшая длина корней отмечена при внесении в среду культивирования препарата Ф-2 в концентрации 10 мг/л.
Введение в питательную среду флоридзина способствовало значительному усилению ризогенеза побегов ежевики на начальном этапе культивирования. Так, уко-реняемость побегов сорта Торнфри через 2 нед после посадки составляла 80 % при использовании препарата Ф-2, что в 2 и 4 раза больше, чем в вариантах соответственно без регуляторов роста и при добавлении ИМК (рис. в). Укореняемость побегов ежевики сорта Смутстем на среде с Ф-3 в течение 2 нед достигала 93 %, тогда как в контроле — 53 %, причем длина корней увеличивалась в 1,7-3,0 раза. Этот факт имеет важное практическое значение, так как появляется возможность высадки пробирочных растений в нестерильные условия всего через 2 нед культивирования (на среде укоренения) против 4-6 нед по общепринятой технологии.
На начальных этапах культивирования ИМК ингибировала корнеобразование побегов ежевики, а затем способствовала их максимальной укореняемости (100 %). Добавление флоридзина в питательную среду, содержавшую ИМК, в первые 14 сут культивирования в большинстве случаев снимало или ослабляло ингибирующее действие кислоты на ризогенез. На побегах ремонтантной малины сорта Калашник высокий эффект, сравнимый с таковым при действии ИМК, был достигнут при использовании препарата Ф-3; Ф-2 оказался менее эффективным. Следовательно, при выборе того или иного препарата необходимо учитывать биологические особенности каждой культуры. Малино-ежевичные гибриды также характеризовались специфической реакцией на воздействие различных регуляторов роста. Так, отмечена положительная реакция побегов гибрида Логанберри на введение в питательную среду флоридзина (независимо от препарата) в течение всего периода укоренения (рис. г). Как и в случае с побегами ежевики, на начальном этапе укоренения при использовании флоридзина в смеси с ИМК ингибирующий эффект последней снижался, чего не наблюдалось у побегов гибрида Санберри, высота которых уменьшалась в 1,5-1,7 раза. Для укоренения побегов этих гибридов оптимальной оказалась среда без регуляторов роста или с одним флоридзином, причем наибольшая высота растений (20,4 против 17,7 мм в контроле) отмечена при использовании препарата Ф-2 в концентрации 10 мг/л.
Характерной особенностью малино-ежевичного гибрида Краснодарская была положительная реакция на внесение в среду ИМК еще на начальном этапе культивирования; добавление флоридзина чаще всего снижало укореняемость (рис. д). Через 1 мес культивирования укореняемость этого гибрида при внесении в среду препарата Ф-2 достигала 100 %, а длина корней была соответственно в 2 и 5 раз больше, чем в вариантах без регуляторов роста и при добавлении ИМК.
Число укоренившихся побегов жимолости при введении в среду препарата Ф-2 (без ИМК) возрастало до 70 % в первые 2 нед после высадки на питательную среду; Ф-1 в этом варианте оказался низкоэффективным (рис. е). Однако при совместном применении флоридзина (Ф-1 и Ф-2) и ИМК через 1 мес культивирования укореняе-мость возрастала до 100 %, причем оптимальная концентрация препарата Ф-1 была на порядок ниже, чем Ф-2.
Итак, для стимуляции ризогенеза in vitro трудноукореняющихся плодовых культур (груша, рябина) целесообразно использовать совместное воздействие на микропобеги ИМК и флоридзина. Добавление препаратов флоридзина в среду культивирования позволило существенно увеличить число укоренившихся побегов и интенсивность развития корневой системы легко- (жимолость) и среднеукореняющихся образцов (ежевика, малино-ежевичные гибриды и др.), причем появилась возможность более ранней (на 2-3 нед) высадки пробирочных растений в нестерильные условия и сокращения периода выращивания посадочного материала. При добавлении ИМК в среду культивирования на начальном этапе укоренения ризогенез ингибировался. При этом флоридзин как отдельно, так и в комплексе с ИМК оказывал положительное влияние на укореняемость побегов и развитие корней и, как правило, уменьшал ингибирующее действие кислоты на ризогенез. Напротив, в случае положительной реак- ции какого-либо сорта (например малино-ежевичный гибрид сорта Краснодарская) на введение ИМК в питательную среду уже на начальном этапе культивирования добавление флоридзина подавляло ризогенез.
Таким образом, флоридзин оказывает существенное влияние на корнеобра-зование in vitro микропобегов плодовых и ягодных культур как при совместном внесении в культуральную среду с индолилмасляной кислотой, так и отдельно. Это важно подчеркнуть, так как ранее полагали, что положительный эффект от применения фенольных соединений может быть достигнут только при совместном использовании с индолилмасляной кислотой или другими ауксинами (7). Стимулирующий эффект флоридзина зависит от видовой и сортовой специфики растений, а также от их принадлежности к группе легко- или трудноукореняемых видов. Кроме того, разные формы флоридзина (Ф-1, Ф-2, Ф-3) оказывают неодинаковое действие на ризогенез, что может быть обусловлено следовыми количествами продуктов окисления и распада этого соединения, образующихся при изготовлении этих препаратов (2). Представляет интерес изучение продуктов превращения флоридзина в культуральной среде в зависимости от объекта и условий культивирования, а также от присутствия ауксинов или других фитогормонов.
Л И Т Е Р А Т У Р А
-
1. К е ф е л и В.И. Природные ингибиторы роста и фитогормоны. М., 1974.
-
2. О с т р е й к о С.А. Физиологически активные соединения и покой плодовых растений. В сб.:
-
3. О с т р е й к о С.А., К о в а л е в а А.Ф., Б а к у н Т.В. и др. О неглю-козидированном фло-ретине и его роли в ростовых процессах у яблони. Мат. симп. «Применение физиологически активных веществ в садоводстве» (19-22 декабря 1972 г.). М., 1972: 111-117.
-
4. J o n e s O.P., H a t f i e l d S.G.S. Root initiation in apple shoots cultured in vitro with auxins and phenolic compounds. J. Hort. Sci., 1976, 51, 4: 495-499.
-
5. З а п р о м е т о в М.Н. Специализированные функции фенольных соединений в растениях. Физиол. раст., 1993, 40, 6: 921-931.
-
6. К у л а е в а О.Н. Восприятие и преобразование гормонального сигнала у растений. Анализ проблемы и введение к публикации материалов Международного симпозиума «Восприятие и трансдукция гормональных сигналов у растений» (Москва, 1994). Физиол. раст., 1995, 42, 5: 661-671.
-
7. Т р у ш е ч к и н В.Г., П о л и к а р п о в а Ф.Я., Я к о в л е в а В.А. О влиянии некоторых фенольных соединений на корнеобразование и прирост зеленых черенков клонового подвоя яблони парадизка краснолистная. В сб.: Плодоводство и ягодоводство Нечерноземной полосы. М., 1975, 8: 181-188.
-
8. W e l a n d e r M. In vitro rooting of the apple rootstock M 26 in adult juvenile growth phases and acclimatization of the plantlets. Physiol. Plant., 1983, 58: 231-238.
-
9. J a m e s D.J., K n i g t h V.H., T h u r b o n I.J. Micropropagation of red raspberry and the influence of phloroglucinol. Scientia Horticulturae, 1980, 12, 4: 313-319.
-
10. B r o o m e O.C., Z i m m e r m a n R.H. In vitro propagation of blackberry. Hort. Sci., 1978, 13, 2: 151-153.
-
11. О с т р е й к о С.А., Д р о з д о в с к и й Э.М. Способ получения флоридзина. А.с. СССР ¹ 1601829, 1990.
-
12. Д о с п е х о в Б.А. Методика полевого опыта. М., 1985.
-
13. О с т р е й к о С.А., П о п о в Ю.Г. Влияние флоридзина и гибберелловой кислоты на рост
каллусной ткани яблони в культуре in vitro. Тез. докл. IV Всес. конф. «Культура клеток растений и биотехнология» (3-6 октября 1983 г.). Кишинев, 1983: 33-34.
-
14. Б а к у н Т.В. Изучение некоторых регуляторов роста в плодовом питомнике. Автореф. канд. дис. М., 1975.
Плодоводство и ягодоводство Нечерноземной полосы. М., 1971, 3: 278-286.
Всероссийский селекционно-технологический институт садоводства и питомниководства, 115598, Москва, М-598, ул. Загорьевская, 4


