Обоснование принципа фотон-захватной терапии злокачественных новообразований
Автор: Шейно И.Н., Ижевский П.В., Липенгольц А.А.
Журнал: Саратовский научно-медицинский журнал @ssmj
Рубрика: Онкология
Статья в выпуске: 4 т.9, 2013 года.
Бесплатный доступ
Цель: исследование физического эффекта локального возрастания дозы в биологической ткани при наличии в ней гадолиний-содержащего препарата под действием рентгеновского излучения. Материал и методы. Экспериментальными и тремя независимыми расчетными методами получены распределения поглощенной дозы в тканеэквивалентном фантоме, содержащем модель опухоли с заданной концентрацией гадолиния. Результаты. Присутствие гадолиний-содержащего препарата в биологической ткани (1 % Gd по массе) приводит к локальному возрастанию поглощенной дозы до двух раз под действием рентгеновского излучения. Различие в результатах, полученных расчетными и экспериментальными методами, не превышает 12%. Заключение. Результаты исследования подтвердили основные теоретические предпосылки фотон-захватной терапии, а также правомерность использования методов расчетного моделирования процесса формирования дозы в биологической ткани, необходимых для дозиметрического планирования фотон-захватной терапии
Рентгеновское излучение, фантомные исследования, фотон-захватная терапия
Короткий адрес: https://sciup.org/14917866
IDR: 14917866
Текст научной статьи Обоснование принципа фотон-захватной терапии злокачественных новообразований
Ц Введение. Термин «фотон-захватная терапия» (ФЗТ) предложен В. Ф. Хохловым [1] по аналогии с процессами, протекающими при нейтрон-захватной терапии. Физический принцип ФЗТ основан на увеличении локального энерговыделения в биологической ткани, при наличии в ней специальных препаратов, содержащих «тяжелые» элементы (с большим атом-
Адрес: 123182, г. Москва, ул. Живописная, д. 46.
Тел.: 8-903-618-00-54
ным номером Z), при облучении фотонами рентгеновского спектра [2].
Выделение энергии обусловлено электронами фотопоглощения и сопутствующего Оже-каскада на атомах элементов с большим Z, входящих в состав известных препаратов, содержащих: йод (53I): Йодопомидол , Йод-дезоксиуридин ; гадолиний (64Gd): Магневист , Приновист , Ультравист , Дипентаст и др. ; платину (78Pt): Цисплатин , Карбоплатини и др., а также перспективных препаратов, содержащих наночастицы золота (79Au).
Как ожидается, при достижении оптимального соотношения концентраций препарата, содержащего указанные элементы, в опухоли и в нормальной ткани и при облучении фотонами оптимального спектра возможно создать в облучаемой мишени дозу, губительную для опухоли и в то же время толерантную для нормальных тканей.
К достоинствам фотон-захватной терапии, в сравнении с традиционными методами лучевой терапии, относится то, что подведение необходимой терапевтической дозы к биологической мишени (опухоли) осуществляется созданием определенной концентрации препарата, а не нацеливанием и фокусировкой пучка излучений.
Важным элементом лучевой терапии является дозиметрическое планирование. В случае ФЗТ расчетные методы оценки формирования дозового поля излучения в биологической ткани определяются количественным описанием двух процессов: динамикой распространения в биологической ткани введенного препарата и формированием поля излучений и последующего энерговыделения в ткани с учетом изменения концентрации препарата.
Цель работы: исследование физического эффекта локального возрастания дозы в биологической ткани при наличии в ней гадолиний-содержащего препарата под действием рентгеновского излучения. Расчетными и экспериментальными методами получены распределения поглощенной дозы в тканеэквивалентном фантоме, содержащем модель опухоли с заданной концентрацией гадолиния, которые подтвердили основные теоретические принципы фотон- захватной терапии. Результатами установлена правомерность использования современных методов расчетного моделирования процесса формирования дозы в биологической ткани, необходимых для дозиметрического планирования ФЗТ.
Материал и методы. Для сравнительной количественной оценки физического эффекта локального возрастания дозы в ткани при наличии в ней гадолиний-содержащего препарата под действием рентгеновского излучения произведены расчетные исследования дозовых распределений в фантоме из тканеэквивалентного материала, содержащем модель опухоли (рис. 1). Для расчета распределения дозы по фантому использованы программы: 1) MCNP5 [3] (США) и EGSnrc [4] (Канада), реализующие метод Монте-Карло; 2) RADUGA [5] (ИПМ РАН, Россия), использующая метод дискретных ординат для решения переноса излучений.
Энергетическое распределение потока фотонов соответствовало модельному представлению спектра [6] острофокусной рентгеновской трубки прострельного типа при анодном напряжении 150 кВ и токе 120 мкА, использованной в установке РАП-150М
Для сравнения результатов расчета с экспериментальными данными проведены измерения поглощенной дозы в водном фантоме при облучении его на установке РАП-150М (анодное напряжение 150 кВ и токе 0,1 мА). Водный фантом представляет собой полиэтиленовый цилиндрический контейнер диаметром 13 см и высотой 6 см, наполненный водой на 4 см. В него была помещена конструкция из вставленных друг в друга поликарбонатных контейнеров диаметром 15 мм и высотой 5 мм, наполненных дистиллированной водой. Два контейнера в центре сборки были наполнены водным раствором препарата Маг-невист ™ с содержанием гадолиния 13 мг/мл. Определение поглощенной дозы производилось с помощью дозиметрических пленок Gafchromic HD-810 производства ISP Corporation (США), помещенных на дно каждого поликарбонатного контейнера. Схема проведения эксперимента приведена на рис. 2.
Результаты. Для расчетных фантомов (рис. 1) с помощью программам EGSnrc, MCNP5 и RADUGA
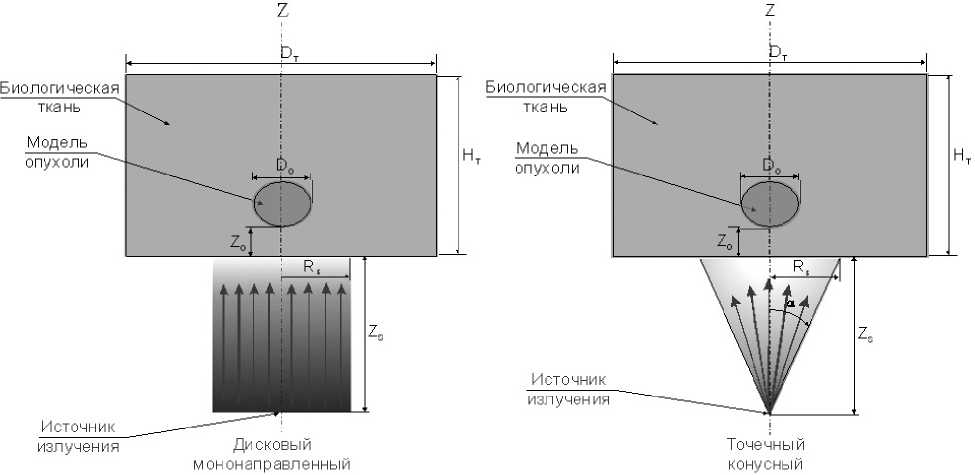
Рис. 1. Расчетные фантомы с моделью опухоли при облучении параллельным (а) и конусным (б) источниками фотонов: DO=1 см, HT=6 см, DT=10 см, RS=1,73 см, Z0=3 см, α=30°
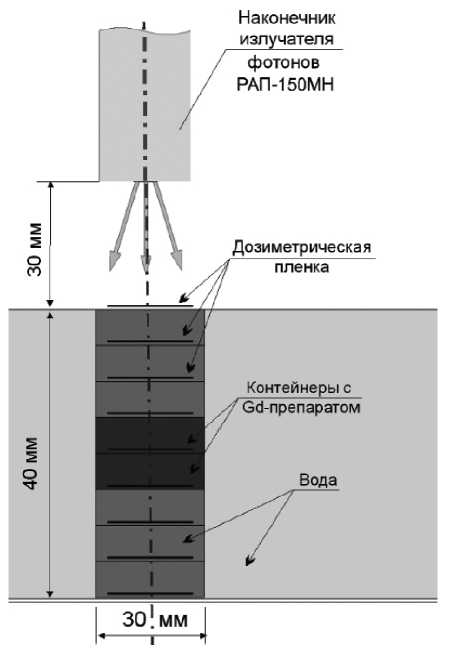
Рис. 2. Схема эксперимента
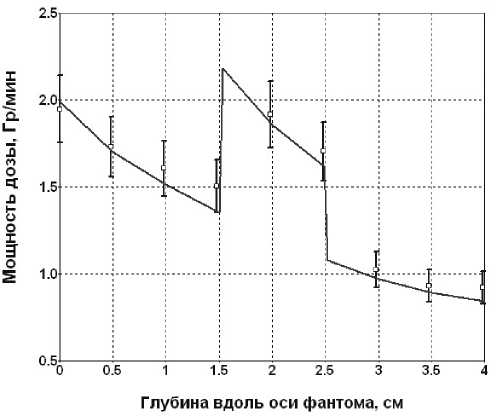
Рис. 4. Сравнение экспериментальных (точки) и расчетных (линии) распределений мощностей поглощенных доз фотонов по глубине фантома в условиях эксперимента (см. рис. 2).
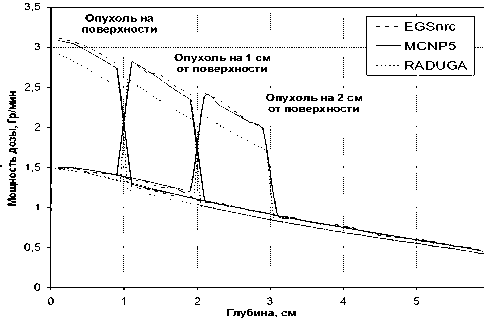
а)
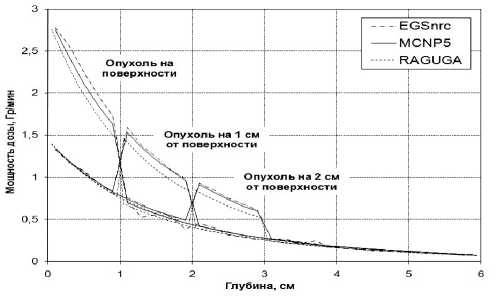
б)
Рис. 3. Распределения мощностей поглощенных доз фотонов по оси фантома с моделью опухоли, содержащей 1 % гадолиния, для различных вариантов ее расположения, полученные по программам EGSnrc, MCNP5, RADUGA: а) мононаправленный источник; б) конусный источник
были получены результаты расчетных распределений мощности поглощенных доз фотонов по оси фантома при добавлении в модель опухоли гадолиний содержащего препарата (содержание гадолиния в биологической ткани 10 мг/г) и без препарата. Статистическая погрешность результатов расчета методом Монте-Карло не превышала 1 % [7]. Расчеты велись для случаев различного местоположения опухоли: с Z0 =0 см («поверхностная» опухоль) и на глубине Z0 =1 см и 2 см.
Результаты расчетов мощностей поглощенных доз вдоль оси фантома для двух видов источников фотонов приведены на рис. 3.
Результаты измерений мощности поглощенной дозы в водном фантоме, в отдельных секциях которого находился раствор Gd-содержащего препарата, приведены на рис. 4 в сравнении с расчетными данными, полученными по программе MCNP5 для геометрии эксперимента (см. рис. 2). Доверительный интервал экспериментальных оценок поглощенной дозы (P=0,95) оценен по методу [8] с учетом рекомендаций [9].
Максимальное расхождение между результатами расчетов и экспериментальными данными не превышает 12%.
Форма кривых распределений мощностей поглощенных доз фотонов по глубине фантома в значительной степени подобна тем, которые приведены на рис. 2б для конусного источника.
Обсуждение. Результат расчетов мощностей поглощенных доз вдоль тканеэквивалентного фантома без опухоли показал, что оценки программ MCNP5 и EGSnrc расходятся между собой в диапазоне до 2%. Оценки по программе RADUGA лежат стабильно ниже на 10% для плоского мононаправленного источника, а для конусного источника различаются не более чем на 4% с результатами программ MCNP5 и EGSnrc. По полученным результатам в случае присутствия модели опухоли с гадолиний-содержащим препаратом внутри фантома наблюдалось локальное возрастание дозы в 2 раза для параллельного пучка фотонов. Для расходящегося пучка локальное возрастание дозы до двух раз характерно только на поверхностных опухолях, в глубинных опухолях доза возрастает в меньшее число раз. Расхождение между результатами программ MCNP5 и EGSnrc составило 2-3%.
Сравнение результатов расчетов по программам EGSnrc, MCNP5 и RADUGA показало, что программа RADUGA несколько занижает результаты (до 10%) в сравнении с программами, использующими прямой метод расчета поглощенной дозы методом Монте-Карло.
Результаты измерений мощности поглощенной дозы в водном фантоме, в отдельных секциях которого находился раствор Gd-содержащего препарата, согласуются с расчетными данными, полученными по программе MCNP5 (рис.4). Форма кривых распределений мощностей поглощенных доз фотонов по глубине фантома в значительной степени подобна тем, которые приведены на рис. 2б для конусного источника.
Максимальное расхождение между результатами расчетов и экспериментальными данными не превышает 12%, что позволяет сделать вывод о достоверности расчетных результатов.
Заключение. В результате проведенных расчетных (тремя независимыми методами) и экспериментальных исследований подтверждена и количественно оценена величина физического эффекта локального возрастания поглощенной дозы в биологической ткани при наличии в ней элементов с большим атомным номером Z — основного принципа фотон-захватной терапии. Тем самым получено физическое обоснование результатов радиобиологических экспериментальных исследований [8].
Работы по созданию технологии фотон-захватной терапии ведутся в последние годы. Интерес к этому виду лучевой терапии обусловлен необходимостью разработки новых и эффективных методов лучевой терапии со сравнительно низкой стоимостью облу-чательной аппаратуры, возможностью ее массового применения в медицинских учреждениях.
Для скорейшего внедрения данного метода в клиническую практику требуется осуществить комплекс исследований и разработок в соответствии с действующими правилами проведения доклинических исследований.
Список литературы Обоснование принципа фотон-захватной терапии злокачественных новообразований
- Способ фотон-захватной терапии опухолей: пат. 2270045 (РФ)/В.Ф. Хохлов, В.Н. Кулаков, И.Н. Шейно, Т. А. Насонова, В.Н. Митин, О.А.Добрынина. 20.02.2006
- Sheino I.N. Dose-supplementary therapy of malignant tumors//Proceedings of ICNCT-12/ed. by Y. Nakagawa, T. Kobayashi and H. Fukuda. [12th International Congress on Neutron Capture Therapy. October 9-13, 2006, Kagawa Japan]. P. 531-534
- X-5 Monte Carlo Team//MCNP -A General Monte Carlo N-Particle Transport Code, Version 5. Vol. I: Overview and Theory. LA-UR-03-1987, Los Alamos National Lab. (April 2003)
- Kawrakow I., Rogers D.W. O. The EGSnrc code system: Monte Carlo simulation of electron and photon transport. National Research Council of Canada, PIRS-701, 2003
- Nikolaeva O.V., Germogenova ТА., Bass L. P., Kuznetsov VS. The Discrete Ordinate Methods development to the Transport Equation solving//The 3D code Raduga-5.1 and multiprocessors computers: Proc. of the 19-th International Conference on Transport Theory. (19th ICTT). Budapest, 2005. P. 115
- Shchegolkov I.V., Sheino I.N., Molin A.A. Semiempirical Model of X-ray Tube Facility//Nuclear Physics Methods and Accelerators in Biology and Medicine: AIP Conference Proceedings 1204. N. Y, 2009. P. 188-191
- Щегольков И.В., Шейно И.Н., Хохлов В.Ф., Липен-гольц А.А. Моделирование распределений поглощенной дозы методом Монте-Карло в технологии фотон-захватной терапии//Медицинская физика. 2010. № 4. С. 12-16
- Calibration Method For GAFCHROMIC R XR-R/International Specialty Products. NJ, 2007. 25 p.
- AAPM protocol for 40-300 kV X-ray beam dosimetry in radiotherapy and radiobiology/C.-M. Chair, C.W. Ma Coffey L.A. DeWerd [et. al.]//Med. Phys. 2001. Vol. 28, № 6. P. 868-893
- Использование гадолиний-содержащего препарата для повышения эффективности рентгеновского облучения при лечении экспериментальных опухолей/Н.Г. Даренская, О.А. Добрынина, ТА. Насонова [и др.]//Медицинская радиология. 2006. Т. 51, № 4. С. 5-11.


