Образование «шубы» медного купороса вокруг медного катода в зависимости от напряжения между электродами в водной суспензии
Автор: Ибраимов Т.К., Ташполотов Ы., Садыков Э.
Журнал: Бюллетень науки и практики @bulletennauki
Рубрика: Естественные науки
Статья в выпуске: 11 т.10, 2024 года.
Бесплатный доступ
Изучен процесс образования кристаллогидрата медного купороса (CuSO4×5H2O) в водной суспензии при подаче напряжения на медные электроды. Рассматриваются факторы, влияющие на интенсивность образования медного купороса, включая приложенное напряжение, расстояние между электродами и состав воды. В экспериментах использовались медные электроды размером 10×2 см. Расстояние между электродами варьировалось от 2 до 10 см. На электроды подавалось напряжение в диапазоне от 2 до 29 В. Приведены результаты экспериментов, анализ влияния различных параметров на процесс кристаллизации, а также обсуждение возможных механизмов реакции.
Медные электроды, электрическое поле, водная суспензия, электрофизическая ионизация, медный купорос, миграция ионов
Короткий адрес: https://sciup.org/14131424
IDR: 14131424 | УДК: 544.6: | DOI: 10.33619/2414-2948/108/02
Formation of a “coat” of copper sulfate around the copper cathode depending on the voltage between the electrodes in an aqueous
This article studies the process of formation of copper sulfate crystallohydrate (CuSO4×5H2O) in an aqueous suspension when voltage is applied to copper electrodes. The factors influencing the intensity of the formation of copper sulfate, including the applied voltage, the distance between the electrodes and the composition of the water, are considered. Copper electrodes measuring 10×2 cm was used in the experiments. The distance between the electrodes varied from 2 to 10 cm. The electrodes were supplied with a voltage in the range from 2 to 29 V. The results of experiments, an analysis of the influence of various parameters on the crystallization process, as well as a discussion of possible reaction mechanisms are presented.
Текст научной статьи Образование «шубы» медного купороса вокруг медного катода в зависимости от напряжения между электродами в водной суспензии
Бюллетень науки и практики / Bulletin of Science and Practice
Медный купорос (CuSO 4 ×5H 2 O) представляет собой одно из важнейших соединений меди, широко применяемое в сельском хозяйстве, химической промышленности и других отраслях. Метод электрохимического осаждения медного купороса на катоде при подаче внешнего напряжения в электролитах, содержащих ионы меди и сульфатов, известен уже достаточно давно. Ранее исследователи уделяли внимание изучению электрохимических процессов на медных электродах, особенностям электролиза воды и образования двойного электрического слоя (ДЭС) [1–3].
Некоторые работы [4, 5] указывали на важность внешнего напряжения и электрического поля в процессах электролитического осаждения меди и других металлов. Однако вопросы, связанные с образованием кристаллогидратов, таких как CuSO 4 ×5H 2 O, в электролитах на основе питьевой воды, требуют более детального исследования. Известно, что медный купорос традиционно получают путем взаимодействия меди с серной кислотой и последующей кристаллизации. Однако этот метод имеет свои недостатки, включая потребление концентрированной кислоты, значительные энергетические затраты и экологическую нагрузку, связанную с побочными продуктами. Предлагаемый инновационный метод электрофизической ионизации(электролиз), использующий питьевую воду, представляет значительный интерес по следующим причинам:
-
1. Экологичность и доступность сырья: Питьевая вода доступна практически в любом регионе и уже содержит необходимые для процесса ионы, включая сульфат-анионы (SO42-). Электролиз в водной среде позволяет избежать использования концентрированных кислот и других химически агрессивных реагентов, что делает процесс экологически чистым.
-
2. Упрощение производственного процесса: использование питьевой воды в качестве электролита позволяет проводить процесс в относительно простых условиях без необходимости подготовки специализированных растворов. Это может способствовать организации малых производств медного купороса в любых районах, где использование сложного химического оборудования затруднено.
-
3. Снижение затрат: метод электролиза для получения медного купороса требует относительно небольших энергетических затрат и не нуждается в дорогостоящих химикатах. Это позволяет снизить себестоимость конечного продукта. К тому же возможность регулировать условия электролиза (напряжение, расстояние между электродами) дает контроль над процессом и выходом продукта.
-
4. Возможность переработки медных отходов: Электролитический метод дает возможность использовать отходы медных изделий в качестве электродов. Это способствует вторичной переработке меди и снижению потребления природных ресурсов.
-
5. Обогащение питьевой воды микроэлементами: Одной из перспектив применения данного метода является обогащение питьевой воды ионами меди в контролируемых количествах. Медный купорос обладает антисептическими свойствами, и добавление его в питьевую воду может использоваться для дезинфекции и обогащения воды медью, необходимой для здоровья человека в малых дозах.
Таким образом, получение медного купороса методом электролиза из питьевой воды не только актуально с точки зрения научных исследований в области электрохимии и материаловедения, но и обладает существенным прикладным потенциалом. Этот метод может стать экономически эффективной и экологически безопасной альтернативой традиционным способам производства медного купороса.
Настоящая работа направлена на изучение механизмов образования CuSO4^5H2O при подаче напряжения на медные электроды в водной суспензии, а также на выявление основных факторов, влияющих на этот процесс.
Материал и методы исследования
-
1. Характеристика образцов воды: В качестве электролита использовалась питьевая вода, содержащая типичные ионы: HCO 3 -, SO 4 2-, Cl-, Ca2+, Mg2+. Концентрация сульфат-ионов (SO 42- ) составляла примерно 50 мг/л.
-
2. Устройство и электроды: В экспериментах использовались медные электроды размером 10×2 см. Расстояние между электродами варьировалось от 2 до 10 см. На электроды подавалось напряжение в диапазоне от 2 до 29 В.
-
3. Методы измерений: Проводились измерения напряжения, силы электрического поля, ионов меди (Cu2+) и сульфат-ионов (SO 4 2-) с использованием стандартных потенциометрических методов. Образование CuSO 4 ×5H 2 O оценивалось методом гравиметрии и рентгенофазовым анализом (РФА).
-
4. Экспериментальная процедура: В водную суспензию помещались медные электроды, после чего к ним подключалось регулируемое напряжение [6, 7]. После определенного времени эксперимента оценивалось количество осажденного медного купороса.
В данном исследовании основное внимание уделялось электрохимическим процессам, происходящим при подаче напряжения на медные электроды в водной суспензии, и их влиянию на образование медного купороса (CuSO 4 ×5H 2 O). Для этого проводились несколько этапов эксперимента, в ходе которых оценивались различные параметры и наблюдалось кристаллическое осаждение CuSO 4 ×5H 2 O.
Подготовка материалов и оборудования
В качестве электролита использовалась питьевая вода, содержащая различные ионы, включая сульфат-ионы (SO 4 2-), гидрокарбонаты (HCO3-), ионы кальция (Ca²⁺), магния (Mg²⁺) и другие соли. Важно было удостовериться в достаточной концентрации сульфат-ионов (около 50 мг/л) для обеспечения условий формирования сульфата меди.
Использовались два медных электрода размером 10×2 см, закрепленных на держателях в электролизной ячейке. Расстояние между электродами варьировалось от 2 до10 см.
Для подачи напряжения использовался регулируемый источник постоянного тока, позволяющий изменять напряжение в диапазоне от 2 до 29 В с точностью до 0,1 В.
Установка параметров и проведение электролиза
Медные электроды помещались в сосуд с питьевой водой, при этом обеспечивалась возможность регулировки расстояния между электродами. Электроды подключались к источнику постоянного тока, который подавал регулируемое напряжение.
Эксперименты проводились при различных значениях напряжения (2, 5, 10, 15, 20, 25, и 29 В) и различных расстояниях между электродами (2 см, 4 см, 6 см, 8 см и 10 см) для исследования влияния этих параметров на образование CuSO 4 ×5H 2 O.
Напряжение подавалось на электроды в течение фиксированного времени (например, 30 минут) для каждого эксперимента. За это время происходили электрохимические реакции на поверхности электродов .
Методы измерений и анализа
Измерение напряжения и силы электрического поля . При каждом эксперименте фиксировалось напряжение, подаваемое на электроды, и измерялась сила электрического поля (E), рассчитываемая как отношение приложенного напряжения (U) к расстоянию между электродами (d): E=U/d. Это позволяло оценить интенсивность электрического поля в электролите.
Гравиметрия . После завершения электролиза раствор оставляли на некоторое время для образования кристаллов CuSO 4 ×5H 2 O. Затем осажденный медный купорос собирался на фильтре, высушивался и взвешивался с использованием аналитических весов. Полученные данные использовались для оценки массы образовавшегося медного купороса при разных условиях эксперимента.
Рентгенофазовый анализ (РФА). Для подтверждения состава и фазовой структуры образовавшихся кристаллов использовался рентгенофазовый анализ. Этот метод позволял идентифицировать фазу кристаллического вещества и убедиться, что образовавшиеся кристаллы соответствуют CuSO 4 ×5H 2 O.
Эксперименты проводились в несколько серий, при этом изменялись только отдельные параметры (напряжение и расстояние между электродами) для изучения их влияния на процесс образования медного купороса. Каждая серия экспериментов повторялась трижды для обеспечения достоверности полученных результатов. В промежутках между экспериментами измерялась температура электролита и рН раствора, так как изменение этих параметров может влиять на процессы кристаллизации и электрохимические реакции.
После завершения экспериментов результаты гравиметрического анализа использовались для построения зависимостей массы образовавшегося CuSO 4 ×5H 2 O от приложенного напряжения и расстояния между электродами. Данные измерений концентраций ионов меди (Cu2+) и сульфатов (SO 4 2-) были обработаны для определения изменения их концентраций в процессе электролиза. Результаты РФА были сопоставлены с эталонными значениями для подтверждения фазы кристаллов, что обеспечивало высокую точность определения образовавшегося соединения.
Результаты
В результате проведения данного исследования было выявлено, что на образование медного купороса (CuSO 4 ×5H 2 O) существенно влияют параметры электрического поля (напряжение и расстояние между электродами) и состав электролита. Экспериментальные данные подтвердили, что увеличение напряжения и уменьшение расстояния между электродами приводят к ускорению процесса кристаллизации CuSO 4 ×5H 2 O вблизи катода.
Таким образом, этот экспериментальный подход позволил изучить условия, способствующие образованию медного купороса, и предложить оптимальные параметры для его электролитического осаждения. На Рисунке 1 представлена зависимость массы осадка от расстояния между электродами.
m, gr 100

10 12
d, cm
Рисунок 1. Зависимость массы осадка от расстояния между электродами
На Рисунке 2 приведена зависимость массы образовавшегося CuSO4^5H2O от от напряженности электрического поля между электродами
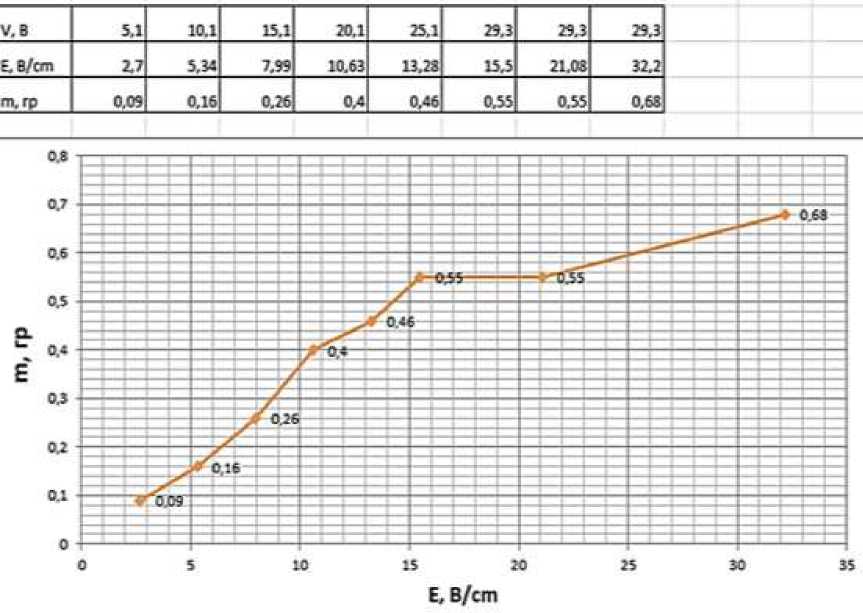
Рисунок 2. Зависимость массы осадка от напряженности электрического поля между электродами
Анализ полученных результатов
Из графика зависимости 1 следует, что масса образовавшегося CuSO 4 ×5H 2 O увеличивается с уменьшением расстояния между электродами. При высоких напряжениях (10–15 В) и малом расстоянии (2 см) электрическое поле достигает значительных значений, что усиливает миграцию ионов меди к катоду и увеличивает локальную концентрацию Cu2+. Это, в свою очередь, способствует кристаллизации медного купороса в непосредственной близости от катода. Такие результаты согласуются с данными в литературе, где указывается, что интенсивное электрическое поле может ускорять электрохимические процессы на катоде, способствуя образованию различных кристаллогидратов [4].
Однако, в отличие от предыдущих исследований, данная работа демонстрирует прямую зависимость между расстоянием между электродами и количеством осажденного CuSO 4 ×5H 2 O. Также наблюдается влияние состава воды, особенно наличия сульфат-ионов, на процесс образования медного купороса. В ходе экспериментов было установлено, что при отсутствии достаточного количества SO42- в растворе процесс кристаллизации замедляется, что подчеркивает их важную роль.
Для анализа зависимости массы осадка от напряженности электрического поля между электродами следует рассмотреть основные тенденции, которые обычно наблюдаются на Рисунке 2. Из графика зависимости 1 видно, что при увеличении напряженности электрического поля с 3 В/см до 15,5 В/см масса осадка растет практически прямо пропорционально напряженности. Однако при дальнейшем росте напряженности поля до 32,5 В/см масса осадка медного купороса на катоде замедляется, то есть при определенной напряженности электрического поля увеличение массы осадка замедляется или достигает плато. Это свидетельствует о том, что электрическое поле до 15,5 В/см усиливает миграцию ионов меди (Cu2+) к катоду и ускоряет процессы кристаллизации медного купороса (CuSO4×5H2O) в непосредственной близости от катода. Также это указывает на достижение оптимальных условий для кристаллизации, после которых дальнейшее увеличение напряженности не приводит к значительному приросту массы осадка, что может быть связано с ограниченной скоростью миграции ионов или насыщением раствора.
Из Рисунка 1 видно, что с увеличением расстояния между электродами масса осадка уменьшается, то есть большее расстояние снижает эффективность процесса осаждения, поскольку электрическое поле становится менее интенсивным. Это проявляется на графике в виде более низкой массы осадка при одинаковой напряженности электрического поля для большего расстояния. На основе графика можно определить оптимальную напряженность электрического поля для максимального осаждения медного купороса, что может быть особенно полезно для промышленных приложений с целью обеспечения максимального выхода продукта. Для более детального анализа следует рассмотреть численные значения, тренды, точки перегиба и оценить, как изменение параметров влияет на эффективность процесса.
Заключение
-
1. Настоящее исследование показало, что образование медного купороса (CuSO 4 ×5H 2 O) вблизи медного катода в водной суспензии зависит от нескольких факторов, включая приложенное напряжение, расстояние между электродами и состав воды.
-
2. Экспериментальные данные демонстрируют, что наибольшая масса осажденного CuSO 4 ×5H 2 O достигается при высоком напряжении (15 В) и малом расстоянии между электродами (2 см). Это обусловлено усиленным электрическим полем, которое способствует ускоренной миграции ионов меди (Cu2+) к катоду, увеличивая вероятность их взаимодействия с сульфат-ионами (SO 4 2-) и последующей кристаллизации медного купороса.
Результаты исследования указывают на оптимальные условия для промышленного производства медного купороса (CuSO 4 ×5H 2 O) методом электрофизической ионизации в водной среде. Наибольшая эффективность осаждения медного купороса достигается при подаче высокого напряжения (15 В) и поддержании малого расстояния между медными электродами (2 см). Эти условия создают усиленное электрическое поле, ускоряющее миграцию ионов меди (Cu2+) и их взаимодействие с сульфат-ионами (SO42_), что способствует образованию кристаллов медного купороса.
Для внедрения данной технологии в производство рекомендуется использовать питьевую воду, обогащенную сульфат-ионами, и регулировать параметры электролиза (напряжение и межэлектродное расстояние) для обеспечения максимального выхода CuSO 4 ×5H 2 O. Такой подход позволяет производить медный купорос экологически чистым и экономически эффективным способом.
Список литературы Образование «шубы» медного купороса вокруг медного катода в зависимости от напряжения между электродами в водной суспензии
- Животовская Г. П. Электрохимические процессы. Челябинск, 2010. 64 с.
- Islam S., Mia M. M., Shah S. S., Naher S., Shaikh M. N., Aziz M. A., Ahammad A. S. Recent advancements in electrochemical deposition of metal-based electrode materials for electrochemical supercapacitors // The Chemical Record. 2022. V. 22. №7. P. e202200013. DOI: 10.1002/tcr.202200013
- Петров В. В. Физическая химия: электрохимические процессы. СПб., 2012. 400 с.
- Lermusiaux L., Mazel A., Carretero-Genevrier A., Sanchez C., Drisko G. L. Metal-induced crystallization in metal oxides // Accounts of Chemical Research. 2022. V. 55. №2. P. 171-185. DOI: 10.1021/acs.accounts.1c00592
- Кузнецов Н. Н., Михайлов И. И. Электролиз и процессы кристаллизации. Новосибирск, 2020. 300 с.
- Ибрагимов Т. К., Садыков Э., Ташполотов Ы. Извлечение оксидов редкоземельных элементов из сточных вод на основе электрофизической ионизации // Известия Национальной Академии наук Кыргызской Республики. 2022. №5. С. 39-44.
- Ташполотов Ы. и др. Способ преобразования химических элементов на основе эффекта электрофизической ионизации // Вестник Ошского государственного университета. 2021. Т. 1. №1. С. 146-154. DOI: 10.52754/16947452_2021_1_1_146


