Оценка активности аденилатциклазы в тромбоцитах овец после внешнего воздействия G-излучения в различных дозах
Бесплатный доступ
Целью исследования было изучение ферментативной активности аденилатциклазы в тромбоцитах, выделенных из крови 32 овец цыгайской породы (бараны), которые были подвергнуты общему внешнему воздействию g-излучения в дозах 2, 4 и 6 Гр (установка «ГУЖ-24», Россия, источник излучения 137Cs с энергией гамма-квантов 0,67 МэВ при мощности дозы 1 Гр/ч). Общее внешнее воздействие g-излучения в исследованном диапазоне доз приводило к развитию у животных острого лучевого поражения различной степени тяжести. Методом тонкослойной хроматографии определяли базальную и стимулированную простагландином Е1 активность аденилатциклазы в различные сроки радиационного поражения животных (1-30-е cут). В тромбоцитах облучённых животных обнаружили изменения и базальной, и стимулированной простагландином Е1 активности аденилатциклазы. После внешнего воздействия g-излучения отмечали прямо пропорциональную зависимость от дозы базальной (на 1-е и 7-е сут) и стимулированной активности аденилатциклазы (на 7-е сут) в тромбоцитах. В работе делается предположение, что пострадиационные изменения активности аденилатциклазы в тромбоцитах обусловлены как модификацией цитоплазматических мембран клеток и нарушением функционирования мембраносвязанной цАМФ-зависимой сигнальной системы, так и выходом в кровь новых клеток из пула мегакариоцитов костного мозга с качественно иными свойствами.
Внешнее g-излучение, острое лучевое поражение, овцы, тромбоциты, базальная активность аденилатциклазы, стимулированная простагландином е1 активность аденилатциклазы
Короткий адрес: https://sciup.org/170171549
IDR: 170171549 | УДК: 612.111.7:612.014.482.4]-092.9 | DOI: 10.21870/0131-3878-2020-29-4-136-145
Adenylate cyclase activity in sheep platelets following external whole-body G-irradiation with different doses
The paper presents results of study of adenylate cyclase activity in the platelets after external whole-body g-irradiation of 32 tsigai rams (Ovis aries) with 2, 4 and 6 Gy, at the dose rate of 1 Gy/hour. The irradiation caused the development of acute radiation damage of a different degree of severity. To detect changes in the basal and prostoglandin E1 stimulated (PGE1-stimulated) adenylate cyclase activity thin-layer chromatography (TLC) was carried out during the first 30 days of the damage development. After external g-irradiation directly proportional effect of dose on changes in the basal adenylate cyclase activity in the platelets was registered on the 1 and the 7 days of the damage development, the changes in the PGE1-stimulated activity was registered on the 7 day. The study results allow making the suggestion that detected changes in the adenylate cyclase activity in the platelets of irradiated rams may be resulted from the modification of cytoplasmic cell membranes and impaired functioning of membrane-bound cAMP-sensitive signaling pathway. It may be also caused by new cells with qualitatively new properties released from the bone marrow megakaryocytes pool into the bloodstream.
Текст научной статьи Оценка активности аденилатциклазы в тромбоцитах овец после внешнего воздействия G-излучения в различных дозах
Аденилатциклаза – ключевой фермент цАМФ-зависимой сигнальной системы. Активация этой системы осуществляется через трансмембранный каскад: p -адренорецептор - G-белки -аденилатциклаза с помощью гормонов, нейромедиаторов и других соединений, называемых первичными мессенджерами. Выполняя функцию вторичного внутриклеточного мессенджера, цAMФ вызывает метаболические и функциональные сдвиги, изменяющие функции клеток [1]. Через цАМФ-зависимую систему трансмембранной передачи сигналов происходит регуляция метаболизма, пролиферации и дифференцировки клеток, экспрессии генов; она также играет важную роль в кроветворении, клеточном иммунитете, вирусной инфекции, регуляции апоптоза и других процессах [2-4]. Выявлено участие внутриклеточной цАМФ-зависимой системы в поддержании нормального гемостаза и активации тромбоцитов при их агрегации [5]. Получены экспериментальные доказательства участия аденилатциклазной сигнальной системы в увеличении эластичности эритроцитарных мембран и изменении деформируемости эритроцитов [6, 7].
Внешнее воздействие у -излучения приводит в организме млекопитающих к изменению содержания в тканях и периферической крови катехоламинов, кортикостероидов, серотонина и других биологически активных соединений, активирующих определённые сигнальные системы [8]. Отмечены пострадиационные изменения активности ферментов цАМФ-зависимой сигнальной системы в различных клеточных популяциях у лабораторных и сельскохозяйственных животных
Шевченко Т.С.* – главный специалист, к.б.н.; Кобялко В.О. – зав. лаб., к.б.н. ФГБНУ ВНИИРАЭ.
[9-15]. Кроме того, внешнее воздействие γ -излучения на организм животных в дозах 2-10 Гр поражает систему кроветворения, в результате чего резко снижается число клеток костного мозга и периферической крови [8]. Поэтому возникает вопрос, влияет ли такое воздействие на функционирование аденилатциклазы как ключевого фермента цАМФ-зависимой сигнальной системы в клетках периферической крови. Ранее нами было проведено исследование базальной и стимулированной простагландином Е 1 активности аденилатциклазы в лимфоцитах, выделенных из крови овец, подвергнутых общему внешнему воздействию γ -излучения в различных дозах [16].
А целью данной работы стала оценка активности базальной и стимулированной простагландином Е 1 активности аденилатциклазы в тромбоцитах, выделенных из крови овец, подвергнутых общему внешнему воздействию γ -излучения в разных дозах.
Материалы и методы
Эксперимент проведён на 32 овцах цыгайской породы (бараны) со средней живой массой 33,16 ± 0,12 кг в условиях вивария ВНИИРАЭ (Обнинск). Экспериментальные животные были получены из хозяйств Калужской области, имели ветеринарный сертификат и прошли 20-суточный карантин в виварии ВНИИРАЭ. Все работы с животными выполнялись в соответствии с ГОСТ 33215-2014. Рацион был сбалансирован по основным питательным веществам согласно нормам ВНИИ животноводства. Животные были разделены на четыре группы – контрольную (1-я группа, 8 голов) и три опытные (по 8 голов каждая), которых подвергали общему внешнему воздействию γ -излучения на установке «ГУЖ-24», Россия (источник излучения 137Cs с энергией гамма-квантов 0,67 МэВ) при мощности дозы 1 Гр/ч.
Определение клинического состояния подопытных животных проводили по показателям, принятым в клинической диагностике сельскохозяйственных животных: общий вид овец, поведение, реакцию на внешние раздражители, аппетит, температуру тела, частоту пульса и дыхания, функциональное состояние желудочно-кишечного тракта, динамику живой массы. Для оценки степени радиационного поражения использовали гематологические показатели: количество эритроцитов, тромбоцитов, лейкоцитов и лейкоцитарную формулу по стандартным методикам. До начала эксперимента биологические и клинические показатели овец контрольной и опытных групп были равноценными. Условия содержания животных контрольной и опытных групп были идентичными.
Животные опытных групп были подвергнуты общему внешнему воздействию γ -излучения в дозах: 2 Гр – 2-я группа, 4 Гр – 3-я группа и 6 Гр – 4-я группа. Контроль уровня и равномерности облучения подопытных животных осуществляли дозиметром «VAJ-18» (Германия) со сферической ионизационной камерой «VAK-253» (Германия). Неравномерность γ -излучения не превышала ± 15%.
Пробы крови отбирали из яремной вены до облучения и на 1-, 3-, 5-, 7-, 10-, 15-, 20- и 30-е сут после воздействия. В качестве антикоагулянта использовали цитрат натрия (конечная концентрация 0,38%). Популяцию тромбоцитов выделяли из периферической крови овец разработанным нами способом [17]. Изолированные клетки промывали 2 раза в растворе, содержащем NaCl, KCl, K2HPO, MgCl2, глюкозу и N-2-(гидроксиэтил)пиперазин N′-2-этансульфоновую кислоту в концентрации 145, 5, 0,5, 1, 3 и 10 ммоль/л соответственно), рН 7,4. Подсчёт количества клеток в полученных суспензиях проводили в камере Горяева. Жизнеспособность выделенных кле- ток, определяемая с помощью окрашивания 0,1%-ным раствором трипанового синего, составляла в среднем 90-95%. Перед проведением ферментной реакции аликвоту суспензии тромбоцитов лизировали с помощью замораживания и оттаивания.
Данные определения базальной и стимулированной активности аденилатциклазы в тромбоцитах всех 32 овец до начала эксперимента рассматривали как объединённый контроль (исходные данные).
Активность аденилатциклазы в лизатах клеток определяли в соответствии с условиями, описанными ранее [18]. В качестве меченых субстратов ферментных реакций использовали [14С] -АТФ и [3Н] -цАМФ («Amersham», Великобритания). Разделение продуктов ферментных реакций проводили методом тонкослойной хроматографии на пластинах «Силуфол УФ-254» (Чехия). Среда инкубации для анализа активности аденилатциклазы включала: АТФ; ГТФ; МgSO 4 ; этиленгликоль-ди/ β -аминоэтиловый эфир/-N,N-уксусной кислоты (ЭГТА); креатинфосфат; трис-HCl (0,5: 0,1; 10; 2; 5; 50 ммоль/л соответственно), 40 ед/мл креатинкиназы; 37 КБк [14С]-АТФ (рН 7,4; tº 30 ºС). Гормон-стимулированную активность аденилатциклазы определяли по разнице ферментативной активности с простагландином Е 1 в концентрации 10-5 моль/л и без него.
Подсчёт радиоактивности всех образцов проводили на жидкостно-сцинтилляционном счётчике «SL-4220» («Intertechnique», Франция).
Статистическую обработку результатов осуществляли с использованием t-критерия Стьюдента и пакета программ Microsoft Excel 2003. Различия между контрольными и опытными значениями считали достоверными при p<0,05.
Результаты и обсуждение
Общее внешнее воздействие γ -излучения в исследованных дозах от 2 до 6 Гр приводило к развитию у животных острого лучевого поражения различной степени тяжести. Клинико-гематологическое обследование овец показало, что доза облучения 2 Гр вызывала лучевое поражение лёгкой степени тяжести, 4 Гр – средней, а 6 Гр – тяжёлой. Облучение овец в дозе 2 Гр не оказывало летального воздействия на животных на протяжении 45 сут наблюдения (сублетальная доза). При воздействии γ -излучения в дозе 4 Гр в течение 45 сут наблюдения погибло 50% овец (LD 50/45 – полулетальная доза) и 100% – при дозе 6 Гр в течение 45 сут (LD 100/45 – летальная доза).
Базальная активность аденилатциклазы – это активность синтезирующего цАМФ фермента, связанного с каталитической субъединицей, в отсутствие стимулирующего или ингибирующего действия на клетку физиологически активных соединений [1]. Величина базальной активности аденилатциклазы в тромбоцитах всех 32 необлучённых овец составила 10,9 ± 1,9 пмоль/мин × 108 клеток, что сравнимо с величиной базальной активности аденилатциклазы в тромбоцитах крупного рогатого скота, равной 13,3 ± 0,4 пмоль/мин × 108 клеток [15]. Базальная активность аденилатциклазы в тромбоцитах контрольных овец практически не менялась в течение всего эксперимента (табл. 1).
После общего внешнего воздействия γ-излучения базальная активность аденилатциклазы в тромбоцитах возрастала на 1-е сут у животных всех трёх опытных групп в 1,77; 2,46 и 3,40 раза соответственно (табл. 1). На 3-и сут базальная активность исследуемого фермента в тромбоцитах овец первых двух опытных групп возвращалась к исходным данным, тогда как в третьей группе повышалась в 1,67 раза. На 5-е сут базальная активность аденилатциклазы увеличивалась в тромбоцитах овец 1-й группы в 3,41 раза и уменьшалась в тромбоцитах 2-й и 3-й групп в 2,14 и 2,6 раза соответственно. На 7-е сут величина показателя у животных 1-й группы мало отличалась от контроля и значительно увеличивалась у овец 2-й и 3-й групп – в 3,54 и 5,15 раза соответственно. При этом у овец 1-й группы базальная активность аденилат-циклазы в тромбоцитах на 10-е сут оказывалась выше в 2,15 раза в сравнении с необлучённы-ми животными, тогда как у животных двух других опытных групп величина показателя возвращалась к исходным данным. На 15-е сут у овец 1-й и 2-й групп наблюдали снижение активности фермента до контрольных значений, а на 20-е сут – в 2,17 и 2,06 раза. На 30-е сут базальная активность аденилатциклазы в тромбоцитах приближалась к исходным данным. Т.е. базальная активность аденилатциклазы в тромбоцитах при общем внешнем воздействии у-излучения на организм овец в изучаемом диапазоне доз заметно увеличивалась на 1-е (при всех дозах), 5-е (при дозе 2 Гр) и 7-е сут (при дозах 4 и 6 Гр). В остальные сроки у разных групп животных отмечали уменьшение величины показателя до контрольных значений и ниже.
Иными словами, у овец, подвергнутых воздействию у -излучения в сублетальной дозе, наблюдали усиление базальной активности аденилатциклазы в тромбоцитах на 1-е, 5-е и 10-е сут. На 20-е сут у этой группы животных отмечали угнетение активности фермента. В остальные сроки исследования базальная активность аденилатциклазы в тромбоцитах соответствовала контрольным значениям. У овец, облучённых в полулетальной дозе, наблюдали активацию базальной активности аденилатциклазы в тромбоцитах на 1-е и 7-е сут и угнетение активности фермента на 5-е и 20-е сут. У животных, подвергнутых внешнему воздействию у -излучения в летальной дозе, отмечали усиление базальной активности аденилатциклазы в тромбоцитах на 1-е и 7-е сут и угнетение – на 5-е сут.
Таблица 1 Базальная активность аденилатциклазы в тромбоцитах (пмоль/мин х 10 8 клеток) облучённых и необлучённых овец
|
Сроки до и после облучения, сут |
Группы животных |
|||
|
К |
1 |
2 |
3 |
|
|
Исходный уровень |
Объединённый контроль (исходные данные) |
10,9 ± 1,9 |
10,9 ± 1,9 |
10,9 ± 1,9 |
|
1 |
11,3 ± 1,4 |
19,3 ± 2,6* |
26,8 ± 7,1* |
37,1 ± 10,1* |
|
3 |
10,5 ± 1,2 |
9,4 ± 2,1 |
9,7 ± 3,0 |
18,2 ± 12,6 |
|
5 |
13,7 ± 1,8 |
37,2 ± 2,0* |
5,1 ± 0,6* |
4,2 ± 0,8* |
|
7 |
10,9 ± 1,6 |
13,6 ± 6,0 |
38,6 ± 8,6* |
56,1 ± 12,1* |
|
10 |
11,9 ± 1,7 |
23,4 ± 3,4* |
9,5 ± 2,1 |
7,7 ± 2,2 |
|
15 |
10,8 ± 2,3 |
14,0 ± 5,7 |
8,2 ± 0,6* |
8,6 |
|
20 |
12,4 ± 1,9 |
5,0 ± 0,9* |
5,3 ± 1,8* |
6,9 |
|
30 |
11,2 ± 1,3 |
11,6 ± 2,3 |
7,6 ± 1,6 |
14,5 |
* Отличия от контроля (исходные данные) достоверны – р<0,05.
Следовательно, при радиационном поражении животных разной степени тяжести были обнаружены изменения базальной активности аденилатциклазы в тромбоцитах, которые носили фазовый характер. Первую фазу активации наблюдали на 1-е сут, вторую – на 5-7-е сут после воздействия. Была также выявлена прямо пропорциональная зависимость базальной активности аденилатциклазы в тромбоцитах от дозы у -излучения на 1-е и 7-е сут (рис. 1).
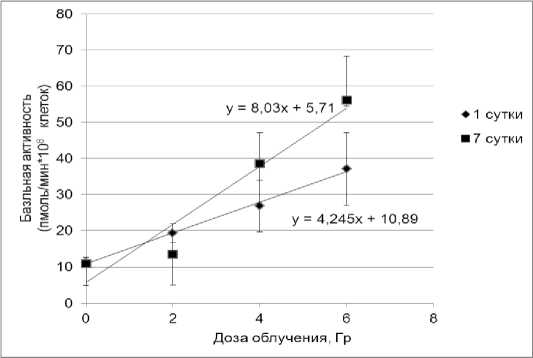
Рис. 1. Зависимость базальной активности аденилатциклазы от дозы на 1-е и 7-е сут после внешнего воздействия у-излучения.
Стимулированная простагландином Е 1 активность аденилатциклазы в тромбоцитах необ-лучённых овец составила 15,7 ± 5,7 пмоль/мин х 108 клеток (табл. 2). Этот показатель на 1-е сут после общего внешнего воздействия у -излучения в тромбоцитах животных 1-й группы оставался на уровне контроля, а в тромбоцитах животных 2-й и 3-й групп возрастал в 6,85 и 3,64 раза соответственно. На 3-и сут стимулированная активность фермента в тромбоцитах овец 1-й группы была ниже контроля в 1,76 раза, в тромбоцитах 2-й группы – в 2,38 раза, а в клетках 3-й группы, напротив, возрастала в 3,64 раза. На 5-е сут стимулированная активность аденилат-циклазы в тромбоцитах овец 2-й и 3-й групп возвращалась к исходным данным, а на 7-е сут значения показателя в тромбоцитах овец всех опытных групп (1-й, 2-й и 3-й) были в 1,63, 5,70 и 9,05 раза выше контроля соответственно. На 10-е сут показатель у животных 1-й группы возрастал в 4,97 раза, у 3-й группы – в 4,3 раза, тогда как у овец 2-й группы снижался в 1,6 раза по сравнению с исходным уровнем. На 15-е сут стимулированная активность аденилатциклазы в тромбоцитах овец 1-й и 2-й групп снижалась в 1,91 и 1,89 раза, а на 20 и 30-е сут – возрастала в 2,04 и 1,88 раза у овец 1-й группы и в 2,51 и 1,25 раза у овец 2-й группы. У животных 3-й группы стимулированная активность аденилатциклазы в тромбоцитах на 15-е сут увеличивалась в 2,68 раза, на 30-е сут – в 3,05 раза.
Таблица 2 Стимулированная простагландином Е 1 активность аденилатциклазы в тромбоцитах (пмоль/мин х 10 8 клеток) облучённых и необлучённых овец
|
Сроки до и после облучения, сут |
Группы животных |
|||
|
К |
1 |
2 |
3 |
|
|
Исходный уровень |
Объединённый контроль (исходные данные) |
15,7 ± 5,7 |
15,7 ± 5,7 |
15,7 ± 5,7 |
|
1 |
17,2 ± 3,3 |
13,4 ± 3,4 |
107,5 ± 27,5* |
57,1 ± 19,0* |
|
3 |
16,5 ± 2,3 |
8,9 ± 3,4 |
6,6 ± 6,3 |
41,0 ± 24,0 |
|
5 |
15,4 ± 1,9 |
- |
13,4 ± 3,4 |
11,1 ± 3,3 |
|
7 |
17,2 ± 0,8 |
25,6 ± 7,2 |
89,5 ± 16,5* |
142,1 ± 3,3* |
|
10 |
13,3 ± 2,5 |
70,2 ± 21,7* |
9,8 ± 4,5 |
67,5 ± 29,5* |
|
15 |
13,5 ± 1,7 |
8,2 ± 3,1 |
8,3 ± 0,3 |
42,1 |
|
20 |
15,6 ± 1,9 |
32,1 ± 2,7* |
39,4 ± 2,7* |
41,7 |
|
30 |
16,4 ± 2,4 |
29,5 ± 11,0 |
19,7 ± 3,6 |
48,0 |
* Отличия от контроля (исходные данные) достоверны – р<0,05.
Иными словами, у животных, подвергшихся общему внешнему воздействию γ -излучения в дозах от сублетальной до летальной, наблюдали изменение стимулированной простагландином Е 1 активности аденилатциклазы в тромбоцитах. После воздействия γ -излучения в сублетальной дозе величина показателя возрастала на 7-е, 10-е, 20-е и 30-е сут (в 1,6-4,5 раза). При полулетальной дозе стимулированная простагландином Е 1 активность аденилатциклазы в тромбоцитах овец возрастала на 1-е, 7-е и 20-е сут (в 2,5-6,9 раза). После облучения животных в летальной дозе активность фермента в тромбоцитах была увеличенной во все исследованные сроки (в 2,6-9,1 раза), кроме 5-х сут, когда величина показателя приближалась к исходным данным. Т.е. у животных, подвергнутых общему внешнему воздействию γ -излучения, выявили усиление стимулированной простагландином Е 1 активности аденилатциклазы в тромбоцитах на 1-е, 7-10-е и 20-30 сут. В остальные сроки отмечали угнетение стимулированной активности фермента, значения которой были ниже контрольных. Была также выявлена прямо пропорциональная зависимость стимулированной простагландином Е 1 активности аденилатциклазы в тромбоцитах от дозы γ -излучения на 7-е сут (рис. 2).
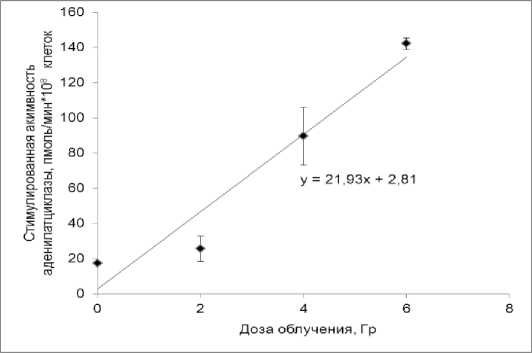
Рис. 2. Зависимость, стимулированная простагландином Е 1 , активности аденилатциклазы от дозы на 7-е сутки после внешнего воздействия γ -излучения.
Таким образом, с 1-х сут после внешнего воздействии γ -излучения на организм овец в дозах от сублетальной до летальной обнаружили выраженные изменения базальной и стимулированной активности аденилатциклазы в тромбоцитах.
Следовательно, в начальный период радиационного поражения овец была выявлена определённая детерминанта постлучевых процессов в ключевом ферменте системы цАМФ – аденилатциклазе. Аденилатциклаза является трансмембранным ферментным комплексом, состоящим из двух субъединиц: каталитической и регуляторной [1]. Процессы, происходящие в этом ферментном комплексе после воздействия внешнего γ -излучения in vivo, затрагивают обе эти субъединицы, поскольку базальная активность аденилатциклазы связана с каталитической субъединицей фермента, а стимулированная – с регуляторной. Функциональная активность фермента в первую очередь зависит от конформации макромолекулы и её взаимодействий с мембранными составляющими, так как аденилатциклаза встроена в цитоплазматическую мембрану клетки [8]. Известно, что биологические мембраны, наряду с ДНК, рассматриваются в качестве одной из мишеней воздействия ионизирующей радиации на клетки [19]. Поэтому ранние изменения активности аденилатциклазы могут быть инициированы радиационно-индуцированным нарушением структурно-функционального состояния плазматических мембран исследованных клеток.
В то же время, может быть и другая причина модификации активности фермента в тромбоцитах при облучении овец, поскольку наблюдаемые изменения и базальной, и стимулированной простагландином Е 1 активности аденилатциклазы в разные сроки весьма различны.
Тромбоциты - небольшие (с диаметром 2-4 мкм) дисковидные безъядерные клетки, образующиеся при фрагментации своих предшественников мегакариоцитов в костном мозге. Срок их жизни в кровеносном русле составляет в норме 5-10 сут, в результате чего к 7-10-м сут тромбоцитарная популяция в периферической крови значительно обновляется [20]. И если воздействие Y -излучения на активность аденилатциклазы в тромбоцитах в начальный период лучевого поражения реализуется, в основном, через нарушения в цитоплазматической мембране, то изменение активности фермента на 7-10-е сут, по-видимому, связано с выходом в кровь новых клеток из пула мегакариоцитов костного мозга с качественно иными свойствами. При этом у «обновлённой» популяции тромбоцитов у овец, облучённых в суб- и полулетальной дозах в период разгара лучевой патологии (15-е сут), была значительно снижена стимулированная простагландином Е 1 активность аденилатциклазы, т.е. ухудшена эффективность передачи гормонального сигнала в клетки.
Следовательно, развитие острой лучевой патологии овец при внешнем воздействии у -излучения в дозах от сублетальной до летальной сопровождается модификацией функционирования аденилатциклазы в относительно радиорезистентных тромбоцитах. Модификация функционирования аденилатциклазы в тромбоцитах овец, проявляя фазовый характер изменений, является зависимой от степени радиационного поражения на 1-е и 7-е сут. Необходимо отметить, что лучевое поражение организма млекопитающих разной степени тяжести опосредуется влиянием радиации на мембраносвязанную аденилатциклазную или цАМФ-зависимую сигнальную систему, осуществляющую регуляцию метаболизма клеток. В связи с этим, можно предположить, что радиационно-индуцированное изменение функционирования цАМФ-зависимой сигнальной системы в тромбоцитах может приводить к искажению клеточных ответов на воздействие нейрогуморальных сигналов. В результате этого возможны проявления дис-координации биохимических и физиологических процессов, возникновение внутриклеточных повреждений, оказывающих влияние на способность тромбоцитов к агрегации и адгезии, а, кроме того - инициированию их гибели.
Заключение
Экспериментальные данные, полученные в работе, свидетельствуют о том, что общее внешнее воздействие Y -излучения на организм овец в дозах от сублетальной до летальной вызывает пострадиационные изменения активности аденилатциклазы в тромбоцитах. Изменения активности аденилатциклазы в ранние сроки могут быть инициированы радиационно-индуцированной модификацией структурно-функционального состояния плазматических мембран исследованных клеток и нарушением функционирования мембраносвязанной цАМФ-зави-симой сигнальной системы. Изменение активности фермента на 7-10-е сут, по-видимому, связано с выходом в кровь новых клеток тромбоцитов из пула мегакариоцитов костного мозга с качественно иными свойствами.
Результаты выполненных исследований дополняют современные представления о характере формирования радиационного ответа при облучении в высоких дозах, могут быть полезными при прогнозировании последствий пострадиационных нарушений.
Список литературы Оценка активности аденилатциклазы в тромбоцитах овец после внешнего воздействия G-излучения в различных дозах
- Авдонин П.В., Кожевникова Л.М. Регуляция экспрессии и функциональной активности аденилатциклазы //Биологические мембраны. 2007. Т. 24, № 1. C. 4-31.
- Whitefield J.F., Bounton A.L., Macmanus J.P., Korska M., Tsang B.K. The regulation of cell proliferation by calcium and cyclic AMP //Mol. Cell Biochem. 1979. V. 27. P. 155-179.
- Green D.R. Overview: apoptotic signaling pathways in the immune system //Immunol. Rev. 2003. V. 193. P. 5-9.
- Орловская И.А., Козлов В.А., Топоркова Л.Б. Внутриклеточные сигнальные системы в регуляции апоптоза эритроидных клеток //Иммунология. 2006. Т. 27, № 5. С. 312-316.
- Шатурный В.И., Шахиджанов С.С., Свешникова А.Н., Пантелеев М.А. Активаторы, рецепторы и пути внутриклеточной сигнализации в тромбоцитах крови //Биомедицинская химия. 2014. Т. 60, № 2. С. 182-200.
- Minetti G., Low P.S. Erythrocyte signal transduction pathways and activates adenylate cyclase in human erythrocyte membrane at physiological calcium plasma concentrations //Blood Cells Mol. Dis. 1997. V. 263. P. 223-228.
- Муравьёв А.В., Кошелев В.Б., Фадюкова О.Е., Тихомирова И.А., Маймистова А.А., Булаева С.В. Роль активации аденилатциклазной системы эритроцитов в изменении микрореологических свойств их мембран //Биологические мембраны. 2011. Т. 28, № 3. С. 174-180.
- Кудряшов Ю.Б. Радиационная биофизика (ионизирующие излучения). М.: Физматлит, 2004. 448 c.
- Чубанов В.С., Рогов Ю.И., Конопля Е.Ф., Шолух М.В. Функциональное взаимодействие компонентов аденилатциклазной системы печени крыс после пренатального воздействия -излучения //Радиационная биология. Радиоэкология. 1999. Т. 39, № 4. С. 394-398.
- Щукин В.М. Метаболизм циклических нуклеотидов в лимфоидных органах жвачных животных при внешнем и внутреннем радиационном воздействии: автореф. дисс… канд. биол. наук. М.: Московская государственная академия ветеринарной медицины и биотехнологии им. К.И. Скрябина, 2000. 18 с.
- Шевченко Т.С., Коноплева И.В. Активность аденилатциклазы в лимфоцитах и тромбоцитах облучённого крупного рогатого скота //Сельскохозяйственная биология. 2011. № 2. С. 63-67.
- Шевченко Т.С., Кобялко В.О. Активность системы цАМФ в лимфоцитах и тромбоцитах овец при действии внешнего гамма-излучения in vivo //Радиационная биология. Радиоэкология. 2015. Т. 55, № 4. С. 411-419.
- Шевченко Т.С., Коноплева И.В. О внешнем воздействии гамма-излучения на активность аденилатциклазы в клетках крови овец //Сельскохозяйственная биология. 2015. Т. 50, № 4. С. 495-502.
- Шевченко Т.С. Динамика активности аденилатциклазы в лимфоцитах коров при общем внешнем воздействии гамма-излучения //Проблемы биологии продуктивных животных. 2016. № 3. С. 65-74.
- Шевченко Т.С., Кобялко В.О. Оценка активности аденилатциклазы в лимфоцитах овец после общего внешнего воздействия гамма-излучения в различных дозах //Радиационная биология. Радиоэкология. 2017. Т. 57, № 2. С. 171-178.
- Физиологические, биохимические и биометрические показатели нормы экспериментальных животных. Справочник. СПб: Изд-во «ЛЕМА», 2013. 116 с.
- Шевченко Т.С. Выделение клеточных популяций из периферической крови сельскохозяйственных животных //Сельскохозяйственная биология. 2007. № 6. С. 123-126.
- Шевченко А.С. Определение активности ферментов метаболизма циклического аденозинмонофосфата в клетках крови овец и лошадей //Сельскохозяйственная биология. 1988. № 6. С. 124-125.
- Бурлакова Е.Б., Аткарская М.В., Фаткуллина Л.Д., Андреев С.Г. Радиационно-индуцированные изменения структурного состояния мембран клеток крови человека //Радиационная биология. Радио-экология. 2014. Т. 54, № 2. С. 162-168.
- Мазуров А.В. Физиология и патология тромбоцитов. М.: Литерра, 2011. 480 с.


