Оценка факторов закрытия гемодинамически значимого функционирующего артериального протока у новорожденных с очень низкой и экстремально низкой массой тела на фоне медикаментозного лечения препаратом педеа
Автор: Савченко Ольга Анатольевна, Кривцова Людмила Алексеевна
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: Клинические исследования
Статья в выпуске: 4 т.28, 2013 года.
Бесплатный доступ
Гемодинамически значимый функционирующий артериальный проток (ГЗ ФАП) - основная патология глубоко недоношенных детей, определяющая прогноз для жизни и процент перинатальных осложнений в раннем неонатальном периоде. С момента регистрации в октябре 2008 г. Фармкомитетом РФ раствора ибупрофена для внутривенного введения (препарат Педеа производства фирмы “Orphan Europe”) определена тактика раннего медикаментозного закрытия ГЗ ФАП. Однако данный препарат эффективен не у всех новорожденных с ОНМТ и ЭНМТ, нуждающихся в коррекции данного состояния. В статье описаны результаты медикаментозного лечения новорожденных с ЭНМТ и ОНМТ с ГЗ ФАП. Определены прогностические факторы, влияющие на эффективность закрытия артериального протока на фоне медикаментозного лечения препаратом Педеа.
Факторы закрытия гемодинамически значимого функционирующего артериального протока, недоношенные новорожденные с очень низкой и экстремально низкой массой тела, раствор ибупрофена для внутривенного введения (препарат педеа), эхокардиография
Короткий адрес: https://sciup.org/14919896
IDR: 14919896 | УДК: 616.131.3-053.32-036+615.225
Factors of closing of the hemodynamically significant patent ductus arteriosus in newborn babies with extremely low body weight receiving drug therapy with pede
Hemodynamically significant patent ductus arteriosus (HSPDA) is a main pathology in the prematurely born babies determining prognosis of life and complication rate in the early neonatal period. From the moment of the registration of ibuprofen solution for the intravenous use (Pede, Orphan Europe) by the Russian Pharmacology Committee in October, 2008, the tactics of the early pharmacological closing of HSPDA was developed. However, Pede is efficacious only in a part of newborns with very low body weight (VLBW) and extremely low body weight (ELBW) requiring correction of HSPDA. The article presents results of drug therapy in newborn babies with VLBW and ELBW and HSPDA. The study determined the prognostic factors affecting efficacy of ductus arteriosus closing during drug therapy with Pede.
Текст научной статьи Оценка факторов закрытия гемодинамически значимого функционирующего артериального протока у новорожденных с очень низкой и экстремально низкой массой тела на фоне медикаментозного лечения препаратом педеа
Внедрение современных перинатальных технологий в практическое здравоохранение и широкое использование методов интенсивной терапии в лечении недоношенных новорожденных привело к существенному увеличению выживаемости детей с очень низкой (ОНМТ) и экстремально низкой массой тела (ЭНМТ). Прогноз их жизни и здоровья стали определять не только респираторные, но и гемодинамические нарушения, обусловленные функционирующим гемодинамически значимым артериальным протоком (ГЗ ФАП).
ГЗ ФАП негативно воздействует на легочную ткань путем перегрузки малого круга кровообращения и нарушения механики легких. Такие дети требуют длительной искусственной вентиляции легких (ИВЛ), а это фактор риска формирования бронхолегочной дисплазии. При ГЗ ФАП происходит обкрадывание мезентериального кровотока и гипоперфузия желудочно-кишечного тракта, что является фактором риска формирования некротизирующего энтероколита. Выраженная флюктуация мозгового кровотока и снижение конечной диастолической и средней скорости кровотока приводит к внутрижелудочковым кровоизлияниям и опасности перивентрикуляр-ной лейкомаляции. Мы не можем сказать, что ГЗ ФАП – единственная причина данных заболеваний, исходя из того, что эти заболевания многофакторные. ГЗ ФАП, скорее всего, выступает маркером тяжести их течения [2, 4, 5, 9, 10].
В нашей стране до недавнего времени отсутствовали единые диагностические и терапевтические подходы в отношении открытого артериального протока (ОАП) у недоношенных новорожденных. Не было официально зарегистрированных препаратов для медикаментозного закрытия. Хирургическая коррекция повышала риск невропатологических исходов и тяжелой ретинопатии недоношенных [11].
С момента регистрации в октябре 2008 г. Фармкоми-тетом РФ раствора ибупрофена для внутривенного введения (препарат Педеа производства фирмы “Orphan Europe”) и разработки протокола ведения новорожденных с ГЗФАП появилась возможность раннего медикаментозного закрытия ГЗФАП и тем самым снижения процента перинатальных осложнений и числа хирургической коррекции, вызванных данным состоянием [1]. Однако медикаментозная терапия связана с побочными эффектами, обусловленными фармакодинамикой препарата, а также отсутствием эффекта на терапию у некоторой категории новорожденных [5]. Поиск предикторов, влияющих на эффективность закрытия ГЗФАП на фоне терапии препаратом Педеа, активно ведется за рубежом. Известны попытки установить связь между эффективностью Педеа и уровнем натрийуретического гормона как предиктора левожелудочковой дисфункции, следовательно, и тяжести гемодинамических нарушений [16], низким гестационным возрастом и массой тела при рождении [13], женским полом ребенка [12], ролью этнической принадлежности [3] и диаметром протока [6]. Следовательно, актуальным на сегодняшний день является поиск факторов, влияющих на закрытие протока, что позволит индивидуализировать подход к медикаментозной терапии ГЗ ФАП у глубоко недоношенных детей.
Цель: определение прогностических факторов, влияющих на эффективность закрытия ГЗФАП у новорожденных с ЭНМТ и ОНМТ на фоне медикаментозного лечения препаратом Педеа.
Материал и методы
Под нашим наблюдением находился 41 новорожденный ребенок, родившийся с массой тела менее 1500 г, из них с массой тела менее 1000 г – 28 детей (68,3%). Гестационный возраст детей составлял 23–30 недель. Дети находились на лечении в отделении реанимации и интенсивной терапии новорожденных БУЗОО “Клинический родильный дом №1” (Омск). У всех детей проводился анализ данных материнского анамнеза, состояния ребенка после рождения, течения раннего неонатального периода, оценивались данные клинического осмотра, инструментальных методов исследования (нейросоно-графия, эхокардиография), лабораторных исследований. Эхокардиографическое (ЭхоКГ) исследование проводилось всем новорожденным в течение первых 48 ч после рождения аппаратом “LOGIQ book XP” c микроконвекс-ными датчиками частотой сканирования 5 МГц в соответствии с рекомендациями фирмы-производителя. Всем детям был диагностирован ГЗФАП. Критерии значимости протока устанавливались по ЭхоКГ-признакам в соответствии с протоколом [1]. После получения информированного согласия родителей, исключения жизнеугрожающего инфекционного заболевания, кровотечения в течение последних 24 ч, нарушения функции почек (креатинин более 140 мкмоль/л, мочевины более 14 ммоль/ л, диурез менее 1 мл/кг/ч), НЭК, тромбоцитопении (менее 60X109/л), геморрагического синдрома, дуктус-зави-симого врожденного порока сердца начинали курс медикаментозного лечения раствором ибупрофена для внутривенного введения (препарат Педеа) [1].
Курс терапии состоял из трех внутривенных введений препарата с интервалом между введениями 24 ч. Доза рассчитывалась в зависимости от массы тела: 1-я инъекция – 10 мг/кг, а 2 и 3-я инъекции – 5 мг/кг. Вводился препарат в виде короткой инфузии в течение 15 мин в неразведенном виде, при этом введение других препаратов, включая энтеральное питание, прекращалось. Через 48 ч после последней инъекции (6-е сутки жизни) проводилось ЭхоКГ-исследование, по результатам которого все дети были разделены на две группы. Группа А – ГЗ ФАП закрылся под воздействием препарата Педеа, группа В – ГЗ ФАП не закрылся под воздействием препарата Педеа.
Материалы исследований подвергнуты статистической обработке с помощью пакета прикладных программ STATISTICA 6.1 (лицензионное соглашение BXXR904Е306823FAN10). Проверка нормальности распределения количественных признаков проведена с помощью критерия Шапиро–Уилка. Значения признаков ввиду наличия распределения, отличного от нормального, представлены в тексте в виде Me [QU; QL], где Me – медиана, QU – нижний квартиль, QL – верхний квартиль. Проверка статистических гипотез осуществлялась путем выявления различий между сравниваемыми группами с применением критерия хи-квадрат, U-критерия Манна– Уитни (сравнение двух независимых переменных). Направление и силу связи между явлениями определяли с помощью коэффициента Спирмена. Если rs находился в пределах от 0 до +0,3 или –0,3, то такую связь расценивали как слабую. Связь от +0,3 до +0,7 или от –0,31 до –0,7 считалась средневыраженной. Коэффициент корреляции от +0,71 до +1,0 или от –0,71 до –1,0 свидетельствовал о наличии сильной прямой либо сильной обратной (отрицательной) связи между сопоставляемыми признаками.
При построении прогностических моделей использовали многофакторный логистический регрессионный анализ (методика со свободным членом – B0). Приемлемый уровень значимости для статистики Вальда полученных в ходе регрессионного анализа свободного члена и коэффициентов уравнения логит-регрессии составлял от 5 до 15%. Во всех процедурах статистического анализа критический уровень значимости р принимался равным 0,05.
Результаты и обсуждение
По результатам исследования было выявлено, что в группу А вошли 33 новорожденных (80,5%), в группу В – 8 детей (19,5%). Дети в сравниваемых группах были сопоставимы по полу (в группе А девочек – 45,5%, в группе В – 50,0%; р=0,467). На фоне медикаментозного лечения в группе В по сравнению с группой А отмечалась более низкая масса тела при рождении (соответственно 850 и 990, р=0,037) и срок гестации (соответственно 26 и 27 недель, р=0,036), таблица 1. Незакрытие протока на фоне применения препарата Педеа коррелирует с малым гестационным возрастом (rs=+0,344; p=0,027) и массой тела при рождении (rs=+0,33s2; p=0,034).
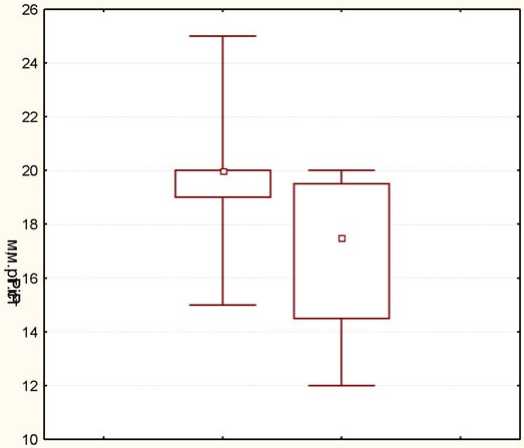
Группы
□ Median □ 25%-75% Min-Max
Рис. 1. Пиковое давление на вдохе (PiP) в 1-е сутки жизни у детей с закрывшимся (группа А) и незакрывшимся (группа В) ГЗФАП на фоне терапии препаратом Педеа
дистресс-синдрома новорожденных получили 23 (79%) матери детей группы А, и 4 (33%) матери детей группы В. В результате терапия кортикостероидами была в большей мере проведена у матерей детей, вошедших в группу А (х2=7,98), р=0,004. Кортикостероиды не только уменьшают тяжесть дыхательных нарушений, но и стимулируют выработку кортизола у новорожденного, который снижает синтез простагландинов, что в свою очередь способствует констрикции протока [14]. Таким образом, антенатальное применение кортикостероидов является фактором, повышающим эффективность препарата Педеа при закрытии артериального протока.
Состояние детей при рождении расценивалось как тяжелое либо крайне тяжелое за счет дыхательных нарушений (тахипное, ослабленное неравномерное дыхание, рассеянная крепитация, бледность/цианоз кож
Анализ анамнестических данных показал, что соматический и акушерско-гинекологический анамнез был отягощен у матерей детей обеих групп в равной степени и не являлся фактором, определяющим эффективность медикаментозного лечения ГЗ ФАП.
Курс глюкокортикоидов (дексаметазон, бетаметазон) с целью антенатальной профилактики респираторного
Таблица 1
Сравнение исследуемых групп по массе тела, сроку гестации и полу
На основании полученных данных было бы ошибочно утверждать, что значение Pip является фактором не-закрытия протока на фоне препарата Педеа. Низкие показатели PiP у новорожденных группы В не могут отображать истинной ситуации и говорить о менее тяжелых дыхательных нарушениях при рождении. PiP сопряжен с дыхательным объемом, который напрямую зависит от массы тела при рождении, а в группу В в сравнении с группой А вошли новорожденные с более низкой массой тела.
Мониторинг артериального давления показал, что на
Таблица 2
Результаты сравнения артериального давления на 2-е сутки жизни групп детей, получавших препарат Педеа
|
Показатели |
Статистические параметры |
Группа А, n=33 |
Группа В, n=8 |
U** |
p |
|
САД (мм рт. ст.) |
Median [Q25–Q75] |
55 [48;60] |
48 [42,5;51] |
68 |
0,035* |
|
ДАД (мм рт. ст.) |
Median [Q25–Q75] |
29 [24;32] |
18,5 [16,5;24] |
31 |
0,001* |
|
АД среднее (мм рт. ст.) |
Median [Q25–Q75] |
26 [25;28] |
27 [24;27,5] |
119,5 |
0,068 |
|
Систолодиастолич. разница (мм рт. ст.) |
Median [Q25–Q75] |
38 [32;41] |
29 [25;57] |
106 |
0,392 |
Примечание: * – статистически значимые отличия между группами (p<0,05); ** – сравнение двух независимых групп критерием Манна–Уитни.
2-е сутки жизни (до введения препарата Педеа) у детей, вошедших в группу В, отмечались более низкие в сравнении с группой А показатели артериального давления, что может являться фактором незакрытия протока (табл. 2).
С целью установления предикторов закрытия протока на фоне медикаментозной терапии проведена обработка полученных данных с использованием логистического регрессионного анализа и построена математическая модель расчета вероятности закрытия ГЗФАП на фоне медикаментозной терапии. В ходе проведенного анализа установлено, что предикторами закрытия ГЗФАП являются масса тела при рождении (p=0,017), систолическое (p=0,013) и диастолическое (р=0,000) артериальное давление на 2-е сутки жизни (табл. 3).
Было получено стандартное уравнение регрессии следующего вида:
¥=18321 -97732X1 — 0,0288X2 - 0,3571X3, где:
C1 – масса тела при рождении, кг;
С2 – систолическое артериальное давление, мм рт. ст.;
С3 – диастолическое артериальное давление, мм рт. ст.
Подставив значения переменных, влияющих на исход (масса тела при рождении, показатели систолического и диастолического артериального давления), получаем значение Y, характеризующее данную модель.
Для вычисления вероятности незакрытия протока было получено следующее уравнение, описывающее данную модель:
Р=[1/(1+е=)] *100
Р – риск незакрытия протока, %;
е – основание натурального логарифма (е=2,71);
Y – стандартное уравнение регрессии.
Отношение шансов рассчитывается по формуле:
0Ш=р/(1-р)
Поясним расчет оценки вероятности незакрытия ГЗФАП на фоне терапии препаратом Педеа на клинических примерах.
Пример 1: Масса тела при рождении 0,6 кг, показатели систолического артериального давления 49 мм рт. ст., диастолического – 19 мм рт. ст. на 2-е сутки жизни. Подставим данные в уравнение, получим:
18,321–9,77321*0,6–0,02881*49–0,35712*19=
=18,12–5,8639–1,4117–6,7853=4,0591 (значение Y) Р=[1/(1+e-y)] *100=98,1%, т.е при таких исходных данных уравнение логистической регрессии оценивает вероятность незакрытия ГЗФАП – 0,981(98,1%), а величина ОШ – 52,63.
В нашем исследовании установлено, что чем ниже значения артериального давления на 2-е сутки жизни (до начала терапии препаратом Педеа) и масса тела при рождении, тем выше риск неэффективности медикаментозной терапии препаратом Педеа в закрытии ГЗФАП.
Список литературы Оценка факторов закрытия гемодинамически значимого функционирующего артериального протока у новорожденных с очень низкой и экстремально низкой массой тела на фоне медикаментозного лечения препаратом педеа
- Дегтярев Д.Н. и др. Протокол ведения недоношенных детей с гемодинамически значимым функционирующим артериальным протоком/под ред. Н.Н. Володина, Е.Н. Байбариной. -М., 2009. -34 с.
- Николаева Г.В., Бабак О.А., Милева О.И. Влияние открытого артериального протока на развитие ретинопатии у недоношенных детей//Рос. педиатр. офтальмология. -2010. -№ 2. -С. 11-13.
- Durrmeyer X.et al. Are cytochrome P450 CYP2C8 and CYP2C9 polymorphisms associated with ibuprofen response in very preterm infants?//PLoS One. -2010. -Vol. 5, No. 8. -P. 123-129.
- Dollberg S., Lusky A., Reichman B. Patent ductus arteriosus indomethacin and necrotizing enterocolitis in very low birth weight infants: a population-based study//J. Pediatr. Gastroenterol. Nutr. -2005. -Vol. 40, No. 2. -P. 184-188.
- Tauzin L. et al. Influence of persistent ductus arteriosus of mortality and morbidity in very low birth weight infants//Acta Paediatr. -2012. -Vol. 101, No. 4. -P. 419-423.
- Tauzin L. et al. Effect of persistent patent ductus arteriosus on mortality and morbidity in very low-birthweight infants//Acta Paediatr. -2012. -Vol. 101, No. 4. -P. 419-423.
- Dani C. et al. Fate of the ductus arteriosus in children at 23-27 weeks of gestation: from spontaneous closure to ibuprofen resistance//Acta Paediatr. -2008.-Vol. 97, No. 9. -P. -1176-1180.
- Gagliardi L. et al. Necrotising enterocolitis in very low birth weight infants in Italy: incidence and non-nutritional risk factors//J. Pediatr. Gastroenterol. Nutr. -2008. -Vol. 47, No. 2. -P. 206-210.
- Bertino E. et al. Necrotizing enterocolitis: risk factor analysis and role of gastric residuals in very low birth weight infants//J. Pediatr. Gastroenterol. Nutr. -2009. -Vol. 48, No. 4. -P. 437-442.
- Kabra N.S. et al. Neurosensory impairment after surgical closure of the ductus arteriosus in extremely low birth weight children: results from the Trial of Indomethacin Prophylaxis in Preterms//J. Pediatr. -2007. -Vol. 150, No. 3. -P. 229-234.
- Popat H., Kapoor V., Travadi J. Ductus arteriosus in infants №29 weeks of gestation -the results and the factors affecting the closure//Indian Pediatr. -2012. -Vol. 49, No. 8. -P. 615-620.
- Katakam L.I. et al. Safety and efficacy compared with indomethacin ibuprofen for treatment of patent ductus arteriosus//Am. J. Perinatol. -2010. -Vol. 27, No. 5. -P. 425 -429.
- Eronen M. et al. The effect of antenatal dexamethasone administration on the fetal and neonatal ductus arteriosus. A randomized double-blinded study//Am. J. Dis. Child. -1993. -Vol. 147, No. 2. -P. 187-192.
- Shimada S. et al. Treatment of patent ductus arteriosus after exogenous surfactant in baboons with hyaline membrane disease//Pediatr. Res. -1989. -Vol. 26, No. 5. -P. 565-569.
- Czernik C. et al. Urinary NT-proBNP and ductal closure in preterm infants//J. Perinatol. -2013. -Vol. 33, No. 3. -P. 212-217.


