Оценка эффективности гемофильтрации у пациентов с панкреонекрозом
Автор: Буткевич А.Ц., Истратов В.Г., Бровкин А.Е., Наливайский А.А., Рябков М.Г.
Журнал: Московский хирургический журнал @mossj
Рубрика: Клинические исследования
Статья в выпуске: 4 (38), 2014 года.
Бесплатный доступ
В условиях развития полиорганной недостаточности патогенетически обоснованным является проведение эфферентной терапии, направленной на элиминацию эндогенных токсических субстанций из организма; детоксикационная терапия - важнейшая часть комплексной терапии острого дестуктивного панкреотита. В настоящее время наиболее перспективным способом экстракорпоральной коррекции гомеостаза и деток- сикации представляется использование продленной вено-венозной гемофильтрации. Нами проводилась ПВВГФ в двух режимах: низкопоточной и высокопоточной гемофильтрации. Низкопоточную ПВВГФ осуществляли у наиболее тяжелых пациентов (часто с нестабильной гемодинамикой) на аппаратах Prisma (GAMBRO DASCOS. р. А., Via Modene, Italy) с использованием гемофильтров GAMBRO (Polyflux 21) и замещающего раствора Prismasol. Нами установлено, что прогрессивно увеличивающийся уровень мочевины объективно отражает прогностически неблагоприятный исход в течение заболевания у пациентов с нарастающей ПОН. Напротив, раннее начало сеансов гемофильтрации у пациентов с низкими значениями почечных шлаков более благоприятно отражается на степени выраженности полиорганных нарушений. Таким образом, проведение экстракорпоральной детоксикации на начальных стадиях заболевания, при отсутствии явлений выраженной ПОН, благоприятно влияет на прогноз и исход заболевания.
Острый деструктивный панкреатит, токсические метаболиты, экстракорпоральная детоксикация
Короткий адрес: https://sciup.org/142211173
IDR: 142211173 | УДК: 616-089;
Текст научной статьи Оценка эффективности гемофильтрации у пациентов с панкреонекрозом
В настоящее время нет единого подхода к консервативной терапии панкреонекроза: в различных клиниках, в разные периоды происходил неоднократный пересмотр тактики ведения больных с панкреонекрозом (ПН) [1]. Несмотря на развитие современной медицины, методов диагностики и лечения, сохраняются высокий уровень летальности при тотальных и субтотальном ПН и частота осложнений, приводящих к гибели пациента [2, 3, 4, 5, 6].
Основными задачами базисной терапии является: адекватное обезболивание, блокада секреции поджелудочной железы (ПЖ) (создание функционального покоя), дезинтоксикация, улучшение периферического кровообращения, коррекция волемических нарушений, водно-электролитных расстройств и КЩС, профилактика вторичных инфекци- онных осложнений, коррекция дыхательной, сердечнососудистой, печеночно-почечной недостаточности. Необходимым условием лечения является проведение данной терапии в условиях отделения реанимации (ОРИТ), для динамического контроля лабораторных показателей и непрерывной коррекции гомеостаза.
Течение тяжелого острого деструктивного панкреатита (ОДП), всегда связанно с различными по тяжести проявлениями полиорганной недостаточности (ПОН), вследствие прогрессирования эндогенной интоксикации. «Ранние» токсемические и «поздние» септические осложнения ОДП по-прежнему остаются основной причиной смерти у наиболее тяжелой категории больных [7].
В условиях развития ПОН патогенетически обоснованным является проведение эфферентной терапии, направленной на элиминацию эндогенных токсических субстан- ций из организма; детоксикационная терапия – важнейшая часть комплексной терапии ОДП. В настоящее время наиболее перспективным способом экстракорпоральной коррекции гомеостаза и детоксикации представляется использование продленной вено-венозной гемофильтрации (ПВВГФ) [8, 9, 10].
Цель исследования: определение уровня токсических метаболитов анаэробной неклостридиальной инфекции (АНИ) при ОДП для оценки эффективности комплексной терапии при включении в лечение методов экстракорпоральной детоксикации.
Диагностику метаболитов АНИ осуществляли методом газожидкостной хроматографии и масс-спектрометрии (ГХ–МС), позволяющим в различных средах организма пациента идентифицировать летучие жирные кислоты (ЛЖК) – пропионовую, изомасляную, масляную; токсические метаболиты (ТМ) группы фенолов, крезолов и др., которые являются специфическими конечными продуктами метаболизма анаэробных бактерий [11].
Материал и методы
Проведено исследование 78 больных ОДП, разделенных на 2 группы пациентов: первая группа – 58 больных стерильным панкреонекрозом (СПН), вторая группа – 20 пациентов с инфицированным панкреонекрозом (ИПН). Оценку тяжести состояния больных при поступлении осуществляли с помощью интегральных шкал Арасне II, Ranson и SAPS. Результаты бальной оценки пациентов по указанным шкалам балльной оценки при поступлении представлены в таблице 1.
В группе пациентов со СПН у 7 больных (12,1%) в связи с нарастанием выпота в брюшной полости была выполнена видеолапароскопия, санация и дренирование брюшной полости. В дальнейшем в ОРИТ проводили консервативное лечение, включающее в себя антибактериальную терапию (карбапенемы) в максимальных дозировках, блокаторы секреции ПЖ (октреотид), массивную инфузионную терапию, экстракорпоральные методы детоксикации.
Все пациенты с ИПН оперированы в различные сроки. Объем оперативного вмешательства зависел от тяжести со-
Таблица 1
Средний балл оценки состояния пациентов с панкреонекро-зом по разным прогностическим шкалам
В настоящее время ПВВГФ осуществляется при помощи насосной технологии (рис. 1) с использованием высокопроницаемого фильтра [12]. Кровь обычно поступает из центральной (чаще подключичной) вены по 2-просветному катетеру (рис. 2) в фильтр, где за счет создания гидравлического градиента давления происходит процесс конвекции, во время которой происходит движение веществ через полупроницаемую мембрану фильтра, что идентично процессу гломерулярной фильтрации (рис. 3).
Потери жидкости при гемофильтрации должны быть замещены раствором, содержащим необходимые электролиты. Поскольку высокопористые синтетические мембраны (из полисульфона, полиамида, полиакрилнитрила и др.),
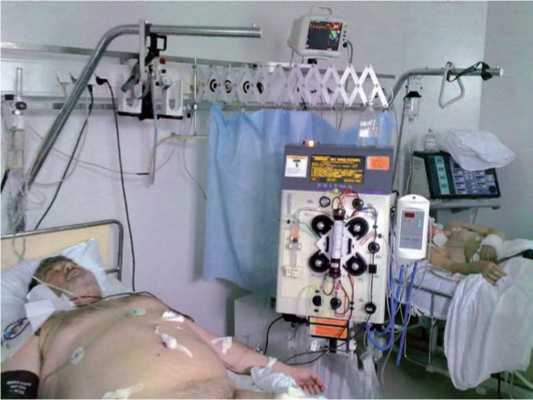
Рис. 1. Больной Б. Проводится низкопоточная ПВВГФ на аппарате Prisma (гемофильтр АN-69, скорость кровотока 120 - 140 мл/мин)
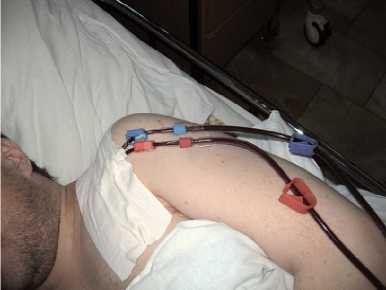
Рис. 2. Катетеризация подключичной вены двухпросветным катетером для проведения ПВВГФ
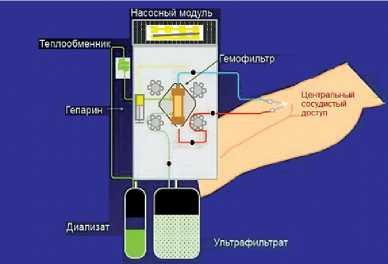
Рис. 3. Схематическое изображение процесса ПВВГФ используемые при гемофильтрации, в отличие от мембран, применяемых в гемодиализе (проницаемость до 30000 D), имеют гораздо больший коэффициент просеивания для средних молекул, то достигается их адекватный клиренс. Производительность фильтра зависит от гидравлической проницаемости мембраны, площади эффективной поверхности, а также от коллоидно-осмотического давления крови, гематокрита, сопротивления экстракорпорального контура, трансмембранного давления и скорости кровотока.
Возмещение ультрафильтрата производится стерильными пакетированными растворами (4,5 л) с осмолярностью от 286 до 320 мосм/л, содержащими лактатный или бикар-бонатный буфер для ощелачивания крови. Нужно отметить, что скорость удаления жидкости может быть сравнительно высока (например, до 9 л/ч). Замещающий раствор можно вводить в артериальную линию крови до гемофильтра (предилюция) или в венозную линию (постдилюция). Объем замещения за один сеанс гемофильтрации составляет от 14 до 60 литров.
Нами применяется введение замещающего раствора после гемофильтра (post-dilution). Гепаринизацию проводим под контролем времени активированного свертывания 150 ЕД гепарина на 1 кг массы тела больного.
Немаловажным является вопрос о минимальном объеме возмещения ультрафильтрата и частоте проведения гемофильтрации. Принято считать, что объем воды в теле пациента составляет около 60% массы тела (приблизительно 40% составляет внутриклеточная жидкость и 20% – внеклеточная). При средней массе в 80 кг полный дренаж внутриклеточного и внеклеточного пространства составляет 48 литров (80×0,6 = 48 л). По данным многих исследователей, приближение уровня средних молекул к физиологической норме происходит при объеме замещения 25 литров [13].
По нашим данным, достаточно проведения интермиттирующей гемофильтрации в объеме 18–22,5 л в течение суток ежедневно. Необходимо отметить, что ведение пациентов с ОДП, осложненным ПОН, в условиях реанимационного отделения требует прове- дения массивной инфузионной терапии, что в свою очередь может привести к синдрому гипергидратации, вплоть до развития отека легких. Интермиттирующая гемофильтрация на сегодняшний день – один из самых эффективных методов борьбы с неконтролируемой гипергидратацией, который позволяет за довольно короткий период времени (2–3 часа) решить эту проблему.
Нами проводилась ПВВГФ в двух режимах: низкопоточной и высокопоточной гемофильтрации. Низкопоточную ПВВГФ осуществляли у наиболее тяжелых пациентов (часто с нестабильной гемодинамикой) на аппаратах Prisma (GAMBRO DASCOS. р. А., Via Modene, Italy) с использованием гемофильтров GAMBRO (Polyflux 21) и замещающего раствора Prismasol. Среднее время каждой процедуры при низкопоточной гемофильтрации со скорость кровотока 120–180 мл/мин составляло 12–14 часов; максимальный объем замещения – 1500 мл/час, всего до 24000 мл в сутки.
Высокопоточную гемофильтрацию проводили у более стабильных больных на аппаратах Аquarius (Edvards, USA) в течение 6–8 часов, со скоростью кровотока до 200 мл/мин, с максимальным объемом замещения до 3000 мл/час, всего до 24000 мл за время процедуры. Ряду пациентов выполняли сеансы плазмафереза на аппарате PCS2, фирмы Haemonetics (USA).
Среднее количество процедур ПВВГФ, проведенное пациентам с ОДП, было различным (табл. 2). Отмечено, что развитие острой почечной недостаточности (ОПН) более выражено у пациентов с ИПН. Более позднее начало проведение процедур пациентам ИПН часто связано с их более тяжелым состоянием, невозможностью провеждения процедуры после оперативного вмешательства на фоне гемокоагуляционных расстройств и опасности развития ДВС-синдрома.
Несмотря на проводимую интенсивную терапию, от прогрессирующей ПОН и панкреатогенного шока умерло 2 пациента со СПН (летальность – 3,4%); в группе больных ИПН умерло 9 (послеоперационная летальность – 45%).
Результаты
Одной из самых частых причин высокой летальности у пациентов с различными формами ПН является разви-
Таблица 2
Применение методов экстракорпоральной детоксикации при панкреонекрозе
|
Масштаб панкреонекроза |
Гемофильтрация |
|||
|
Группа СПН |
Группа ИПН |
Число больных |
Среднее Кол-во процедур |
|
|
Мелкоочаговый |
30 |
2 |
23 |
5 |
|
Крупноочаговый |
18 |
10 |
13 |
- |
|
Субтотально- |
- |
- |
- |
7 |
|
тотальный |
10 |
8 |
7 |
|
|
ВСЕГО: |
58 |
20 |
22 |
5 |
вающаяся панкреатогенная токсемия и ПОН как на ранних, так и на более поздних стадиях заболевания [15]. Нами при помощи ГХ–МС были выделены токсические метаболиты группы фенолов и крезолов, объективно отражающие тяжесть ПОН и связанной с ней ОПН. Высокий уровень летальности в группе пациентов с ИПН связан с обширностью поражения ПЖ, забрюшинной клетчатки, часто молниеносным течением заболевания с развитием тяжелого панкреатогенного шока и ПОН. В частности, развитие тяжелой острой почечной недостаточности (ОПН) значительно ухудшало прогноз течения заболевания, несмотря на проводимые сеансы гемофильтрации.
Динамика изменений уровня фенолов и крезолов в ходе проводимого лечения пациентов со СПН отражает эффективность детоксикации (рис. 4). У пациентов с ИПН отмечен исходно более высокий уровень данных метаболитов, что объясняется более тяжелой степенью проявления ПОН (рис. 5).
Повышенное значение ТМ (фенолов и крезолов) у пациентов с ПН находит свое отражение в развитии ОПН и сопровождается повышением уровня мочевины (в среднем 6,8±1,5) и креатинина (в среднем 114,9±0,5) у пациентов
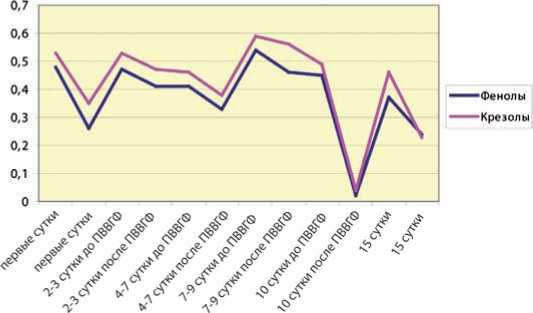
Рис. 4. Динамика колебаний фенолов и крезолов в плазме пациентов со СПН на фоне ПВВГФ (ммоль/л)
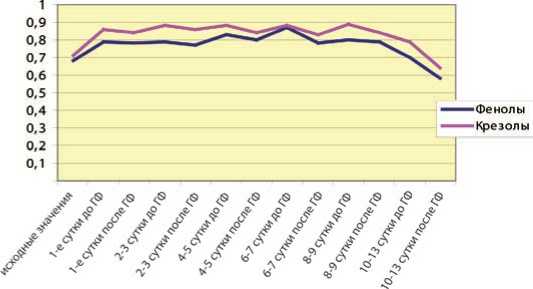
Рис. 5. Динамика колебаний фенолов и крезолов в плазме пациентов с ИПН на фоне ПВВГФ (ммоль/л)
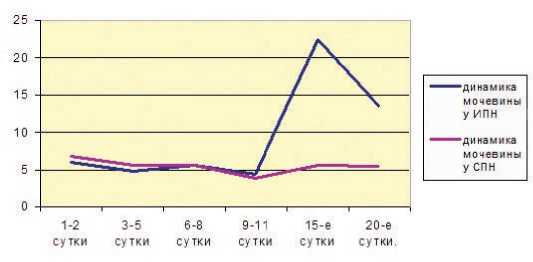
Рис. 6. Динамика колебаний мочевины у больных со СПН и ИПН (ммоль/л)
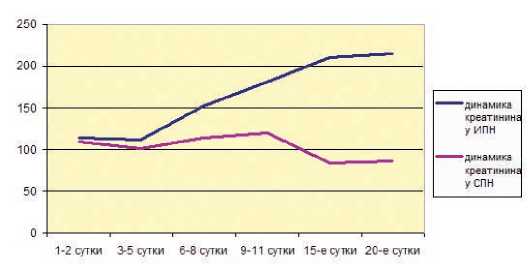
Рис. 7. Динамика колебаний креатинина у пациентов со СПН и ИПН (ммоль/л)
со СПН, и более высоким повышением мочевины (в среднем до 18,3±2 ммоль/л) и креатинина (в среднем до 215,2± ±5 ммоль/л) у больных с ИПН (рис. 6, 7).
Выявлены различные значения ТМ группы фенолов и крезолов у пациентов с различным исходом заболевания (рис. 8, 9). Для объективизации тяжести состояния использовалась шкала АРАСНЕ II. У пациентов с высокой балльной оценкой отмечались высокие значения ТМ группы фенолов и крезолов. Подтверждением данных значений явились и исход заболевания у разных групп больных, и развитие ОПН как одного из важных звеньев ПОН.
Пациенты с ИПН были разделены на две группы: у пациентов первой группы отмечались исходно высокие значения уровня мочевины и креатинина на момент начала проведе-
|
Арасне II (баллы) |
Выжившие больные |
|
|
Фенолы (ммоль/л) |
Крезолы (ммоль/л) |
|
|
18 - 20 |
0,63±0,04 |
0,51± 0,09 |
|
20 - 25 |
0,71±0,03 |
0,62±0,05 |
|
25 и > |
0,78±0,03 |
0,70±0,07 |
Рис. 8. Среднее значение ТМ группы фенолов и крезолов в сыворотке крови в первые трое суток от начала лечения у пациентов со СПН ния ПВВГФ. Пациенты второй группы отличались низкими значениями мочевины и креатинина. Обеим группам пациентов проводили сеансы ультрафильтрации в различных режимах, в различные сроки от начала заболевания. Нами отмечено, что у пациентов с исходно выраженными проявлениями ОПН (высокие значения мочевины и креатинина),
|
Арасне II (баллы) |
Умершие больные |
|
|
Фенолы (ммоль/л) |
Крезолы (ммоль/л) |
|
|
18-20 |
0,67±0,04 |
0.,72±0,02 |
|
20-25 |
0,81±0,03 |
0,78±0,01 |
|
25 и > |
0,93±0,03 |
0,98±0,06 |
Рис. 9. Среднее значение ТМ группы фенолов и крезолов в сыворотке крови в первые трое суток от начала лечения у пациентов с ИПН несмотря на проведение сеансов ПВВГФ, показатели мочевины и креатинина снижаются незначительно, и степень полиорганных нарушений остается достаточно высокой (рис. 10, 11).
Нами установлено, что прогрессивно увеличивающийся уровень мочевины объективно отражает прогностически неблагоприятный исход в течение заболевания, у пациентов с нарастающей ПОН (рис. 12). Напротив, раннее начало сеансов гемофильтрации у пациентов с низкими значениями почечных шлаков более благоприятно отражается на степени выраженности полиорганных нарушений (рис. 13, 14).
Больной Б., 1952 г.р., и/б № 4101, госпитализирован в экстренном порядке 18.07.2011 после злоупотребления алкоголем с клиникой ОДП. При поступлении состояние тяжелое (АРАСНЕ-II – 21 балл). Сознание спутанное. Кожные покровы нормальной окраски. Дыхание в легких везикулярное, про-
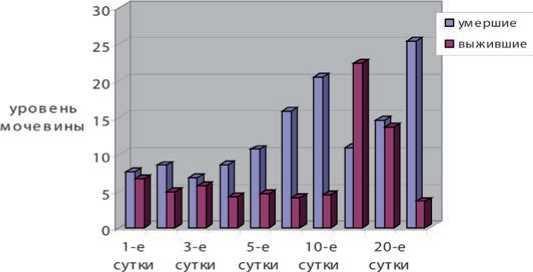
Рис. 12. Динамика концентрации мочевины в плазме пациентов с различным исходом заболевания (ммоль/л)
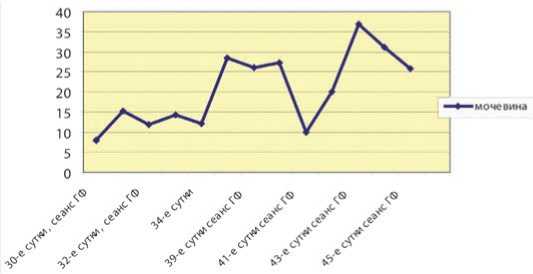
Рис. 10. Динамика колебаний мочевины в плазме пациентов с ИПН, при исходно высоких значениях (ммоль/л)
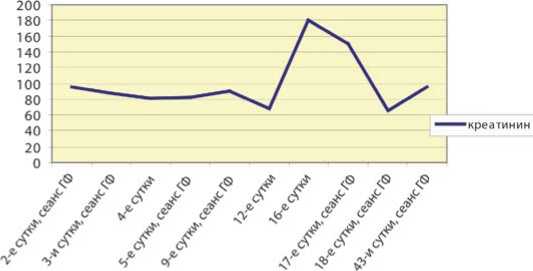
Рис. 13. Динамика концентрации креатинина в плазме пациентов с ИПН при исходно низких значениях (ммоль/л)
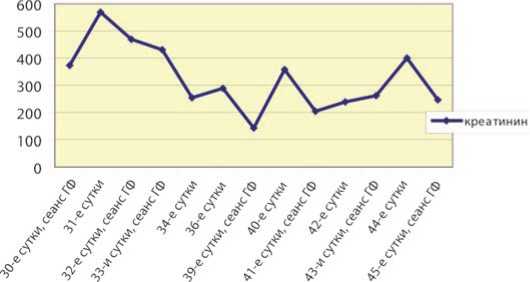
Рис. 11. Динамика колебаний креатинина в плазме пациентов с ИПН при исходно высоких значениях (ммоль/л)
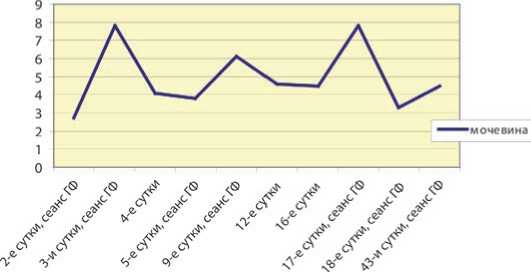
Рис. 14. Динамика концентрации мочевины в плазме пациентов с ИПН при исходно низких значениях (ммоль/л)
водится во все отделы, хрипов нет. ЧДД = 22 в мин. Ps = 120 в мин., ритмичный, удовлетворительного наполнения. АД = 140/80 мм рт. ст. Язык влажный, у корня обложен белым налетом. Живот увеличен в размерах за счет подкожной клетчатки, симметричный, участвует в акте дыхания, слегка вздут, несколько напряжен и болезненный в эпигастральной области, правом и левом подреберьях. Определяются положительные симптомы Мейо-Робсона, Воскресенского. Симптом Щеткина-Блюмберга – отрицательный. Выслушивается ослабленная перистальтика. Край печени на 1 см выступает из-под края реберной дуги. Стул и диурез без особенностей.
В клиническом анализе крови: НВ – 159 г/л; лейкоциты 25,8·10/л, амилаза крови 505 ед., мочевина – 6,0 ммоль/л; креатинин – 78 ммоль/л. Госпитализирован в ОРИТ, где проводилась интенсивная терапия, включая антибиоти-котерапию (меронем 1,0×3 раза в день в/в). Несмотря на проведение интенсивной терапии, состояние оставалось тяжелым. КТ органов брюшной полости (рис. 15): ОДП с поражением парапанкреатической клетчатки. УЗИ брюшной полости в динамике: увеличение ПЖ, нечеткость контуров, появление и нарастание количества свободной жидкости в брюшной полости, появление жидкостных скоплений в забрюшинном пространстве. 21.07.2011 выполнена лечебнодиагностическая лапароскопия: в малом тазу – мутный, желтый выпот до 200 мл, отмечаются множественные бляшки стеатонекроза на сальнике, желудок оттеснен кпереди, желчный пузырь увеличен в размерах, не напряжен. Петли тонкой кишки дилятированы, паретичны. Подпеченочное пространство и малый таз дренированы.
Несмотря на проводимую интенсивную терапию, состояние больного оставалось тяжелым, отмечалось прогрессирование ПОН: ЧДД – 25 в мин., SРО2 – 80 %; ЧСС – 100 в мин. Начато проведение экстракорпоральной детоксикации (ультрафильтрация) на аппарате Prisma с использованием гемофильтра АN-69 со скоростью кровотока 120–140 мл/мин; удалено в общей сложности 14727 мл ультрафильтрата. После окончания гемофильтрации отмечено уменьшение дыхательной недостаточности, ясное сознание. По данным ГХ-МС выявлено снижение уровня токсического метаболита – ди2бетатиэти-лальфааланин, обладающего выраженным церебротоксическим действием (рис. 16). При повторных сеансах ППВГФ отмечено снижение уровня крезолов (рис. 17).
На фоне продолженной консервативной терапии отмечена стабилизация состояния пациента, нормализация анализов. УЗИ брюшной полости: ПЖ уменьшилась в размерах, свободной жидкости в брюшной полости нет, в забрюшинном пространстве размеры жидкостных скоплений уменьшились. КТ брюшной полости при выписке: отмечается положительная динамика в виде уменьшения размеров поджелудочной железы, уменьшения зон инфильтрации парапанкреатиче-ской клетчатки. В проекции хвоста поджелудочной желе- зы патологическая зона неоднородно-жидкостной плотности 94х45 мм, протяженностью 55 мм (рис. 18).
12.08.2011 больной выписан на амбулаторное лечение.
Выводы
Оценка по шкале АРАСНЕ II, объективно отражает тяжесть со-
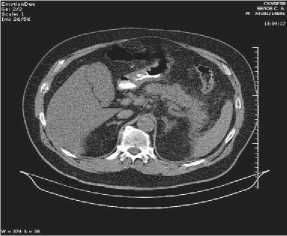
Рис. 15. Больной Б. КТ брюшной полости. Картина ПН с поражением па-рапанкреатической клетчатки
стояния пациентов и имеет прогностическую ценность в исходе заболевания, и коррелирует с уровнем токсических метаболитов группы
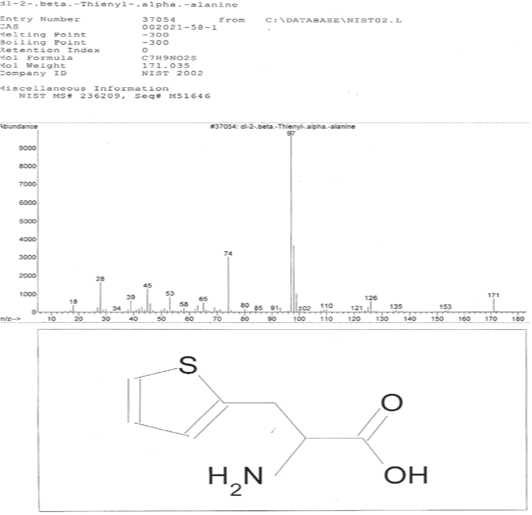
Рис. 16. Масс-спектр ди-2-бетатиэнилальфааланина
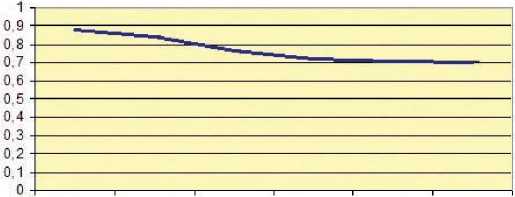
Исходное Проведен 2-е сутки 3-е сутки 4-е сутки 5-е сутки значение сеанс ГФ, 1-е сутки
Рис. 17. Больной Б. Динамика уровня крезолов на фоне проведенного сеанса ПВВГФ (ммоль/л)
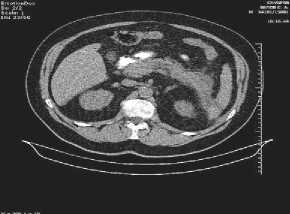
Рис. 18. Больной Б. КТ брюшной полости. Положительная динамика в виде уменьшения размеров ПЖ, уменьшения зон инфильтрации парапанкреатической клетчатки. В проекции хвоста ПЖ патологическая зона неоднородно-жидкостной плотности 94 x 45 мм, протяженностью 55 мм фенолов и крезолов. Выявлена зависимость между уровнем токсических метаболитов группы фенолов и крезолов и проявлениями ОПН. Так же уровень метаболитов данной группы позволяет объективизировать и прогнозировать развитие ОПН до момента изменения уровня мочевины и креатинина, что позволяет использовать данные значения, как показания для проведения методов экстракорпоральной детоксикации, предупреждая развитие тяжелой поли-органной и почечной недостаточности.
Проведение экстракорпоральной детоксикации на начальных стадиях заболевания, при отсутствии явлений выраженной ПОН, благоприятно влияет на прогноз и исход заболевания.
Список литературы Оценка эффективности гемофильтрации у пациентов с панкреонекрозом
- Затевахин И.И., Цициашвили М.Ш., Будурова М.Д., Алту-нин А.И. Панкреонекроз (диагностика, прогнозирование и лечение). М., 2007. 224 с.
- Ермолов А.С., Иванов П.А., Гришин А.В., Благовестов Д.А. Патогенетические подходы к диагностике и лечению острого панкреатита//Хирургия. 2007. № 5. С. 4-8.
- Прудков М.И., Шулутко А.М., Галимзянов Ф.В., Левит А.Л., Ковалевский А.Д., Алферов С.Ю. Некротизирующий панкреатит. Хирургия малых доступов. Екатеринбург: «ЭКС-Пресс», 2002. 48 с.
- Gullo L., Migliori M., Olah A. et al. Acute pancreatitis in five European countries: etiology and mortality//Pancreas. 2002. Vol. 24. P. 223-237.
- Rebours V., Levy P., Bretagne J.F., Bommelaer G., Hammel P., Ruszniewski P. Do guidelines influence medical practice? Changes in management of acute pancreatitis 7 years after the publication of the French guidelines//Eur. J. Gastroenterol. Hepatol. 2012. Vol. 24, № 2. Р. 143-148.
- Tavernier M., Paye F. Severity assessment and medical treatment of acute pancreatitis//Rev. Prat. 2011. Vol. 61, № 2. Р. 222-224.
- Нестеренко Ю.А., Мищенко А.Н., Михайлусов С.В. Гнойнонекротические осложнения острого панкреатита. М.: ВУНМЦ МЗ РФ, 1998. 179 с.
- Ronco C., Bellomo R., Homel P., et al. Effects of different doses in continuous veno-venous hemofiltration//Lancet. 2000. Vol. 356. P. 26-30.
- Bellomo R., Honore P.M., Matson J. R. et al. Extracorporeal blood treatment (EBT) methods in SIRS/Sepsis. Consensus statement. Position paper. ADQI III Conference//Int. J. Artif. Organs. 2005. Vol. 28. P. 450-458.
- Сажин А.В., Свиридов С.В., Любова А.Е. Продленная заместительная почечная терапия в комплексном лечении панкрео-некроза.//Российский медицинский журнал. 2012. № 6. С. 5-10.
- Истратов В.Г., Казенков В.В., Амеров Д.Б. и др. Использование хроматографических органоспецифических спектров метаболитов в оценке источника интоксикации в раннем послеоперационном периоде у хирургических больных//Альманах анестезиологии и реаниматологии. 2003. № 3. С. 26.
- Bellomo R., Honore P.M., Matson J. R. et al. Extracorporeal blood treatment (E B T) methods in SIRS/Sepsis. Consensus statement. Position paper. ADQI III Conference//Int. J. Artif. Organs. 2005. Vol. 28. P. 450-458.
- Sharma A., Hermann D.D., Mehto R.L. Clinical bent and approach of ultrafiltration in асШ:е heart failure//Cardiology. 2001. Vol. 96. P. 144-154.
- Савельев B.C., Филимонов М.И., Бурневич С.З. Панкреонекрозы. М.: МИА, 2008. 264 с.
- Поляков И.В., Золотухин К.Н., Лейдерман И.Н. Стандартный протокол проведения нутритивной поддержки в хирургическом отделении реанимации и интенсивной терапии. Первые результаты внедрения//Хирургическая практика. 2013. № 2. С. 46-50.


