Оценка эффективности хирургического лечения критической ишемии конечности на фоне атеросклеротического поражения артерий
Автор: Мухамадеев Ильдус Султанович, Березина Ирина Анатольевна, Котельникова Людмила Павловна, Степанов Руслан Алексеевич
Журнал: Ульяновский медико-биологический журнал @medbio-ulsu
Рубрика: Клиническая медицина
Статья в выпуске: 1, 2017 года.
Бесплатный доступ
Цель - изучить особенности нарушений кровообращения и гнойно-некротических очагов при критической ишемии конечности на фоне атеросклеротического поражения артерий и оценить ближайшие результаты хирургического лечения критической ишемии нижних конечностей (КИНК). Материалы и методы. Изучены особенности нарушений кровообращения и гнойно-некроти- ческих очагов при КИНК на фоне атеросклеротического поражения артерий у 80 больных. Соотношение мужчин и женщин составило 6:1. Все пациенты поступили с признаками КИНК - болями в состоянии покоя, наличием очага некроза. Проведено восстановление кровотока в нижней конечности оперативным путем с оценкой ближайших результатов. Результаты. Дооперационное цветное дуплексное сканирование и брюшная аортография с ангиографией нижних конечностей выявили в подавляющем большинстве случаев поражение поверхностной бедренной (ПББА) (95 %) и подколенной артерии (72,75 %). Окклюзионно-стенотический процесс в подвздошных артериях обнаружили только у трети больных (35,75 %). Окклюзию ПББА регистрировали значимо чаще, чем малоберцовой артерии (71,25 и 47,5 % соответственно, p=0,00). Вовлечение в процесс артерий стопы обнаружили у 35 % больных атеросклерозом. Хирургический этап включал в себя реконструктивно-восстановительные операции на артериях пораженной конечности и ликвидацию гнойно-некротического очага, которую производили как одномоментно с реконструктивно-восстановительной сосудистой операцией (40 чел.), так и поэтапно (до и/или после реваскуляризации) (40 чел.). Выводы. Обнаружено многоуровневое поражение артерий с преобладанием изменений в бедренно-подколенно-берцовом сегменте и формированием сухого некроза 2-4 пальцев стопы в 50 % случаев. Реваскуляризация бедренно-подколенно-берцовых сегментов с использованием аутовен, артериальных или венозных аллографтов, синтетических протезов позволила в раннем послеоперационном периоде эффективно восстановить кровоток в 96,25 % случаев и в 97,50 % избежать ампутации конечности. Последовательность выполнения реваскуляризации и санации гнойно-некротического очага на стопе и голени существенно не влияла на длительность заживления язвенных дефектов.
Атеросклероз, критическая ишемия нижних конечностей, методы реваскуляризации
Короткий адрес: https://sciup.org/14113260
IDR: 14113260 | УДК: 617.58-005.4-036.111-02:616.137.8 | DOI: 10.23648/UMBJ.2017.25.5247
Efficacy evaluation of surgical treatment of critical limb ischemia with atherosclerotic arterial disease
The objective of the paper is to study the characteristics of circulatory disorders and necrotic foci with critical limb ischemia on the background of atherosclerotic arterial involvement and to evaluate the short-term results of critical lower limb ischemia (CLLI) surgical treatment. Materials and Methods. The features of circulatory disorders and necrotic foci with CLLI on the background of atherosclerotic arterial involvement were studied in 80 patients. The male to female ratio was 6:1. All patients demonstrated CLLI signs upon admission to hospital, i.e. rest pain, focal necrosis. Surgical blood flow recovery of the lower limbs was conducted, the short-term results were assessed. Results. In most cases the preoperative color duplex scanning and abdominal aortography with lower limb angiography revealed superficial femoral artery lesion (95 %) and the popliteal artery lesion (72.75 %). Stenoses and occlusive processes in iliac arteries were found only in one third of patients (35.75 %). Occlusion of the superficial femoral artery was recorded much more often than that of the peroneal artery (71.25 % and 47.5 % respectively, p=0.00). 35 % of patients with atherosclerosis demonstrated the involvement of the foot arteries. Operative treatment included surgical repair of the affected limb arteries and the elimination of purulonecrotic focus, which was conducted simultaneously with reconstructive vascular surgery (40 patients), and in incremental steps (before and/or after revascularization) (40 patients). Conclusion. Multilevel arterial involvement with changes in the femoral, popliteal, and tibial segments and coagulation necrosis of the 2-4th toes was detected in 50 % of cases. Revascularization of femoral, popliteal and tibial segments with vein grafts, venous or arterial allografts, and synthetic prostheses allowed us to restore blood flow effectively in the early postoperative stage in 96.25 % of cases and in 97.50 % of cases to avoid limb amputation. The sequence of revascularization and purulonecrotic focus debridement on the foot and lower limb did not affect the duration of ulcerous defect repair.
Текст научной статьи Оценка эффективности хирургического лечения критической ишемии конечности на фоне атеросклеротического поражения артерий
Введение. Атеросклероз служит основной причиной развития критической ишемии нижних конечностей (КИНК). Количество пациентов с КИНК увеличивается с возрастом, а около 60 % из них страдает также ишемической болезнью сердца и хронической недостаточностью мозгового кровообращения (ХНМК) [1]. Известно, что риск развития фатальных сердечно-сосудистых осложнений увеличивается вместе с прогресси- рованием хронической артериальной недостаточности (ХАН) нижних конечностей [2]. К основным проявлениям КИНК относят гнойно-некротические изменения на стопе и голени: язвы, некрозы пальцев, гангрену стопы, которые могут привести к развитию сепсиса, ампутации конечности. Основным методом лечения, позволяющим сохранить конечность, остается ее реваскуляризация, которую выполняют как рентгеноэндоваску- лярным, так и оперативным способами [3]. Для восстановления кровотока используют аутовенозные шунты, реже – протезы и гомографты [4, 5]. Успешная операция в сочетании с консервативным лечением позволяет избежать ампутации конечности в течение года в 75 % и более случаев [4]. В то же время тромбоз шунтов и протезов приводит к рецидиву КИНК, необходимости ампутации конечности. Совершенствование способов восстановления артериального кровотока в конечности остается актуальной хирургической проблемой.
Цель исследования. Изучить особенности нарушений кровообращения и гнойнонекротических очагов при критической ишемии конечности на фоне атеросклеротического поражения артерий и оценить ближайшие результаты хирургического лечения КИНК.
Материалы и методы. Под нашим наблюдением находилось 80 больных с атеросклеротическим поражением магистральных сосудов нижних конечностей и КИНК. Среди пациентов большую часть составляли мужчины (86,25 %) в возрасте от 50 до 70 лет (средний возраст – 63,48 ± 9,43 года). Соотношение мужчин и женщин составило 6:1. Все пациенты поступили с признаками КИНК – болями в состоянии покоя, наличием очага некроза. Медиана продолжительности заболевания составляла 730 дней и варьировала от 365 до 1095 дней. Длительность клинических проявлений ишемии на момент госпитализации колебалась от 30 до 91 дня с медианой 45,5. У 67 пациентов на момент госпитализации были диагностированы различные сопутствующие заболевания или их комбинация: артериальная гипертензия (35 чел. (43,75 %)), патология брахиоцефальных артерий с ХПМК II–IV ст. (25 чел. (31,25 %)) и ишемическая болезнь сердца (24 чел. (30 %)). Ранее 28,75 % (23 чел.) больных перенесли различные оперативные вмешательства по поводу ХАН нижних конечностей и ХНМК, общее количество которых составило 46 на 80 чел. (1,7 вмешательства на одного пациента).
Диагностику нарушений кровообращения до реваскуляризации и в послеоперационном периоде проводили с помощью допплерографии с использованием аппарата
Wingmed-100 (Германия), ультразвукового дуплексного исследования на импульсноволновой допплеровской установке Philips Envisor HD (Германия). Также выполняли ангиографию артерий нижних конечностей. Для оценки состояния микроциркуляторного русла дистальных отделов пораженной конечности, а также мониторинга эффективности проводимой сосудистой лекарственной терапии проводили измерение напряжения кислорода в тканях (tcpO 2 ) стопы и голени с помощью аппарата TINA TCM 4 (Radiometer, Дания).
Для оценки тяжести гнойно-некротического процесса на стопе и голени разработали и использовали собственную балльную шкалу, где одному баллу соответствовало наличие поверхностного некроза или язвы без поражения подкожно-жировой клетчатки; двум баллам – некроз кожи и клетчатки без поражения сухожилий; трем баллам – некроз всех структур без поражения кости; четырем баллам – некроз с деструкцией кости; пяти баллам – гангрена стопы. Оценку течения раневого процесса выполняли в динамике с помощью pH-метрии раневого отделяемого универсальной индикаторной бумагой с эталонной шкалой pH 0–12 (Lach-Ner, Чехия). Бактериологическое исследование язвенного экссудата выполняли при поступлении и после оперативного вмешательства диско-диффузионным методом с антибиотикограммой.
Статистическую обработку полученных данных проводили с помощью пакета прикладных статистических программ Excel 2007, Statistica for Windows 6.0, Statistica 6.0, Statistica 8.0 (StatSoft, USA). Применяли стандартные методы описательной статистики: вычисление средних величин, стандартных отклонений, интерквартильного размаха (25-й; 75-й квартили), медианы, моды. Проверку гипотезы о нормальном распределении данных осуществляли с использованием теста Shapiro–Wilk. Для выявления преобладающих изменений проводили сравнение относительных частот выборки. Для обнаружения значимых различий в рассматриваемых группах использовали стандартные методы непараметрической статистики – Mann– Whitney U-test. Вероятность справедливости нулевой гипотезы принимали при p<0,05.
Результаты и обсуждение. Все пациенты с атеросклерозом на момент госпитализации имели КИНК длительностью более 45 сут, что свидетельствовало не только о позднем обращении больных за медицинской помощью, но и о несвоевременном выявлении терминальной ХАН и направлении пациентов в специализированные лечебные учреждения. У 85 % больных диагностировали различные заболевания и их комбинации, среди которых преобладала патология брахиоцефальных артерий и ишемическая болезнь сердца. Полученные данные подтвердили мультифокальный характер атеросклеротического поражения с вовлечением нескольких значимых анатомо-функциональных сосудистых бассейнов, поражение которых взаимосвязано и увеличивает риск развития инфаркта миокарда, инсульта, количество летальных исходов от сердечно-сосудистых заболеваний [1, 2].
При поступлении у пациентов диагностировали язвенно-некротическое поражение дистальных отделов конечности, тяжесть которого колебалась от двух до четырех баллов по предложенной шкале (38,75; 23,75; 27,5 % соответственно). У большинства больных гнойно-некротический процесс различной тяжести локализовался в пределах одного-двух пальцев (41,25 %), что было значимо чаще по сравнению с прочими анатомическими зонами стопы (p=0,00). Поражение трех и более пальцев стопы имело место у 8,75 % пациентов и встречалось не реже, чем некрозы межпальцевых промежутков (p=0,35), пяточной (p=0,55), тыльной (p=0,73) поверхности стопы, и значимо чаще плантарных язв (p=0,03). Поражение пяточной области диагностировали в виде поверхностных и глубоких некрозов размерами от 0,5 до 1,5 см. Язвы тыла стопы (7,25 %) имели неправильную форму диаметром от 2 до 5 см с некротизированными краями в равной степени без или с вовлечением подлежащих сухожилий разгибателей пальцев (3,75 %, p=1,00). Плантарные язвы с поражением сухожилий обнаруживали недостоверно реже (1,25 %, p=0,09, p=0,06), чем дефекты пяточной и тыльной поверхностей стопы. Некрозы межпальцевых промежутков (5 %) были представлены в виде влаж- ного поверхностного и глубокого повреждения клетчатки межпальцевого промежутка.
У 11,25 % пациентов при поступлении находили некротизированные незаживающие раны/язвы разной степени тяжести, в т.ч. с деструкцией головок и/или опилов плюсневых костей, после ранее выполненных в условиях других больниц ампутаций пальцев.
У 16,25 % пациентов гнойно-некротический очаг был представлен плоскими, покрытыми плотным фибрином язвами голени диаметром от 1 до 4 см, в 2,50 % случаев – с поражением подлежащих сухожилий и мышц. Тотальное поражение (гангрена) всех пальцев с переходом на тыл стопы, деструкцией фаланг и плюсневых костей выявлено только в 1,25 % случаев. Наши исследования подтверждают данные литературы о наличии у большинства больных КИНК некрозов пальцев и стопы на фоне атеросклеротического поражения сосудов язв стопы и голени, [4]. Использование предложенной балльной шкалы позволяет уточнить глубину поражения тканей, локализацию процесса, что влияет на выбор способа местного лечения гнойно-некротического процесса. При первичном осмотре тяжесть язвенно-некротического поражения дистальных отделов конечности соответствовала 2–4 баллам, причем у большинства (42,5 %) процесс локализовался в пределах одного-четырех пальцев.
По данным УЗДГ артерий нижних конечностей наибольшую скорость кровотока (ЛСК) фиксировали в бедренной артерии (45 (35–55) см/с) по сравнению с таковой в других артериальных сегментах пораженной конечности (p=0,00). На уровне подколенной артерии медиана ЛСК составила 20 (15–25) см/с, на задней большеберцовой (ЗББА) – 10 см/с, на передней большеберцовой (ПББА) – 8,5 см/с (p=0,0000). Регистрировали одинаково низкие показатели лодыжечно-плечевого индекса на уровне ЗББА и ПББА (0,39 и 0,35 соответственно, p=0,09). На уровне подколенной артерии коллатеральный характер кровотока преобладал у 86,25 % больных (p=0,0000), на уровне ЗББА – у 78,75 %, ПББА – у 66,25 % (р=0,08). Отсутствие кровотока в ЗББА встречалось реже, чем в ПББА (16,25 и 33,75 % соответственно, p=0,01). По- лученные данные свидетельствуют о плохом прогнозе течения заболевания, так как только у 5 % больных с лодыжечно-плечевым индексом ниже 0,4 удается избежать ампутации конечности в течение года даже после ее реваскуляризации [4].
Медиана значений транскутанного напряжения кислорода в тканях голени и стопы в проекции ЗББА составила 5,5 (3,5–9,5) мм рт. ст. (Shapiro–Wilk, W=0,9196, p=0,02), в проекции артерии тыла стопы (АТС) – 5 (2–8) мм рт. ст. (Shapiro–Wilk, W=0,9007, p=0,06). Значимых различий между данными точек замера TcpО 2 не обнаружено (M-W U-Test, p=0,23). Оценка микроциркуляторного русла стопы с помощью транскутанного измерения напряжения кислорода в тканях показала критически низкие значения TcpО 2 в точках измерения.
Данные дооперационного цветного дуплексного сканирования и брюшной аортографии с ангиографией нижних конечностей в подавляющем большинстве выявили поражение поверхностной бедренной (95 %) и подколенной артерий (72,75 %). Окклюзион-но-стенотический процесс в подвздошных артериях обнаружили только у трети больных (35,75 %). Окклюзию ПББА регистрировали значимо чаще, чем малоберцовой артерии (71,25 и 47,5 % соответственно, p=0,00) и с одинаковой частотой в сравнении с ЗББА (67,5 %, p=0,61). Вовлечение в процесс артерий стопы выявили у 35 % больных атеросклерозом (рис. 1).
Поражение двух-трех артерий голени фиксировали чаще, чем окклюзию одной берцовой артерии (n=75; 73,75 % и n=21; 26,25 % соответственно, p=0,00).
В соответствии с результатами доопера-ционного комплексного клинического и инструментального исследования кровотока у пациентов с КИНК обнаружено многоуровневое атеросклеротическое поражение артериального русла нижних конечностей, протяженность которого у большинства составляла 2–3 сегмента с преобладанием бедренно-подколенноберцового (n=47; 58,75 %) (рис. 2).
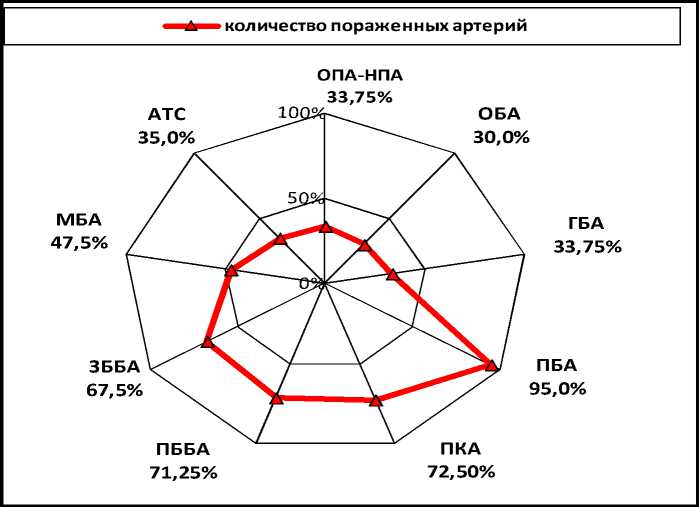
Рис. 1. Частота поражения артерий нижних конечностей по данным ангиографического исследования и дуплексного сканирования
^^^■сегменты поражения П-Б-ПКА
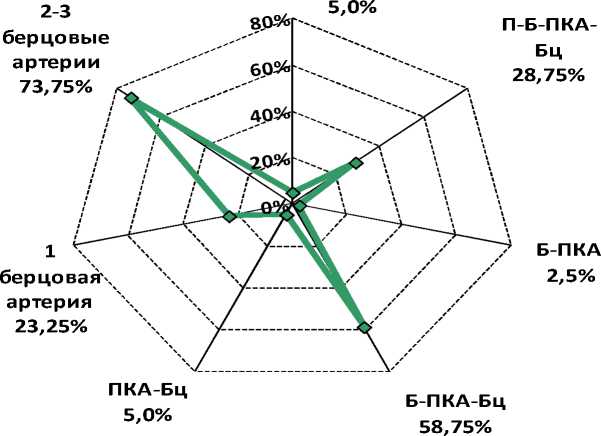
Рис. 2. Сегменты поражения артерий у больных с критической ишемией нижних конечностей
Смещение кривых распределения частот поражения артерий нижних конечностей (рис. 1, 2) в сторону инфраигвинального и инфрапоплитеального уровней с преимущественной окклюзией двух-трех берцовых артерий свидетельствовало о том, что причиной развития КИНК служило тяжелое окклюзионное поражение периферического артериального русла с преобладанием двух- и трехуровневого поражения в основном бедренно-подколенно-берцового сегмента [6].
При изучении микробного пейзажа язв до начала лечения в 41,25 % случаев (33 чел.) диагностировали моноинфекцию в виде грам-мположительной кокковой флоры (Staphylococcus aureus). В 18,75 % (15 чел.) высевали грамотрицательные бактерии в виде Escherichia coli, у 10 % больных (8 чел.) – в виде Pseudomonas aeruginosa. Грамотрицательные факультативные анаэробы Proteus vulgaris получены у 13,75 % (11 чел.) и Klebsiella pneumoniae – у 7,5 % (6 чел.) больных. В 8,75 % (7 чел.) посевов флора не обнаружена.
При наличии экссудата в гнойно-некротическом очаге выполняли pH-метрию. Кислотность раневого отделяемого составила 4 (4–5), что свидетельствовало о сдвиге рН в кислую сторону, что в условиях ишемии являлось благоприятным фактором для роста и развития патогенной флоры.
Лечение пациентов с терминальной ХАН проводили в соответствии с общепринятыми стандартами (TASС II, Национальные рекомендации по ведению пациентов с сосудистой артериальной патологией, Москва, 2010). Для улучшения региональной гемодинамики и микроциркуляции применяли спазмолитики, прямые антикоагулянты, в т.ч. низкомолекулярные гепарины, гликозаминогликаны (сулодексид) и простагландины Е1 (алпростан, вазапростан).
Хирургический этап включал реконструктивно-восстановительные операции на артериях пораженной конечности и ликвидацию гнойно-некротического очага, которую производили как одномоментно с реконструктивно-восстановительной сосудистой операцией (40 чел.), так и поэтапно (до и/или после реваскуляризации) (40 чел.). Временной интервал между санацией гнойно-некротического очага и реваскуляризацией составлял 13 (6–19) сут, промежуток между восстановлением кровотока и ликвидацией некроза – 3,10 ± 1,73 дня.
Реваскуляризация бедренно-подколенного сегмента выше и ниже колена была выполнена 34 пациентам, из них 17 – с использованием аутовен, 11 – артериальных/веноз-ных аллографтов и 6 – синтетических протезов. Бедренно-берцовые реконструкции произведены в 26 случаях с восстановлением кровотока по одной (16 чел.), двум (9 чел.) и трем (1 чел.) берцовым артериям. Подколенно-берцовое шунтирование выполнено 7 пациентам с реваскуляризацией одной (5 чел.) и двух (2 чел.) артерий голени. Многоуровневый характер окклюзионного поражения артериального русла и необходимость реваскуляризации максимального числа артерий в четырех случаях потребовали применения трансплантата «сложной архитектоники», установленного единым блоком в аорто-бед-ренно-глубокобедренно-подколенно-берцо-вой позиции. С этой целью использованы ал-лоартериальные трансплантаты с естественной бифуркацией ветвей. Применение алло-графтов, особенно при отсутствии аутовены, позволяет полноценно восстановить кровоток при КИНК даже в сложных ситуациях [7].
У 29 пациентов (36,25 %) с гемодинамически значимыми стенозами аорто-подвздошного сегмента и вовлечением бифуркации бедренных артерий подпупартовые и инфра-поплитеальные реконструкции были дополнены коррекций путей притока: аорто- или подвздошно-бедренным шунтированием, эндартерэктомией из терминального отдела наружной подвздошной артерии, бифуркацией бедренных артерий с профундопластикой. В пяти случаях для разгрузки инфраигвинального шунта в условиях критической ХАН в дополнение к реконструкции выполняли артерио-лизацию венозного русла стопы и голени.
Эффективная реваскуляризация конечности позволяет избавить пациента от болей в состоянии покоя, избежать ампутации, санировать гнойно-некротический очаг. Способы восстановления кровотока в бедренно-подколенно-берцовом сегменте весьма разнообразны и зависят от характера поражения периферических артерий, правильного выбора вида, диаметра шунта или протеза, состояния аорты, подвздошных артерий, периферического артериального русла [3–5, 7–9].
При сравнении исходных и послеоперационных показателей ультразвуковой допплерографии достоверной разницы в ЛСК в бедренной артерии не выявлено (M-W U Test, p=0,11). В подколенной артерии, ЗББА, ПББА по результатам контрольной УЗДГ получено значимое увеличение ЛКС по сравнению с дооперационными значениями (M-W U Test, p=0,00).
После реваскуляризации конечности напряжение кислорода в тканях в проекции ЗББА увеличилось с 5,5 (3,5–9,5) до 33 (21,5– 40) мм рт. ст., а в проекции АТС – с 5 (2–8) до 31,62 (21,0–41,5) мм рт. ст.
Хирургическая обработка гнойно-некротического очага включала экзартикуляцию и/или ампутацию пораженных пальцев с резекцией головок соответствующих плюсневых костей (27 чел.); некрэктомию язвенных дефектов, иногда дистальную резекцию стопы (2 чел.). В 23 случаях санацию гнойнонекротического очага дополнили ультразвуковой кавитацией раневой поверхности аппаратом Sonoca-185 (Германия). После восстановления кровотока и удаления некротического очага больным выполняли санационные перевязки. При наличии выраженного экссудата использовали сорбционные повязки, а для очищения раневой поверхности и стимуляции грануляционного процесса применяли покровные материалы. При низкой степени экссудации использовали гидрогелевый и пленочный перевязочный материал для создания в ране «парникового эффекта», а затем применяли комбинацию сорбционнопокровных повязок. На фоне лечения на 3-и сут отмечали появление грануляционной ткани в ранах, на 7-е – уменьшение диаметра раневого канала и/или язвы. К 15–18-м сут раны/язвы имели тенденцию к заживлению вторичным натяжением и/или краевой эпите-лизации. При наличии обширных дефектов выполняли кожную пластику собственными тканями, либо свободным лоскутом, либо «марочным» способом.
При контрольной pH-метрии в ранах и язвах на стопе и голени после восстановления кровотока и санации очага инфекции показатель pH равнялся 8 (7–8), что свидетельствовало о значимом смещении значения в сторону щелочной среды, необходимой для заживления раны (в сравнении с исходным кислым pH 4 (M-W U Test, p=0,00).
Медиана длительности госпитализации, а также основного этапа заживления язвенных дефектов при одномоментной и поэтапной (до и после восстановления кровотока) санации гнойно-некротического очага существенно не различалась – 20,5 (15–29) и 16,0 (11,5–27,5) сут соответственно (M-W U Test p=0,20).
В 10 (12,5 %) случаях в раннем послеоперационном периоде зарегистрирован тромбоз шунта, в 9 случаях из них выполнены повторные хирургические вмешательства, одному пациенту проведено интенсивное консервативное лечение. Эффективное восстановление кровотока в раннем послеоперационном периоде было достигнуто в 96,25 % случаев, а в 97,5 % удалось уберечь конечность от ампутации. Двум больным выполнили ампутацию конечности на уровне голени (1 чел.) и бедра (1 чел.). Летальных исходов в раннем послеоперационном периоде не было.
Эффективность прямой реваскуляризации нижней конечности в лечении КИНК с наложением бедренно-подколенно-берцовых анастомозов в сочетании с санацией гнойнонекротического очага на стопе и голени выше, чем непрямой, и позволяет сохранить конечность в 86–96,5 % [10–12]
Выводы:
-
1. Для больных с критической ишемией конечности на фоне атеросклероза характерно многоуровневое поражение артерий с преобладанием изменений в бедренно-подколенно-берцовом сегменте и формированием сухого некроза 2–4 пальцев стопы.
-
2. Последовательность выполнения реваскуляризации и санации гнойно-некротического очага на стопе и голени существенно не влияет на длительность заживления язвенных дефектов стопы и голени.
-
3. Реваскуляризация бедренно-подколенно-берцовых сегментов с использованием аутовен, артериальных или венозных алло-графтов, синтетических протезов позволяет в раннем послеоперационном периоде эффективно восстановить кровоток в 96,25 % случаев и в 97,5 % избежать ампутации конечности.
Список литературы Оценка эффективности хирургического лечения критической ишемии конечности на фоне атеросклеротического поражения артерий
- Murabito J.M., Evans J.C., Larson M.G., Nieto K., Levy D., Wilson P.W. Framingham study the ankle-brachial index in the elderly and risk of stroke, coronary disease and death: the Framingham study. Arch. Intern. Med. 2003; 163 (16): 1939-1942.
- Muluk S.C., Muluk V.S., Kelley M.E., Whittle J.C., Tierney J.A., Webster M.W., Makaroun M.S. Outcome events in patients with claudication: a 15-year study in 2777 patients. J. Vasc. Surg. 2001; 33 (2): 251-258.
- Egorova N.N., Goillerme S., Gelijns A., Morrissey N., Dayal R., Mckinsey J.F., Nowygrod R. An Analysis of the outcomes of a decade of experience with lower extremity revasculatization including limb savage, lengths of stay, and safety. J. Vasc. Surg. 2010; 51 (4): 878-885.
- Pennywell D.J., Tan T-W., Zhang W.W. Optimal management of onfrainguinal arterial occlusive desease. Vasc. Health Risk Manag. 2014; 10: 599-608.
- Kinlay S. Outcomes for clinical studies assessing drug and revasculatization therapies for claudication and critical limb ischemia in peripheral artery disease. Circulation. 2013; 19, 127 (11): 1241-1250.
- Ruenda C.A., Nehler M.R., Perry D.J, McLafferty R.B., Casserly I.P., Hiatt W.R. Patterns of artery disease in 450 patients undergoing revascularization for critical ischemia: implications for clinical trial design. J. Vasc. Surg. 2008; 47 (5): 995-999.
- Randon C., Jacobs B., De Ryck F., Beele Y., Vermassen F. Fifteen years of infrapopliteal arterial reconstructions with cryopreserved venous allografts for limb salvage. J. Vasc. Surg. 2010; 51 (4): 869-877.
- Balzer K.M., Weis-Muller B.T. Results of open vascular surgical therapy in chronic peripheral artery disease. Vasa. 2011; 40 (5): 359-367.
- Петухов А.В. Современное состояние проблемы лечения критической ишемии нижних конечностей. Новости хирургии. 2006; 4 (14): 97-106.
- Бокерия Л.А. Темрезов М.Б., Коваленко В.И., Янбаев А.К., Гаджиев О.Г. Хирургическое лечение больных с первичной критической ишемией нижних конечностей. Анналы хирургии. 2010; 1: 16-19.
- Гавриленко А.В., Жидков В.И., Котов А.Э. Современная стратегия хирургического лечения больных с атеросклеротическим поражением аортоподвздошного сегмента. Анналы хирургии. 2015; 1: 23-28.
- Бокерия Л.А., Коваленко В.И., Калитко И.М., Кочубей А.А., Матвиенко А.А., Темрезов М.Б., Петров А.П. Микрохирургическая реваскуляризация голени и стопы в лечении больных с критической ишемией нижних конечностей. Анналы хирургии. 2009; 6: 91-95.


