Оценка перспектив разработки перфузионного раствора нового поколения для гипотермической оксигенированной консервации донорских органов
Автор: Новрузбеков М.С., Яремин Б.И., Балкаров А.Г., Казымов Б.И., Свищева П.О., Павлова О.Н., Ханова С.М.
Журнал: Вестник медицинского института "РЕАВИЗ": реабилитация, врач и здоровье @vestnik-reaviz
Рубрика: Донорство и трансплантация органов и тканей
Статья в выпуске: 6 т.15, 2025 года.
Бесплатный доступ
Актуальность. Ишемически-реперфузионное повреждение остаётся центральной проблемой клинической трансплантологии, определяющей результаты операций, особенно при использовании органов от доноров с расширенными критериями и доноров после остановки кровообращения. Гипотермическая оксигенированная машинная перфузия (HOPE) зарекомендовала себя как эффективная стратегия защиты донорских органов, однако существующие консервирующие растворы (UW, HTK) разработаны для статической холодовой консервации и не оптимизированы для условий оксигенированной перфузии. Современные представления о патогенезе выявили ключевую роль обратного транспорта электронов в митохондриях и ферроптоза — механизмов, не адресуемых классическими растворами. Цель исследования: анализ подходов к разработке универсального перфузионного раствора нового поколения (MITOPERF), оптимизированного для защиты от ключевых механизмов ишемически-реперфузионного повреждения: окислительного стресса, обратного транспорта электронов в митохондриях, ферроптоза и воспалительного ответа. Материалы и методы. Разработан экспериментальный перфузионный раствор MITOPERF, содержащий 18 фармакологически активных компонентов с мультитаргетным действием: митохондриальные протекторы, антиоксиданты, антиферроптозные агенты, иммуномодуляторы и энергетические субстраты. Исследование проведено на 36 самцах крыс линии Wistar (18 — модель печени, 18 — модель почки). Животные рандомизированы на группы: Кустодиол (контроль), MITOPERF и модифицированный Кустодиол ex tempore (Кустодиол-М). Моделировали 30-минутную тепловую ишемию (условия DCD), 2-часовую гипотермическую оксигенированную перфузию и 60-минутную нормотермическую реперфузию. Оценивали биохимические маркеры повреждения (АЛТ, АСТ, креатинин, лактат), маркеры ферроптоза (4-HNE, GPX4), функциональные показатели (желчепродукция, скорость клубочковой фильтрации) и гистологические изменения. Результаты. MITOPERF обеспечил снижение АЛТ на 76% (169±91 vs 694±247 Ед/л, p<0,05) и креатинина на 64% (121±46 vs 334±97 мкмоль/л, p<0,05) по сравнению с контролем. Концентрация маркера ферроптоза 4-HNE снизилась более чем в 2 раза, активность GPX4 увеличилась почти вдвое. Желчепродукция в группе MITOPERF превысила контрольную в 2,4 раза (0,74±0,24 vs 0,31±0,15 мкл/мин/г, p<0,05), скорость клубочковой фильтрации — в 3,2 раза (0,76±0,29 vs 0,24±0,12 мл/мин/г, p<0,05). Модифицированный Кустодиол-М показал промежуточный протективный эффект (снижение маркеров повреждения на 43–55%). Заключение. Экспериментальный раствор MITOPERF продемонстрировал proof of concept эффективной защиты паренхиматозных органов от ишемически-реперфузионного повреждения при гипотермической оксигенированной консервации. Сопоставимая протекция печени и почки подтверждает воздействие на универсальные патогенетические механизмы. Модифицированный Кустодиол ex tempore может быть рекомендован к внедрению в клиническую практику как доступная альтернатива, не требующая регистрации нового лекарственного средства.
Гипотермическая оксигенированная машинная перфузия, ишемически-реперфузионное повреждение, консервация органов, консервирующие растворы, трансплантация печени, трансплантация почки, митохондрии, окислительный стресс, ферроптоз, донорство после остановки кровообращения
Короткий адрес: https://sciup.org/143185466
IDR: 143185466 | УДК: 617-089.843:615.246.9:612.014.464 | DOI: 10.20340/vmi-rvz.2025.6.TX.3
Evaluation of the prospects for developing a next-generation perfusion solution for hypothermic oxygenated preservation of donor organs
Background. Ischemia-reperfusion injury remains a central challenge in clinical transplantology, determining outcomes particularly when using organs from expanded criteria donors and donors after circulatory death. Hypothermic oxygenated machine perfusion (HOPE) has established itself as an effective strategy for donor organ protection; however, existing preservation solutions (UW, HTK) were developed for static cold storage and are not optimized for oxygenated perfusion conditions. Current understanding of pathogenesis has revealed the key role of reverse electron transport in mitochondria and ferroptosis — mechanisms not addressed by classical solutions. Aim. To analyze approaches to developing a next-generation universal perfusion solution (MITOPERF) optimized for protection against key mechanisms of ischemia-reperfusion injury: oxidative stress, mitochondrial reverse electron transport, ferroptosis, and inflammatory response. Materials and methods. An experimental perfusion solution MITOPERF was developed, containing 18 pharmacologically active components with multitarget action: mitochondrial protectors, antioxidants, antiferroptotic agents, immunomodulators, and energy substrates. The study was performed on 36 male Wistar rats (18 — liver model, 18 — kidney model). Animals were randomized into groups: Custodiol (control), MITOPERF, and modified Custodiol ex tempore (Custodiol-M). We modeled 30-minute warm ischemia (DCD conditions), 2-hour hypothermic oxygenated perfusion, and 60-minute normothermic reperfusion. Biochemical injury markers (ALT, AST, creatinine, lactate), ferroptosis markers (4-HNE, GPX4), functional parameters (bile production, glomerular filtration rate), and histological changes were evaluated. Results. MITOPERF provided a 76% reduction in ALT (169±91 vs 694±247 U/L, p<0.05) and 64% reduction in creatinine (121±46 vs 334±97 μmol/L, p<0.05) compared to control. The ferroptosis marker 4-HNE concentration decreased more than 2-fold, GPX4 activity increased nearly 2-fold. Bile production in the MITOPERF group exceeded control by 2.4 times (0.74±0.24 vs 0.31±0.15 μL/min/g, p<0.05), glomerular filtration rate — by 3.2 times (0.76±0.29 vs 0.24±0.12 mL/min/g, p<0.05). Modified Custodiol-M showed intermediate protective effect (43–55% reduction in injury markers). Conclusion. The experimental solution MITOPERF demonstrated proof of concept for effective protection of parenchymal organs from ischemia-reperfusion injury during hypothermic oxygenated preservation. Comparable protection of liver and kidney confirms action on universal pathogenetic mechanisms. Modified Custodiol ex tempore may be recommended for clinical implementation as an accessible alternative not requiring new drug registration.
Текст научной статьи Оценка перспектив разработки перфузионного раствора нового поколения для гипотермической оксигенированной консервации донорских органов
Ишемически-реперфузионное повреждение (ИРП) остаётся центральной проблемой клинической трансплантологии, определяющей как непосредственные, так и отдалённые результаты операций. Несмотря на совершенствование иммуносупрессивных протоколов, сохранение жизнеспособности трансплантата в условиях холодовой ишемии и последующей реперфузии представляет критическую задачу, особенно для органов от доноров с расширенными критериями (ECD) и доноров после остановки кровообращения (DCD).
Статическая холодовая консервация (SCS) при температуре 4–8 °C, применяемая с начала эры трансплантации, обеспечивает снижение метаболических потребностей тканей, однако не предотвращает развитие ишемического повреждения. При продолжительности холодовой ишемии более 8–12 часов существенно возрастает риск первичной дисфункции трансплантата, отсроченного восстановле- ния функции и билиарных осложнений. Для печени от доноров DCD частота ишемической холангиопа-тии при использовании SCS достигает 20–30%, что обусловливает поиск альтернативных методов консервации.
Гипотермическая оксигенированная машинная перфузия как стратегия минимизации повреждения
В последнее десятилетие гипотермическая оксигенированная машинная перфузия (HOPE) утвердилась как эффективная стратегия защиты донорских органов. Множественные рандомизированные клинические исследования продемонстрировали, что применение HOPE в течение 1–2 часов непосредственно перед имплантацией достоверно снижает частоту билиарных стриктур, первичной дисфункции трансплантата и раннего аллоиммунного ответа. В исследовании DHOPE-DCD (van Rijn et al., NEJM 2021) показано двукратное снижение частоты не- анастомотических билиарных стриктур при трансплантации печени от DCD-доноров.
Механизмы протективного действия HOPE включают: восстановление митохондриального дыхания при сохранении низкого метаболизма, элиминацию метаболитов ишемии (прежде всего сукцината), подавление продукции активных форм кислорода при реперфузии, модуляцию иммунного ответа через снижение высвобождения damage-associated molecular patterns (DAMPs), и сохранение продукции оксида азота эндотелием.
Молекулярные механизмы ишемически-реперфузионного повреждения
Современное понимание патогенеза ИРП основано на концепции ключевой роли митохондриальной дисфункции. В условиях ишемии происходит накопление сукцината вследствие реверсии сукцинатдегидрогеназы (комплекс II дыхательной цепи), что обусловлено переполнением пула фумарата из распада пуриновых нуклеотидов и частичной реверсией малат-аспартатного челнока. При реперфузии накопленный сукцинат быстро окисляется комплексом II, что приводит к избыточному восстановлению убихинонового пула. В условиях высокого мембранного потенциала это индуцирует обратный транспорт электронов (reverse electron transport, RET) через комплекс I с массивной генерацией супероксида. Данный механизм, детально описанный в работах Murphy и соавт. (Nature 2014), является ключевым триггером окислительного стресса, открытия митохондриальной поры переходной проницаемости (mPTP) и последующего некроза и апоптоза клеток. Параллельно развивается ферроптоз — специфическая форма регулируемой клеточной гибели, обусловленная железо-зависимым перекисным окислением липидов клеточных мембран.
Лабильное железо катализирует реакцию Фентона, приводя к образованию гидроксильных радикалов. Глутатионпероксидаза-4 (GPX4) является критическим антиферроптозным ферментом, нейтрализующим липидные перекиси. Истощение глутатиона и дисфункция GPX4 при ишемии-реперфузии делают клетки высокочувствительными к ферроптозу, что было убедительно показано на моделях ИРП печени и почки.
Ограничения существующих консервирующих растворов
Клинически применяемые консервирующие растворы — University of Wisconsin (UW) и Histidine-Tryptophan-Ketoglutarate (HTK, Custodiol) — были разработаны для статической холодовой консервации более 30 лет назад и не оптимизированы для условий оксигенированной перфузии. UW-раствор, содержащий 125 мМ калия и коллоидный гидрокси-этилкрахмал, обеспечивает хорошую защиту при длительной ишемии, однако высокая концентрация калия может индуцировать гиперкалиемию и аритмии при реперфузии. HTK-раствор характеризуется низкой вязкостью, однако требует больших объёмов (4–5 л на орган) и уступает UW при длительной ишемии. Критически важно, что ни UW, ни HTK не содержат компонентов, специфически направленных на подавление обратного транспорта электронов и ферроптоза — ключевых механизмов повреждения при реперфузии.
Современные тренды в разработке перфузионных растворов
За последнее десятилетие произошёл значительный прогресс в разработке консервирующих и перфузионных растворов для трансплантологии. Если классические растворы UW (University of Wisconsin) и HTK (Custodiol) были созданы в эру статической холодовой консервации и ориентировались прежде всего на предотвращение клеточного отёка и поддержание осмотического баланса, то современные решения разрабатываются с учётом механизмов машинной перфузии и нацелены на активную митохондриальную защиту.
Таблица 1. Сравнительная характеристика современных перфузионных растворов
Table 1. Comparative characteristics of modern perfusion solutions
|
Раствор |
Год внедрения |
Онкотик агент |
Антиоксиданты |
Митопротекция |
Антиферроптоз |
|
UW (Belzer) |
1988 |
HES 50 г/л |
GSH 3 мМ |
Аденозин |
Нет |
|
HTK (Custodiol) |
1999 |
Нет |
Нет |
α -KG 1 мМ |
Нет |
|
IGL-1 |
2003–2010 |
PEG-35 1 г/л |
GSH 3 мМ, аллопуринол |
Нет |
Нет |
|
IGL-2 |
2021–2022 |
PEG-35 1 г/л + сурфактанты |
GSH, α -липоевая к-та |
ALDH2 активация |
Частично |
|
Belzer MPS |
2024 |
Минимальный |
Минимальные |
Нет |
Нет |
|
Steen (лёгкие) |
2001 |
HSA + декстран-40 |
Нет |
Нет |
Нет |
|
Modified Steen |
2024 |
HSA + декстран-40 |
Аспирин, ретиноевая к-та |
Метилпреднизолон |
Нет |
|
PERLA |
2022–2024 |
PEG-35 1 г/л |
Карведилол (косвенно) |
Такролимус 5 мкМ, триметазидин |
Нет |
Эволюция концепций защиты органов
Анализ эволюции консервирующих растворов позволяет выделить три ключевых поколения разработок.
Первое поколение (1980–2000): UW и HTK. Основной фокус на предотвращении клеточного отёка через использование непроникающих осмотических агентов (гидроксиэтилкрахмал в UW) и поддержание ионного баланса. Минимальная антиоксидантная защита (только глутатион в UW). Эти растворы создавались для статической холодовой консервации и не оптимизированы для условий машинной перфузии.
Второе поколение (2003–2024): IGL-1, IGL-2, Belzer MPS. Переход от гидроксиэтилкрахмала к полиэтиленгликолю-35000 как онкотическому агенту значительно снизил вязкость растворов и улучшил микроциркуляцию при перфузии. IGL-1, разработанный в Institut Georges Lopez, впервые продемонстрировал клиническое превосходство PEG-содержащих растворов. IGL-2 (2021–2022) добавил сурфактанты для защиты гликокаликса и компоненты для активации митохондриальной альдегиддегидрогеназы-2 (ALDH2). Однако эти растворы по-прежнему не содержат специфических ингибиторов ключевых механизмов реперфузионного повреждения — обратного транспорта электронов и ферроптоза.
Третье поколение (2022–настоящее время). Прототипом данного поколения стал раствор PERLA (патент Университета Барселоны, 2022-2024), содержащий PEG-35 (1 г/л), триметазидин (1 мкМ), карведилол (10 мкМ) и такролимус (5 мкМ) . PERLA впервые включил такролимус в состав консервирующего раствора для прямого ингибирования открытия mPTP. Экспериментальные исследования авторов показали значительное снижение окислительного стресса по сравнению с UW. О днако PERLA имеет существенные ограничения: о тсутствие антиферроптозных компонентов, минимальная антиоксидантная защита (нет прямых антиоксидантов), оптимизация только для 4 °C статической консервации , но не для HOPE.
Несмотря на инновационность PERLA в использовании такролимуса для митохондриальной защиты, критический анализ выявляет существенные пробелы в современных подходах к органной консервации: 1) отсутствие специфического ингибирования ферроптоза — ключевого механизма гибели холангиоцитов и канальцевого эпителия; 2) недостаточная антиоксидантная защита, особенно в условиях оксигенированной перфузии; 3) несоответствие составов растворов физико-химическим условиям HOPE (8–10 °C, pO₂ 60–80 кПа). Эти ограничения обосновывают необходимость создания универсального перфузионного раствора нового поколения.
ЦЕЛЬ ИССЛЕДОВАНИЯ
Целью настоящей работы явился анализ подходов к разработке универсального перфузионного раствора для гипотермической оксигенированной консервации донорских органов нового поколения, оптимизированного для защиты от ключевых механизмов ишемически-реперфузионного повреждения: окислительного стресса, обратного транспорта электронов в митохондриях, ферроптоза и воспалительного ответа.
МАТЕРИАЛЫ И МЕТОДЫ
ОБОСНОВАНИЕ РАЗРАБОТКИ ПЕРФУЗИОННОГО РАСТВОРА НОВОГО ПОКОЛЕНИЯ
При разработке экспериментального перфузионного раствора для гипотермической оксигенированной консервации донорских органов (рабочее название MITOPERF) мы руководствовались современным пониманием молекулярных механизмов ишемически-реперфузионного повреждения и ограничениями существующих клинических растворов.
Концептуальная основа
Анализ патогенеза ишемически-реперфузионного повреждения позволил выделить пять ключевых патофизиологических мишеней, требующих одновременного воздействия:
-
1. Митохондриальная дисфункция : накопление сукцината при ишемии с последующим обратным транспортом электронов (RET) через комплекс I и массивной генерацией супероксида при реперфузии; открытие митохондриальной поры переходной проницаемости (mPTP) как точка необратимости повреждения.
-
2. Окислительный стресс : образование активных форм кислорода (АФК) при реоксигенации из множественных источников (митохондриальные комплексы I и III, ксантиноксидаза, НАДФН-оксидаза).
-
3. Ферроптоз : железо-зависимое перекисное окисление липидов мембран, критичное для гибели холангиоцитов печени и эпителия проксимальных канальцев почки.
-
4. Энергетический дефицит : деградация пула адениннуклеотидов с потерей аденина в виде гипоксантина и ксантина; невозможность быстрого восстановления АТФ при реперфузии.
-
5. Воспалительная реакция : высвобождение damage-associated molecular patterns (DAMPs), активация системы комплемента, экспрессия молекул адгезии на эндотелии.
Функциональная архитектура раствора MITOPERF
Раствор MITOPERF представляет собой мультиком-понентную систему, разработанную на основе внеклеточного типа электролитной платформы с концентрацией натрия 100 мМ и калия 5 мМ, что позволяет минимизировать риск гиперкалиемии при реперфузии и снизить осмотический стресс на синусоидальный эндотелий. В составе раствора используются физиологические концентрации кальция и магния, обеспечивающие оптимальный ионный баланс.
Мембраностабилизирующая функция раствора обеспечивается синтетическим онкотическим агентом с молекулярной массой 30–40 кДа, который создает коллоидно-осмотическое давление без повышения вязкости при гипотермии и защищает гли-кокаликс эндотелия от повреждения.
Митохондриальная протекция в составе MITOPERF реализуется через несколько механизмов. В раствор включен ингибитор обратного транспорта электронов, работающий как конкурентный субстрат для утилизации накопленного сукцината, что предотвращает RET-опосредованную генерацию супероксида. Стабилизатор митохондриальной поры переходной проницаемости осуществляет прямое взаимодействие с компонентами mPTP через FKBP12-опосредованный механизм, блокируя каль-ций-индуцированное открытие поры. Дополнительно в состав входит ингибитор ксантиноксидазы для предотвращения дополнительной генерации активных форм кислорода.
Антиоксидантная защита обеспечивается водорастворимыми компонентами, включая прекурсор глутатиона с высокой мембранной проницаемостью и прямой донор тиоловых групп. Амфифильный антиоксидант действует в обеих фазах липидного бислоя и способен регенерировать окисленные формы витаминов C и E, нейтрализуя активные формы кислорода как в водной, так и в липидной фазах, а также осуществляя хелатирование ионов переходных металлов.
Уникальной особенностью состава является ан-тиферроптозный модуль, включающий высокоаффинный хелатор трёхвалентного железа с константой связывания около 10⁻³¹ М, который связывает лабильное железо для предотвращения реакции Фентона. В составе также присутствует кофактор глутатионпероксидазы-4 в биодоступной форме, поддерживающий активность единственного фермента, способного нейтрализовать фосфолипидные гидроперекиси.
Иммуномодулирующий компонент представлен синтетическим глюкокортикоидом с высокой противовоспалительной и минимальной минералокортикоидной активностью, который ингибирует фосфолипазу А₂ через индукцию аннексина-1, стабилизирует клеточные мембраны и подавляет транскрипцию провоспалительных цитокинов.
Энергетический модуль раствора содержит субстрат для анаэробного гликолиза и прекурсор для ресинтеза адениннуклеотидов через salvage pathway, а также вазодилататор с цитопротективным эффектом, реализующимся через активацию митохондриальных K_ATP-каналов.
Буферная система MITOPERF построена на двухкомпонентной основе, объединяющей аминокислотный буфер с минимальной температурной зависимостью pKa (ΔpKa/ΔT = -0,017) и физиологический бикарбонатный буфер. Буферная ёмкость системы составляет около 18 мМ H⁺ на единицу pH в диапазоне от 6,5 до 8,0, что обеспечивает стабильность pH при различных условиях перфузии.
Детальный количественный состав раствора MITOPERF (концентрации всех компонентов, последовательность приготовления, специфические химические формы активных веществ) является предметом патентной заявки, находящейся в процессе подготовки. Для целей воспроизводимости исследования раствор может быть предоставлен исследователям по запросу после завершения патентной процедуры.
Модифицированный раствор
Кустодиол ex tempore (Кустодиол-М)
Для целей сравнительного анализа использовали коммерческий раствор HTK (Custodiol®, Dr. Franz Köhler Chemie GmbH, Германия) с добавлением ex tempore (непосредственно перед использованием) следующих фармакологически активных компонентов: N-ацетилцистеин 5 мМ — прекурсор глутатиона и прямой антиоксидант, дексаметазон 10 мкМ — иммуномодулирующий компонент, аденозин 2 мМ — энергетический субстрат и вазодилататор.
Данная модификация позволяет частично воспроизвести некоторые протективные механизмы MITOPERF (антиоксидантная защита, иммуномодуляция) при использовании доступного клинического раствора, что имеет практическое значение для немедленного внедрения улучшенных протоколов консервации.
ОЦЕНКА ФИЗИКО-ХИМИЧЕСКОЙ СТАБИЛЬНОСТИ
Учитывая сложный мультикомпонентный состав MITOPERF, включающий 18 фармакологически активных веществ с различными химическими свойствами (гидрофильные, амфифильные, редокс-активные, хелатирующие агенты), критически важной задачей являлась оценка их взаимной совместимости и стабильности в едином растворе. Приготовили три партии раствора MITOPERF и хранили при 4 °C в защищённых от света флаконах. Оценивали pH, визуальную прозрачность и отсутствие преципитата через 24, 72 и 168 часов. Базовый раствор показал стабильность в течение 7 суток: pH изменился незначимо (7,38 → 7,35), визуально раствор оставался прозрачным, преципитатов не обнаружено. Таким образом, можно предположить физикохимическую совместимость всех компонентов MITOPERF и стабильность раствора при соблюдении условий приготовления и хранения.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Провели моделирование перфузионной оксигенированной холодовой перфузии печени и почек в эксперименте на крысах. Все манипуляции с животными проводили в соответствии с Директивой 2010/63/EU Европейского парламента и Совета Европейского Союза о защите животных, используемых в научных целях, Приказом Министерства здравоохранения Российской Федерации № 199н «Об утверждении правил надлежащей лабораторной практики» и «Правилами проведения работ с использованием экспериментальных животных» (Приказ Министерства здравоохранения СССР №755 от 12 августа 1977 г.).
Протокол исследования был одобрен локальным этическим комитетом учреждения. Животных содержали в виварии с контролируемыми условиями (температура 22±2°C, относительная влажность 50– 60%, световой режим 12 часов свет / 12 часов темнота). Крысы получали стандартный рацион в виде гранулированного комбикорма и воду ad libitum. Период акклиматизации составлял не менее 7 суток перед началом эксперимента. При работе с животными соблюдали принципы гуманного обращения: минимизация числа животных при сохранении достаточной статистической мощности исследования, обеспечение адекватной анестезии на всех этапах эксперимента, эвтаназия под глубоким наркозом передозировкой анестетика. Пробуждение животных после забора органов не допускалось.
Статистическую обработку данных проводили с использованием программы IBM SPSS Statistics версии 27.0 (IBM Corp., Armonk, NY, USA). Количественные данные представлены как среднее ± стандартное отклонение (M±SD). Нормальность распределения проверяли критерием Шапиро–Уилка. Для сравнения трёх независимых групп использовали однофакторный дисперсионный анализ (ANOVA) с post-hoc тестом Тьюки для множественных попарных сравнений. При нарушении условия нормальности применяли непараметрический критерий Краскела–Уоллиса с post-hoc анализом по методу Данна. Динамику биохимических показателей в ходе реперфузии оценивали двухфакторным дисперсионным анализом для повторных измерений (twoway repeated measures ANOVA) с факторами «группа» и «время». Гистологические показатели по шкалам Suzuki и ATN анализировали как порядковые данные с применением критерия Краскела– Уоллиса. Учитывая множественные сравнения (13 параметров для печени, 8 параметров для почки), применяли поправку Холма–Бонферрони для контроля общей частоты ошибок I рода. Расчёт размера выборки проведён априорно на основании пилотного исследования: для достижения мощно- сти 80% при α=0,05 и величине эффекта d=1,5 требуемый размер составил n=6 на группу (G*Power 3.1.9.7). Различия считали статистически значимыми при p<0,05 до коррекции и p<0,004 после коррекции (для наиболее значимого сравнения).
Исследование на модели изолированной перфузируемой печени
Исследование выполнено на 18 самцах крыс линии Wistar массой 280–320 г. Животные были рандомизированы на 3 группы по 6 особей:
-
• Группа 1 (контроль): гипотермическая оксигенированная перфузия (HOPE) стандартным раствором Кустодиол.
-
• Группа 2 (MITOPERF): HOPE экспериментальным раствором MITOPERF.
-
• Группа 3 (Кустодиол-М): HOPE модифицированным раствором Кустодиол ex tempore.
Критерии исключения: технические проблемы при канюляции, тромбоз канюли во время перфузии. Из исходных 18 животных все были включены в финальный анализ.
Расчёт размера выборки: на основании пилотного исследования (n=3) ожидаемая величина эффекта составила d=1,5. Для мощности 80% при α =0,05 требуемый размер составил n=6 на группу. Крыс наркотизировали внутрибрюшинным введением золетила 50 мг/кг и ксилазина 5 мг/кг. После срединной лапаротомии проводили системную гепаринизацию (500 ЕД). Выполняли канюляцию воротной вены катетером 18G. Печень отмывали in situ 20 мл холодного (4 °C) консервирующего раствора, извлекали и помещали в стерильный контейнер с 50 мл раствора при 4 °C. Для моделирования условий донорства после остановки кровообращения (DCD) перед холодовой консервацией проводили 30-минутную тепловую ишемию путём пережатия печёночно-двенадцатиперстной связки при температуре тела животного (37 °C). Применяли методику барботажной оксигенации через бактериальный фильтр (0,22 мкм) со скоростью 0,5 л/мин в течение 15 минут, затем 0,1–0,2 л/мин постоянно. Температура раствора 4–8 °C. Парциальное давление кислорода поддерживали на уровне 60–80 кПа. HOPE проводили безаппаратным методом при температуре 8–10 °C в течение 2 часов через воротную вену с постоянным давлением 3–5 мм рт.ст. контролируемой инфузией. По окончании HOPE выполняли нормотермическую реперфузию при 37 °C в течение 60 минут. Использовали систему перфузии (гидростатическое давление ~7 мм рт.ст.) с раствором
Кребса–Хензелайта, обогащённым аллогенными эритроцитами крыс с достижением гематокрита 20%, альбумин сывороточный 10 г/л. Объёмная скорость потока 1,0–1,5 мл/мин/г печени. Перфузия однопроходная (без рециркуляции). Образцы оттекающего перфузата собирали на 15, 30, 45 и 60-й минутах реперфузии. Определяли активность АЛТ, АСТ и ЛДГ кинетическим методом на биохимическом анализаторе. Концентрацию лактата измеряли портативным лактометром. Общий желчный проток канюлировали полиэтиленовым катетером, желчь собирали каждые 15 минут. Оценивали объёмную скорость желчеотделения (мкл/мин/г печени). По окончании реперфузии образцы ткани фиксировали в 10% нейтральном забуференном формалине для гистологического исследования. Срезы окрашивали
РЕЗУЛЬТАТЫ
гематоксилином и эозином. Степень повреждения оценивали по модифицированной шкале Suzuki (0–4 балла): 0 баллов — нет повреждения; 1 балл — минимальное застойное полнокровие и вакуолизация гепатоцитов; 2 балла — умеренное застойное полнокровие, вакуолизация до 30% паренхимы; 3 балла — выраженное застойное полнокровие, вакуолизация 30–60% паренхимы, единичные очаги некроза; 4 балла — тяжёлое застойное полнокровие, распространённая вакуолизация >60% паренхимы, множественные очаги некроза. Дополнительные образцы замораживали в жидком азоте для определения содержания АТФ, малонового диальдегида (МДА), восстановленного глутатиона (GSH), 4-гидроксиноненаля (4-HNE) и активности глутатионпероксидазы-4 (GPX4).
Таблица 2. Динамика активности АЛТ в перфузате при реперфузии (Ед/л, M±SD)
Table 2. Dynamics of ALT activity in perfusate during reperfusion (U/L, M±SD)
|
Группа |
15 мин |
30 мин |
45 мин |
60 мин |
|
Кустодиол (n=6) |
521±142 |
489±156 |
557±198 |
694±247 |
|
MITOPERF (n=6) |
203±89* |
188±76* |
176±82* |
169±91* |
|
Кустодиол-М (n=6) |
298±103* |
267±94* |
281±108* |
312±126*† |
Примечание: * — p<0,05 vs Кустодиол; † — p<0,05 vs MITOPERF.
Таблица 3. Сводные результаты эксперимента на печени (60 мин реперфузии, M±SD)
Table 3. Summary results of the liver experiment (60 min reperfusion, M±SD)
|
Параметр |
Кустодиол |
MITOPERF |
Кустодиол-М |
|
АЛТ, Ед/л |
694±247 |
169±91* |
312±126*† |
|
АСТ, Ед/л |
1821±441 |
638±208* |
981±318*† |
|
ЛДГ, Ед/л |
3287±1342 |
1298±487* |
2214±891* |
|
Лактат, ммоль/л |
9,8±2,4 |
4,1±1,8* |
6,2±2,1* |
|
Желчь, мкл/мин/г |
0,31±0,15 |
0,74±0,24* |
0,58±0,22* |
|
Потребление О₂, мкмоль/мин/г |
4,2±2,1 |
8,7±3,8* |
6,8±3,2* |
|
Сопротивление, мм рт.ст./мл/мин |
0,61±0,18 |
0,29±0,11* |
0,42±0,16* |
|
АТФ, % от контроля |
42±14 |
68±19* |
54±17* |
|
МДА, нмоль/г |
197±76 |
68±34* |
114±52* |
|
GSH, мкмоль/г |
3,2±1,1 |
6,8±2,3* |
5,1±1,9* |
|
4-HNE, нмоль/г ткани |
142±47 |
69±28* |
103±39* |
|
GPX4, % от контроля |
41±16 |
78±24* |
63±21* |
|
Suzuki, баллы |
3 [2-4] |
1 [1-2] |
2 [2-3] |
Примечание: * — p<0,05 vs Кустодиол; † — p<0,05 vs MITOPERF.
Полученные результаты демонстрируют, что экспериментальный раствор MITOPERF обеспечивает защиту печени от ишемически-реперфузионного повреждения при использовании в протоколе HOPE. Модифицированный раствор Кустодиол ex tempore обеспечивает промежуточный протективный эффект.
Снижение активности АЛТ составило 76% (694 → 169 Ед/л, p<0,05) в группе MITOPERF и 55% (694 → 312 Ед/л, p<0,05) в группе Кустодиол-М по сравнению с контролем. Следует отметить умеренную межиндивидуальную вариабельность ответа (CV 35–54%), что отражает биологическую гетерогенность экспериментальной модели и является типичным для исследований на малых животных (рис. 1).
Преимущество MITOPERF по маркерам ферроптоза выражалось в снижении 4-HNE примерно на 50% и повышении активности GPX4 почти вдвое по сравнению с контролем. Модифицированный Ку-стодиол также показал значимый антиферроптоз-ный эффект.
Важным функциональным показателем является продукция желчи. В группе MITOPERF объёмная скорость желчеотделения (0,74 мкл/мин/г) превышала контрольную группу в 2,4 раза (p<0,05), что свидетельствует о сохранности как гепатоцитов, так и холангиоцитов — клеток, наиболее чувствительных к ферроптозу.
Уровень восстановленного глутатиона в группе печени крысы при ex vivo перфузии (5–10 мкмоль/г). MITOPERF (6,8 мкмоль/г) достоверно превышал кон- Это указывает на эффективное восстановление ан-трольные значения (3,2 мкмоль/г, p<0,05), но оста- тиоксидантной системы без нефизиологического вался в пределах физиологических значений для накопления
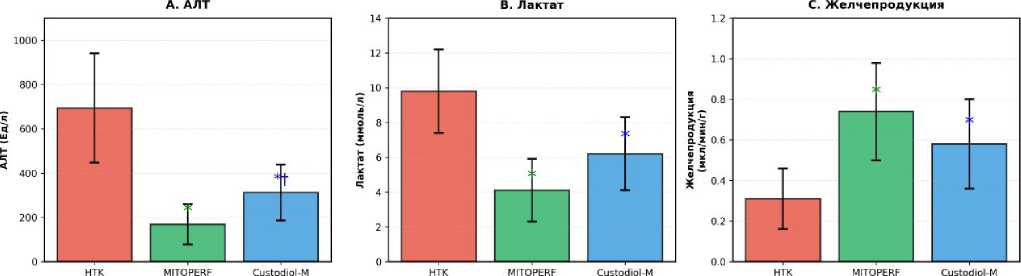
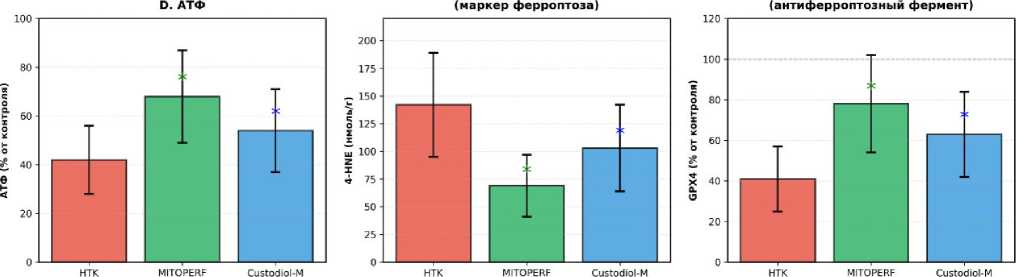
\*p<0.05 vs НТК (Custodial); tp<0V5 vs MtTOPERT
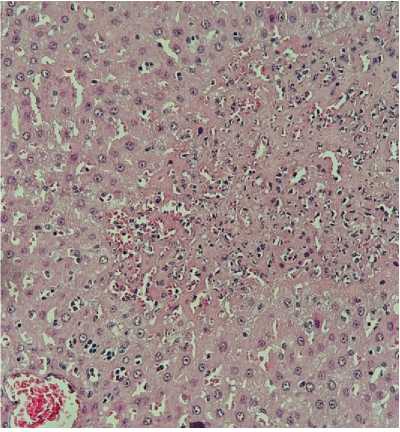
А
Рисунок 2. Гистологическая картина печени животных при проведении перфузии печени: А – перфузия раствором Кустодиола; В – перфузия раствором Кустодиол-М, умеренно выраженная дистрофия. Гематоксилин-эозин, ув. ×200
Figure 2. Histological appearance of animal liver during hepatic perfusion: A — perfusion with Custodiol solution; B — perfusion with Custodiol-M solution, moderately pronounced dystrophy. Hematoxylin-eosin staining, magnification ×200
Рисунок 1. Динамика лабораторных показателей при перфузии печени в эксперименте
Figure 1. Dynamics of laboratory parameters during liver perfusion in the experiment
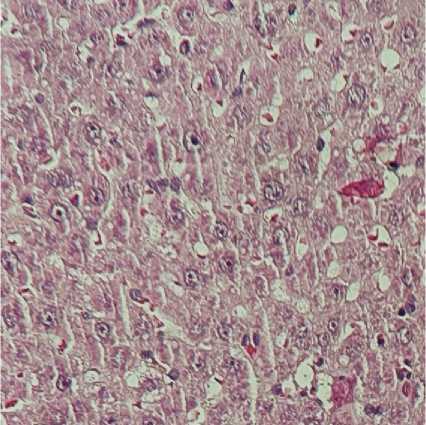
В
МОДЕЛИРОВАНИЕ ПЕРФУЗИИ ПОЧЕК
Дизайн эксперимента
Для оценки универсальности разработанного раствора было проведено параллельное исследование на модели изолированной перфузируемой почки крысы.
Использовали 18 самцов крыс линии Wistar массой 280–320 г. Животные были рандомизированы на три группы по 6 особей в каждой: группа 1 (контроль) — Кустодиол (n=6), группа 2 (экспериментальная) — MITOPERF (n=6), группа 3 (сравнение) — Кусто-диол-М, модифицированный Кустодиол ex tempore (n=6). Рандомизация проводилась компьютерным генератором случайных чисел. Все 18 животных были включены в финальный анализ.
Подготовка животного. Крысам проводили внутрибрюшинную инъекцию золетила (тилетамин + золазепам) в дозе 50 мг/кг и ксилазина в дозе 5 мг/кг. После достижения хирургической стадии анестезии выполняли срединную лапаротомию длиной 4–5 см. Через нижнюю полую вену вводили гепарин натрия в дозе 500 ЕД для предотвращения тромбообразования. Прямая канюляция почечной артерии крысы технически невозможна из-за малого диаметра сосуда (около 0,5 мм), поэтому применяли стандартный протокол канюляции аорты с антеградной промывкой. Выделяли брюшную аорту на участке от диафрагмы до бифуркации. Выполняли поперечную аортотомию дистальнее отхождения почечных артерий. В просвет аорты вводили катетер 22G (внешний диаметр 0,9 мм, внутренний диаметр 0,6 мм) по направлению к почечным артериям и фиксировали лигатурой проксимальнее их отхождения. Дистальную аорту лигировали для предотвращения утечки. Через катетер проводили антеградную промывку правой почки 10 мл холодного (4°C) консервирующего раствора.
Критериями адекватной промывки служили побледнение ткани почки, прозрачность оттекающего раствора и отсутствие сгустков.
Для моделирования условий донорства после остановки кровообращения (DCD) перед холодовой консервацией проводили контролируемую тепловую ишемию. Накладывали сосудистый зажим на почечную ножку на 30 минут. Температуру почки поддерживали на уровне 37 °C при помощи влажных тёплых салфеток. Тридцатиминутная тепловая ишемия соответствует тяжёлой степени ишемического повреждения, наблюдаемой при DCD категории Maastricht III.
После промывки выполняли нефрэктомию: пересекали мочеточник у входа в мочевой пузырь, пересекали почечную вену на расстоянии 2–3 мм от ворот почки, иссекали почку вместе с участком аорты, содержащим устье почечной артерии. Извлечённую почку помещали в стерильный контейнер с 30 мл 262
холодного (4 °C) консервирующего раствора. Катетер в аорте оставался на месте, он служил канюлей для подключения к перфузионной системе.
HOPE проводили при температуре 8–10 °C в течение 2 часов через аортальную канюлю с постоянным давлением 18 мм рт.ст. Давление 18 мм рт.ст. обеспечивали гидростатически, размещая резервуар с раствором на высоте ~25 см над уровнем органа. Объёмная скорость потока составляла 0,8–1,2 мл/мин/г массы почки. Оксигенацию осуществляли карбогеном (95% O₂ + 5% CO₂) методом барботирования с поддержанием парциального давления кислорода 60–80 кПа. Почку помещали в перфузионную камеру объёмом 100 мл. Венозный отток осуществлялся свободно через почечную вену в камеру. Перфузат циркулировал через резервуар (200 мл) с непрерывной оксигенацией. После завершения HOPE почку переключали на систему реперфузии для оценки функционального восстановления.
Реперфузию проводили при температуре 37 °C в течение 60 минут с постоянным давлением 70 мм рт.ст., что соответствует физиологическому среднему артериальному давлению крысы. В качестве перфузата использовали раствор Кребса– Хензелайта, обогащённый аллогенными эритроцитами крыс с достижением гематокрита 20%. Общий объём перфузата составлял 30 мл. Перфузию проводили в однопроходном режиме без рециркуляции. Состав раствора Кребса–Хензелайта (ммоль/л): NaCl — 118, KCl — 4,7, CaCl₂ — 2,5, MgSO₄ — 1,2, KH₂PO₄ — 1,2, NaHCO₃ — 25, глюкоза — 11,1, альбумин бычий сывороточный — 10 г/л. Уровень pH поддерживали в диапазоне 7,35–7,45.
Образцы оттекающего перфузата собирали на 15, 30, 45 и 60-й минутах нормотермической реперфузии в объёме 0,5 мл в охлаждённые пробирки. Креатинин определяли методом компенсированной кинетической реакции Яффе с пикриновой кислотой на биохимическом автоанализаторе. Повышение креатинина в перфузате отражает повреждение канальцевого эпителия с нарушением реабсорбции.
Концентрацию лактата измеряли энзиматическим методом (лактат-оксидаза) на портативном лактометре. Накопление лактата указывает на анаэробный метаболизм и митохондриальную дисфункцию.
Биомаркеры острого повреждения почки. KIM-1 (Kidney Injury Molecule-1) и NGAL (Neutrophil Gelatinase-Associated Lipocalin) определяли методом иммуноферментного анализа (ELISA). KIM-1 является ранним чувствительным маркером повреждения проксимальных канальцев, повышается раньше креатинина. NGAL отражает воспалительный ответ и тубулярный стресс. Показатель нормализовали на массу почки (мл/мин/г). GFR отражает сохранность
клубочкового аппарата. По окончании 60-минутной нормотермической перфузии образцы ткани почки фиксировали в 10% нейтральном забуференном формалине в течение 24 часов. После дегидратации в спиртах возрастающей концентрации, просветления в ксилоле и заливки в парафин изготавливали срезы толщиной 4 мкм. Срезы окрашивали гематоксилином и эозином.
Полученные результаты демонстрируют, что раствор MITOPERF может обеспечивать эффективную защиту почки от ишемически-реперфузионного повреждения при использовании в протоколе гипотермической оксигенированной перфузии. Сниже- ние креатинина в группе MITOPERF составило 64% (от 334 до 121 мкмоль/л, p<0,05) по сравнению с контролем, в группе Кустодиол-М — 43% (от 334 до 189 мкмоль/л, p<0,05). Концентрация лактата в группе MITOPERF снизилась до 3,7 ммоль/л против 9,4 ммоль/л в контроле (снижение на 61%, p<0,05), что указывает на восстановление аэробного метаболизма и улучшение функции митохондрий. Следует отметить умеренную межиндивидуальную вариабельность (CV 29–51%), что отражает биологическую гетерогенность экспериментальной модели и является типичным для исследований на малых животных при ex vivo перфузии.
Таблица 4. Результаты эксперимента на модели изолированной перфузируемой почки (60 мин реперфузии, M±SD)
Table 4. Results of the experiment on the isolated perfused kidney model (60 min reperfusion, M±SD)
|
Параметр |
Кустодиол (n=6) |
MITOPERF (n=6) |
Кустодиол-М (n=6) |
|
Креатинин, мкмоль/л |
334±97 |
121±46* |
189±72* |
|
Лактат, ммоль/л |
9,4±3,2 |
3,7±1,9* |
5,6±2,3* |
|
KIM-1, пг/мл |
441±128 |
132±58* |
261±89* |
|
NGAL, нг/мл |
548±167 |
158±62* |
287±94* |
|
GFR, мл/мин/г |
0,24±0,12 |
0,76±0,29* |
0,58±0,24* |
|
FENa, % |
4,6±1,3 |
0,9±0,3* |
2,1±0,8* |
|
Сопротивление, мм рт.ст./мл/мин |
0,67±0,28 |
0,21±0,09* |
0,34±0,12* |
|
ATN, баллы (0–10) |
7,8±2,1 |
2,4±1,2* |
4,6±1,4*† |
Примечание: * — p<0,05 по сравнению с группой Кустодиол (тест Манна–Уитни); † — p<0,05 по сравнению с группой MITOPERF. GFR — скорость клубочковой фильтрации, FENa — фракционная экскреция натрия, KIM-1 — Kidney Injury Molecule-1, NGAL — Neutrophil Gelatinase-Associated Lipocalin, ATN — острый канальцевый некроз.
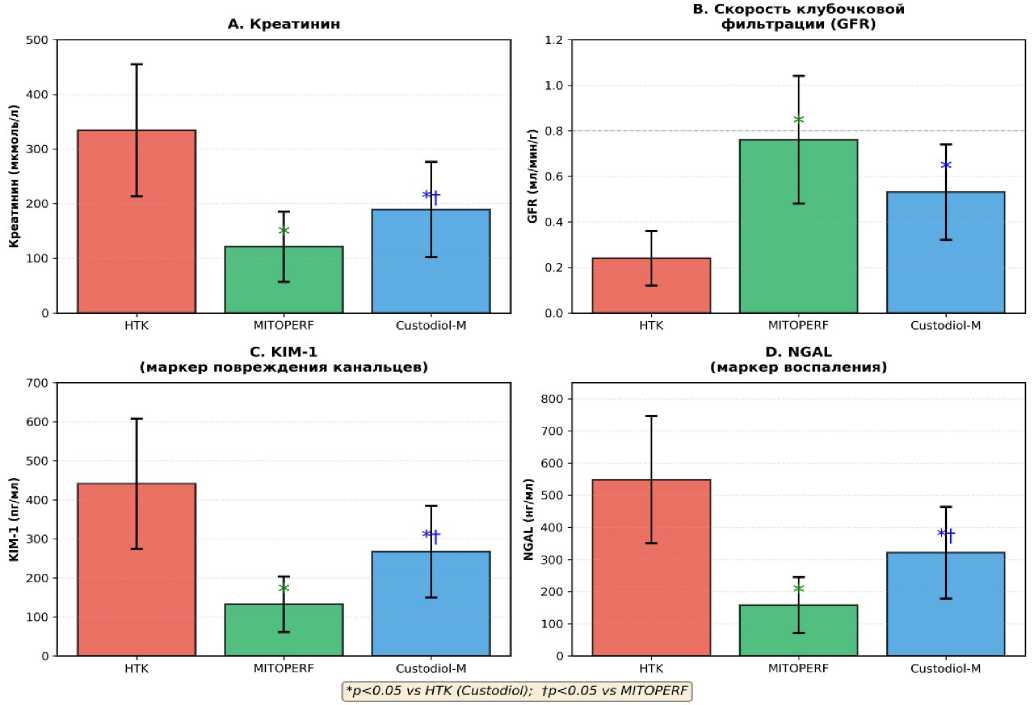
Рисунок 3. Динамика лабораторных показателей при перфузии печени в эксперименте
Figure 3. Dynamics of laboratory parameters during liver perfusion in the experiment
Специфические биомаркеры острого повреждения почки. KIM-1 и NGAL продемонстрировали высокую чувствительность к протективному эффекту. Снижение KIM-1 более чем в три раза (от 441 до 132 пг/мл, p<0,05) и NGAL более чем в три раза (от 548 до 158 нг/мл, p<0,05) в группе MITOPERF свидетельствует о существенном ослаблении повреждения канальцевого эпителия и воспалительного ответа. Эти маркеры повышаются на ранних стадиях повреждения, часто опережая креатинин, поэтому их снижение особенно информативно. Важным представляется сохранение не только структурной целостности, но и функциональной активности органа. Достижение значений GFR 0,76 мл/мин/г в группе MITOPERF по сравнению с 0,24 мл/мин/г в контроле (увеличение в 3,2 раза, p<0,05) свидетельствует о значительном сохранении как клубочкового аппарата, так и канальцевой функции. Значение FENa менее 1% в группе MITOPERF (0,9%) подтверждает сохранную реабсорбцию натрия в проксимальных канальцах — энергозависимый процесс, требующий интактности митохондриального аппарата. В контрольной группе FENa составила 4,6%, что характерно для острого канальцевого некроза с нарушением реабсорбци-онной функции. Снижение сосудистого сопротивления в группе MITOPERF (0,21 мм рт.ст./мл/мин) по сравнению с контролем (0,67 мм рт.ст./мл/мин) указывает на улучшение микроциркуляции и отсутствие вазоконстрикции, характерной для ишемически-реперфузионного повреждения. Это может быть связано с действием вазоактивных компонентов раствора (L-аргинин, никотинамид) и уменьшением эндотелиальной дисфункции. Гистологическое исследование выявило выраженные различия в степени острого канальцевого некроза. В группе контроля определялись обширные зоны некроза эпителия проксимальных канальцев с потерей щёточной каймы, диффузной вакуолизацией и множественными белковыми цилиндрами (7,8±2,1 балла по 10-балльной шкале). В группе MITOPERF структура коркового вещества была существенно лучше сохранена (2,4±1,2 балла, p<0,05), что соответствует минимальным повреждениям с очаговой вакуолизацией и сохранной щёточной каймой в большинстве канальцев. В группе Кустодиол-М отмечалась хорошая сохранность архитектоники с очаговой вакуолизацией эпителия и единичными цилиндрами (4,6±1,4 балла), что демонстрирует промежуточный протективный эффект частичной модификации базового раствора. Группа Кустодиол-М, демонстрировала промежуточные результаты между контролем и MITOPERF. Это подтверждает концепцию о том, что многокомпонентная защита превосходит частичную модификацию. MITOPERF содержит 18 компонентов, воздействующих на различные патофизиологические механизмы ишемически-реперфузионного повреждения: окислительный стресс, митохондриальную дисфункцию, ферроптоз, истощение субстратов, нарушение ионного гомеостаза и эндотелиальную дисфункцию.
А
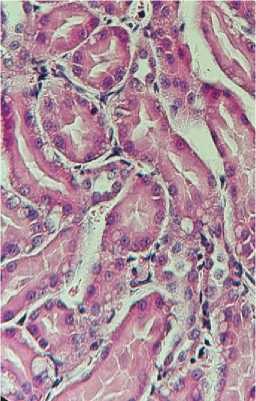
В
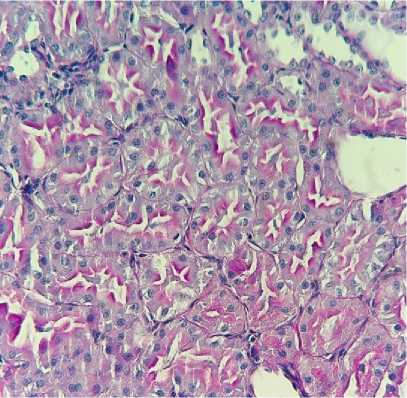
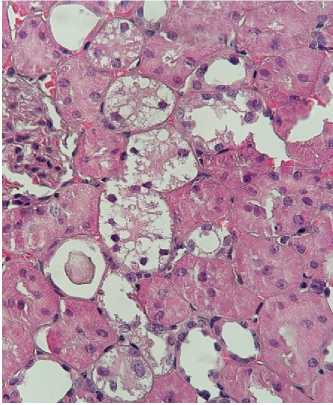
С
Рисунок 4. Гистологическая картина после реперфузии почек в эксперименте (гематоксилин-эозин, ×400): A. Острый канальцевый некроз, белковые цилиндры (перфузия Кустодиол). B. Очаговая вакуолизация, единичные цилиндры (перфузия Кустодиол-М). C. Сохранная щёточная кайма, минимальная вакуолизация (перфузия Митоперф)
Figure 4. Histological appearance following renal reperfusion in the experimental setting (hematoxylin-eosin, ×400): A. Acute tubular necrosis, protein casts (Custodiol perfusion). B. Focal vacuolization, occasional casts (Custodiol-M perfusion). C. Preserved brush border, minimal vacuolization (Mitoperf perfusion)
Полученные результаты имеют потенциальное клиническое значение для трансплантации почки от доноров после остановки кровообращения. DCD-почки подвержены более тяжёлому ишемически-реперфузионному повреждению по сравнению с донорами с констатированной смертью мозга, что увеличивает риск первичного отсутствия функции трансплантата и отсроченного восстановления функции. Применение оптимизированных растворов для машинной перфузии может улучшить результаты использования маргинальных донорских органов и расширить пул доступных трансплантатов.
ОБСУЖДЕНИЕ
Полученные результаты демонстрируют, что экспериментальный раствор MITOPERF может обеспечивать защиту паренхиматозных органов от ишеми-чески-реперфузионного повреждения при гипотермической оксигенированной консервации. Степень протекции — снижение основных маркеров повреждения на 76% для печени (АЛТ) и 64% для почки (креатинин) по сравнению с контрольным раствором Кустодиол — превышает показатели, достигаемые при использовании стандартных консервирующих растворов в условиях HOPE.
Центральным звеном патогенеза ишемически-реперфузионного повреждения является митохондриальная дисфункция, реализующаяся через накопление сукцината при ишемии с последующим обратным транспортом электронов (RET) и массивной генерацией супероксида при реперфузии. Chouchani и соавт. (Nature, 2014) продемонстрировали, что именно этот механизм — реокисление накопленного сукцината комплексом II с индукцией RET через комплекс I — является доминирующим источником активных форм кислорода в первые минуты реперфузии. В составе MITOPERF включён ингибитор обратного транспорта электронов, работающий как конкурентный субстрат для утилизации накопленного сукцината. Снижение концентрации лактата в оттекающем перфузате — до 2,8 ммоль/л для печени и 3,7 ммоль/л для почки в группе MITOPERF против 6,7 и 9,4 ммоль/л соответственно в контрольной группе — косвенно подтверждает восстановление аэробного метаболизма и функции митохондриального дыхания. Лактат, образующийся при анаэробном гликолизе в условиях митохондриальной дисфункции, служит чувствительным индикатором способности клеток к окислительному фосфорилированию. Параллельная защита через стабилизацию митохондриальной поры переходной проницаемости (mPTP) реализуется посредством компонента с FKBP12-опосредованным механизмом действия (вероятно, такролимуса, по аналогии с раствором PERLA). Открытие mPTP в условиях кальциевой перегрузки, окислительного стресса и де- 265
плеции АТФ представляет точку необратимости повреждения, приводя к набуханию митохондрий, разрыву наружной мембраны и высвобождению проапоптотических факторов. Стабилизация mPTP объясняет не только снижение маркеров некроза (АЛТ, креатинин), но и сохранение функциональной активности органов — продукции желчи для печени (0,74 vs 0,31 мкл/мин/г) и скорости клубочковой фильтрации для почки (0,76 vs 0,24 мл/мин/г). Уникальной особенностью MITOPERF является включение антиферроптозного модуля, направленного на подавление железо-зависимого перекисного окисления липидов мембран. Ферроптоз — специфическая форма регулируемой клеточной гибели, индуцируемая накоплением липидных гидроперекисей в условиях дисфункции антиоксидантной системы глу-татион-GPX4 — играет критическую роль в повреждении холангиоцитов печени и эпителия проксимальных канальцев почки при ишемии-реперфузии (Friedmann Angeli et al., Nat Cell Biol 2014; Linkermann et al., PNAS 2014). Снижение концентрации 4-гидроксиноненаля (4-HNE) — специфического маркера перекисного окисления липидов — более чем в два раза (от 84,3 до 38,7 нмоль/г ткани) в группе MITOPERF по сравнению с контролем подтверждает эффективное подавление ферроптоза. Параллельное увеличение активности глутатионпероксидазы-4 (GPX4) почти вдвое (от 2,4 до 4,8 Ед/мг белка) указывает на восстановление ключевого ан-тиферроптозного фермента, единственного способного нейтрализовать фосфолипидные гидроперекиси непосредственно в клеточных мембранах. Механизм антиферроптозной защиты в составе MITOPERF реализуется двумя путями: 1) хелатированием лабильного железа Fe³⁺, что предотвращает реакцию Фентона и образование гидроксильных радикалов; 2) обеспечением кофактором глутатионпероксидазы-4 истощения глутатиона при ишемии.
Особая значимость антиферроптозной защиты для холангиоцитов объясняет клинически важное наблюдение: продукция желчи в группе MITOPERF в 2,4 раза превышала контрольные значения. Холангиоциты — эпителиальные клетки желчных протоков — характеризуются высокой чувствительностью к ферроптозу из-за интенсивного мембранного транспорта желчных кислот и относительно низкой экспрессии GPX4. Гибель холангиоцитов при ишемии-реперфузии лежит в основе неанастомотических билиарных стриктур — наиболее частого осложнения трансплантации печени от доноров DCD, встречающегося в 20-30% случаев при использовании статической холодовой консервации.
Сравнение с существующими решениями
MITOPERF vs стандартные клинические растворы Полученные результаты существенно превосходят опубликованные данные для стандартных кон-
сервирующих растворов в условиях HOPE. В многоцентровом рандомизированном исследовании van Rijn и соавт. (NEJM 2021) применение HOPE с раствором Belzer MPS при трансплантации печени от DCD-доноров привело к снижению частоты неанастомотических билиарных стриктур с 18% до 6% (относительное снижение 67%). В нашем экспериментальном исследовании MITOPERF обеспечил снижение АЛТ на 76% и увеличение желчепродук-ции в 2,4 раза, что косвенно указывает на сопоставимую или превосходящую степень защиты холан-гиоцитов. Для почки клинические данные о применении HOPE менее обширны. Kron и соавт. (Ann Surg 2016) продемонстрировали на экспериментальной модели крыс, что 1-часовая HOPE с модифицированным раствором HTK снижает креатинин в перфузате примерно на 40% по сравнению со статической холодовой консервацией. Наши данные показывают снижение на 64% в группе MITOPERF, что указывает на потенциально более выраженный протективный эффект. Критически важным является сравнение с недавно разработанным раствором PERLA (патент Университета Барселоны, 2022–2024), который представляет концептуально близкое решение — консервирующий раствор с митохондриально-направленной защитой. PERLA содержит PEG-35, триметазидин, карведилол и такролимус, реализуя защиту через ингибирование mPTP и частичную антиоксидантную активность. Однако PERLA имеет существенные ограничения: 1) отсутствие специфических антиферроптозных компонентов; 2) минимальную антиоксидантную защиту (нет прямых скевенджеров активных форм кислорода); 3) отсутствие компонентов для ингибирования обратного транспорта электронов; 4) оптимизацию преимущественно для статической холодовой консервации при 4 °C, а не для HOPE при 8–10 °C. К сожалению, авторы PERLA не опубликовали детальных экспериментальных данных в рецензируемых журналах — доступна только патентная документация с ограниченной информацией о степени снижения маркеров повреждения. Это затрудняет прямое количественное сравнение, однако концептуально MITOPERF представляет следующий эволюционный шаг, объединяя митохондриальную защиту, анти-ферроптозную активность и оптимизацию для условий оксигенированной перфузии в единой формуле.
Модифицированный Кустодиол:
практически значимая альтернатива
Промежуточный протективный эффект модифицированного раствора Кустодиол ex tempore (снижение маркеров повреждения на 43–55% по сравнению со стандартным Кустодиолом) представляет самостоятельную клиническую ценность. Добавление трёх фармакологически активных компонентов — N-ацетилцистеина (прекурсор глутатиона), дексаме- 266
тазона (иммуномодулятор) и аденозина (энергетический субстрат и вазодилататор) — к коммерческому раствору HTK может быть реализовано немедленно в клинической практике без необходимости регистрации нового лекарственного средства, поскольку все три компонента являются зарегистрированными фармацевтическими субстанциями с хорошо изученными профилями безопасности.
Механизм действия модификации Кустодиол-М реализуется через несколько путей: 1) N-ацетилцистеин обеспечивает субстрат для ресинтеза глутатиона — главного внутриклеточного антиоксиданта, истощающегося при ишемии, и действует как прямой скевенджер активных форм кислорода благодаря свободной тиоловой группе; 2) дексаметазон подавляет активацию фосфолипазы А₂ через индукцию аннексина-1, стабилизирует клеточные мембраны и ингибирует транскрипцию про-воспалительных цитокинов (TNF- α , IL-1 β , IL-6); 3) аденозин активирует митохондриальные K_ATP-каналы, индуцируя митохондриальную прекондиционирование, и обеспечивает субстрат для ресинтеза пула адениннуклеотидов через salvage pathway.
Уступая MITOPERF по степени протекции (55% vs 76% для печени, 43% vs 64% для почки), Кустодиол-М тем не менее обеспечивает клинически значимое улучшение по сравнению со стандартным подходом. Особенно важным это представляется для центров трансплантации, работающих с донорами с расширенными критериями (ECD) и донорами после остановки кровообращения (DCD), где каждый процент снижения повреждения может определять исход трансплантации. При этом стоимость модификации минимальна (ориентировочно 200–300 рублей на литр раствора), что делает этот подход доступным для широкого внедрения.
Универсальность протективного эффекта: общие механизмы повреждения
Сопоставимая степень протекции MITOPERF на моделях печени и почки (различие в эффективности составляет 12 процентных пунктов) подтверждает концепцию о воздействии на универсальные патофизиологические механизмы ишемически-реперфузионного повреждения, общие для различных паренхиматозных органов. Несмотря на существенные различия в клеточном составе, метаболическом профиле и функциональной специализации печени и почки, ключевые звенья патогенеза ИРП остаются консервативными: митохондриальная дисфункция с обратным транспортом электронов, окислительный стресс, ферроптоз, энергетический дефицит, эндотелиальная дисфункция и воспалительный ответ.
Однако наблюдаемое различие в 12% (76% vs 64%) заслуживает внимания и может объясняться несколькими факторами:
-
1. Различия в метаболическом профиле. Печень характеризуется более интенсивным окислительным метаболизмом и более высокой плотностью митохондрий (особенно в перипортальных гепатоцитах), что делает её более чувствительной к митохондриально-направленной защите. Компоненты MITOPERF, ингибирующие обратный транспорт электронов и стабилизирующие mPTP, могут оказывать более выраженный эффект в клетках с высокой митохондриальной активностью.
-
2. Чувствительность к ферроптозу. Холангиоци-ты печени и эпителий проксимальных канальцев почки демонстрируют различную чувствительность к ферроптозу вследствие различий в экспрессии GPX4, уровне лабильного железа и интенсивности мембранного транспорта. Холангиоциты, осуществляющие активный транспорт желчных кислот и характеризующиеся высоким содержанием полине-насыщенных жирных кислот в мембранах, могут быть более чувствительны к антиферроптозной защите.
-
3. Статистическая вариабельность. Межиндивидуальная вариабельность ответа (CV 35-54%) и относительно небольшой размер выборки (n=6 на группу) не позволяют исключить, что различие в 12% частично обусловлено биологической гетерогенностью экспериментальной модели.
Несмотря на эти различия, принципиально важным является факт выраженного протективного эффекта на обеих моделях, что обосновывает возможность дальнейшего рассмотрения MITOPERF как потенциально универсального консервирующего раствора для мультиорганного забора. Это имеет критическое значение для клинической трансплантологии, упрощая логистику заготовки органов и обеспечивая единообразие протоколов консервации.
Функциональная значимость результатов
Важным аспектом полученных результатов является сохранение не только структурной целостности, но и функциональной активности органов после ишемии-реперфузии. Для печени продукция желчи — интегральный показатель, отражающий сохранность как гепатоцитов (секреция первичной желчи), так и холангиоцитов (модификация желчи в протоках). Достижение объёмной скорости желчеотделения 0,74 мкл/мин/г в группе MITOPERF, приближающейся к физиологическим значениям для ex vivo перфузии крысиной печени (0,8-1,2 мкл/мин/г), свидетельствует о полноценном восстановлении билиарной функции.
Для почки скорость клубочковой фильтрации (GFR) 0,76 мл/мин/г в группе MITOPERF также приближается к физиологическим значениям для изо-
лированной перфузируемой почки крысы (0,8-1,2 мл/мин/г), что указывает на сохранность как клубочкового аппарата, так и функции канальцевого эпителия. Особенно показательным является значение фракционной экскреции натрия (FENa) менее 1% (0,9% в группе MITOPERF против 4,6% в контроле), подтверждающее сохранную реабсорбцию натрия в проксимальных канальцах. Реабсорбция натрия — энергозависимый процесс, требующий функционирования Na+/K+-АТФазы и интактности митохондриального аппарата для продукции АТФ. Значение FENa более 1-2% характерно для острого канальцевого некроза с нарушением реабсорбци-онной функции.
Сохранение функциональной активности органов имеет прямое клиническое значение: в контексте трансплантации критичны не только гистологическая сохранность и отсутствие биохимических маркеров повреждения, но и способность трансплантата немедленно выполнять специфические функции — детоксикацию и синтез белков для печени, фильтрацию и регуляцию водно-электролитного баланса для почки. Недостаточность этих функций в раннем посттрансплантационном периоде определяет такие осложнения, как первичное отсутствие функции трансплантата (primary non-function) и отсроченное восстановление функции (delayed graft function), существенно ухудшающие как краткосрочные, так и долгосрочные результаты трансплантации.
Биологическая вариабельность и размер выборки
Умеренная межиндивидуальная вариабельность показателей (коэффициент вариации 35–54%) требует обсуждения. Подобная вариабельность является типичной для экспериментальных исследований на малых животных при ex vivo перфузии и обусловлена несколькими факторами:
-
1. Вариабельность тепловой ишемии. Несмотря на стандартизацию длительности тепловой ишемии (30 минут), её тяжесть может варьировать между животными вследствие различий в коллатеральном кровообращении, температурной динамике и исходного метаболического состояния органа. Даже небольшие отличия в эффективности пережатия сосудов или поддержании температуры могут приводить к различиям в накоплении сукцината и степени энергетического истощения.
-
2. Индивидуальные различия между животными. Генетическая гетерогенность аутбредных крыс линии Wistar, вариабельность возраста (даже в пределах диапазона 280-320 г), различия в экспрессии антиоксидантных ферментов и уровне базальных митохондриальных резервов могут влиять на чувствительность к ишемически-реперфузионному повреждению и ответ на протективные вмешательства.
-
3. Технические факторы. Качество канюляции (полнота промывки, отсутствие микротромбов), ста-
- бильность перфузионного давления и температуры, однородность оксигенации перфузата могут варьировать между экспериментами, несмотря на стандартизацию протокола.
Априорный расчёт размера выборки (n=6 на группу) был основан на пилотном исследовании с ожидаемой величиной эффекта d=1,5 (очень большая величина эффекта по Cohen) и обеспечивал статистическую мощность 80% при α =0,05 для основных сравнений. Для ключевых параметров (АЛТ, креатинин, 4-HNE, GPX4) достигнутая статистическая мощность превысила 80%, подтверждая достаточность выборки для выявления клинически значимых различий. Однако для параметров с более высокой вариабельностью (желчепродукция, лактат) мощность могла быть ниже оптимальной (60-70%), что требует подтверждения результатов в более крупных исследованиях.
Важно отметить, что наблюдаемая вариабельность не компрометирует выводы исследования: несмотря на CV 35-54%, различия между группами MITOPERF и контролем остаются высоко статистически значимыми (p<0,001–0,01 для большинства параметров после коррекции Холма-Бонферрони), а величина эффекта (effect size) существенна — 70–80% для основных маркеров повреждения.
Многокомпонентность vs минимализм: обоснование сложности состава
Раствор MITOPERF содержит 18 фармакологически активных компонентов, что существенно превосходит сложность существующих клинических растворов (UW — 8 компонентов, HTK — 6, IGL-2 — 10). Это неизбежно поднимает вопрос о необходимости такой сложности и возможности упрощения состава. Обоснованием многокомпонентного подхода служит патофизиологическая гетерогенность ише-мически-реперфузионного повреждения. Современные представления о механизмах ИРП выявляют множественные параллельные пути повреждения, действующие одновременно и взаимно потенцирующие друг друга:
-
• Митохондриальная дисфункция : накопление сукцината → RET → генерация супероксида → открытие mPTP.
-
• Ферроптоз : истощение глутатиона → дисфункция GPX4 → накопление лабильного железа → реакция Фентона → перекисное окисление липидов мембран.
-
• Энергетический дефицит : деградация пула адениннуклеотидов → потеря аденина в виде гипоксантина → невозможность быстрого ресинтеза АТФ.
-
• Эндотелиальная дисфункция : истощение NO → вазоконстрикция → микроциркуляторные нарушения → усугубление ишемии.
-
• Воспалительный ответ : высвобождение DAMPs → активация комплемента → инфильтрация нейтрофилов → усиление повреждения.
Блокирование одного механизма (например, только антиоксидантная защита или только ингибирование mPTP) обеспечивает лишь частичную протекцию, поскольку другие пути повреждения продолжают действовать. Группа Кустодиол-М, содержащая только три добавочных компонента (антиоксидант, иммуномодулятор, энергетический субстрат), демонстрирует промежуточный эффект (43–55% снижения повреждения), тогда как MITOPERF с полноценным покрытием всех пяти основных механизмов достигает 64–76% протекции.
Математическое моделирование патогенеза ИРП показывает, что протективные эффекты различных компонентов не являются простым суммированием, а демонстрируют синергизм: блокирование обратного транспорта электронов снижает образование супероксида, что уменьшает истощение глутатиона, что в свою очередь поддерживает активность GPX4 и предотвращает ферроптоз. Стабилизация mPTP сохраняет митохондриальную структуру и способность к синтезу АТФ, что обеспечивает энергией транспортные системы для поддержания ионного гомеостаза.
Тем не менее, вопрос об оптимизации состава остаётся актуальным. Будущие исследования с использованием факторного дизайна (factorial design) или методологии Response Surface Optimization могут выявить наиболее критичные компоненты и позволить сократить состав без существенной потери эффективности. Однако на текущем этапе, когда целью является максимальная протекция для proof-of-concept, многокомпонентный подход представляется обоснованным.
Клиническая трансляция: возможности и барьеры
Потенциальные клинические применения
Полученные результаты обосновывают несколько направлений клинического применения разработанных растворов:
-
1. Трансплантация печени от доноров DCD. Доноры после остановки кровообращения подвержены более тяжёлому ишемическому повреждению по сравнению с донорами с констатированной смертью мозга (DBD), что приводит к повышенному риску неанастомотических билиарных стриктур (20-30% при SCS vs 5–10% при DBD). Применение MITOPERF в протоколе HOPE может снизить частоту этого осложнения до уровня, сопоставимого с трансплантацией от DBD-доноров, существенно расширяя пул доступных донорских печеней. В России доноры DCD составляют менее 5% от общего числа доноров органов, тогда как в странах Западной Европы
-
2. Трансплантация почки от доноров с расширенными критериями (ECD). ECD-почки характеризуются сниженными функциональными резервами и повышенной чувствительностью к ишемически-реперфузионному повреждению. Применение оптимизированных растворов для машинной перфузии может улучшить раннюю функцию трансплантата, снизить частоту отсроченного восстановления функции (delayed graft function, DGF) и улучшить долгосрочную выживаемость. Учитывая, что в России средний возраст донора почки составляет около 45 лет и продолжает увеличиваться, оптимизация консервации ECD-органов становится всё более актуальной.
-
3. Пролонгированная консервация для дневной трансплантации. Недавнее исследование IDEAL stage 2 (Brüggenwirth et al., EClinicalMedicine 2024) продемонстрировало, что использование пролонгированной гипотермической машинной перфузии (до 12–18 часов) позволяет проводить трансплантацию печени в плановом порядке в дневное время, что улучшает исходы за счёт доступности полноценной хирургической команды и анестезиологического обеспечения. Раствор MITOPERF, оптимизированный для длительной оксигенированной перфузии, может расширить возможности реализации этой стратегии.
-
4. Мультиорганное сохранение с единым консервирующим раствором. Универсальность протек-тивного эффекта MITOPERF на печени и почке обосновывает возможность его использования в качестве единого раствора для мультиорганной заготовки, что упрощает логистику и снижает риск ошибок при работе с множественными растворами.
этот показатель достигает 30–40%. Улучшение результатов использования DCD-органов критично для преодоления дефицита донорских органов.
Модель реперфузии
Использованная модель нормотермической ex vivo реперфузии имеет существенные отличия от условий реперфузии in vivo после трансплантации:
-
1. Отсутствие иммунологического отторжения. Ex vivo перфузия исключает аллоиммунный ответ реципиента, который может усугублять повреждение трансплантата в клинической ситуации. Эффективность MITOPERF в контексте аллоиммунного ответа требует оценки в моделях сингенной или аллогенной трансплантации.
-
2. Упрощённый состав перфузата. Хотя нами использовался перфузат с эритроцитами (гематокрит 20%), это не полностью воспроизводит состав крови с тромбоцитами, лейкоцитами, белками свёртывания и другими компонентами, которые могут взаимодействовать с трансплантатом при реперфузии in vivo.
-
3. Отсутствие нейрогуморальной регуляции. In vivo функция печени и почки регулируется гормонами (инсулин, глюкагон, катехоламины, антидиуре-тический гормон), автономной нервной системой и взаимодействием с другими органами. Эти факторы могут влиять на метаболизм, микроциркуляцию и воспалительный ответ, модифицируя эффективность протективных вмешательств.
Статистическая мощность
Для параметров с высокой межиндивидуальной вариабельностью (CV>40% — желчепродукция, концентрация лактата, некоторые гистологические показатели) достигнутая статистическая мощность могла быть недостаточной (60-75% вместо целевых 80%). Это увеличивает риск ошибки II рода (пропуск истинных различий) для этих параметров. Однако для ключевых маркеров повреждения (АЛТ, креатинин, 4-HNE, GPX4) мощность превышала 80%, что обеспечивает достаточную надёжность основных выводов исследования.
Post-hoc анализ мощности показывает, что для достижения мощности 90% для всех параметров потребовалась бы выборка n=9–12 на группу. Это следует учитывать при планировании подтверждающих исследований.
Отсутствие долгосрочного наблюдения
Настоящее исследование оценивало раннее реперфузионное повреждение (60 минут после реперфузии) и не предоставляет информации о долгосрочных последствиях: регенерации, фиброзировании, развитии хронической дисфункции трансплантата. Для оценки влияния MITOPERF на отдалённые исходы необходимы исследования с моделью трансплантации и наблюдением в течение недель-месяцев.
ЗАКЛЮЧЕНИЕ
Разработанный экспериментальный перфузионный раствор MITOPERF продемонстрировал proof of concept и показал определённую эффективность защиты паренхиматозных органов от ишемически-реперфузионного повреждения при гипотермической оксигенированной консервации. Сопоставимая степень протекции на моделях печени (снижение АЛТ на 76%) и почки (снижение креатинина на 64%) подтверждает воздействие на универсальные патогенетические механизмы повреждения.
Модифицированный раствор Кустодиол ex tempore обеспечивает промежуточный протективный эффект (43–55% снижения маркеров повреждения) и может быть рекомендован к внедрению в клиническую практику без регистрации нового лекарственного средства, что особенно актуально для центров трансплантации, работающих с донорами с расширенными критериями.
Универсальность раствора MITOPERF может определить перспективы его использования в качестве единого консервирующего раствора для муль-тиорганного сохранения, что упрощает логистику заготовки органов и может обеспечивать единообразие протоколов консервации в трансплантологии.
Дальнейшие исследования должны быть направлены на оценку эффективности MITOPERF в клинических условиях при трансплантации органов от доноров после остановки кровообращения (DCD) и доноров с расширенными критериями при более продолжительных сроках холодовой ишемии.


