Оценка пребиотической активности экстрактов растений для разработки препаратов, стимулирующих кишечную микрофлору
Автор: Самойлова З.Ю., Безматерных К.В., Смирнова Г.В., Октябрьский О.Н.
Журнал: Вестник Пермского университета. Серия: Биология @vestnik-psu-bio
Рубрика: Микробиология
Статья в выпуске: 4, 2016 года.
Бесплатный доступ
Проведена оценка пребиотической активности высоких и низких доз водных экстрактов лекарственных растений, зеленого и черного чая путем слежения за изменением интенсивности образования биопленок и колониеобразующей способности зрелых сессильных культур бактерий Escherichia coli BW25113 при культивировании на свежей среде в присутствии экстрактов. Показано, что высокие и низкие дозы экстрактов Arctostaphylos uva-ursi, Vaccinium vitis-idaea, зеленого и черного чая стимулируют биопленкообразование, однако оказывают неоднозначные эффекты на колониеобразующую способность. Высокая пребиотическая активность выявлена у низких доз экстрактов A. uva-ursi и V. vitis-idaea, а также у высоких доз экстрактов зеленого чая. Экстракты Betula pendula и Laminaria japonica не влияли на изменение биопленкообразования, однако высокие дозы проявляли умеренную бактерицидную активность.
Бактериальные биопленки, экстракты растений, пребиотики
Короткий адрес: https://sciup.org/147204796
IDR: 147204796 | УДК: 579.61:579.22
Evaluation of prebiotic activity of plant extracts towards development of preparations stimulating intestinal microflora
The investigation was aimed at evaluation of prebiotic activity of both high and low doses of aqueous medicinal plant extracts, green and black tea. Ability to retain biofilm formation and bacterial survival in mature sessile cultures of Escherichia coli BW25113 was measured during incubation in a fresh medium supplied with different doses of extracts. Both high and low doses of Arctostaphylos uva-ursi, Vaccinium vitis-idaea, green and black tea induced biofilm formation but had vаrious effects on bacterial survival. The highest prebiotic activity was observed in low doses of A. uva-ursi and V. vitis-idaea, and in high doses of green tea as well. The extracts of Betula pendula and Laminaria japonica did not affect biofilm formation but demonstrated moderate bactericidal activity.
Текст научной статьи Оценка пребиотической активности экстрактов растений для разработки препаратов, стимулирующих кишечную микрофлору
В настоящее время совокупную микрофлору кишечника человека рассматривают как отдельный орган, который вносит значительный вклад в поддержание здоровья макроорганизма. Кишечные бактерии образуют биопленки на стенках эпителия кишечника, не только препятствуя адгезии болезнетворных мик-рооргантмов, но и участвуя в процессах обмена веществ (синтез витаминов. переваривание отдельных компонентов пищи и т.д) [Von Rosenvinge et al., 2013]. В связи с этим, одним из актуальных направлений современной науки является поиск веществ и разработка на их основе препаратов-пребиотиков, стимулирующих микрофлору7 кишечника человека и повышающих сопротивляемость макроорганизма к действию неблагоприятных факторов окружающей среды.
Перспективными источниками веществ, обладающих пребиотической активностью, могут быть экстракты растений, которые широко применяются в народной медицине для профилактики и лечения различных заболеваний. Экстракты растений представляют собой смеси высокоактивных биологических веществ, в частности, полифенолов. В низких дозах эти вещества способны выполнять функции
(С Самойлова 3. Ю.. Безматерных К. В., Смирнова Г. В , Октябрьский О. Н., 2016
регуляторных молекул и стимулировать защитные системы клетки. Известно. что полифенолы растений способны оказывать противовоспалительноСк противоопухолевое, антиоксидантное действие, а также положительные эффекты при заболеваниях сердечно-сосудистой и нервной системы [Hanh Shen. Lou, 2007]. Считается, что механизмы положительного влияния субстратов растительного происхождения на организм опосредованы через воздействие на активность кишечной микрофлоры [Halliwell, Rafter. Jenner, 2005; Parkar, Stevenson. Skinner. 2008]. Являясь представителями нормальной микрофлоры человека и животных, бактерии Escherichia сой хорошо изучены в физиологическом и генетическом отношении и поэтому’ являются удобными тест-системами для оценки пробиотической активности экстрактов растений.
Ранее нами было изучено антиоксидантное действие низких доз экстрактов растений и индивидуальных полифенолов на планктонные культуры бактерий Е. сой [Smirnova et al_ 2009, 2012; Okty-abrsky et al., 2009], а также стимулирующее влияние растительных субстратов на образование планктонными культурами Е. сой биопленок [Samoilova et al., 2014]. В научной литературе данные о ВЛИЯНИИ высоких доз растительных субстратов на биопленкообразование противоречивы.
Малоизученным остается влияние экстрактов растений на биопленкообразование зрелых ссе-сильных культур бактерий. Преимуществом и новизной нашего исследования является одновременное изучение в динамике эффектов высоких и низких доз экстрактов растений на биопленкообразование кишечных бактерий и их колониеобра-зутошую способность.
Материалы и методы
В работе использовали штаммы Е. сой BW25113 (wt) из коллекции Keio [Baba et al., 2006]. Биопленки получали следующим образом. Ночные культуры бактерий выращивали в пробирках при 37 °C без встряхивания на минимальной среде М9 (5 мл) [Millen 1972] с добавлением 2.0 г/л глюкозы в течение 16-18 ч. Затем, после центрифугирования при 8000g в течение 5 мин. на центрифуге Thermo Scientific (Германия). клетки из ночной культуры ресуспсндировали в лунках полистироловых 96-луночных планшетов со свежей средой М9 с добавлением 4.0 г/л глюкозы. 0.2%-ных казаминовых кислот тиамина (10.0 мкг/мл) до значения оптической плотности при 600 нм (OD^oo) 0.1. Конечный объем среды составил 200 мкл. Далее эти культуры выращивали в течение 22 ч. при 37°С.
Полученные зрелые биопленки дважды отмывали физиологическим раствором (0.9% NaCI) и ресуспсндировали в 200 мкл свежей среды М9 с добавлением 4.0 г/л глюкозы, 0.2%-ных казаминовых кислот, тиамина (10.0 мкг/мл) и экстрактов растений (действующая доза составляла 0.83 или 6.64 мг сухого вещества/мл). Затем биопленки культивировали в течение 3 ч. на термостатируемом шейкере GFL (Германия) при 37°С, 330 об/мин, каждый час с помощью планшетного спектрофотометра xMark™ Bio-Rad (США) определяя изменение интенсивности биопленкообразования модифицированным методом окрашивания биопленок генцианвиолетом [O’Toole. Kolter, 1998; Naves et al., 2008]. Среду удаляли, и лунки дважды отмывали 200 мкл стерильного физиологического раствора. Лунки подсушивали на воздухе и окрашивали 150 мкл 0.1%-ным раствором красителя генцианового фиолетового в течение 30 мин. Далее краситель удаляли и пятикратно отмывали лунки дистиллированной водой и подсушивали планшеты на воздухе в течение часа. Затем в каждую лунку добавляли 200 мкл 96%-ного этанола, 125 мкл раствора переносили в новый планшет, в котором измеряли светопоглощение OD^o. Интенсивность биоплекообразования рассчитывали согласно формуле
BF = АВ - CW, где АВ - значение OD?^, окрашенных биопленок. CW - значение OD540 окрашенных лунок без клеток.
Для определения колониеобразующей способности лунки планшетов с биопленками дважды отмывали и ресуспсндировали в 200 мкл физиологического раствора. Затем подвергали ультразвуковой дезинтеграции (2 пульса продолжительностью 1 мин, с перерывом в 1 мин, между пульсами, 37 kHz, 30W) в ультразвуковой бане Ultrasonic cleaning unit Elmasonic SI0 H. Elma (Германия). Далее готовили 10-кратные разведения в физиологическом растворе. Капли по 10 мкл высевали на чашки с LB-агаром (1.5%). Подсчет колоний производили через 24 ч. после инкубирования чашек при 37°С.
Тестируемые экстракты растений готовили из отечественных коммерческих препаратов ОАО «Красногорсклексредства» и ЗАО «Иван-Чай» (Россия), зеленый и черный чай - из продуктов марки Greenfield «Golden Ceylon», Greenfield tea Ltd (Великобритания).
Перечень экстрактов приведен в таблице Сухую навеску (1 г) заливали 30 мл горячей воды и заваривали на водяной бане в течение 30 мин., охлаждали, фильтровали на мембранном фильтре. Для получения концентрированных экстрактов пользовались концентратором IKA RV10 (Германия). Во всех экспериментах использовали свежие экстракты.
Результаты и их обсуждение
В начале культивирования зрелых биопленок Е. сой BW25113 на свежей среде в отсутствие экстрактов растений показатель OD^n составил 0.116 ± 0.012, а через час резко упал до 0.076 ± 0.007, а к концу культивирования понизился до 0.061 ± 0*007. В присутствие низкой дозы (0*83 мг сухого вещества/мл) экстрактов Г vitis-idaea, A. ava-arsi. зеленого и черного чая через час после начала культивирования наблюдалось, напротив, достоверное увеличение интенсивности биопленкообра-зования (БПО) в 2.3, 4.2, 2.3 и 1*9 раза, соответственно. по сравнению с необработанными экстрактами биопленками (рис* 1)* Через 2 ч* низкие дозы указанных экстрактов повышали биопленкообра-зование в 7 9,4 х 3 3 и 2 раза, соответственно.
Перечень испытуемых экстрактов растений
|
Название коммерческого препарата |
Латинское название растений |
|
Зеленый чай |
Camellia sinensis |
|
Черный чай |
Camellia sinensis |
|
Uvae ursi folia, толокнянки листья |
Arctostaphylos uva-ursi |
|
Vitis-idaeae folia, брусники листья |
Coccinium vitis-idaea |
|
Betulae folia, берёзы листья |
Benda pendula |
|
Laminariae thali, ламинарии слоевища |
Laminaria japonica |
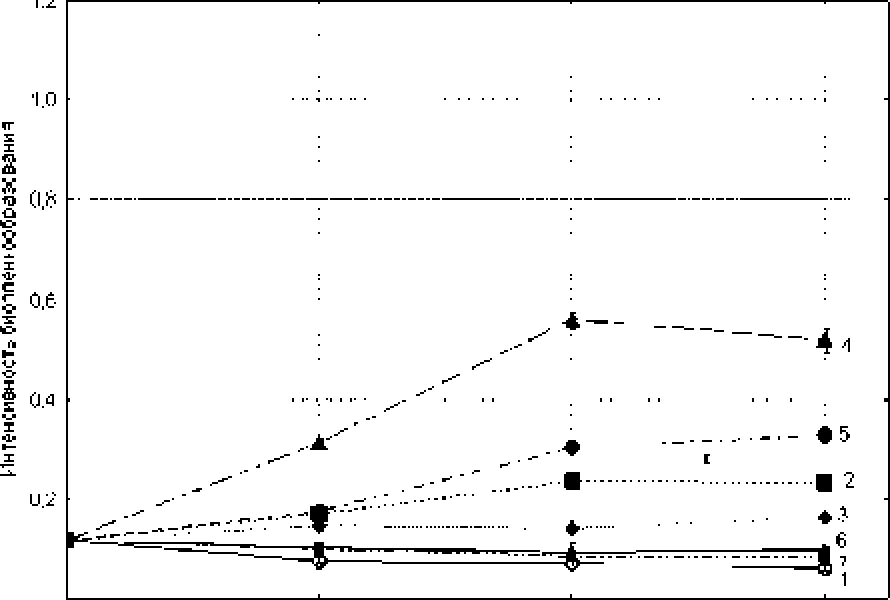
Время. ч
Рис. L Изменение интенсивности биоплен-кообразования Е. colt BW25113 при инкубации с низкими дозами экстрактов (0 83 мг сухого вещества/мл):
1 - контроль (без экстракта); 2 - С sinensis (зеленый чай); 3 - С. sinensis (черный чай); 4 - А. uva-«rsi\ 5 - I" vitis-idaea; 6 -В. pendula; 1 -L. japonka
В конце культивирования наблюдалось БПО в 8.5, 5.4, 3.8 и 2.7 раза, соответственно. Примечательно, что при этом низкие дозы всех экстрактов, за исключением В. pendukh стимулировали повышение колониеобразующих единиц (КОЕ) бактерий в составе сессильных культур (рис. 2). Низкие дозы всех испытуемых экстрактов оказывали стимулирующее влияние на колониеобразутошую способность бактерий, повышая показатель КОЕ в 1.9 (зеленый чай) - 7.6 (толокнянка) раза. Максимальный стимулирующий эффект на БПО и ный стимулирующий эффект на БПО и колониеобразующую способность Е. со И BW25113 на протяжении всего периода культивирования оказывали низкие дозы Л. uva-ursi и К 17Г^г-/^^<7*
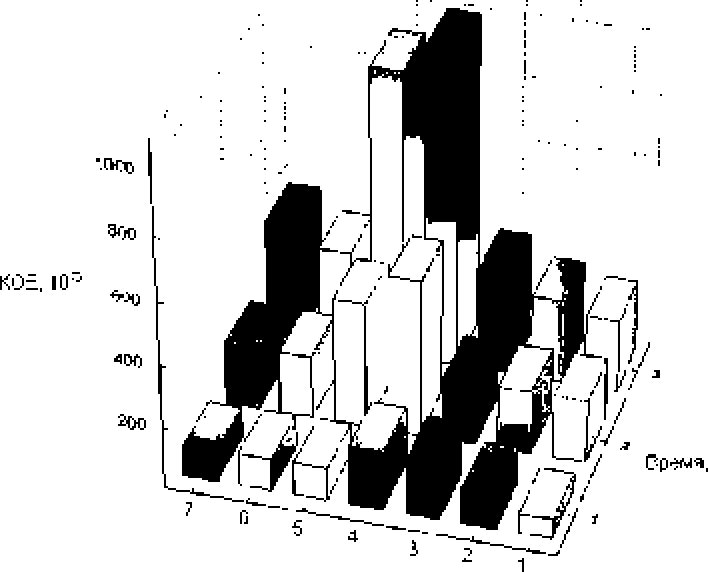
Рис. 2* Изменение показателя колониеобразующих единиц биопленок при культивировании в присутствии низких доз экстрактов.
Обозначения как на рис. 1
В целом действие высоких доз (6.64 мг сухого вещества/мл) экстрактов на БПО имело еще более выраженный стимулирующий характер (рис. 3). Через час обработки высокими дозами экстрактов А» uva-ursi, Г* vitis-idaea, зеленого и черного чая БПО увеличивалось в 5.4, 5.4, 2.5 и 1.7 раза, соответственно, по сравнению с необработанными экстрактами биопленками. При этом экстракты К vi-iis-idaea и В. pendula (6.64 мг сухого вещества/мл) снижали показатель КОЕ в 7.5 н 1.7 раза. А высокие дозы экстракта Л+ uva-ursi повышали КОЕ в 2 раза (рис. 4).
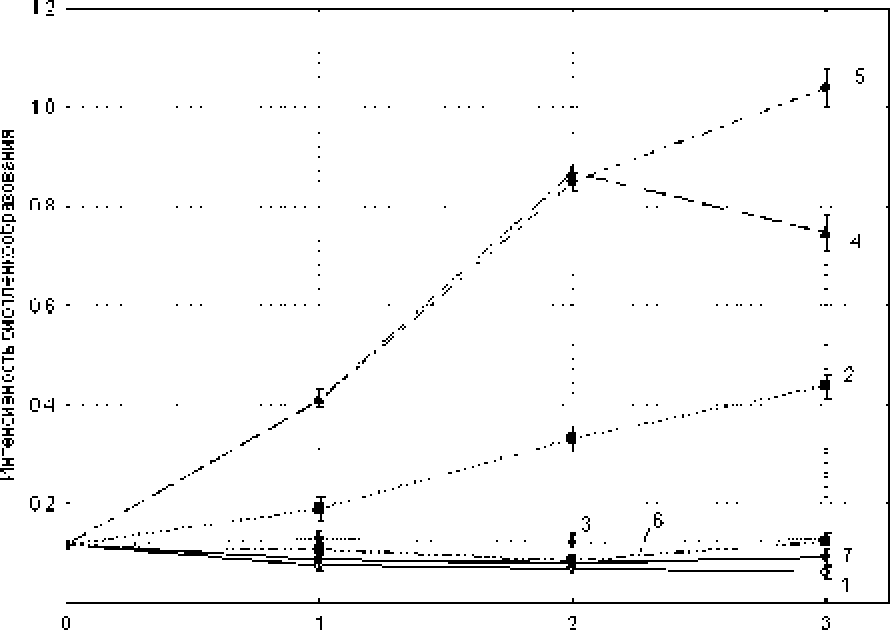
бремя ч
Рис* 3, Изменение интенсивности биоплен-кообразования Е. соii BW25113 при инкубации с высокими дозами экстрактов (6.64 мг сухого вещества/мл)*
Обозначения как на рис. 1
Через 2 ч. после начала культивирования А. uva-ursi, С. vitis-idaea, зеленого и черного чая БПО увеличилось в 12.0, 12*0, 4*6 и 1.7 раза, соответст- венно. Повышение интенсивности БПО в присутствии высоких доз A. uva-ursi и V. vitis-idaea сопровождалось понижением КОЕ б 2*6 и 2.3 разак соответственно. Хотя высокие дозы экстрактов В. pendula и L. japonica нс влияли на БПО* в их присутствии отмечалось достоверное снижение КОЕ в 2*7 и 2.0 раза, соответственно. К концу культивирования высокие дозы экстрактов .4. uva-ursh И vitis-idaea, зеленого, черного чая и березы стимулировали БПО в 12.0, 17.0, 7.2, 2.1 и 2.0 раза. При этом высокие дозы экстрактов зеленого чая стимулировали колониеобразующую способность в 1.7 раза, а экстракт В. pendula снижал показатель КОЕ в 1.4 раза.
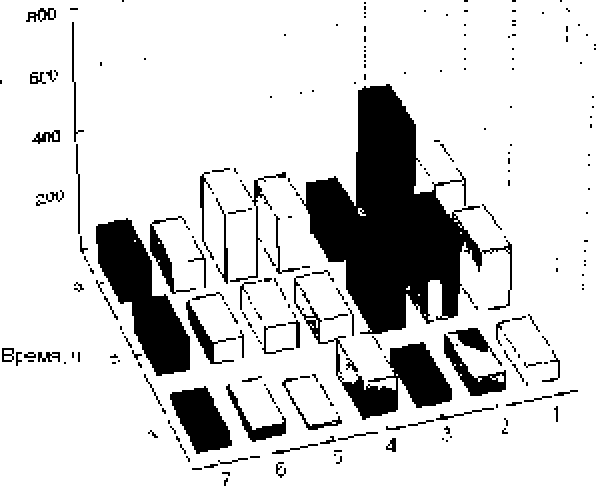
Рис 4* Изменение показателя колониеобра-зутощих единиц биопленок при культивировании в присутствии высоких доз Экстрактов.
Обозначения как на рис. 1
Б совокупности, наши результаты свидетельствуют о стимулирующем влиянии высоких и низких доз экстрактов A. uva-ursi. К vitis-idaea, зеленого и черного чая на БПО кишечных бактерий и неоднозначном влиянии на показатель КОЕ.
Учитывая оба исследованных показателя, в наших условиях наиболее высокой пребиотической активностью обладали низкие ДОЗЫ A. uva-ursi и К vitis-idaea, а также высокие дозы зеленого чая.
Наблюдаемые нами стимулирующие эффекты на БПО могли быть вызваны подавлением подвижности и стимуляцией факторов адгезии гра-мотрицательных бактерий [LaPlante et al.? 2012]. Имеются сведения о пребиотических эффектах компонентов зеленого чая на бактерии spp. Bifidobacterium и Lactobacillus [Lee et al., 2006: Tzounis et al., 2008]* Сообщается, что высокие дозы J< vitis-idaea и В. pendula (10-20 мг сухого веса/мл) оказывали бактерицидные эффекты на бактерии Е. coli [Wojnicz et al * 2012]. В наших условиях используемые дозы указанных экстрактов были ниже* однако 6.64 мг сухого вещества/мл приводили к снижению показателя КОЕ* Высокие дозы экстрактов В. pendula и L. japonica также проявляли умеренную бактерицидную активность.
Заключение
Выявленные стимулирующие эффекты НИЗКИХ доз экстрактов Л. uva-ursi, К vitis-idaea, а также высоких доз зеленого чая на БПО и колониеобразующую способность свидетельствуют о высокой пребиотической активности, а также указывают на перспективность создания пребиотических препаратов на основе указанных растений.
В целом выявленные эффекты расширяют представления о физиологии И ЭКОЛОГИИ кишечных бактерий, однако лежащие в их основе механизмы нуждаются в дальнейшем исследовании.
Работа поддержана грантом РФФИ-Урал №14-04-96031.
Список литературы Оценка пребиотической активности экстрактов растений для разработки препаратов, стимулирующих кишечную микрофлору
- Baba T. et al. Construction of Escherichia coli strain K-12 in-frame, single-gene knockout mutants: the Keio Collection//Mol. Biol. Syst. Biol. 2006. Vol. 2: 0008.
- Halliwell B., Rafter J., Jenner A. Health promotion by flavonoids, tocopherols, tocotrienols, and other phenols: direct or indirect effects? Antioxidants or not?//Am. J. Clin. Nutr. 2005. Vol. 81(suppl.). P. 268S-276S.
- Han X., Shen T., Lou H. Dietary polyphenols and their biological significance//Int. J. Mol. Sci. 2007. Vol. 8. P. 950-988.
- LaPlante K.L. et al. Effects of cranberry extracts on growth and biofilm production of Escherichia coli and Staphylococcus species//Phytother. Res. 2012. Vol. 26. P. 1371-1374.
- Lee H.C. et al. Effect of tea phenolics and their aromatic fecal bacterial metabolites on intestinal microbiota//Res. Microbiol. 2006. Vol. 157. P. 876-884.
- Miller J.H. Experiments in molecular genetics. Cold Spring Harbor: Cold Spring Harbor Laboratory Press, 1972
- Naves P. et al. Measurement of biofilm formation by clinical isolates of Escherichia coli is methoddependent//J. Appl. Microbiol. 2008. Vol. 105. P. 585-590.
- Oktyabrsky O. et al. Assessment of antioxidant activity of plant extracts using microbial test systems//J. Appl. Microbiol. 2009. Vol. 106. P. 1175-1183.
- O’Toole G.A., Kolter R. Initiation of biofilm formation in Pseudomonas fluorescens WCS365 proceeds via multiple, convergent signaling pathways: a genetic analysis//Mol. Microbiol. 1998. Vol. 28. P. 449-461.
- Parkar S.G. Stevenson D.E., Skinner M.A. The potential influence of fruit polyphenols on colonic microflora//Int. J. Food Microbiol. 2008. Vol. 124. P. 295-298.
- Samoilova Z. et al. Medicinal plant extracts can variously modify biofilm formation in Escherichia coli//Antonie van Leeuwenhoek. 2014. Vol. 105. P. 709-722
- Smirnova G.V. et al. Influence of polyphenols on Escherichia coli resistance to oxidative stress//Free Radic. Biol. Med. 2009. Vol. 46. P. 759-768.
- Smirnova G. et al. Influence of plant polyphenols and medicinal plant extracts on antibiotic susceptibility of Escherichia coli//J. Appl. Microbiol. 2012. Vol. 113. P. 192-199.
- Tzounis X. et al. Flavanol monomer-induced changes to the human faecal microflora//Br. J. Nutr. 2008. Vol. 99. P. 782-792.
- Von Rosenvinge E.C. et al. Microbial biofilms and gastrointestinal diseases//Pathogens and disease. 2013. Vol. 67. P. 25-38.
- Wojnicz D. et al. Medicinal plant extracts affect virulence factors expression and biofilm formation by the uropathogenic Escherichia coli//Urol. Res. 2012. Vol.40. P. 683-697.


