Оценка результатов малоинвазивного лечения ятрогенных стриктур и функции детрузора после реконструкций дистальных отделов мочеточника
Автор: Панферов А.С., Бекреев Е.А., Ястребов Виталий Сергеевич, Медведева Е.В., Елагин В.В.
Журнал: Экспериментальная и клиническая урология @ecuro
Рубрика: Реконструктивная урология
Статья в выпуске: 4 т.17, 2024 года.
Бесплатный доступ
Введение. Травмы мочеточника встречаются в 1-2,5% случаев всех поражений мочеполовых органов. На долю ятрогенных повреждений приходится более 80% случаев. Их количество связано с активным внедрением в практику малоинвазивных методов лечения. Выбор реконструктивной операции у данных пациентов зависит от функционального состояния почек и мочеточников, протяженности и уровня стриктуры. Особое значение имеет методика Боари, что связано с общим эмбриогенезом нижних мочевых путей. В случае наличия натяжения в зоне анастомоза предпочтительно применять методику psoas-hitch.
Стриктуры дистальных отделов мочеточника, операция боари, функциональные характеристики нижних мочевыводящих путей
Короткий адрес: https://sciup.org/142243848
IDR: 142243848 | DOI: 10.29188/2222-8543-2024-17-4-124-133
Evaluation of the results of minimally invasive treatment of iatrogenic strictures and detrusor function after the distal ureter reconstructions
Introduction. Injuries to the ureter occur in 1-2,5% of cases of all lesions ofthe genitourinary organs. Iatrogenic injuries account for more than 80% of cases. Their number is associated with the active application of minimally invasive treatment methods into practice. The choice of reconstructive surgery in these patients depends on the functional state of the kidneys and ureters, the extent and level of stricture. Of particular importance is the Boari technique, which is associated with the general embryogenesis of the lower urinary tract. If there is tension in the anastomosis ar ea, it is preferable to use the psoas-hitch technique.
Текст научной статьи Оценка результатов малоинвазивного лечения ятрогенных стриктур и функции детрузора после реконструкций дистальных отделов мочеточника
экспериментальная и клиническая урология № 4 2024
Травмы мочеточника встречаются в 1-2,5% случаев всех поражений мочеполовых органов. Выделяют несколько основных групп ятрогенных стриктур мочеточников: посттравматические, поствоспалительные и постлучевые [1].
Отмечается высокая частота повреждения мочеточника при хирургических, гинекологических и эндо-урологических операциях (табл. 1) [2]. Такие вмешательства сами по себе могут также негативно влиять на функцию мочевого пузыря за счет нарушения тазовой иннервации и кровоснабжения [3]. На долю ятрогенных повреждений приходится более 80% случаев [4]. Увеличение количества связано с активным внедрением в практику малоинвазивных методов лечения.
После уретероскопии стриктуры мочеточника возникают у 3-11% у пациентов,а после ретроградной интраренальной хирургии ятрогенное повреждение мочеточника возникает в 46,5% [5, 6].
На долю проксимальной локализации стриктур мочеточника приходится до 70% случаев, на другие отделы мочеточника – 30% [5].
Выбор реконструктивной операции у данных пациентов зависит от функционального состояния почек и мочеточников, протяженности и уровня стриктуры: при локализации в верхней трети целесообразна уре-теро-уретеростомия, трансуретеро-уретеростомия, уретерокаликостомия; в средней трети – уретеро-уре-теростомия, трансуретеро-уретеростомия или операция Боари; в нижней трети – прямая реимплантация, операция Боари или psoas-hitch [4]. Использование собственных неизмененных тканей мочевых путей является наиболее предпочтительным и физиологичным вариантом хирургического лечения сужений и облитераций мочеточника. При стриктурах в дистальных отделах мочеточника операцией выбора является уретероцистоанастомоз. Применение в качестве трансплантатов для реконструкции мочеточников различных кишечных сегментов является важным этапом развития урологии [7].
Особое значение имеет методика Боари, что связано с общим эмбриогенезом нижних мочевых путей.
При этом возможно использование антирефлюкс-ных методик: интравезикальных (операция Коэна), трансвезикальных (операция Политано–Лидбеттера) и экстравезикальные (операция Лич–Грегуара).
Уретероцистоанастомоз выполняется пациентам со стриктурами нижней трети мочеточника, протяженностью до 5 см. При стриктуре мочеточника от 4 до 15 см целесообразно использовать методику Боари [8].
В случае наличия натяжения в зоне анастомоза предпочтительно применять методику psoas-hitch.
При более протяженном повреждении мочеточника используется кишечная пластика.
О.В. Гаина и соавт. провели ретроспективный анализ реконструктивных лапароскопических и открытых операций у больных с различной этиологией стриктур мочеточников: урологические, гинекологические, хирургические вмешательства, опухоли мочеточников, лучевая терапия. Авторы сделали вывод о преимуществах лапароскопической техники в виде снижения риска осложнений, времени вмешательства, кровопотери, сроков госпитализации [9].
В.А. Воробьев с соавт. продемонстрировали успешные результаты реконструктивной операции по Боари без использования антирефлюксных методик [4]. Частота развития вторичного рефлюкс-пиелонеф-рита в послеоперационном периоде сопоставима с данными других авторов [10].
-
K. Bausch и соавт. в ретроспективном исследовании сообщают об эффективности лапароскопической робот-ассистированной пластики нижней трети
мочеточника без использования антирефлюксных методик [11]. Отечественные авторы также отмечают эффективность и безопасность робот-ассистированных вмешательств как способа лечения посттравматических стриктур нижней трети мочеточника, позволяющего проводить симультанные реконструктивные операции [12, 13].
Высокая эффективность лапароскопической пластики мочеточника по Боари и psoas hitch показана в исследованиях G . Zhang и соавт. [14] и M . Singh и соавт. [15]. Все пациенты после операции не имели симптомов рефлюкса или инфекции мочевых путей.
Согласно данным литературы, малоинвазивные методы лечения стриктур мочеточников различной этиологии наиболее эффективны по сравнению с открытыми вмешательствами [16].
При этом использование антирефлюксных методик не оказывает статистически значимого влияния на результаты хирургического лечения [17].
Б.К. Комяков с соавт. при изучении уродинамиче-ских характеристик нижних мочевыводящих путей показали, что восстановление мочеточника за счет тканей мочевого пузыря достоверно уменьшает его функциональную емкость, снижает эластичность стенки, проявляясь склонностью к нейрогенной дисфункции мочевого пузыря и пузырно-лоханочным рефлюксам [18].
Демченко В.Н. и соавт. оценили эффективность использования лоскутов из мочевого пузыря различной длины. В своей работе в большинстве случаев авторы применили технику операции Боари с использованием антирефлюксного механизма при натяжении в зоне анастомоза. Авторы также отметили,что дан-
Таблица 1. Этиология стриктур верхних мочевых путей Table 1. Etiology of strictures of the upper urinary tract
МАТЕРИАЛЫ И МЕТОДЫ
В основу работы легли результаты лечения 42 пациентов, находящихся на стационарном лечении в клинике МЦ «Медассист» с 2019 по 2024 год, которым выполнены лапароскопические реконструктивные операции по поводу стриктуры нижней трети мочеточника.
Средний возраст больных составил 53,8±4,35 года. Из них у 9 пациентов (21,4%) диагностирована стриктура выше подвздошных сосудов, у 33 (78,6 %) пациентов – ниже подвздошных сосудов. У 27 (64,3%) больных в анамнезе были урологические вмешательства (урете-роскопия, контактная уретеролитотрипсия, стентирование мочеточника, уретероцистонеоанастомоз, уре-теролитотомия, ТУР мочевого пузыря), у 8 (19,0%) – экстирпация матки или кесарево сечение. Пяти (11,9%) пациентам проводилось лечение по поводу злокачественных заболеваний органов малого таза (экстирпация матки с резекцией мочеточника) и мочекаменной болезни (дистанционная уретеролитотрипсия). У 2 (4,8 %) пациентов имели место идиопатические стриктуры мочеточников (табл. 2).
Всем больным выполнялось оперативное лечение в объеме лапароскопической пластики мочеточника по методике Боари и psoas-hitch.
Описание оперативного вмешательства
После стандартной обработки операционного поля под многокомпонентной анестезией в условиях тотальной миорелаксации в мочевой пузырь устанавливался катетер Фолея №18 Ch. Далее на 1 см выше пупка устанавливался оптический троакар 10 мм. Создавался карбоксиперитонеум с давлением 12 мм рт. ст. Пациента переводили в положение Тренделенбурга. В левой паховой области устанавливали два рабочих троакара 10 и 5 мм. В правой паховой области устанавливали два троакара 5 мм. Выделялись мочеточники до и проксимальнее предполагаемой стриктуры для избежания натяжения в области анастомоза (рис. 1).
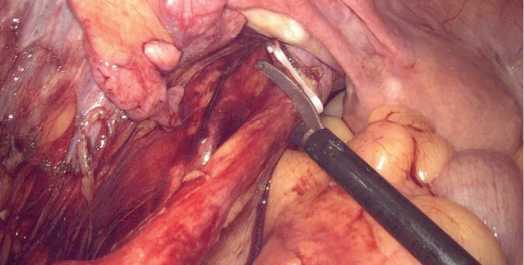
Рис. 1. Пересечение мочеточника проксимальнее предполагаемой стриктуры
Fig. 1. The transection of the ureter is proximal to the intended structure
Выделялся лоскут из передней стенки мочевого пузыря (рис. 2), мочеточник пересекался над местом стриктуры. В мочеточник проводился стент-катетер №6 Ch, дистальный конец стент-катетера проводился в мочевой пузырь (рис. 3).
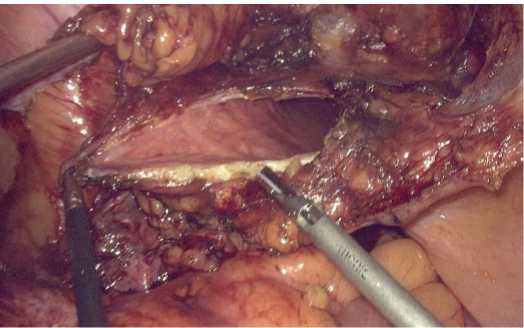
Рис. 2. Выделение лоскута мочевого пузыря
Fig. 2. Cutting out of the bladder flap
Таблица 2. Этиология стриктур мочеточников у пациентов
Table 2. Ureteral strictures’ etiology of patients
|
Этиология Etiology |
n, % |
|
Урологические вмешательства (уретероскопия, контактная уретеролитотрипсия, стентирование мочеточника, уретероцистонеоанастомоз, уретеролитотомия, ТУР мочевого пузыря) Urological interventions (ureteroscopy, contact ureterolithotripsy, ureteral stenting, ureterocystoneoanastomosis, ureterolithotomy, bladder resection) |
27 (64,3) |
|
Гинекологические операции (экстирпация матки, кесарево сечение) Gynecological operations (extirpation of the uterus, cesarean section) |
8 (19,0) |
|
Гинекологические злокачественные заболевания и связанные с ними операции (экстирпация матки, резекцией мочеточника, дистанционная лучевая терапия) Gynecological malignant diseases and related operations (extirpation of the uterus, ureteral resection, remote radiotherapy) |
5 (11,9) |
|
Идиопатические причины Idiopathic causes |
2 (4,8) |
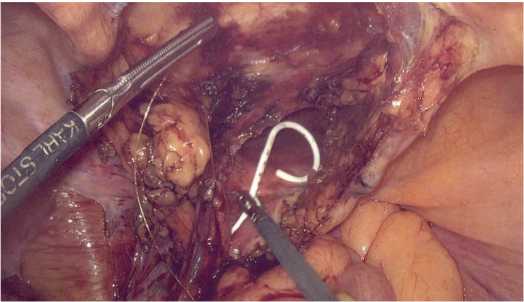
Рис. 3. Установка стент-катетера в мочеточник
Fig. 3. Stent-catheter insertion into the ureter
Накладывался мочеточниково-пузырный анастомоз, тубуляризация лоскута мочевого пузыря на стент-катетере непрерывным швом при помощи синтетической рассасывающейся моноволоконной нити из полидиоксанона 4/0, игла ½ (рис. 4).
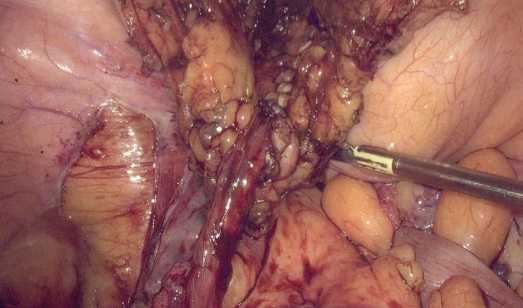
Рис. 4. Тубуляризация лоскута мочевого пузыря на стент-катетере
Fig. 4. Tubularization of the bladder flap on a stent-catheter
Стенка мочевого пузыря ушивалась непрерывным швом (синтетическая рассасывающаяся моноволокон-ная нить из полидиоксанона 4/0, игла ½) с последующим контролем его герметичности. При использовании методики psoas-hitch лоскут мочевого пузыря фиксировался к поясничной мышце (рис. 5). Устанавливали дренаж в пространство малого таза. Троакары поочередно удалялись с контролем гемостаза.
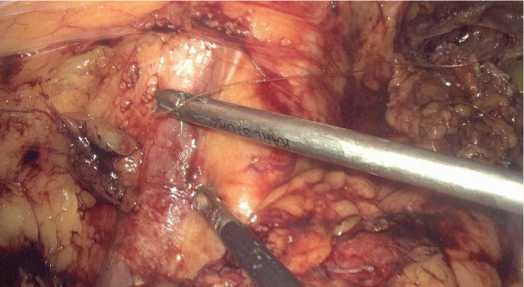
Рис. 5. Фиксация лоскута мочевого пузыря к поясничной мышце
Fig. 5. Fixation of the bladder flap to the lumbar muscle
Тридцати трем (78,6%) пациентам оперативное пособие выполнялось в объеме операции Боари, 9 (21,4%) пациентам была применена методика psoashitch. Средняя продолжительность операции составила 126±34,45 мин, средний объем кровопотери – 110,34±47,37 мл. Срок послеоперационной госпитализации – 4,09±0,54 дней. Сроки дренирования мочевого пузыря составили 8,5±2,04 дней, мочеточника – 29,5±2,86 дней. В послеоперационном периоде у всех пациентов выявлена I степень осложнений по Clavien-
Таблица 3. Результаты оперативного лечения
Table 3. Тhe results of surgical treatment
|
Характеристика операций Characteristics of operations |
Результаты Results |
||||||||
|
Методика Methodology |
|
||||||||
|
Продолжительность (мин) Duration (min) |
126±34,45 |
||||||||
|
Кровопотеря (мл) Blood loss (ml) |
110,34±47,37 |
||||||||
|
Осложнения по Clavien-Dindo Complications by Clavien-Dindo Количество пациентов, % Number of patients, % |
I 42 (100%) |
II 0 |
III 0 |
IIIa 0 |
IIIb 0 |
IV 0 |
IVa 0 |
IVb 0 |
V 0 |
|
В послеоперационном периоде требовалось внутривенное введение анальгетиков In the postoperative period, intravenous administration of analgesics was required |
|||||||||
|
Визуально аналоговая шкала (ВАШ), баллы Visually analog scale (VAS), points |
1 сутки 1 day |
2 сутки 2 days |
3 сутки 3 days |
||||||
|
5,96±0,67 |
1,68±0,46 |
||||||||
|
Сроки дренирования мочевого пузыря (дни) Timing of bladder drainage (days) |
8,5±2,04 |
||||||||
|
Сроки дренирования мочеточника (дни) Timing of ureter drainage (days) |
29,5±2,86 |
||||||||
|
Койко-день Lenth of stay |
4,09±0,54 |
||||||||
Dindo (требовалось внутривенное введение анальгетиков). Выраженность болевого синдрома оценивалась по визуальной аналоговой шкале (ВАШ). Она уменьшалась к третьим суткам после операции: в 1-е сутки – 5,96±0,67 баллов, на 3-и сутки – 1,68±0,46 балов (табл. 3).
РЕЗУЛЬТАТЫ
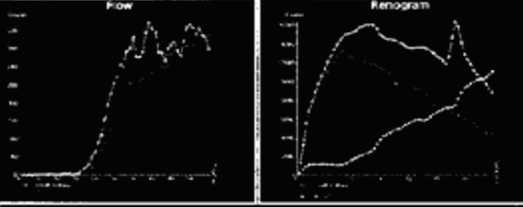
По данным мультиспиральной компьютерной томографии (МСКТ) органов мочевыделительной системы, за период наблюдения рецидива не выявлено ни у одного из исследуемых. По данным динамической нефросцинтиграфии, после проведения оперативного лечения зафиксировано улучшение функциональных показателей работы почек у основной массы исследуемых пациентов (n = 39; 92,9%) (рис. 6, 7).
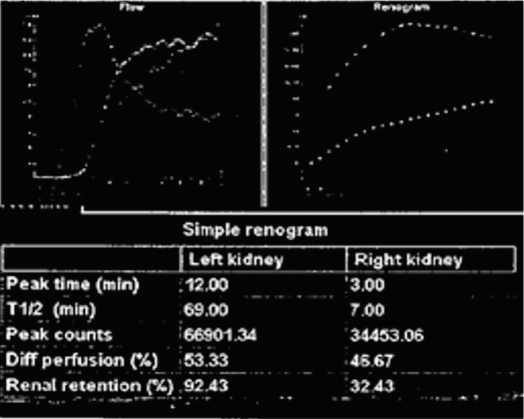
Рис. 6. Динамическая нефросцинтиграфия до оперативного лечения
Fig. 6. Dynamic nephroscintigraphy before surgical treatment
По данным ультразвукового исследования (УЗИ) c наполненным мочевым пузырем: у 27 (64,3%) пациентов расширения полостной системы со стороны оперированного мочеточника не выявлено, у 8 (19,0%) – выявлены признаки гидронефроза I и у 7 (16,7%) – II степени, что указывает на наличие пассивного рефлюкса у 15 (35,7%) пациентов. Атаки пиелонефрита зафиксированы у 3 (7,1%) пациентов, при этом данные
|
Simple renogram |
||
|
1 |
| Left kidney |
[Right kidney |
|
Peak time (mln) i |
17 00 |
5.00 " ’" |
|
Т1Г2 (mln) |
464 |
12.00 |
|
Peak counts | |
16269 67 |
1321267 |
|
i Diff perfusion (%) |
61.96 |
46 04 |
|
Renal retention (%) |
63.ca ' ~ |
35.16 |
Рис. 7. Динамическая нефросцинтиграфия после оперативного лечения Fig. 7. Dynamic nephroscintigraphy after surgical treatment пациенты имели в анамнезе:дистанционную лучевую терапию на органы малого таза (n=1; 2,4%); открытую пластику мочеточника по Боари (n=1; 2,4 %); инфраве-зикальную обструкцию (доброкачественная гиперплазия предстательной железы) – у 1 (2,4%) пациента, после хирургического устранения которой атак пиелонефрита зафиксировано не было (табл. 4).
Оценка симптомов гиперактивного мочевого пузыря проводилась при помощи опросника «Russian version of the OA B Awareness Tool». Сумма баллов не превышала порогового значения 8, что соответствует удовлетворительному качеству жизни (рис. 8).
Таблица 4. Отдаленные результаты хирургического лечения
Table 4. Long-term results of the surgical treatment
Параметр Parameter
Значение Meaning
Проходимость мочеточника (МСКТ) Patency of the ureter
Динамическая нефросцинтиграфия, степень обструкции, n (%) Dynamic nephroscintigraphy, degree of obstruction, n (%)
Т1/2 достигнуто T1/2 achieved
100%
Т1/2 не достигнуто T1/2 not achieved
Пассивный рефлюкс (УЗИ), n (%) Passive reflux (ultrasound), n (%)
39 (92,9)
3 (7,1)
Полный разрыв мочеточника с участком деваскуляризации менее 2 см
Complete ureteral rupture with devascularization area less than 2 cm
15 (35,7)
Эпизоды пиелонефрита, n (%)
Episodes of pyelonephritis, n (%)
3 (7,1)
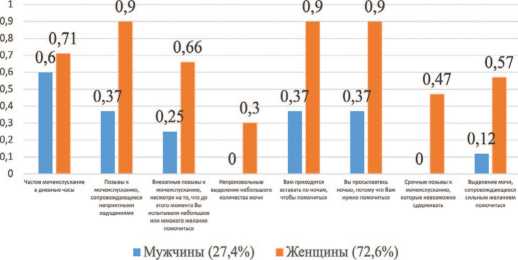
Рис. 8. Оценка симптомов гиперактивного мочевого пузыря (Russian version of the OAB Awareness Tool)
Fig. 8. Assessment of symptoms of an overactive bladder (Russian version of the OAB Awareness Tool)
Все пациенты имели невыраженную симптоматику гиперактивности мочевого пузыря.
Во всех случаях выполнена цистометрия (напол- нения и опорожнения). Исследование производилось непосредственно до операции и через 3 месяца после (рис. 9, 10).
Детрузорное давление (итоговое) PdetE - 15.8 cmHzO
Везикальное давление (макс.) PvesX = 35.7 cmHzO
Объем мочевого пузыря Vmax = 369.0 ml
|
Позыв |
Первый |
Норм. |
Сильн. |
Ургент. |
Цист.Емк |
|
|
Comp |
ml/cmHzO] |
10.5 |
13.4 |
16.6 |
26.4 |
24.6 |
|
Pdet |
cmHzO] |
7 |
8 |
10 |
15 |
16 |
|
Pves |
cmHzO] |
2 |
3 |
3 |
8 |
9 |
|
Pabd |
cmHzO] |
-5 |
-5 |
-7 |
-7 |
-7 |
|
Рига |
cmHzO] |
0 |
0 |
0 |
0 |
0 |
|
Vinf |
ml] |
63 |
94 |
149 |
369 |
369 |
Везикальное давление (итоговое) PvesE - 8.9 cmHzO
-
< г 70 - -- -- не>
-
< г 400 ----- 600>
Markl Mark2 МагкЗ Магк4 Marks < IS - # - - - 45>
0 0 0 00
0 0 0 00
0 0 0 00
0 0 0 00
0 0 0 00
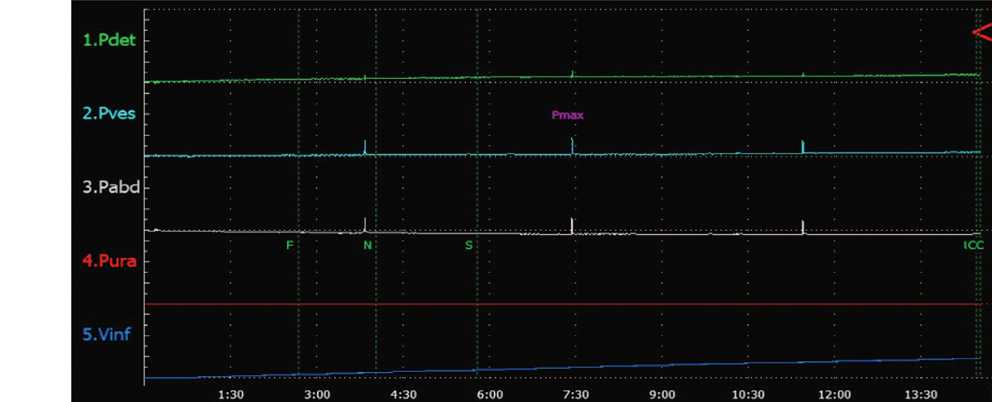
Рис.9. Цистометрия наполнения до оперативного лечения
Fig.9. Filling cystometry before surgical treatment
Детрузорное Везикальное Объем мочеся
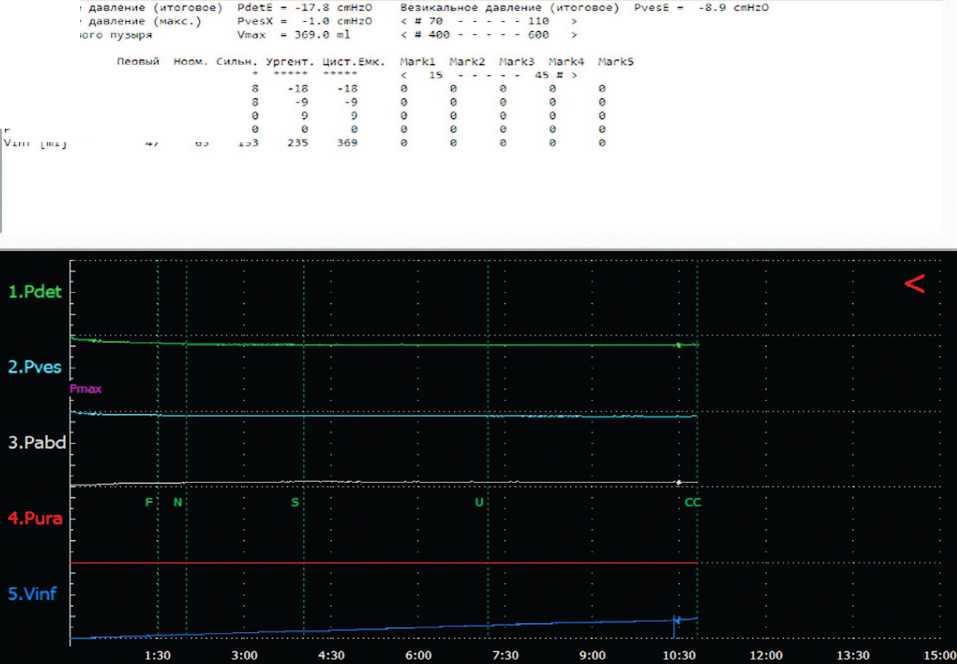
Рис.10. Цистометрия наполнения после оперативного лечения
Fig.10. Filling cystometry after surgical treatment
|
Позыв: |
Первый |
норм. |
Сильн. |
|
comp [ml/cmHzO] |
----- |
----- |
|
|
Pdet [cmHzO] |
-15 |
-16 |
-18 |
|
Pves [cmHzO] |
-8 |
-8 |
-8 |
|
Pabd [cmHzO] |
7 |
8 |
10 |
|
Рига [cmHzO] |
0 |
0 |
0 |
|
Vinf [ml] ' |
47 |
63 |
133 |
В зависимости от длины лоскута мочевого пузыря пациенты были разделены на 2 группы: I группа – пациенты с длиной лоскута мочевого пузыря до 5 см; II группа – пациенты с длиной лоскута мочевого пузыря свыше 5 см. В первой группе показатель детрузорного давления составил 13,6±3,1 см.вод.ст. до и 24,6±4,7 см.вод.ст. после операции. Во второй – 12,3±2,1 см.вод.ст. до и 19,2±3,7 см.вод.ст. после операции. Максимальная цистометрическая емкость в первой группе исследуемых до операции была 397±34,2 мл; после – 405±37,9 мл. Во второй группе 374±24,4 мл до и 394±28,7 мл – после операции. Максимальная скорость мочеиспускания в первой группе составила 8,6±4,3 мл/сек до и 16,7±3,1 мл/сек – после операции. Во второй группе – 12,7±2,7 до и 17,1±3,4 мл/сек после операции. Объем остаточной мочи в первой группе – 155±27,9 мл до операции и 47,8±18,4 мл – после операции. Во второй группе – 87±14,7 мл – до и 29,5±12,4 – после операции (табл. 5).
По данным цистометрического исследования,не выявлено достоверной связи между объемом используемого лоскута и развитием дисфункционального мочеиспускания; детрузорная гиперактивность выявлена до операции в 7,1% случаев (n=3); после – в 9,5% случаев (n=4). Клинически значимого изменения максимальной цистометрической емкости после проведения подобного пособия не зафиксировано.
ОБСУЖДЕНИЕ
При анализе результатов лечения 42 пациентов с ятрогенными повреждениями дистальных отделов мочеточника выявлено, что реконструктивные операции с использованием методик по Боари и psoas-hitch являются высокоэффективными. У части пациентов (n=3;
-
7,1 %), имеющих в анамнезе инфравезикальную обструкцию (n=1; 2,4%), операции на мочевом пузыре или повторные пластики с использованием лоскутных методик (n=1; 2,4%), дистанционную лучевую терапию в области органов малого таза (n=1; 2,4%), зафиксированы атаки пиелонефрита. Данных пациентов следует относить к группе высокого риска развития рецидивирующей мочевой инфекции. По данным цистометрии, вне зависимости от длины лоскута мочевого пузыря, не выявлено достоверной связи между реконструкцией дистальных отделов мочеточника и развитием дисфункционального мочеиспускания; несмотря на увеличение детрузорного давления выше порогового значения, клинической гиперактивности не было выявлено ни у одного из исследуемых, частота рефлюкс-пиелонефритов достоверно не увеличивается; клинически значимого изменения максимальной цистометрической емкости не зафиксировано.
ВЫВОДЫ
-
1. Реконструктивные операции при ятрогенных повреждениях нижней трети мочеточника с использованием методик по Боари и psoas-hitch являются высокоэффективными (n=39, 92,9%).
-
2. После реконструктивных операций с использованием техники Боари и psoas-hitch у ряда пациентов отмечен пассивный рефлюкс, не проявляющий себя клинически.
-
3. Пациенты, имеющие в анамнезе инфравезикаль-ную обструкцию, операции на мочевом пузыре или повторные пластики с использованием лоскутных методик, дистанционную лучевую терапию на область органов малого таза, имеют высокие риски рецидивирующей мочевой инфекции за счет активного и пассивного рефлюксов.
Таблица 5. Результаты оценки функционального состояния мочевого пузыря
Table 5. The results of the assessment of the functional state of the bladder
Параметр Parameter
I группа Group I
II группа Group II
Критерии сравнения Comparison criteria
До операции Before the operation
После операции After the operation
До операции Before the operation
После операции After the operation
Детрузорное давление, см.вод.ст.
Detrusor pressure, сentimetre of water
13,6±3,1
24,6±4,7
12,3±2,1
19,2±3,7
Цистометрическая емкость, мл Cystometric capacity, ml
397±34,2
405±37,9
374±24,4
394±28,7
Максимальная скорость мочеиспускания, мл/сек Max. urination rate, ml/sec
8,6±4,3
16,7±3,1
12,7±2,7
17,1±3,4
Объем остаточной мочи, мл Volume of residual urine, ml
155±27,9
47,8±18,4
87±14,7
29,5±12,4
-
4. По данным цистометрии, не выявлено достоверной связи между длиной используемого лоскута мочевого пузыря и развитием дисфункционального мочеиспускания; несмотря на увеличение детрузорного давления выше порогового значения, клинической гипер-
- активности не было выявлено ни у одного из исследуемых, частота рефлюкс-пиелонефритов достоверно не увеличивается; клинически значимого изменения максимальной цистометрической емкости не зафиксировано.
ПШАТШ/ШИИШ
ЛИТЕРАТУРА/REFERENCES нижних мочевых путей после восстановительных операций на тазовых отделах мочеточников. Экспериментальная и клиническая урология 2014;(1):36-9. [Komyakov B.K., Ochelenko V.A., Al-Attar T.H. Functional state of the lower urinary tract after pelvic reconstructive surgery. Eksperimentalnaia i klinicheskaia urologiia = Experimental and Clinical Urology 2014;(1):36-9. (In Russian)].
Сведения об авторах:
Панферов А.С. – к.м.н., руководитель центра урологии медицинского центра «Медассист»; доцент кафедры медицинской биоинженерии Юго-Западного государственного университета; Курск, Россия;
Курск, Россия; РИНЦ Author ID 1066007,
Курск, Россия; РИНЦ Author ID 1011874,
Вклад авторов:
Панферов А.С. – концепция и дизайн исследования, 35%
Бекреев Е.А. – сбор и обработка материала, 25%
Ястребов В.С. – статистическая обработка и написание текста, 20%
Медведева Е.В. – сбор материала и написание текста, 15%
Елагин В.В. – написание текста, 5%
Конфликт интересов: Авторы заявляют об отсутствии конфликта интересов.
Финансирование: Исследование проведено без финансовой поддержки.
Список литературы Оценка результатов малоинвазивного лечения ятрогенных стриктур и функции детрузора после реконструкций дистальных отделов мочеточника
- Поляков Н.В., Кешишев Н.Г., Медведев П.Е., Гурбанов Ш.Ш., Серебряный С.А., Меринов Д.С. Малоинвазивные методы лечения повреждений мочеточников. Экспериментальная и клиническая урология 2020;(3):132-40. [Polyakov N.V., Keshishev N.G., Medvedev P.E., Gurbanov Sh.Sh., Serebryany S.A., Merinov D.S. Minimally invasive methods of treatment of ureteral injuries. Eksperimentalnaia i klinicheskaia urologiia = Experimental and Clinical Urology 2020;(3):132-40. (In Russian)]. https://doi.org/10.29188/2222-8543-2020-12-3-132-140.
- Аляев Ю.Г., Глыбочко П.В., Рапопорт Л.М., Газимиев М.А., Акопян Г.Н. Рентген-эндоскопическая хирургия первичных и вторичных стриктур верхних мочевых путей. Вопросы урологии и андрологии 2017;5(4):5-12. [Alyaev Yu.G., Glybochko P.V., Rapoport L.M., Gazimiev M.A., Hakobyan G.N. X-ray endoscopic surgery of primary and secondary strictures of the upper urinary tract. Voprosy urologii i andrologii = Urology and Andrology 2017;5(4):5-12. (In Russian)]. https://doi.org/10.20953/2307-6631-2017-4-5-12.
- Дерменжи Т.В., Свинцицкий В.С., Неспрядько С.В., Стаховский Э.А., Яцина А.И., Кабанов А.В. Уродинамическое исследование у больных инвазивным раком шейки матки. Клиническая онкология 2015;20(4):19-22. [Dermenzhi T.V., Svintsitsky V.S., Nespryadko S.V., Stakhovsky E.A., Yatsyna A.I., Kabanov A.V. Urodynamic examination in patients with invasive cervical cancer. Klinicheskaia onkologiia = Clinical Oncology 2015;20(4):19-22. (In Russian)].
- Воробьев В.А., Белобородов В.А., Вяткина Е.А. Результаты хирургического лечения стриктур мочеточников методом Боари. Сибирское медицинское обозрение 2019;(6):107-11. [Vorobyov V.A., Beloborodov V.A., Vyatkina E.A. The results of surgical treatment of ureteral strictures by the Boari method. Sibirskoe meditsinskoe obozrenie = Siberian Medical Review 2019;(6):107-11. (In Russian)]. https://doi.org/10.20333/2500136-2019-6-107-111.
- Яровой С.Ю., Максимов В.А., Медведев Е.В., Ачба З.О., Шоуа А.Б., Маркарян С.В. Отдаленные результаты использования стентов из никелида титана при стриктурах мочеточников различной локализации – собственный опыт. Вестник урологии 2016;(1):12-23. [Yarovoy S.Yu., Maksimov V.A., Medvedev E.V., Achba Z.O., Shoua A.B., Markaryan S.V. Long‒term results of using titanium nickelide stents for ureteral strictures of various localization – own experience. Vestnik urologii = Urology Herald 2016;(1):12-23. (In Russian)].
- Котов С.В., Неменов А.А., Перов Р.А., Соколов Н.М. Систематизированный подход в оценке уретероскопических осложнений. Экспериментальная и клиническая урология 2022;15(2)32-7. [Kotov S.V., Semenov A.A., Perov R.A., Sokolov N.M. A systematic approach to the assessment of urethroscopic complications. Eksperimentalnaia i klinicheskaia urologiia = Experimental and Clinical Urology 2022;15(2)32-7. (In Russian)]. https://doi.org/10.29188/2222-8543-2022-15-2-32-37.
- Комяков Б.К., Очеленко В.А. Кишечная пластика мочеточников Урология 2014;(2):84-89. [Komyakov B.K., Ochelenko V.A. Intestinal plastic surgery of ureters. Urologуa = Urologiia 2014;(2):84-9. (In Russian)].
- Поляков Н.В., Кешишев Н.Г., Качмазов А.А., Григорьева М.В., Гурбанов Ш.Ш., Ковченко Г.А. и соавт. Оперативное лечение стриктур нижней трети мочеточника после лучевой терапии органов малого таза. Онкоурология 2016;12(3):68-73. [Polyakov N.V., Keshishev N.G., Kachmazov A.A., Grigorieva M.V., Gurbanov Sh.Sh., Kravchenko G.A., et al. Surgical treatment of stricture of the lower third of the ureter after radiation therapy of the pelvic organs. Onkourologiia = Сancer Urology 2016;12(3):68-73. (In Russian)]. https://doi.org/10.17650/1726-9776-2016-12-3-68-73.
- Гаина О.В., Апросимов А.Л., Лапин И.В., Котов С.В., Гуспанов Р.И., Юсуфов А.Г. Анализ отдаленных результатов реконструктивно-пластических операций при вторичных стриктурах. Кардиоваскулярная терапия и профилактика 2021;20(1S):45-59. [Ganina O. V., Abrosimov A. L., Lapin I. V., Kotov S. V., Gubanov R. I., Yusufov A. G. Analysis of long-term results of reconstructive plastic surgery for secondary strictures. Kardiovaskuliarnaia terapiia i profilaktika = Cardiovascular therapy and Prevention 2021;20(1S):1-118. (In Russia)]. https://doi.org/10.15829/1728-8800-2021-1S.
- Забродина Н.Б., Галлямов Э.А., Коваленко А.В., Сысоев А.М., Бехтева М.Е. Лапароскопическая пластика мочеточников у онкологических пациентов. Онкоурология 2020;16(2):118-25. [Zabrodina N.B., Gallyamov E.A., Kovalenko A.V., Sysoev A.M., Bekhteva M.E. Laparoscopic ureteral plastic surgery in cancer patients. Onkourologiia = Сancer Urology 2020;16(2):118-25. (In Russian)]. https://doi.org/10.17650/1726-9776-2020-16-2-118-125.
- Bausch K, Sauter R, Subotic S, Halbeisen FS, Seifert HH, Feicke A. Long-term outcome of non-antireflux robotic-assisted robot-assisted laparoscopic ureter reimplantation in ureteral obstruction. J Endourol 2022;36(9):1183-91. https://doi.org/10.1089/end.2022.0055.
- Рева И.А., Колонтарев К.Б., Раснер П.И., Гвоздев М.Ю., Пушкарь Д.Ю. Роботассистированная коррекция ятрогенной травмы тазового отдела мочеточника. Фарматека 2016;(S1):54-8. [Reva I.A., Kolontarev K.B., Rasner P.I., Gvozdev M.Yu., Pushkar D.Yu. Robot-assisted correction of iatrogenic injury of the pelvic ureter. Farmateka = Pharmateca 2016;(S1):54-8. (In Russian)].
- Мосоян М.С., Шанава Г.Ш., Никулин Р.Е. Робот-ассистированная хирургия при лечении послеоперационных стриктур нижней трети мочеточника. Креативная хирургия и онкология 2023;13(1):21-6. [Mosoyan M.S., Shanava G.Sh., Nikulin R.E. Robot-assisted surgery in the treatment of postoperative strictures of the lower third of the ureter. Kreativnaia khirurgiia i onkologiia = Creative Surgery and Oncology 2023;13(1):21-6. (In Russian)]. https://doi.org/10.24060/2076-3093-2023-3.
- Zhang G, Zhao J, Zhao G, Niu Z, Liu P, Sun L. Laparoscopic ureteral reimplantation with a Boari flap for long-segment ureteric avulsion or ureteric strictures: our experience. Int Urol Nephrol 2022;54(8):1865-70. https://doi.org/10.1007/s11255-022-03224-2.
- Singh M, Garg G, Sankhwar SN, Kumar M. Laparoscopic ureteroneocystostomy for mid and lower ureteric strictures: Experience from a tertiary center. Urol Ann 2018;10(3):243-8. https://doi.org/10.4103/UA.UA_137_17.
- Забродина Н.Б., Галлямов Э.А., Коваленко А.В., Сысоев А.М., Бехтева М.Е., Иванцов К.А. Методы видеоэндоскопической коррекции стриктур мочеточника. Урология 2020;(2):41-5. [Zabrodina N.B., Gallyamov E.A., Kovalenko A.V., Sysoev A.M., Bekhteva M.E., Ivantsov K.A. Methods of video endoscopic correction of ureteral strictures. Urologya = Urologiia 2020;(2):41-5. (In Russian)]. https://doi.org/10.18565/urology.2020.2.41-45.
- Носов А.К., Румянцева Д.И., Мамижев Э.М., Лушина П.А., Щекутеев Н.А., Беркут М.В. Левосторонняя аппендикоуретеропластика у пациентов онкологического профиля. Онкоурология 2022;18(1):127–35. [Nosov A.K., Rumyantseva D.I., Mamizhev E.M., Lushina P.A., Shchekuteeva N.A., Berkut M.V. Left-sided appendicoureteroplasty in oncological patients. Onkourologiia = Сancer Urology 2022;18(1):127-35. (In Russian)]. https://doi.org/10.17650/1726-9776-2022-18-1-127-135.
- Комяков Б.К., Очеленко В.А., Ал-Аттар Т.Х. Функциональное состояниенижних мочевых путей после восстановительных операций на тазовых отделах мочеточников. Экспериментальная и клиническая урология 2014;(1):36-9. [Komyakov B.K., Ochelenko V.A., Al-Attar T.H. Functional state of the lower urinary tract after pelvic reconstructive surgery. Eksperimentalnaia i klinicheskaia urologiia = Experimental and Clinical Urology 2014;(1):36-9. (In Russian)].
- Демченко В.Н., Щукин Д.В., Хареба Г.Г., Гарагатый А.И., Мальцев А.В., Страховецкий В.С. Сравнение результатов реконструкции мочеточника за счет тубуляризованных лоскутов мочевого пузыря различной длины. Sciences of Europe 2020;50(50-2):35-41. [Demchenko V.N., Shchukin D.V., Khareba G.G., Garagaty A.I., Maltsev A.V., Strahovetsky V.S. Comparison of the results of ureteral reconstruction due to tubularized bladder flaps of various lengths. Sciences of Europe 2020;50(50-2):35-41. [(In Russian)].
- Демченко В.Н., Гарагатый А.И., Щукин Д.В., Мальцев А.В., Страховецкий В.С. Функциональные изменения мочевого пузыря после операции Боари. The Scientific Heritage 2020;46(46-3):11-6. [Demchenko V.N., Garagaty A.I., Shchukin D.V., Maltsev A.V., Strahovetsky V.S. Functional changes of the bladder after Boari surgery. The Scientific Heritage 2020;46(46-3):11-6. (In Russian)].
- Демченко В.Н., Щукин Д.В., Стецишин Р.В., Хареба Г.Г., Гарагатий А.И. «Экстремальная» реконструкция мочеточника с помощью тубуляризованного лоскута мочевого пузыря. Znanstvena Misel 2020;41(41-1):16-23. [Demchenko V.N., Shchukin D.V., Stetsishin R.V., Khareba G.G., Garagatiy A.I. «Extreme» reconstruction of the ureter using a tubularized bladder flap. Znanstvena Misel 2020;41(41-1):16-23. (In Russian)].


