Оценка риска модификации течения респираторных заболеваний, обусловленного воздействием факторов среды обитания и образа жизни населения с учетом региональных особенностей территории
Автор: Н.В. Зайцева, С.В. Клейн, Д.А. Кирьянов, М.В. Глухих, М.Ю. Цинкер, П.Д. Свинцова
Журнал: Анализ риска здоровью @journal-fcrisk
Рубрика: Профилактическая медицина: актуальные аспекты анализа риска здоровью
Статья в выпуске: 1 (52), 2026 года.
Бесплатный доступ
Осуществлена оценка риска модификации течения респираторных заболеваний вирусной природы (грипп, ОРВИ, COVID-19), обусловленного воздействием факторов среды обитания и образа жизни населения с учетом региональных особенностей территории Российской Федерации. В работе использованы данные федерального статистического наблюдения за 2010–2019 гг. по 82 субъектам РФ. Анализировалась инцидентность ОРВИ и гриппа. Комплекс социально-гигиенических детерминант (СГД) был представлен 112 показателями, сгруппированными в семь доменов. Для оценки вклада неуправляемых погодно-климатических факторов (мощность УФ-излучения, влажность, температура, скорость ветра, отклонение от среднемноголетней температуры) использована множественная линейная регрессия. Для оценки влияния остальных факторов среды обитания и образа жизни применена искусственная нейронная сеть (многослойный персептрон). Риск рассчитывался как произведение вероятности заболевания (Δp), обусловленной СГД, тяжести течения (g) и коэффициента модификации длительности болезни (w). Установлено, что ≈ 60 % фактически регистрируемой годовой инцидентности ОРВИ и гриппа объясняется совместным воздействием исследуемых факторов. Погодно-климатические факторы оказали более стабильное и значительное влияние на заболеваемость по сравнению с другими факторами среды обитания. На основе расчетных значений риска за 2012–2019 гг. предложена четырехуровневая шкала для его классификации (минимальный, допустимый, настораживающий, высокий) с описанием соответствующих управленческих мероприятий. Сценарные расчеты показали, что наиболее значимыми в снижении инцидентности ОРВИ и гриппа в порядке его снижения оказывались показатели системы здравоохранения, образа жизни, социально-демографические показатели, показатели фоновой заболеваемости, экономические показатели и санитарно-эпидемиологические показатели (0,52, 0,49, 0,45, 0,32, 0,28 и 0,21 случая на 100 тыс. населения соответственно). Установлено, что среди управляемых факторов среды наибольший вклад в снижение заболеваемости вносит увеличение числа привитых лиц (в среднем 0,8 случая на 100 тыс. населения). Разработанный методический подход, основанный на каскаде математических моделей, позволяет количественно оценить вклад управляемых и неуправляемых факторов в модификацию течения эпидемического процесса респираторных вирусных инфекций (ОРВИ и грипп). Полученные результаты и шкала риска могут быть использованы для обоснования адресных профилактических и противоэпидемических мероприятий с учетом региональной специфики.
Грипп, ОРВИ, COVID-19, факторы среды обитания, оценка риска, региональные особенности
Короткий адрес: https://sciup.org/142247478
IDR: 142247478 | УДК: 613; 614 | DOI: 10.21668/health.risk/2026.1.01
Assessing risks of modified clinical course of respiratory diseases caused by environmental exposures and lifestyle factors considering regional specificity
The aim of this study was to estimate the risk of modified clinical course of viral respiratory diseases (influenza, ARVI, COVID-19) due to environmental exposures and effects of lifestyle factors considering regional peculiarities in the Russian Federation. The study relied on using data from federal statistical reports issued in 2010–2019 for 82 Russian regions. ARVI and influenza incidence was analyzed. A set of social and hygienic determinants (SHD) was represented by 112 indicators grouped in 7 domains. Multiple linear regression was used to estimate contributions made by unmanageable weather and climatic factors (UV-radiation intensity, humidity, air temperature, wind speed, deviation from average long-term temperature levels). An artificial neural network (multilayer perceptron) was used to assess effects produced by other environmental and lifestyle factors. Risk was calculated as a product of disease likelihood (Δp), determined by SHD, disease severity (g) and coefficient of modified disease duration (w). Approximately 60 % of actually registered annual ARVI and influenza incidence was found to be caused by combined effects of the analyzed factors. Weather and climatic factors had more stable and considerable effect on this incidence relative to other environmental exposures. A four-level scale for risk classification was created based on its calculated values over 2012–2019 (minimal, permissible, alerting, and high) together with outlining relevant risk management activities. Scenario calculations allowed revealing the most significant factors for decreasing ARVI and influenza incidence. If ranked in the descending order, they were quality of the public healthcare system, lifestyle, sociodemographic indicators, background incidence rates, economic indicators, and sanitary-epidemiological indicators (0.52, 0.49, 0.45, 0.32, 0.28 and 0.21 cases per 100 thousand people respectively). An increase in the number of vaccinated people was found to make the greatest contribution to incidence decline among all manageable factors (on average, 0.8 cases per 100 thousand people). The developed methodical approach based on a cascade of mathematical models, makes it possible to quantify contributions made by manageable and unmanageable factors to modified course of respiratory epidemics (ARVI and influenza). The study results and the risk scale can be used for substantiating targeted preventive and anti-epidemic activities, regional specificity taken in account.
Текст научной статьи Оценка риска модификации течения респираторных заболеваний, обусловленного воздействием факторов среды обитания и образа жизни населения с учетом региональных особенностей территории
Кирьянов Дмитрий Александрович – кандидат технических наук, заведующий отделом математического моделирования систем и процессов (e-mail: ; тел.: 8 (342) 237-18-04; ORCID: .
Глухих Максим Владиславович – кандидат медицинских наук, старший научный сотрудник – заведующий лабораторией методов комплексного санитарно-гигиенического анализа и экспертиз, отдел системных методов санитарногигиенического анализа и мониторинга (e-mail: ; тел.: 8 (342) 237-18-04; ORCID: .
Цинкер Михаил Юрьевич – кандидат физико-математических наук, старший научный сотрудник лаборатории ситуационного моделирования и экспертно-аналитических методов управления (e-mail: ; тел.: 8 (342) 237-18-04; ORCID: .
Свинцова Полина Денисовна – математик лаборатории ситуационного моделирования и экспертно-аналитических методов управления (e-mail: ; тел.: 8 (342) 237-18-04; ORCID: .
Вирусные респираторные заболевания, включая грипп, острые респираторные вирусные инфекции (ОРВИ) и COVID-19, представляют собой серьезную проблему общественного здравоохранения во всем мире в целом и в Российской Федерации в частности. Данные заболевания формируют высокие уровни заболеваемости, экономического бремени и осложнений, влияющих на общее состояние здоровья населения.
Грипп (J09–J111) определяется как острая респираторная вирусная инфекция, вызываемая вирусами гриппа (чаще Influenza A , B ). По актуальным оценкам, во всем мире ежегодные сезонные эпидемии гриппа приводят к примерно 1 млрд клинических случаев в год, 3–5 млн случаев тяжелых заболеваний и к 290–650 случаем смерти2 [1]. Отсутствуют точные и верифицированные оценки урона здоровью населения в странах с низким (средним) уровнем дохода (LMICS3); по некоторым сведениям до 99,0 % смертей детей в возрасте до 5 лет связаны с грипп-ассоциированными инфекциями нижних дыхательных путей в данных странах [2].
В настоящее время грипп является единственным представителем ОРВИ (не считая COVID-19), для которого предусмотрена программа4 специфической профилактики в Российской Федерации. В связи с этим, помимо оценки популяционного иммунитета населения, важным направлением в системе эпидемиологического надзора являются профилактические мероприятия, направленные на оценку и улучшение качества среды обитания, на фоне возвращения допандемийного режима циркуляции штаммов гриппа, вирусов ОРВИ [3].
Внезапное и стремительное развитие пандемии COVID-19 сопровождалось значительным ухудшением эпидемиологической ситуации в Российской Федерации в начале 2020-х гг. в виде повышенных уровней заболеваемости и смертности, в том числе госпитальной [4].
В области исследования атрибутивных факторов риска болезней органов дыхания, в том числе вирусной природы, отмечается значительное неравенство в рамках социально-экономического (бед- ность, доступ к базовым санитарно-гигиеническим условиям, первичной медико-санитарной помощи) и санитарно-гигиенического (загрязнение воздуха) измерений статуса населения, особенно в пространственном отношении [5–7].
Согласно теории фундаментальных причин (ТФП), связи между социально-экономическим статусом (СЭС) и смертностью населения сохраняются, несмотря на существенные изменения в профилактике и лечении заболеваний, модифицировании факторов риска [8]. В связи с этим при решении вопросов прогнозирования, оценки и мониторинга состояния здоровья населения важно учитывать социальногигиенический фон, модулирующий его. Учитывая теорию ТФП, концепция «равнозначной восприимчивости перед инфекционным агентом» (Equal Opportunity Infectors) [9] выглядит несостоятельной на современном этапе развития эпидемиологии. Наиболее полной объясняющей способностью обладает принцип учета социально-гигиенических детерминант (СГД), включая погодно-климатические и показатели здоровья, в возникновении и развитии эпидемического процесса [10], так как различия в социально-экономических, географических, генетических факторах могут в значительной степени обусловливать исходы и последствия для здоровья населения, стратифицированного по различным признакам. Необходимость нивелирования социально-экономического неравенства как дифференцирующего фактора объемов обременения заболеваниями среди разных групп населения выдвигают специалисты здравоохранения, социальные работники, политики [11]. Важность учета социально-гигиенических детерминант подтверждается и в отношении инфекционных заболеваний. На примере COVID-19 установлено, что более высокий индекс социальной уязвимости (Social Vulnerability Index, SVI) ассоциирован с повышенным риском инфицирования SARS-CoV-2 (скорректированный коэффициент заболеваемости [aIRR]: 1,18; 95 % ДИ: 1,02–1,36) [12]. В работе A.K. Weaver et al. (2022) подчеркивается важность и перспективность рассмотрения факторов среды обитания (загрязнение воздуха, химическая экспозиция, климат, городская среда) как переменных, обусловливающих наблюдаемые уровни заболеваемости респираторными заболеваниями и их тяжесть [13].
Загрязнение атмосферного воздуха, отсутствие (ограничение) доступа к качественной и безопасной питьевой воде, неэффективное управление сточными водами, неудовлетворительные жилищные условия, высокая плотность населения и низкий уровень СЭС связаны с более высокими показателями смертности и госпитализации по причине COVID-19 во всем мире [14].
По данным L. Hoffmann et al. (2025), внешнесредовые стрессоры в виде загрязнителей атмосферного воздуха (NO2, PM2.5, O3) и метеорологических показателей (температура, осадки) в сочетании с демографическими факторами (пол, возрастная группа) способны модулировать уровни заболеваемости респираторных заболеваний (на примере COVID-19) [15]. Данные результаты подтверждаются в исследовании R.J. Scalsky et al. (2022) на примере данных UK Biobank с использованием индекса множественной депривации (Index of Multiple Deprivation – IMD) [16].
По результатам L. Mohammadi et al. (2022), установлен вклад факторов среды обитания (температура, влажность, географическое положение, система здравоохранения, гигиена и коморбидность с хроническими инфекционными заболеваниями (ХНИЗ)) в выживание, устойчивость и передачу вирусных частиц (SARS-CoV-2) [17]. Исследование Y.-W. Choi et al. (2021) дополняют работы по направлению влияния внешнесредовых факторов на течение эпидемического процесса и показывают значимость таких переменных, как ультрафиолетовое излучение и влажность воздуха, вместе с тем вносят неопределенность в отношении температуры и абсолютной влажности [18]. Факторы среды обитания выступают в качестве триггеров [19] усиления интенсивности эпидемического процесса, модуляторов [20] эпидемиологических волн и требуют реализации тщательного биомониторинга для оценки комплексного экспосома в широком спектре режимов окружающей среды [21]. В работе E.C. Lee et al. (2018) еще до развития пандемии предлагалось развертывать конвергентную систему традиционных источников (данные медицинских учреждений) и цифровых медицинских данных для оптимизации системы эпидемиологического надзора за гриппом на местном и национальном масштабе с учетом социально-гигиенических детерминант [22].
Для традиционных систем эпидемиологического надзора, в частности за гриппом, все чаще рассматривают варианты их дополнения неформальными мелкомасштабными источниками, харак- теризующими эпидемический процесс на индивидуальном уровне, что предоставляет больший объем и динамичность получения данных, несмотря на имеющиеся риски возникновения систематических ошибок (проблема модифицируемых единиц площади – Modifiable Areal Unit Problem (MAUP), пространственная автокорреляция, экологическая ошибка) [23].
Схожие элементы (звенья, признаки, свойства) эпидемических процессов гриппа, ОРВИ и COVID-19 (источник, механизм и пути передачи, тропность к тканям респираторного тракта и др.), а также базовых симптоматических проявлений (основных клинических признаков) зачастую в сочетании с малыми объемами лабораторных исследований (полимеразная цепная реакция, экспресс-тесты на наличие антигенов вируса) не позволяют точно оценивать объемы обременения населения тем или иным вирусным респираторным заболеванием [24]. Несмотря на отсутствие универсального вакцинного препарата и скромные возможности повсеместной рутинной лабораторной диагностики (дифференциации) ОРВИ, схожесть рассматриваемых эпидемических процессов позволяет устанавливать общие, неспецифические мероприятия (нефармацевтические вмешательства, в том числе через улучшение санитарно-эпидемиологической обстановки (ситуации)), в первую очередь направленные на повышение общей резистентности организма путем «антигенной разгрузки» и на профилактику и (или) абортирова-ние процессов передачи [25] вирусных агентов.
Новаторские решения на стыке нескольких наук (эпидемиологии, математики, статистики, информатики, геоинформационных систем и др.) в направлении исследования механизмов, путей и факторов передачи инфекционного начала, подстегнутые развитием информационных технологий [26], расширяют представления об учете множественного пространственного, в том числе на микроуровне, взаимодействия переменных в той или иной степени детерминирующих эпидемические процессы по различным метрикам (заболеваемость, смертность, летальность, индекс репродукции и др.).
Таким образом, результаты исследований в области установления механизмов распространения и факторов передачи респираторных вирусных заболеваний с выделением роли социально-гигиенических детерминант должны использоваться как для оперативно-тактических (эпидемиологический надзор в части оценки и мониторинга нанесенного (потенциального) ущерба, ассоциированного с данными заболеваниями), так и для стратегических це-лей5. Особую важность решение данных вопросов принимает при учете территориального контекста
(пространственной компоненты) как относительно устойчивой системы сложившегося сочетания факторов среды обитания и образа жизни.
Цель исследования – оценка риска модификации течения респираторных заболеваний, обусловленного воздействием факторов среды обитания и образа жизни населения с учетом региональных особенностей территории.
Задачи:
– выполнить оценку влияния неуправляемого погодно-климатического фактора на модификацию течения респираторных заболеваний;
– выполнить оценку влияния факторов среды обитания и образа жизни на модификацию течения респираторных заболеваний;
– выполнить классификацию (шкалирование) полученных уровней риска.
Материалы и методы. В качестве источников данных об инцидентности (первичная заболеваемость) гриппа, ОРВИ и COVID-19, содержащих информацию о числе зарегистрированных случаев заболеваний (по окончательному диагнозу), возрастном составе заболевших, а также о территориальном распределении по субъектам Российской Федерации, служили: форма федерального статистического наблюдения № 1 и № 2 «Сведения об инфекционных и паразитарных заболеваниях» (месячные и годовые данные).
Источниками данных по показателям, характеризующим комплекс СГД, являются формы федерального статистического наблюдения, статистические сборники, статистические бюллетени, показатели и данные Федерального информационного фонда социально-гигиенического мониторинга, иные открытые официальные источники. Общее количество показателей, включенных в анализ и характеризующих комплекс СГД, составило 112 единиц. Показатели условно агрегированы по семи доменам / группам: показатели санитарно-эпидемиологического благополучия населения (24 единицы), образа жизни населения (19 единиц), социально-демографической (25 единиц), экономической сфер (7 единиц), показатели системы здравоохранения (9 единиц), заболеваемости населения (21 единица), погодно-климатические показатели (5 единиц). Итоговый набор данных охватывал период 2010–2019 гг. по 82 субъектам, общее количество первичных данных для анализа составило 145 796 единиц наблюдения.
Риск модификации течения респираторных инфекций вирусной природы представляет собой количественную величину от произведения вероятности ( ∆p ), тяжести заболевания ( g ) и коэффициента модификации ( w ), обусловленных региональными особенностями проживания населения на территории (формула (1)):
R = ΔpСГД+климат·g·w, (1) где ΔpСГД+климат – вероятность респираторных заболеваний вирусной природы, обусловленная ком- плексом СГД, включая погодно-климатические условия;
g – тяжесть течения респираторных заболеваний вирусной природы;
w – коэффициент модификации течения респираторных заболеваний вирусной природы, обусловленный комплексом СГД.
Вероятность наступления нежелательного события ( Δ p ) рассчитывается на основе частотного показателя (инцидентности). Вероятность респираторных заболеваний вирусной природы, обусловленная конкретным воздействием комплекса СГД, включая погодно-климатические условия, определятся как разность ее фактических (наблюдаемых) и фоновых (базовых) уровней в конкретном году по формуле (2):
Δ p СГД+климат = p факт - p фон , (2)
где Δ p СГД+климат – вероятность возникновения респираторных заболеваний вирусной природы, обусловленная комплексом СГД, включая погодно-климатические условия;
p факт – фактический (наблюдаемый) уровень вероятности респираторных заболеваний вирусной природы;
p фон – фоновый (базовый) уровень вероятности респираторных заболеваний вирусной природы.
Фактический (наблюдаемый) уровень вероятности определяется на основе данных о заболеваемости (инцидентности), зарегистрированной в официальных статистических формах учета инфекционной заболеваемости по соответствующей нозологии. Фоновый (базовый) уровень инцидентности представляет собой часть официально зарегистрированной заболеваемости, формируемой вследствие естественного взаимодействия популяций микро- (возбудитель – вирусный агент) и макроорганизмов (восприимчивое население), обусловленного их гено- и фенотипической гетерогенностью, фазовой самоперестройкой, взаимоизменчивостью биологических свойств популяций. Данный уровень является естественным неэлиминируемым ординарным уровнем заболеваемости и принимается как 5-й персентиль распределения показателей инцидентности респираторных заболеваний вирусной природы среди 82 субъектов России.
Степень воздействия комплекса СГД на инцидентность респираторных заболеваний вирусной природы определяется на основе результатов математического моделирования искомых зависимостей и формализуется в виде двух моделей. Первая модель вычисляет значение инцидентности респираторных заболеваний вирусной природы в ответ на изменение погодно-климатических факторов для каждого месяца в году (∆pклимат). Зависимой переменой в модели первого уровня является разность фактического и фонового уровня месячной заболеваемости. В качестве независимых переменных исполь- зовались величины отклонений погодно-климатических показателей6 по месяцам (мощность ультрафиолетового излучения спектра B (Вт/м2); относительная влажность воздуха (%); средняя температура воздуха (°С); скорость ветра (м/с); отклонение от среднемноголетней температуры (%) от значений физиологических оптимумов7), которые рассчитывались по формуле (3):
N min N min
X i < X i , X i X i
ˆ
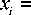
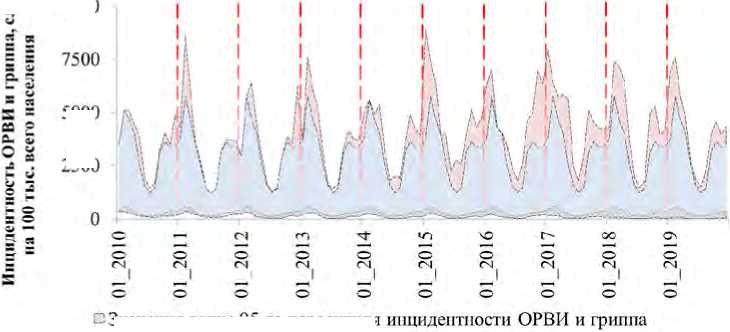
N x min
< X i < X
N max
,0 ,
N \ N \
X > X i max , I X - X i max
В качестве входных данных (независимые переменные) использовались значения 105 показателей всех доменов (погодно-климатические показатели не использовались (результат первой модели)), зависимой переменной являлись значения инцидентности за исключением фона (5-го персентиля) и модельных значений первой модели, формула (5):
12 n
A p СГД A p СГД+климат - E ( a о + E a iXi (t ))■ (5) i = 1 i = 1
Предварительно выполнялась процедура нормализации первичного набора показателей методом min–max:
где x ˆ i – отклонение фактического значения i -го фактора от уровня оптимума;
x i – фактическое значение i -го фактора;
x i N min , x i N max – нижняя и верхняя граница опти-мумов i- го фактора.
Итоговая зависимость уровней дополнительной вероятности возникновения респираторных заболеваний вирусной природы, ассоциированных с погодно-климатическими показателями, описывается множественной линейной регрессионной моделью по формуле (4):
n
A P климат = a 0 + E a^i ( t ), (4)
i = 1
y j =
y j
y m j in
max min ,
’j - yj
где a 0 , a i – параметры множественной линейной
регрессионной модели.
Вторая модель – искусственная нейронная сеть (ИНС) прямого распространения в виде многослойного персептрона с двумя внутренними слоями из 16 и 4 нейронов соответственно (рис. 1).
где y j - нормированное значение j -й переменной; y m j in , y m j ax – минимальное и максимальное значения j -й переменной.
В качестве функции активации нейронов использовалась сигмоидная функция.
Итоговое значение инцидентности, обусловленное воздействием комплекса СГД, рассчитывается как сумма моделей 1 и 2.
Тяжесть течения ( g ) респираторных заболеваний вирусной природы характеризует совокупность особенностей их клинического течения и исходов. На основе данных руководства8, средневзвешенная тяжесть гриппа и ОРВИ составляет 0,006114.
Коэффициент модификации течения респираторных заболеваний вирусной природы ( w ), определяемый комплексом СГД, отражает изменение длительности течения заболевания и также влияет на
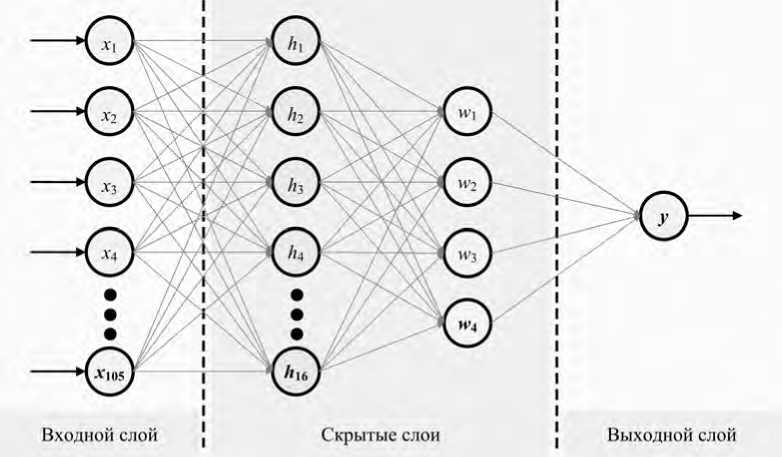
Рис. 1. Схема архитектуры используемой ИНС
итоговое значение риска. Данный коэффициент вычисляется как отношение длительности течения случая заболевания, обусловленной комплексом СГД ( d ), к его базовой длительности ( d ) согласно формуле (7):
^*
w = 1 d I, (7) Id )
где d – базовая длительность течения случая заболевания, d – длительность течения, обусловленная комплексом СГД.
Базовые параметры длительности устанавливаются, исходя из типичной длительности течения рассматриваемых заболеваний, описываемой в официальных клинических рекомендациях9 Министерства здравоохранения Российской Федерации. В настоящем исследовании «базовая» длительность течения ОРВИ / гриппа принимается равной 7,5 дня. Длительность течения, обусловленная комплексом СГД, определяется на основе модели (аналогичной модели 2) связей между ретроспективными значениями10 средней длительности течения случая заболевания по классу болезней органов дыхания и значениями показателей, характеризующих комплекс СГД.
Сбор, обработка, анализ и визуализация данных выполнялись с использованием стандартных программных пакетов для статистического анализа в MS Excel 2010 и RStudio (версия 4.2.0., библиотека neuralnet).
Результаты и их обсуждение. Анализ динамики показателей суммарной инцидентности ОРВИ и гриппом среди 82 субъектов России за 2010– 2019 гг. показывают выраженную внутригодовую сезонность с акцентом на осенне-зимний период, присущую рассматриваемым респираторным заболеваниям вирусной природы (рис. 2). Обращают на себя внимание значимые «всплески» первичной заболеваемости в 2011, 2015, 2017 гг., ассоциированные с подтипами вирусных штаммов A (H1N1) и A (H3N2). В 2016–2017 гг. отмечаются и более «широкие плечи» (пики) заболеваемости, показывая большее распространение штамма в данный эпидемический сезон среди субъектов России. Уровни суммарной инцидентности ОРВИ и гриппа за вычетом 5-го персентиля (базовый, неэлиминируемый уровень) принимались в качестве модифицируемых комплексом СГД. Отдельные оценки данных показателей в разрезе COVID-19 показаны авторами ранее [27].
Результаты анализа мультиколлинеарности погодно-климатических показателей продемонстрировали ее отсутствие среди рассматриваемых независимых переменных по данным матрицы корреляции и значениям VIF (< 5) (табл. 1), т. е. можно считать, что данные достаточно ортогональны (независимы).
По результатам моделирования (табл. 2) связей между уровнями суммарной инцидентности ОРВИ и гриппа, обусловливаемыми комплексом СГД, и набором погодно-климатических показателей получена значимая ( F -критерий < 0,05) модель с умеренным значением коэффициента детерминации ( R 2 = 0,35) с тремя статистически достоверными переменными ( х 1 , х 2 , х 4 ).
Значения выше 95-го персентиля о Значения ниже 5-го персентиля инцидентности ОРВИ и гриппа
Рис. 2. Динамика изменения минимальных и максимальных значений суммарной инцидентности ОРВИ и гриппа среди субъектов России за период 2010–2019 гг.
Таблица 1
Результаты оценки мультиколлинеарности между погодно-климатическими показателями
|
Параметр |
x 1 |
x2 |
x3 |
x4 |
x5 |
|
x1 |
1,00 |
0,578 |
0,202 |
0,196 |
-0,039 |
|
x2 |
0,578 |
1,00 |
0,373 |
0,086 |
-0,014 |
|
x3 |
0,202 |
0,373 |
1,00 |
0,009 |
0,059 |
|
x4 |
0,196 |
0,086 |
0,009 |
1,00 |
-0,061 |
|
x 5 |
-0,039 |
-0,014 |
0,059 |
-0,061 |
1,00 |
|
VIF |
1,55 |
1,68 |
1,17 |
1,05 |
1,01 |
Примечание: x 1 – мощность ультрафиолетового излучения спектра B, Вт/м2; x 2 – относительная влажность воздуха, %; x 3 – средняя температура воздуха, °С; x 4 – скорость ветра, м/с; x 5 – отклонение от среднемноголетней температуры, %; VIF – фактор инфляции дисперсии (англ. Variance Inflation Factor).
Таблица 2
Параметры множественной регрессионной модели связи между уровнями суммарной инцидентности ОРВИ и гриппа и погодно-климатическими показателями
Согласно значениям стандартизованных коэффициентов регрессии (β), наиболее значимыми независимыми переменными в данной модели являются степень отклонения от оптимумов относительной влажности и мощности ультрафиолетового излучения. Данные научной литературы подтверждают, что изменения параметра влажности воздуха относительно гигиенических нормативов могут приводить как к большей восприимчивости организма за счет высушивания слизистых воздухоносных путей
[28], так и к большим возможностям выживания и транспортирования вирусного инфекционного агента за счет большей насыщенности водяными парами с наличием аэрозоля [29]. Оценка ассоциаций между факторами среды обитания проводилась авторами ранее, в том числе с погодно-климатической составляющей [30, 31].
Согласно апробируемому методическому подходу реализовано две модели искусственной нейронной сети для прогнозирования степени влияния
|
b |
*b |
*b |
b3 |
*Ь4 |
bo |
|
-8 349,86 |
39 014,89 |
42,18 |
-0,97 |
-40,03 |
5,12 |
|
SE (b,) |
SE (bi) |
SE (bi) |
SE (b3) |
SE (b4) |
SE (b3) |
|
530,45 |
2 387,39 |
0,92 |
2,65 |
9,59 |
9,48 |
|
R² |
R2 (скор.) |
SE (Y) |
Стандарт. бета-коэффициенты регрессии (β 1 – β 5 ) |
J___ pl ₽2 P3 ₽4 PS |
|
|
0,3489 |
0,3488 |
856,0324 |
|||
|
F -статистика |
df |
||||
|
1 054,2548 |
9 834 |
||||
Примечание: * p -критерий < 0,001.
СПБ
SPB
МУР
MUR
МОС
MOW
КАР
НЕН
ЛЕН
LEN
КАГ
KAG
ПСК
KAR
НОВ
NGR
ТВЕ
ВОЛ
VLG
ЯРО
МАР
TVE
КАЛ
АРХ
ARK
КИР
NEN
КОМ
KOM
ПЕР
ЯМА
YAN
ХАН
ТЮМ
ТОМ
КРН
KYA
КЕМ
ИРК
ЧУК
CHU
SMO
KAL
ИВА
КОС
KOS
YAR
МОЯ
MOS

ВЛА
MAR
ЧУВ
CHV
НИЖ
NIZ
РЯЗ
RYA
МОР
MOR
KIR
PER
KHM TYU
TOM
KEM
IRK
ЯКУ
SAH
МАГ
КАМ
БРЯ
BRY
ОРЛ
ORL
КУС
KUR
ТАТ
TAT
УДМ
UDM
СВЕ
SVE
КУР
KUG
НОС
NVS
ХАК
KHK
БУР
BUR
MAG
KAM
АМУ
AMU
КРЫ
KRY
СВС
SVS
АДЫ ADY
ТУЛ
TUL
ЛИП
LIP
БЕЛ
BEL
КРА
KRA
КАО
KAO
КАБ
KAB
ТАМ
ПЕН
УЛЬ
ULY
САМ
SAM
БАШ
BAS
ЧЕЛ
CHE
ОМС
OMS
АЛТ
ALT
ТУВ
TUV
ЗАБ
ZAB
ЕВР
ХАБ
JEW
KHA
TAM ВОР
VOR РОС ROS СТА STA СЕВ NOR
PNZ
ВОГ
VOG
КАИ
KAI
ЧЕЧ
CHA
ИНГ
ING
САР
SAR
ОРЕ
ORE
АЛР
ALI
ПРИ
PRI
САХ
SAK
Данные отсутствуют –

АСТ AST ДАГ DAG
Min
10 353.3
2 102.0
Данные по модели
Max
24 430.6
случаи ОРВИ и гриппа на

Фактические данные
40 708.7
Рис. 3. Усредненные за 2010–2019 гг. модельные значения суммарной инцидентности ОРВИ и гриппа, обусловленные набором погодно-климатических показателей, случаев на 100 тыс. всего населения факторов среды обитания и образа жизни на суммарные уровни инцидентности ОРВИ и гриппа (R2 = 0,691), а также длительность течения (d ̃) случая болезни органов дыхания (R2 = 0,6) (по 1748 коэффициентов соответственно).
Сравнительный анализ результатов расчетов по первой модели с фактическими данными суммарной инцидентности ОРВИ и гриппа, усредненных за 2010–2019 гг., показал, что полученная модель в целом воспроизводит пространственное распределение интенсивности эпидемического процесса (рис. 3) и указывает на его увеличение с ростом широтности.
По результатам анализа региональной динамики изменения значений суммарной инцидентности ОРВИ и гриппа по первой модели среди субъектов России установлено, что наибольший прирост произошел в Республике Башкортостан (+13,5 % в среднем с 2010–2011 по 2018–2019 гг.), наибольшая убыль – в Кабардино-Балкарской Республике (-28,7 % в среднем с 2010–2011 по 2018–2019 гг.). Наибольший уровень среднемноголетнего значения инцидентности ОРВИ и гриппа (2010–2019 гг.) зафиксирован для Мурманской области (24 430,6 сл. на 100 тыс. всего населения), наименьший – для Карачаево-Черкесской Республики (10 353,3 сл. на 100 тыс. всего населения).
В среднем по каскаду используемых моделей объясняется ≈ 60,0 % фактически регистрируемой годовой суммарной инцидентности ОРВИ и гриппа (рис. 4).
Рассчитаны значения риска по результатам обеих моделей по субъектам России (рис. 5). Значения риска не вычислены за 2010–2011 гг. ввиду отсутст-
вия данных по продолжительности случаев нетрудоспособности по субъектам России. Спецификация модели ИНС с линейным выходом в некоторых сценариях приводила к значениям «отрицательной заболеваемости» и, соответственно, к «отрицательному риску», что, безусловно, не имеет содержательной интерпретации. Так как целевая переменная (заболеваемость) по своей природе является неотрицательной, для выходных значений модели выполнено цен-
зурирование результатов «снизу» по уровню нуля. Рассчитанные модельные значения риска по моделям показывают, что в большей степени значения заболеваемости ОРВИ и гриппа определяются погодноклиматическими факторами, которые относительно стабильны в динамике.
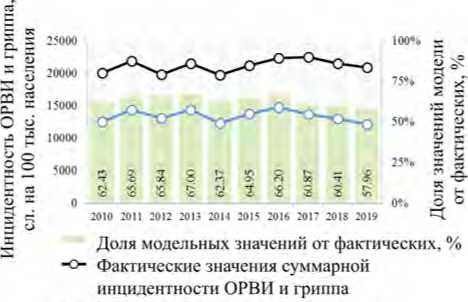
<* Модельные значения суммарной инцидентности ОРВИ и гриппа
Рис. 4. Усредненные за 2010–2019 гг. модельные значения суммарной инцидентности ОРВИ и гриппа, обусловленные набором погодно-климатических показателей, случаев на 100 тыс. всего населения
Таблица 3
Классификация уровней риска модификации течения респираторных заболеваний вирусной природы
Ограничения и перспективы исследования. В качестве ограничений исследования выделены: используемый набор панельных данных (выбранные показатели, период их агрегации); способ построения моделей (множественная линейная регрессия, структура ИНС, функция активации нейронов); выбранные значения физиологических «оптимумов»; выбранный неэлиминируемый уровень инцидентности; времен-на́я (сценарная) условность задания шкалы риска.
Выводы. Таким образом, результаты разработанного методического подхода с использованием методов математического моделирования, в том числе машинного обучения (искусственные нейронные сети), позволили выполнить комплексную оценку влияния на показатели инцидентности ОРВИ и гриппом неуправляемого погодно-климатического фактора (максимальный прирост: Республика Башкортостан (+13,5 % в среднем с 2010–2011 гг. по 2018–2019 гг.); максимальная убыль: Кабардино-Балкарская Республика (-28,7 % за аналогичный период)) и факторов среды обитания и образа жизни (максималь-
ный прирост: Алтайский край (+682,9 % в среднем с 2010–2011 гг. по 2018–2019 гг.); максимальная убыль: Астраханская область (-52,2 % за аналогичный период)) на модификацию течения респираторных заболеваний.
Выполненные расчеты по оценке риска среди 82 рассматриваемых территорий за период 2010–2019 гг. (656 сценариев «регион – год») позволили выделить установившийся многолетний режим взаимодействия популяций микро- и макроорганизмов на фоне относительно стабильных факторов среды обитания и образа жизни населения в виде шкалирования характерных уровней риска с количественной и качественной интерпретацией.
Полученный инструмент оценки риска модификации течения респираторных заболеваний, обусловленного воздействием факторов среды обитания и образа жизни населения с учетом региональных особенностей территории, показал, что 0,92 % случаев «территория – год» пришлись на зону высокого риска, 21,04 % находились в границах допустимого риска, 78,05 % – в зоне низкого риска.
Финансирование. Исследование не имело спонсорской поддержки.


