Оценка риска развития осложнений миелопролиферативных заболеваний на основе метода лазерной допплеровской флоуметрии
Автор: Богомолов А.И., Давыдкин И.Л., Савинов Е.А., Попельнюк Н.С., Наумова К.В.
Журнал: Анализ риска здоровью @journal-fcrisk
Рубрика: Оценка риска в организации здравоохранения
Статья в выпуске: 3 (31), 2020 года.
Бесплатный доступ
Перед системой здравоохранения России стоит множество задач, решение которых требует нестандартных инновационных подходов. Поставленные задачи реализуются в рамках государственной программы «Развитие здравоохранения». Одно из направлений (подпрограмма) - «Развитие и внедрение инновационных методов диагностики, профилактики и лечения, а также основ персонализированной медицины», которое предусматривает широкое использование информационных и цифровых технологий. В рамках персонифицированной медицины актуально (предусматривается) развитие методов, которые бы позволили на предварительной стадии обследования больного выявлять ранние признаки возможного заболевания на основе простой и относительно дешевой технологии диагностики и передавать их в медицинский центр для последующего уточнения диагноза. Массовый характер применения подобных технологий также требует достаточно надежных математических методов и моделей для постановки предварительного диагноза. В настоящее время ведущей причиной смертности во всем мире остаются заболевания сердечно-сосудистой системы, развившиеся ввиду воздействия различных факторов, в том числе при возникновении различных новообразований, а также в ходе проведения химиотерапии. Приводятся данные современной медицины об анамнезе и осложнениях миелопролиферативных заболеваний, обусловленных патологией сосудистой системы, занимающей первое место в мире по смертности. Установлено, что на сосудистый эндотелий, повреждение которого занимает ведущее место в сердечно-сосудистом континууме, может влиять как сама патологическая клеточная масса, так и препараты, используемые для лечения миелопролиферативных неоплазий. Для оценки риска развития осложнений миелопролиферативных заболеваний проведено обследование больных на основе метода лазерной допплеровской флоуметрии. Результаты обрабатывались с помощью модели логистической регрессии. По результатам ROC-анализа полученный диагностический критерий обладает чувствительностью (Sensitivity, 1 - b) и специфичностью (Specificity, 1 - a) 0,87 и 0,96 соответственно, что говорит о высоком качестве диагностики. Метод и модель могут быть использованы в цифровой медицине.
Цифровая медицина, диагностика, миелопролиферативные заболевания, дисфункции сосудистого эндотелия, метод лазерной допплеровской флоуметрии, математическая модель, логистическая регрессия, оценка риска
Короткий адрес: https://sciup.org/142226380
IDR: 142226380 | УДК: 616.155.191-072/.074 | DOI: 10.21668/health.risk/2020.3.19
Assessing risks of developing myeloproliferative diseases complications with laser Doppler flowmetry
Public healthcare in Russia faces many challenges; meeting them requires non-standard and innovative approaches. The set tasks are being solved within the «Public healthcare development» State program. A sub-program within it is called «Development and implementation of innovative diagnostics, prevention, and treatment procedures as well as basics of personified medicine». This sub-program involves wide use of information and digital technologies. Personified medicine envisages developing such methods that would allow early detection of a probable disease even at a preliminary stage in examining a patient; this detection is to be based on a simple and relatively cheap diagnostic technology and to provide a medical center with reliable data on detected signs of a disease for a further diagnosis. Mass use of such technologies also requires truly reliable mathematic procedures and models for putting a preliminary diagnosis. At present cardiovascular diseases are still the leading cause of death all over the world; they develop due to variable factors including influence exerted by malignant neoplasms and also due to chemotherapy. The paper contains data collected by contemporary medical experts on case histories and complications of myeloproliferative diseases caused by vascular system pathology that holds the first rank place as per mortality worldwide. It was detected that both pathological cellular mass and medications applied to treat myeloproliferative neoplasms could produce adverse effects on vascular endothelium damage to which plays the leading role in cardiovascular continuum. To assess risks of myeloproliferative diseases complications, we examined patients using Laser Doppler Flowmetry (LDF). The results were processed with a logistic regression model. As per ROC-analysis results the obtained diagnostic criterion has sensitivity (1 - b) and specificity, (1 - a) that are equal to 0.87 and 0.96 accordingly, and it means diagnostics is high-quality. The procedure and the mode can be applied in digital medicine.
Текст научной статьи Оценка риска развития осложнений миелопролиферативных заболеваний на основе метода лазерной допплеровской флоуметрии
Поставленные задачи в Российской Федерации реализуются в рамках государственной программы «Развитие здравоохранения» (далее – Госпрограм-ма)1. В состав проектной части пилотной Госпро-граммы включен национальный проект «Здравоохранение», который с 2019 г. реализуется по восьми направлениям (подпрограммам). Одно из направлений (подпрограмма) – «Развитие и внедрение инновационных методов диагностики, профилактики и лечения, а также основ персонализированной медицины», которое предусматривает широкое использование инновационных технологий диагностики и лечения заболеваний.
Одной из целей Госпрограммы является снижение к 2024 г. смертности от болезней системы кровообращения до 450 случаев на 100 тысяч населения. С этим связана такая важнейшая пробла медицинской практики, как профилактика и лечение различных нарушений микроциркуляции крови. Трудности изучения микроциркуляции обусловлены очень малыми размерами микрососудов и сильной разветвленностью внутриорганных сосудистых сетей. В настоящее время в нашей стране в клиническую практику активно входят различные методы исследования микроциркуляции крови человека с использованием метода лазерной допплеровской флоуметрии (ЛДФ). Также одним из достоинств метода является его относительная дешевизна, пригодность для цифровой медицины и массового обследования населения с последующей передачей данных по телеметрии в медицинские центры.
У пациентов с онкогематологическими заболеваниями благодаря достижениям современной медицины (своевременная и качественная диагностика, таргетная терапия, мониторинг состояния пациента) вопрос смертельных исходов и инвалидизации смещается в сторону развития осложнений, в первую очередь сердечно-сосудистых событий. Эндотелиальная дисфункция (ЭД) – это патология, связанная с прогрессирующим повреждением сосудистого эндотелия, приводящим к нарушению его функциональных возможностей [1]. В результате происходит сбой в регулировании систем, отвечающих за тонус сосудов, гомеостаз, адгезивные свойства клеток, неопролиферацию сосудов, за счет дисбаланса в релаксирующих и констрикторных механизмах, в выработке анти- и прокоагулянтных веществ и т.д.
Хронические миелопролиферативные заболевания (ХМПЗ) возникают в результате злокачественной трансформации полипотентной гемопоэтической стволовой клетки костного мозга и последующей клональной пролиферации клеток одного или нескольких ростков гемопоэза (эритроидного, миелоидного, мегакариоцитарного), дифференци- рующихся до зрелых форм [2]. ХМПЗ встречаются в основном среди лиц старшего возраста (средний возраст 55 лет), соматический статус которых значимо отягощен факторами сердечно-сосудистого риска. Такие коморбидные состояния, как атеросклероз, гипертоническая болезнь, метаболические нарушения и образ жизни, в разы повышают риск сосудистых катастроф в данной когорте больных. Результаты исследования показали высокую частоту тромботических осложнений среди лиц моложе 60 лет и распространенность латентного начала заболевания. По локализации преобладают тромбозы артериальных сосудов – острые нарушения мозгового кровообращения и инфаркты миокарда [3]. Смертность больных с ХМПЗ в результате цереброваскулярных заболеваний в 1,5 раза выше, чем в популяции [4].
К группе ХМПЗ относят эссенциальную тром-боцитемию (ЭТ), истинную полицитемию (ИП), первичный миелофиброз (ПМФ) и хронический миелолейкоз (ХМЛ).
Истинная полицитемия (ИП) относится к онко-гематологическим миелопролиферативным заболеваниям, сопровождается увеличением числа эритроцитов и, как следствие, повышением вязкости крови, которое, в свою очередь, приводит к нарушению функции эндотелия [5]. Вторичная артериальная гипертензия (АГ) развивается более чем у половины пациентов с ИП, и также является одним из факторов риска развития эндотелиальной дисфункции (ЭД). Сама артериальная гипертензия – важнейшая медико-социальная проблема. АГ занимает одно из первых мест в Российской Федерации и в мире как причина развития кардиоваскулярных осложнений (инсультов, инфарктов миокарда и т.д.) [6]. Согласно данным ряда научных исследований [7–9], у больных, страдающих артериальной гипертензией, в 85 % случаев встречаются сосудистые тромбозы, а риск летального исхода возрастает в 2–5 раз.
При хроническом миелолейкозе (ХМЛ) проблему представляет пожизненный прием препаратов ингибиторов тирозинкиназ (ИТК), которые оказывают влияние на сосудистый эндотелий, что в свою очередь приводит к развитию сердечно-сосудистых осложнений [10–12]. Так, в качестве фактора эндотелиальной дисфункции может выступать химиотерапия.
У больных онкогематологического профиля проблема нарушений микроциркуляции и дисфункции сосудистого эндотелия остается актуальной. На примере истинной полицитемии и хронического миелолейкоза мы можем рассмотреть взаимосвязь между патогенезом самого заболевания и развитием эндотелиальной дисфункции (ЭД). Синдром гипервязкости крови, развивающий за счет миелопроли- ферации у больных ИП, приводит к увеличению сдвигового напряжения на сосудистом эндотелии, происходит дезорганизация эндотелиальных клеток и базальной мембраны. В результате этого активируются механизмы апоптоза эндотелиоцитов, адгезии и агрегации клеток крови. Нарушения данных механизмов приводят к развитию эндотелиальной дисфункции. При хроническом миелолейкозе, напротив, главную роль отдают влиянию препаратов ИТК на эндотелий сосудов, объясняя развитие побочных эффектов, в том числе со стороны сердечнососудистой системы, неселективным ингибированием большого числа тирозинкиназ. Влияние на нормальные тирозинкиназы, которые отвечают за передачу сигналов клетки, приводит к нарушению функции эндотелиальной клетки [13].
Золотым стандартом оценки функции сосудистого эндотелия являются лабораторные методы, основанные на определении концентрации экскретируемых эндотелиоцитами веществ. Среди таких веществ: эндотелин-1, ангиотензин-II, фактор Виллебранда, оксид азота, NO-синтаза, тромбоксан, натрийуретический пептид, гомоцистеин и др. Также стоит отметить ряд непрямых маркеров повреждения сосудистого эндотелия: С-реактивный белок, фибриноген, TNF-α, концентрация липопротеидов высокой (ЛПВП) и низкой плотности (ЛПНП), триглицеридов.
Многие современные авторы отводят ранней диагностике дисфункции сосудистого эндотелия особую роль в выборе тактики ведения пациентов с различными нозологиями с целью замедления прогрессирования проявлений со стороны сердечнососудистой системы [14]. Этому аспекту уделяется большое внимание в современных научных трудах. Происходит поиск и разработка новых методов диагностики эндотелиальной дисфункции на самых ранних этапах. Наиболее часто встречающиеся методы в работах современных исследователей – ЛДФ, капилляроскопия ногтевого ложа и бульбарной конъюнктивы [15, 16].
С целью комплексной оценки состояния микро-циркуляторного русла используют сочетание нескольких методов: ЛДФ, оптической тканевой оксиметрии и пульсоксиметрии. Использование различных нагрузочных проб позволяет оценить не только компенсаторные возможности, но и ранние изменения гемодинамики и отдельные аспекты работы мик-рососудистого русла при той или иной патологии. Данные подходы могут успешно использоваться в практическом здравоохранении для динамического наблюдения за состоянием микроциркуляторного русла, ЭД и оценки эффективности тактики ведения каждого конкретного пациента2.
Цель исследования – определение возможности использования метода лазерной допплеровской флоуметрии (ЛДФ) для раннего выявления и оценки риска развития сердечно-сосудистых осложнений у пациентов с имеющимися миелопролиферативными заболеваниями.
Материалы и методы. Впервые была исследована возможность диагностировать ЭД на ранних стадиях, основываясь только на данных, полученных методом лазерной допплеровской флоумет-рии [17]. Метод ЛДФ основан на оптическом зондировании тканей лазерным излучением (длина волны 632,8 нм) и анализе рассеянного и отраженного излучения от движущихся эритроцитов. Отражение лазерного излучения от движущихся в микрососудах эритроцитов приводит к изменению частоты сигнала, что позволяет определить различные характеристики микроциркуляции (рис. 1).
Основные достоинства использования метода в целом – простота, безопасность и дешевизна по сравнению с дорогостоящими инвазивными методами. Дополнительная мотивация использования ЛДФ – возможность диагностики ЭД на ранней стадии, то есть до момента развития кардиоваскулярных осложнений. Это возможно благодаря тому, что микроциркуляторная система является одной из наиболее быстро реагирующих на воздействие патологических факторов [18].
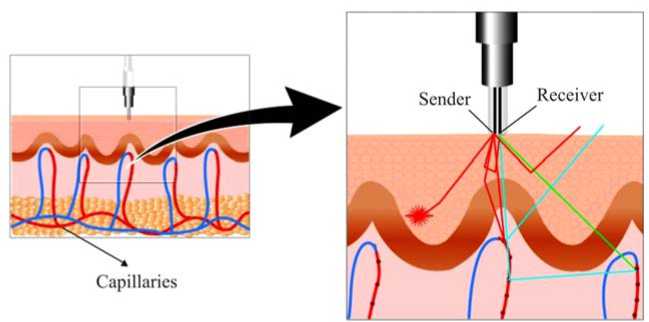
Рис. 1. Использование метода лазерной допплеровской флоуметрии
В последнее время для постановки диагноза по результатам обследования пациентов широко применяются компьютерные технологии и математические модели. Существует целый арсенал математических моделей и компьютерных программ, позволяющих моделировать деятельность сердца и сердечнососудистой системы. Например, графовые модели, системы разностных уравнений, уравнения гемодинамики, нелинейные эконометрические модели, методы распознавания образов и искусственного интеллекта [19–23]. Метод логистической регрессии также применялся ранее к диагностике ЭД, однако в доступной нам литературе мы не встретили данных о применении этого метода для прогнозирования осложнений у пациентов с ХМПЗ3.
Далее исследуются предиктивные свойства регрессионной модели, включающей в себя 12 параметров (табл. 1), измеренных методом ЛДФ с помощью анализатора лазерной микроциркуляции «Лакк-ОП».
Таблица 1
Параметры микроциркуляции
|
Показатель МЦ |
Описание |
Переменная |
|
M |
Средний уровень перфузии |
Х 1 |
|
K v |
Коэффициент вариации микрокровотока |
Х 2 |
|
Aм/СК |
Нормированная амплитуда колебаний микрокровотока, связанная с миогенной регуляцией микрососудов |
Х 3 |
|
S m |
Индекс перфузионной сатурации кислорода |
Х 4 |
|
РКК |
Резервный капиллярный кровоток |
Х 5 |
|
Ан/СК |
Нормированная амплитуда колебаний микрокровотока, связанная с нейрогенной регуляцией микрососудов |
Х 6 |
|
Аэ/СКО |
Нормированная амплитуда колебаний микрокровотока, связанная с эндотелиальной регуляцией микрососудов |
Х 7 |
|
I |
Индекс удельного потребления кислорода в ткани |
Х 8 |
|
D 2 |
Корреляционная размерность |
Х 9 |
|
H o |
Относительная энтропия |
Х 10 |
|
R / S |
Показатель Херста |
Х 11 |
|
ИДП |
Индекс дыхательной пробы |
Х 12 |
Исследование осуществлено у 143 пациентов, из которых 103 имели ХПМЗ (истинная полицитемия и хронический миелолейкоз). Данные нозологии были верифицированы у пациентов лабораторно-инструментальными методами в соответствии с действующими рекомендациями [24, 25]. Для выявления нарушений функции эндотелия проводилось количественное определение уровня эндотелина-1 в сыворотке крови. Причем пациенты с ХМПЗ, уровень эндотели-на-1 у которых был свыше 1,37 фмоль/л, были отнесены в группу с признаками ЭД.
Контрольную группу составили 40 практически здоровых лиц, сопоставимых по полу и возрасту. Для исключения влияния сопутствующей патологии на эндотелий сосудов в исследование не включали пациентов с хронической сердечной недостаточностью II и III стадий (классификация по Стражеско – Василенко), клинически значимыми формами ИБС, другими формами симптоматической артериальной гипертензии, острым нарушением мозгового кровообращения и инфарктом миокарда в течение шести месяцев до начала обследования, хронической бронхолегочной патологией, сахарным диабетом, воспалительными заболеваниями соединительной ткани, курящих пациентов.
Результаты и их обсуждение. Для оценки вероятности развития ЭД, ведущей к сердечно-сосудистым осложнениям, у пациентов использовалась модель логистической регрессии [26].
Исходная выборка была разделена на обучающую и тестовую. Для обучающей выборки случайным образом было выбрано 86 пациентов (60 %), из которых 71 человек имел патологию, а 15 составили контрольную группу. Остальные 57 наблюдений (32 пациента с патологией и 25 из контрольной группы) вошли в тестовую выборку.
Далее используются следующие обозначения: N – объем обучающей выборки, K = 12 – число параметров, вектор параметров, относящихся к наблюдению с номером n :
X n = ( X 1 n , ^ X ) , n = , (1)
где ed – индикатор наличия дисфункции эндотелия (далее – патология), принимающий значения «0» или «1».
Предполагается, что зависимость вероятности возникновения патологии от вектора параметров описывается равенством
P { ed = 1| X n } = f ( Y ( X n ) ) , (2)
где
_ K
-
Y p * ( Xn ) = в 0 + Z P k X kn — линейная комбинация k = 1
показателей МЦ с коэффициентами бета, (3)
и f ( У ) = ——— — логистическая функция.
-
1 + e y
Решением задачи максимизации логарифмической функции правдободобия (4)
N
L(P) = Z jn ln f (Y* (^Xn)) + n=1 (5)
+ ( 1 - j n ) ln ( 1 - f ( Y * ( J X n ) ) )
является вектор коэффициентов регрессии P = arg max L ( p ) .
Таблица 2
Значимые параметры МЦ и соответствующие регрессионные коэффициенты
|
Показатель МЦ |
Переменная |
Среднее, ст. ошибка среднего (патология) |
Среднее, ст. ошибка среднего (контрольная группа) |
Коэффициент регрессии |
Стандартная ошибка коэффициента |
p -value |
|
M |
X 1 |
15,73 ± 0,72 |
18,44 ± 0,34 |
Pj =- 0,996 |
0,285 |
0,00065466 |
|
Kv |
X 2 |
6,38 ± 1,01 |
9,08 ± 0,73 |
Р2 =- 0,628 |
0,153 |
0,00007332 |
|
Aм/СКО |
X 3 |
0,42 ± 0,02 |
0,51 ± 0,02 |
Р3 =- 10,014 |
3,670 |
0,00724567 |
|
Sm |
X 4 |
4,29 ± 0,80 |
5,14 ± 0,27 |
р4 =- 1,027 |
0,324 |
0,00190552 |
|
РКК |
X 5 |
143,81 ± 7,60 |
129,41 ± 2,01 |
Р5 = 0,061 |
0,041 |
0,01402911 |
|
– |
– |
– |
– |
Р0 = 25,001 |
9,833 |
0,01218424 |
В качестве статистики критерия классификации было введено понятие ЭД-индекса как
На первом этапе в анализ включались все переменные; наиболее значимые выделены с помощью метода обратного исключения. Далее для обеспечения максимальной точности классификации на втором этапе переменные сначала исключались в различных сочетаниях. На третьем этапе включались переменные, исключенные на первом этапе. Каждый раз новая модель сравнивалась с первой с помощью анализа ROC-кривой. В результате в наилучшую модель вошло пять переменных (табл. 2).
Для оценки качества диагностики, подбора порога для ЭД-индекса и сравнения с другими моделями использовались ROC-кривые. Пороговое значение классификатора c = 0,887 получено исходя из условия максимума суммы чувствительности и специфичности. По результатам ROC-анализа полученный диагностический критерий на тестовой выборке показал чувствительность (Sensitivity, 1 - в ) и специфичность (Specificity, 1 - а ) 0,875 (28 истинно положительных результатов из 32) и 0,96 (24 истинно отрицательных из 25) соответственно. Площадь (SUC) под ROC-кривой (рис. 2) составляет 0,96, что близко к отличному качеству классификации (уровень значимости модели в целом имеет порядок p < 10E–5).
Таким образом, в терминах теории проверки гипотез ЭД-индекс использовался в качестве статистики критерия проверки нулевой гипотезы об отсутствии патологии. Условие выбора порогового значения эквивалентно выбору байесовского критерия среди критериев с указанной статистикой, обладающего мощностью 0,875 при уровне значимости 0,04.
Итоговая оценка вероятности определялась как кусочно-линейное преобразование ЭД-индекса с целью свести пороговое значение к ожидаемому значению 0,5:
где
g ( x ) = <
x
2c, x +1 - 2 c
0 < x < c
_ 2 ( 1 - c ) ’
c < x < 1
Таким образом, любому вычисленному с использованием модели значению ЭД-индекса, оказавшемуся выше выбранного порогового значения c = 0,887, стало соответствовать некоторое значение Р * > 0,5.
Рассматривая обособленно наиболее значимые в модели параметры (с соответствующими коэффициентами уровня значимости менее 0,005), следует отметить, что классификация, опирающаяся отдельно на каждый из указанных параметров, с тем же критерием выбора порогового значения показала более низкие результаты (табл. 3), чем рассматриваемая модель.
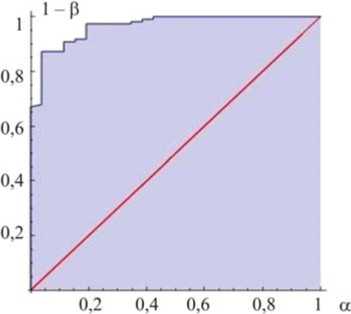
Рис. 2. ROC-кривая
Таблица 3
Показатели качества одномерных моделей
|
Параметр МЦ |
Чувствительность |
Специфичность |
SUV |
|
M |
0,72 |
0,68 |
0,76 |
|
K v |
0,875 |
0,56 |
0,76 |
|
S m |
0,69 |
0,72 |
0,69 |
По результатам исследования разработано программное обеспечение и получено авторское свидетельство.
Выводы. Методы неинвазивной дифференциальной диагностики патологий микроциркуляторного и магистрального ложа на основе современных технологий актуальны по многим причинам. Микроцир-куляторное русло как участок единой сосудистой системы человека весьма уязвим по своей структуре и функции в отношении внешней и / или внутренней агрессии. В мировой статистике заболеваемость и смертность, обусловленные патологией сердечнососудистой системы, занимает первое место. Метод лазерной допплеровской флоуметрии является современным неинвазивным способом оценки функции микроциркуляции. Данный метод является высокочувствительным и отображает тонкие перестройки микроциркуляторного кровотока.
Полученные результаты позволяют сделать вывод, что метод ЛДФ и разработанная регрессионная модель обладают достаточно высокой диагностической эффективностью при раннем выявлении и оценке риска развития сердечно-сосудистых осложнений у пациентов с имеющимися миелопролиферативными заболеваниями.
Финансирование. Исследование не имело спонсорской поддержки.
Список литературы Оценка риска развития осложнений миелопролиферативных заболеваний на основе метода лазерной допплеровской флоуметрии
- Mechanisms of endothelial dysfunction: clinical significance and preventive non-pharmacological therapeutic strategies / S. Taddei, L. Ghiadoni, A. Virdis, D. Versari, A. Salvetti // Curr. Pharm. Des. - 2003. - Vol. 9, № 29. - Р. 2385-2402. DOI: 10.2174/1381612033453866
- Факторы риска тромбозов среди больных хроническими миелопролиферативными заболеваниями / Т.Н. Александрова, В.Н. Ядрихинская, И.И. Мулина, И.Е. Соловьева, Л.Д. Терехова, Н.И. Павлова, Л.Р. Жожиков, Х.А. Куртанов // Вестник северо-восточного федерального университета имени М.К. Аммосова. Серия: Медицинские науки. - 2018. - Т. 13, № 4. - С. 28-32. 10.25587/SVFU.2018.4 (13).20741 DOI: 10.25587/SVFU.2018.4(13).20741
- Experience in treating portal thromboses in patients with chronic myeloproliferative diseases / A.L. Melikyan, G.A. Sukhanova, M.V. Vakhrusheva, I.N. Subortseva, E.B. Orel // Terapevticheskii arkhiv. - 2016. - Vol. 88, № 1. - P. 89-95. DOI: 10.17116/terarkh201688189-95
- Некоторые аспекты профилактики нарушений мозгового кровообращения у пациентов с миелопролиферативными заболеваниями / М.М. Танашян, П.И. Кузнецова, А.А. Раскуражев, О.В. Лагода // Medica mente. Лечим с умом. - 2017. - Т. 3, № 1. - С. 41-44.
- Клинические рекомендации по диагностике и терапии Ph-негативных миелопролиферативных заболеваний / А.Л. Меликян, А.Г. Туркина, К.М. Абдулкадыров, А.Ю. Зарицкий, Б.В. Афанасьев, В.А. Шуваев, Е.Г. Ломаиа, Е.В. Морозова [и др.] // Гематология и трансфузиология. - 2014. - Т. 59, № 4. - С. 31-56.
- Дисфункция эндотелия и артериальная гипертензия / под ред. П.А. Лебедева. - Самара: ОФОРТ, 2010. - 192 с.
- Фудашкин А.А. Эндотелиальная дисфункция у больных артериальной гипертензией, осложненной ишемическим инсультом // Вестник Кыргызско-Российского Славянского университета. - 2015. - Т. 15, № 4. - С. 173-175.
- Association of a difference in systolic blood pressure between arms with vascular disease and mortality: a systematic review and meta-analysis / C.E. Clark, R.S. Taylor, A.C. Shore, O.C. Ukoumunne, J.L. Campbell // Lancet. - 2012. - Vol. 379, № 9819. - Р. 905-916. 10.1016/S0140-6736 (11) 61710-8
- DOI: 10.1016/S0140-6736(11)61710-8
- Prediction of cardiovascular events and allcause mortality with central haemodynamics: a systematic review and meta-analysis / C. Vlachopoulos, K. Aznaouridis, M.F. O'Rourke, M.E. Safar, K. Baou, C. Stefanadis // Eur. Heart J. - 2010. - Vol. 31, № 15. - P. 1865-1871.
- DOI: 10.1093/eurheartj/ehq024
- Clinical Manifestations and Risk Factors for Complications of Philadelphia Chromosome-Negative Myeloproliferative Neoplasms / D. Duangnapasatit, E. Rattarittamrong, T. Rattanathammethee, S. Hantrakool, C. Chai-Adisaksopha, A. Tantiworawit, L. Norasetthada // Asian. Pac. J. Cancer Prev. - 2015. - Vol. 16, № 12. - P. 5013-5018.
- DOI: 10.7314/apjcp.2015.16.12.5013
- European LeukemiaNet recommendations for the management and avoidance of adverse events of treatment in chronic myeloid leukaemia / J.L. Steegmann, M. Baccarani, M. Breccia, L.F. Casado, V. García-Gutiérrez, A. Hochhaus, D.-W. Kim, T.D. Kim [et al.] // Leukemia. - 2016. - Vol. 30, № 8. - P. 1648-1671.
- DOI: 10.1038/leu.2016.104
- Попова А.А., Березикова Е.Н., Маянская С.Д. Эндотелиальная дисфункция и механизмы ее формирования // Сибирское медицинское обозрение. - 2010. - Т. 64, № 4. - С. 7-11.
- Orphanos G.S., Ioannidis G.N., Ardavanis A.G. Cardiotoxity induced by tyrosine kinase inhibitors // Acta Oncologica. - 2009. - Vol. 48, № 7. - P. 964-970.
- DOI: 10.1080/02841860903229124
- Булаева Н.И., Голухова Е.З. Эндотелиальная дисфункция и оксидативный стресс: роль в развитии кардиоваскулярной патологии // Креативная кардиология. - 2013. - № 1. - С. 14-22.
- Методы диагностики эндотелиальной дисфункции / А.Н. Иванов, А.А. Гречихин, И.А. Норкин, Д.М. Пучиньян // Региональное кровообращение и микроциркуляция. - 2014. - Т. 52, № 4. - С. 4-11.
- Канищева Е.М., Федорович А.А. Возможность оценки состояния микроциркуляторного русла и стенок крупных сосудов // Сердце: журнал для практикующих врачей. - 2010. - Т. 9, № 1 (51). - С. 65-70.
- Халепо О.В., Молотков О.В., Ешкина С.Л. Оценка состояния системы микроциркуляции и механизмов регуляции тканевого кровотока у больных при различных вариантах ИБС методом функциональных нагрузочных проб // Региональное кровообращение и микроциркуляция. - 2007. - Т. 6, № 3 (23). - С. 43-46.
- Богоявленский В.Ф., Богоявленская О.В. Клинические аспекты изучения микроциркуляции: итоги и перспективы // Казанский медицинский журнал. - 2011. - Т. 92, № 2. - С. 145-151.
- Математическая модель сердечно-сосудистой системы: препринт / А.П. Фаворский, М.В. Абакумов, Н.Б. Есикова, С.И. Мухин, Н.В. Соснин. - М.: МГУ, 1998. - 16 с.
- Методика математического моделирования сердечно-сосудистой системы / М.В. Абакумов, И.В. Ашметков, Н.Б. Есикова, В.Б. Кошелев, С.И. Мухин, Н.В. Соснин, В.Ф. Тишкин, А.П. Фаворский, А.Б. Хруленко // Математическое моделирование. - 2000. - Т. 12, № 2. - С. 106-117.
- Частные решения уравнений гемодинамики: препринт / И.В. Ашметков, С.И. Мухин, Н.В. Соснин, А.П. Фаворский, А.Б. Хруленко. - М.: Диалог-МГУ, 1999. - 43 с.
- Осредненная нелинейная модель гемодинамики в одном сосуде: препринт / А.Я. Буничева, С.И. Мухин, Н.В. Соснин, А.П. Фаворский. - М: Диалог-МГУ. - 2000. - 21 с.
- Гусев А.В., Кузнецова Т.Ю., Корсаков И.Н. Искусственный интеллект в оценке рисков развития сердечно-сосудистых заболеваний // Журнал телемедицины и электронного здравоохранения. - 2018. - № 3. - С. 18-32.
- Клинические рекомендации по диагностике и лечению хронического миелолейкоза / А.Г. Туркина, А.Ю. Зарицкий, В.А. Шуваев, Е.Ю. Челышева, Е.Г. Ломаиа, Е.В. Морозова, А.К. Голенков, Т.И. Поспелова [и др.] // Клиническая онкогематология. - 2017. - Т. 10, № 3. - С. 294-316.
- Национальные клинические рекомендации по диагностике и терапии ph-негативных миелопролиферативных заболеваний (истинная полицитемия, эссенциальная тромбоцитемия, первичный миелофиброз) (редакция 2018 г.) / А.Л. Меликян, А.М. Ковригина, И.Н. Суборцева, В.А. Шуваев, Т.А. Агеева, В.В. Байков, О.Ю. Виноградова, А.К. Голенков [и др.] // Гематология и трансфузиология. - 2018. - Т. 63, № 3. - С. 275-315.
- Hosmer D.W., Lemeshow S., Sturdivant R.X. Applied logistic regression. - USA: John Wiley & Sons, Inc., 2013. - 527 p.
- Taddei S., Ghiadoni L., Virdis A., Versari D., Salvetti A. Mechanisms of endothelial dysfunction: clinical significance and preventive non-pharmacological therapeutic strategies. Curr. Pharm. Des, 2003, vol. 9, no. 29, pp. 2385-2402.
- DOI: 10.2174/1381612033453866
- Aleksandrova T.N., Yadrikhinskaya V.N., Mulina I.I., Solov'eva I.E., Terekhova L.D., Pavlova N.I., Zhozhikov L.R., Kurtanov Kh.A. Cardiovascular risk factors in patients with chronic myeloproliferative diseases. Vestnik severo-vostochnogo federal'nogo universiteta imeni M.K. Ammosova. Seriya "Meditsinskie nauki", 2018, vol. 13, no. 4, pp. 28-32 (in Russian).
- DOI: 10.25587/SVFU.2018.4(13).20741
- Melikyan A.L., Sukhanova G.A., Vakhrusheva M.V., Subortseva I.N., Orel E.B. Experience in treating portal thromboses in patients with chronic myeloproliferative diseases. Ter Arkh, 2016, vol. 88, no. 1, pp. 89-95. \\
- DOI: 10.17116/terarkh201688189-95
- Tanashyan M.M., Kuznetsova P.I., Raskurazhev A.A., Lagoda O.V. Certain aspects in preventing brain circulation disorders in patients with myeloproliferative diseases. Medicamente. Lechim s umom, 2017, vol. 3, no. 1, pp. 41-44 (in Russian).
- Melikyan A.L., Turkina A.G., Abdulkadyrov K.M., Zaritskii A.Yu., Afanas'ev B.V., Shuvaev V.A., Lomaia E.G., Morozova E.V. [et al.]. Clinical recommendations for diagnosis and therapy of Ph-negative myeloproliferative diseases (polycythemia vera, essential thrombocythemia, primary myelofibrosis). Gematologiya i transfuziologiya, 2014, vol. 59, no. 4, pp. 31-56 (in Russian).
- Endothelium dysfunction and arterial hypertension. In: P.A. Lebedeva ed. Samara, OFORT Publ., 2010, 192 p. (in Russian).
- Fudashkin A.A. Endothelial disfunction in patients with hypertension and history of ischemic stroke. Vestnik Kyrgyzsko-Rossiiskogo Slavyanskogo universiteta, 2015, vol. 15, no. 4, pp. 173-175 (in Russian).
- Clark C.E., Taylor R.S., Shore A.C., Ukoumunne O.C., Campbell J.L. Association of a difference in systolic blood pressure between arms with vascular disease and mortality: a systematic review and meta-analysis. Lancet, 2012, vol. 379, no. 9819, pp. 905-916.
- DOI: 10.1016/S0140-6736(11)61710-8
- Vlachopoulos C., Aznaouridis K., O'Rourke M.F., Safar M.E., Baou K., Stefanadis C. Prediction of cardiovascular events and allcause mortality with central haemodynamics: a systematic review and meta-analysis. Eur. Heart. J., 2010, vol. 31, no. 15, pp. 1865-1871.
- DOI: 10.1093/eurheartj/ehq024
- Duangnapasatit D., Rattarittamrong E., Rattanathammethee T., Hantrakool S., Chai-Adisaksopha C., Tantiworawit A., Norasetthada L. Clinical Manifestations and Risk Factors for Complications of Philadelphia Chromosome-Negative Myeloproliferative Neoplasms. Asian. Pac. J. Cancer Prev., 2015, vol. 16, no. 12, pp. 5013-5018.
- DOI: 10.7314/apjcp.2015.16.12.5013
- Steegmann J.L., Baccarani M., Breccia M., Casado L.F., García-Gutiérrez V., Hochhaus A., Kim D.-W., Kim T.D. [et al.]. European Leukemia Net recommendations for the management and avoidance of adverse events of treatment in chronic myeloid leukaemia. Leukemia, 2016, vol. 30, no. 8, pp. 1648-1671.
- DOI: 10.1038/leu.2016.104
- Popova A.A., Berezikova E.N., Mayanskaya S.D. Mechanism of endothelial dysfunction development. Sibirskoe meditsinskoe obozrenie, 2010, vol. 64, no. 4, pp. 7-11 (in Russian).
- Orphanos G.S., Ioannidis G.N., Ardavanis A.G. Cardiotoxity induced by tyrosine kinase inhibitors. Acta Oncologica, 2009, vol. 48, no. 7, pp. 964-970.
- DOI: 10.1080/02841860903229124
- Bulaeva N.I., Golukhova E.Z. Endothelial dysfunction and oxidant stress: the role in cardiovascular pathology. Kreativnaya kardiologiya, 2013, no. 1, pp. 14-22 (in Russian).
- Ivanov A.N., Grechikhin A.A., Norkin I.A., Puchin'yan D.M. Methods of endothelial dysfunction diagnosis. Regionarnoe krovoobrashchenie i mikrotsirkulyatsiya, 2014, vol. 52, no. 4, pp. 4-11 (in Russian).
- Kanishcheva E.M., Fedorovich A.A. Possibilities for evaluating the condition of miscrovasculature and walls of large blood vessels. Serdtse: zhurnal dlya praktikuyushchikh vrachei, 2010, vol. 9, no. 1 (51), pp. 65-70 (in Russian).
- Khalepo O.V., Molotkov O.V., Eshkina S.L. Assessing microcirculation functioning and mechanisms of tissue circulation regulation in patients suffering from various types of IHD via functional tests under loads. Regionarnoe krovoobrashchenie i mikrotsirkulyatsiya, 2007, vol. 6, no. 3 (23), pp. 43-46 (in Russian).
- Bogoyavlenskii V.F., Bogoyavlenskaya O.V. Clinical aspects of microcirculation research: achievements and perspectives. Kazanskii meditsinskii zhurnal, 2011, vol. 92, no. 2, pp. 145-151 (in Russian).
- Favorskii A.P., Abakumov M.V., Esikova N.B., Mukhin S.I., Sosnin N.V. A mathematical model for the cardiovascular system. Pre-print. Moscow, MGU Publ., 1998, 16 p. (in Russian).
- Abakumov M.V., Ashmetkov I.V., Esikova N.B., Koshelev V.B., Mukhin S.I., Sosnin N.V., Tishkin V.F., Favorskii A.P., Khrulenko A.B. Mathematical techniques for cardiovascular system modeling. Matematicheskoe modelirovanie, 2000, vol. 12, no. 2, pp. 106-117 (in Russian).
- Ashmetkov I.V., Mukhin S.I., Sosnin N.V., Favorskii A.P., Khrulenko A.B. Chastnye resheniya uravnenii gemodinamiki. Preprint [Particular solutions to hemodynamics equations. Pre-print]. Moscow, Dialog-MGU Publ., 1999, 43 p. (in Russian).
- Bunicheva A.Ya., Mukhin S.I., Sosnin N.V., Favorskii A.P. Averaged non-linear model showing hemodynamics in one vessel. Pre-print. Moscow, Dialog-MGU Publ., 2000, 21 p. (in Russian).
- Gusev A.V., Kuznetsova T.Yu., Korsakov I.N. Artificial intellect in assessing risks of cardiovascular diseases development. Zhurnal telemeditsiny i elektronnogo zdravookhraneniya, 2018, no. 3, pp. 18-32 (in Russian).
- Turkina A.G., Zaritskii A.Yu., Shuvaev V.A., Chelysheva E.Yu., Lomaia E.G., Morozova E.V., Golenkov A.K., Pospelova T.I. [et al.]. Clinical Recommendations for the Diagnosis and Treatment of Chronic Myeloid Leukemia. Klinicheskaya onkogematologiya, 2017, vol. 10, no. 3, pp. 294-316 (in Russian).
- Melikyan A.L., Kovrigina A.M., Subortseva I.N., Shuvaev V.A., Ageeva T.A., Baikov V.V., Vinogradova O.Y., Golenkov A.K. [et al.]. National clinical recommendations for diagnosis and therapy of PH-negative myeloproliferative neoplasms (polycythemia vera, essential thrombocythemia, primary myelofibrosis) (edition 2018). Gematologiya i transfuziologiya, 2018, vol. 63, no. 3, pp. 275-315 (in Russian).
- Hosmer D.W., Lemeshow S., Sturdivant R.X. Applied logistic regression. USA, John Wiley & Sons, Inc. Publ., 2013, 527 p.


