Оценка токсичности бактериальной нуклеазы, проведенная в остром эксперименте
Автор: Филимонова М.Н., Равилов Р.Х., Маланьева А.Г.
Статья в выпуске: 1 т.257, 2024 года.
Бесплатный доступ
Цель исследования заключалась в выявлении токсических эффектов бактериальной нуклеазы в остром эксперименте, но без достижения летальности. Для этого нуклеазу использовали в количестве близком к дозе, соответствующей дозе для проявления ее биологических эффектов. Установлено, что бактериальная нуклеаза, введенная внутривенно мышам в дозе 0,5 мг/кг веса животного, не вызывала острых побочных эффектов на внешний вид и поведение мышей, что свидетельствовало об отсутствии токсичности нуклеазы in vivo в выбранной дозе.
Нуклеаза serratia marcescens, бактериальная нуклеаза, внутривенное введение, токсичность, острый эксперимент
Короткий адрес: https://sciup.org/142240699
IDR: 142240699 | УДК: 574/577 | DOI: 10.31588/2413_4201_1883_1_257_261
Assessment of bacterial nuclease toxicity in an acute experiment
The aim of the study was to identify the toxic effects of bacterial nuclease in an acute experiment, but without achieving mortality. For this purpose, the nuclease was used in an amount close to the dose corresponding to the dose for the manifestation of its biological effects. It was found that bacterial nuclease administered intravenously to mice at a dose of 0.5 mg/kg of animal weight did not cause acute side effects on the appearance and behavior of mice, which indicated the absence of toxicity of the nuclease in vivo at the selected dose.
Текст научной статьи Оценка токсичности бактериальной нуклеазы, проведенная в остром эксперименте
Бактериальная нуклеаза – это фермент, который синтезируют и секретируют в окружающую среду грамотрицательные бактерии Serratia marcescens. При физиологических условиях нуклеаза успешно расщепляет ДНК или РНК на нуклеотиды [3]. В настоящее время бактериальная нуклеаза – это хорошо изученный фермент, у которого известны ключевые физикохимические и биохимические свойства, структура и механизм действия [7, 10]. Данные о нуклеазе представлены в таких известных банках данных как SCOP, RCSB, Brenda. Разработаны методы выделения и очистки фермента [12]. Известны биологические эффекты (Таблица 1). Так, показан ее противоопухолевый эффект. При внутрибрюшинном введении нуклеазы в дозе 0,25 мг/кг живой массы мышей происходило торможение развития внутрибрюшинной карциномы Эрлиха более чем на 50 % [1]. Нуклеаза очень активна при деградации ДНК в мокроте [13], приближаясь по эффективности к медицинскому препарату Пульмозим, применяемому при лечении болезней дыхательной системы. Установлен антирабический эффект композиции материалов, ключевым компонентом которой является бактериальная нуклеаза [8]. Под названием Эндовираза (Эндоглюкин) препарат на основе бактериальной нуклеазы применяют в сельском хозяйстве для лечения и профилактики вирусных заболеваний пчел [6]. Показана эффективность Эндовиразы в борьбе с вирусными респираторными инфекциями крупного рогатого скота и птицы [2, 4]. Однако в печати нет сведений, позволяющих охарактеризовать этот фермент токсикометрически. Сведения о невысокой цитотоксичности бактериальной нуклеазы, полученные с использованием ряда культур клеток (Таблица 2), являются недостаточными для токсикометрической характеристики данного вещества. Известно, что начальным этапом для токсикометрической характеристики вещества обычно служит оценка его острой токсичности в опытах in vivo. Учитывая реальное применение бактериальной нуклеазы на практике и его дальнейшие перспективы, цель настоящего исследования заключалась в выявлении токсических эффектов бактериальной нуклеазы в остром эксперименте, но без достижения летальности. В связи с этим нуклеазу использовали в количестве близком к дозе, соответствующей дозе для проявления ее биологических эффектов (Таблица 1).
Материал и методы исследований. Объектом исследования служила гомогенная бактериальная нуклеаза, которую получали выделением из культуральной жидкости S.marcescens и характеризовали чистоту препарата, как описано [11]. Очищенную нуклеазу затем диализовали против дистиллированной воды и лиофилизировали. После этого 1 мг сухой нуклеазы растворяли в 0,2 мл физиологического раствора и центрифугировали при 4 °С для удаления не растворившейся фракции. Концентрацию раствора нуклеазы рассчитывали исходя из поглощения надосадочной жидкости при 280 нм и молярного коэффициента экстинкции 47 292 М-1/см2 [12].
Таблица 1 – Биологические эффекты нуклеазы
|
w Я И я О о я Ч £ о О с S |
н и о Г) |
н О К я S s н н о -©и И Г) |
я 3 о я |
W S я н Я |
о я ч к |
|
Беспородные белые мыши; самцы, вес 2023 г |
Подавление роста раковой опухоли |
Торможение роста внутрибрюшинной карциномы Эрлиха более чем на 50% |
Высокой степени очистки |
0,25мг /кг веса животного |
[1] |
|
Беспородные белые мыши; самцы, вес 10 г |
Антирабич еская активность |
Увеличение выживаемости инфицированных вирусом бешенства мышей более чем на 30 % |
Гомогенная |
1,0 мг/кг веса живот ного |
[8] |
|
Гнойнослизистая мокрота (In vitro) |
Расщепление ДНК в мокроте |
Разжижение мокроты не хуже, чем с Пульмозимом в стандартных для Пульмозима условиях |
Гомогенная |
0,02-34 мкг/мл мокроты |
[12] |
Таблица 2 – Условия определения цитотоксичности бактериальной нуклеазы in vitro
|
Метод определения |
Тип культуры клеток |
Исследование |
|
MTT -тест |
Человеческие фибробласты кожи (HSF) |
[9] |
|
MTS-тест |
Почка эмбрионов человека (HEK293) |
[8] |
|
MTT -тест |
Колоректальный рак человека (HCT-116) |
[9] |
|
MTT -тест |
Рак молочной железы человека (MCF 7) |
[9] |
|
MTS-тест |
Гепатома крысы (H4-II-E-C3) |
[13] |
Ферментативную активность определяли методом, основанным на оценке количества кислоторастворимых низкомолекулярных нуклеотидных фрагментов, образуемых при деградации субстрата (ДНК или РНК) под действием нуклеазы [3].
Испытание токсичности проводили в соответствии с методическими указаниями [5] на половозрелых самцах белых мышей с массой тела 20-21 г, сформированных в 4 группы: контрольную и три опытные (n=5). Основными критериями включения животных в эксперимент было отсутствие клинических признаков заболеваний. После формирования групп грызуны были подвергнуты двухнедельному карантину для последующей оценки их адаптации и физиологического состояния. Содержание животных осуществляли в типовых пластиковых клетках с температурным режимом +18-22 °С в условиях естественного светового цикла на стандартной диете, без ограничений к потреблению пищи и воды.
Дизайн эксперимента был разработан в соответствии с действующими правилами Европейской Конвенции (2010/63/EU) по уходу и защите животных, используемых для исследовательских и иных научных целей, и одобрен Комитетом по этике Казанского федерального университета (Российская Федерация, г. Казань, № 459.06.04.2020).
Объект исследования вводили мышам в хвостовую вену по 0,05 мл/мышь, руководствуясь тем, что кровь, циркулируя по организму, омывает все органы и ткани. Мышам контрольной группы вводили физиологический раствор (физраствор), а опытных групп – по 10,5 мкг нуклеазы в физрастворе/мышь, то есть в дозе 0,5 мг/кг веса животного. Для дальнейшего анализа животных умерщвляли эвтаназией в атмосфере углекислого газа сразу после введения нуклеазы – 1-я опытная группа, через 2 ч после введения – 2-я опытная группа и через 2 недели после введения – 3-я опытная группа – и подвергали вскрытию для исследования органов. Параллельно получали сыворотку крови для анализа динамики изменения содержания нуклеазы в крови, для чего оценивали изменение ДНКазной и РНКазной активностей сыворотки крови, отобранной из сердца животного сразу после начала эвтаназии, но до остановки сердца. Сыворотку выделяли в соответствии с общепринятым методом. Для образования сгустка кровь инкубировали 60 мин. при 25 oC. Затем сгусток удаляли и клетки крови отделяли 10-мин. центрифугированием при 1300 g. Полученные сыворотки хранили при температуре – 20 °С.
Острую токсичность оценивали по таким показателям как клиническое состояние, поведенческая активность, возможная количественная гибель мышей и сроки ее наступления. Контроль за животными и наблюдение для выявления признаков токсикоза продолжали в течение 14 суток от момента введения нуклеазы. В первые сутки учет физиологического состояния проводился каждый час; следующие трое суток – каждые 8 часов; в оставшиеся дни оценка состояния мышей осуществлялась каждые 24 часа.
Данные, полученные в результате исследования, обработаны биометрически с использованием пакета стандартных программ Microsoft Excel.
Результат исследований. В эксперименте была использована гомогенная бактериальная нуклеаза, выделенная, как описано ранее, и охарактеризованная с помощью SDS-PAGE и полносканирующей масс-спектрометрии MALDI-TOF [13]. Ферментативная активность растворенной фракции составляла 389333,3 Ед/мл в час с РНК в качестве субстрата и 294666,6 Ед/мл в час с ДНК. Концентрация нуклеазы перед инъекцией составляла 0,21 мг/мл.
Оценка активности ДНКазы и РНКазы в образцах сыворотки до и после введения нуклеазы мышам показала, что и ДНКазная и РНКазная активности были определены в сыворотке на всех этапах исследования (Рисунок 1). Однако, до введения мышам нуклеазы (контрольная группа) ДНКазная и РНКазная активности соответствовали 30 и 190 Ед/мл в час. Сразу после внутривенного введения нуклеазы (1-я опытная группа) обе активности в сыворотке резко возрастали: соответственно в 350 и в 130 раз. А через два часа после введения нуклеазы (2-я опытная группа) обе активности в сыворотке снижались примерно в 25 и 30 раз, но оставались в 5-10 раз выше, чем в контроле. По истечению 14 суток (3-я опытная группа) показатели РНКазной и ДНКазной активностей сыворотки соответствовали контролю (результаты не показаны).
Таким образом, в сыворотке контрольных мышей по сравнению с вводимым ферментом обе активности были невелики. Сразу после внутривенного введения нуклеазы обе активности в сыворотке резко увеличивались, вероятно, за счет распределения по крови бактериальной нуклеазы. И через два часа после введения нуклеазы (2-я опытная группа) обе активности в сыворотке существенно снижались, но оставались выше, чем в контроле. Повышенные по сравнению с контролем ДНКазная и РНКазная активности сыворотки предполагали наличие в крови остаточных количеств бактериальной нуклеазы. При этом многократное снижение этих активностей спустя 2 ч после введения бактериальной нуклеазы могло быть связано или с протеолизом нуклеазы за счет собственных протеаз сыворотки или с перераспределением бактериальной нуклеазы между кровью и другими тканями мышей, что требует дальнейшего исследования.
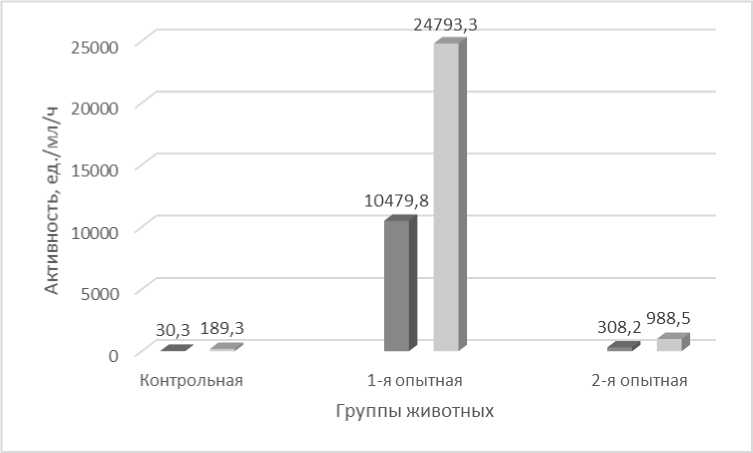
Рисунок 1 – ДНКазная (темные столбики) и РНКазная (светлые столбики) активности в сыворотке крови до введения нуклеазы (контроль), сразу после введения (1-я опытная) и через 2 ч (2-я опытная) после введения нуклеазы в хвостовую вену мышей
При оценке состояния животных по результатам проведенных исследований признаков интоксикации и случаев гибели мышей при однократном введении бактериальной нуклеазы в разовой дозе 0,5 мг/кг веса животного выявлено не было ни сразу, ни через 2 ч, ни через 14 суток после введения. На протяжении всего срока наблюдений общее состояние животных опытных и контрольной групп не различалось, не наблюдалось никаких грубых патологий. Поведенческие реакции не отклонялись от нормы. Реакции на тактильные, болевые, звуковые и световые раздражители были без патологических изменений. Ни у одной мыши не наблюдалось значительных поведенческих изменений, таких как изменение двигательной функции, уровня возбуждения, вегетативных функций и психологического статуса, которые могли бы указывать на эффект нейротоксичности. Отсутствовало влияние введения нуклеазы на аппетит: потребление еды и воды оставалось нормальным, истощение не выявлялось, что свидетельствовало об отсутствии нарушения углеводного, белкового или жирового обменов.
Вскрытие животных как опытных, так и контрольной групп показало, что грудная и брюшная полости не содержали выпота; положение внутренних органов грудной и брюшной полостей анатомически правильное, париетальный и висцеральный листки плевры и брюшины тонкие, блестящие, гладкие. Никаких гистологических изменений в печени, почках, селезенке, сердце, легких мышей, подвергшихся инъекции нуклеазы, не наблюдалось. Состояние волосяного и кожного покровов, окраска слизистых были без патологических изменений: отека, гиперемии, язв, сыпи. Шерсть была блестящей, без очагов аллопеции, зубы сохранены, видимые слизистые оболочки бледно-розовые, блестящие, деформации или отека конечностей не выявлено. Таким образом, оценка токсичности бактериальной нуклеазы, проведенная в остром эксперименте, позволяет заключить, что данный фермент в дозе 0,5 мг/кг веса животного не проявляет органотоксичности.
Заключение. Данные токсикометрии при внутривенном введении бактериальной нуклеазы, а также наблюдение за лабораторными мышами на протяжении 14 суток в постинтоксикационном периоде позволяют заключить, что бактериальная нуклеаза, введенная внутривенно мышам в дозе 0,5 мг/кг веса животного не вызывала острых побочных эффектов на внешний вид и поведение мышей, что свидетельствовало об отсутствии токсичности нуклеазы in vivo в выбранной дозе.
Работа выполнена за счет средств Программы стратегического академического лидерства Казанского (Приволжского) федерального университета (ПРИОРИТЕТ-2030).
Список литературы Оценка токсичности бактериальной нуклеазы, проведенная в остром эксперименте
- Габдуллина, Г. К. Действие нуклеазы Serratia marcescens на клетки и рост асцитной опухоли Эрлиха / Г. К. Габдуллина // Автореферат диссертации на соискание ученой степени кандидата биологических наук. – Казань: Типография издательства Тат. ОК КПСС, 1980. – С.14.
- Живодеров, С. Противостоять вирусам поможет «Эндовираза» / С. Живодеров, А. Рябова // Животноводство России. – 2015. – №10. – С. 3-4.
- Лещинская, И. Выделение и характеристика высокоочищенного препарата нуклеазы Serratia marcescens / И. Лещинская, Н. Балабан, Г. Егорова, В. Таняшин [и др.] // Биохимия. – 1974. – №11. – С. 95-100.
- Порываева, А. Лечебная и профилактическая Эндовираза / А. П. Порываева, Е. В. Печура // Животноводство России. – 2020. – № 2. – С. 26-30.
- Руководство по проведению доклинических исследований лекарственных средств. Ч. 1. Методические рекомендации по изучению общетоксического действия лекарственных средств / Под. ред. А. Н. Миронова // Изучение острой токсичности. Изучение хронической токсичности. – М.: Гриф и К; 2012. – С. 15-19
- Селедцова, Г. В. Изучение действия эндонуклеазы бактериальной на вирус мешотчатого расплода (SBV), поддерживаемого на клеточной линии Vero / Г. В. Селедцова, Э. А. Кащенко, Л. В. Келин, А. А. Рябова // Пчеловодство. – 2016. – № 7. – С. 1-12.
- Friedhoff, P. Analysis of the mechanism of the Serratia nuclease using site-directed mutagenesis / P. Friedhoff, B. Kolmes, O. Gimadutdinow, W. Wende [et al.] // Nucleic Acids Research. – 1996. – № 14. – P. 2632-2639.
- Khismatullina, N. Nuclease Composition with Anti-Rabies Activity / N. Khismatullina, A. Ivanov, E. Martynova, A. Mironov [et al.] //Journal of pure and applied microbiology. – 2014. № 2. – P. 499-504.
- Malanyeva, A. G. The Nuclease from Gram-Negative Bacteria Serratia marcescens is Weakly Cytotoxic at Therapeutic Doses / A. G. Malanyeva, T. Salikhova, A. A. Rizvanov, M. N. Filimonova // Open Access Journal of Veterinary Science & Research. – 2020. – № 2. – P. 1-8.
- Miller, M. A structure of Serratia endonuclease suggests a mechanism for binding to double-stranded DNA / M. Miller, J. Tanner, M. Alpaugh, M. Benedik [et al.] // J. Nature Struct. Biol. – 1994. – № 1. – P. 461-468.
- Ravilov, R. K. Studying of toxicological properties of the "NB" connection possessing antiparasitic action / R. K. Ravilov [et all.] // Research Journal of Pharmaceutical, Biological and Chemical Sciences. – 2018. – Т. 9. – № 6. – P. 1502-1506.
- Vafina, G. A one-step protocol for chromatographic purification of nonrecombinant exogenous bacterial enzyme: nuclease of Serratia marcescens / G. Vafina, E. Bulatov, E. Zainutdinova, M. Filimonova // BioNanoSci. – 2016. – DOI 10.1007/s12668-016-0226-9.
- Vafina, G. Endonuclease from Gram-Negative Bacteria Serratia marcescens Is as Effective as Pulmozyme in the Hydrolysis of DNA in Sputum / G. Vafina, E. Zainutdinova, E. Bulatov, M. Filimonova // Frontiers in Pharmacology. – 2018. – № 9. – P. 1-8.
- Zainutdinova, E. Сombined Effect of Diluted Betadine and Serratia marcescens Nuclease on Viability of Rat Hepatoma Cells / E. Zainutdinova, E. Naumenko, E. Martinova, M. Filimonova // Research Journal of Pharmaceutical, Biological and Chemical Sciences. – 2015. – № 6. – P. 1637-1647.


