Оценка устойчивости инбредных линий свеклы столовой к церкоспорозу (Cercospora beticola sacc.) в полевых и лабораторных условиях
Автор: Тимакова Л.Н., Алексеева К.Л., Соколова Л.М.
Журнал: Овощи России @vegetables
Рубрика: Агрохимия, агропочвоведение, защита и карантин растений
Статья в выпуске: 4 (78), 2024 года.
Бесплатный доступ
Актуальность. Церкоспорозная пятнистость листьев Cercospora beticola) - повсеместно распространенное заболевание свеклы столовой, снижающее урожайность корнеплодов во многих регионах свеклосеяния. Ежегодные потери от церкоспороза составляют до 30-40%, а в годы эпифитотий - 50% и более. Гриб имеет сложную внутривидовую структуру, включает множество патотипов и рас, что следует учитывать при селекции на устойчивость. Основным методом создания устойчивых форм свеклы столовой к С. beticola является отбор церкоспороустойчивых линий при естественном проявлении болезни и на искусственных фонах. В условиях открытого грунта проведение оценки устойчивости свеклы столовой к церкоспорозу не всегда возможно, так как в отдельные жаркие и засушливые годы церкоспороз проявляется слабо. Поэтому для ускорения селекционного процесса важное значение имеют лабораторные методы оценки. Цель исследований - провести иммунологический анализ линий свеклы столовой в полевых и лабораторных условиях для отбора устойчивого материала. Материал и методика. Оценка сортообразцов свеклы столовой на устойчивость к церкоспорозу проводилась в условиях открытого грунта на базе Всероссийского научно-исследовательского института овощеводства - филиале ФГБНУ ФНЦО (Московская обл.). В лабораторных условиях проводилось искусственное инфицирование отделенных листьев свеклы столовой. Объектами исследования явились инбредные линии свеклы столовой 1-6 поколения. Результаты и обсуждение. В результате оценки и отбора выделены линии № 713 и 790 свеклы столовой с повышенной устойчивостью к церкоспорозу. Установлено, что для практической селекции необходимо постоянно и строго вести отбор по признаку устойчивости к церкоспорозу. В лабораторных условиях разработан метод искусственного заражения отделенных листовых пластинок, который позволяет в короткие сроки проводить предварительную оценку большого числа образцов свеклы столовой на устойчивость к церкоспорозу. КЛЮЧЕВЫЕ СЛОВА:
Свекла столовая, церкоспороз, селекция на устойчивость, иммунологическая оценка сортообразцов, естественный и искусственный инфекционный фон, экспресс метод оценки устойчивости
Короткий адрес: https://sciup.org/140305793
IDR: 140305793 | УДК: 635.11:632.488 | DOI: 10.18619/2072-9146-2024-4-28-34
Assessment of the resistance of inbred table beet lines to cercosporosis (Cercospora beticola sacc.) in field and laboratory conditions
Relevance. Cercospora leaf spot Cercospora beticola) is a widespread disease of table beet that reduces the yield of root crops in many beet-growing regions. Annual losses from cercosporosis amount to 30-40%, and in the years of epiphytotic diseases - 50% or more. The fungus has a complex intraspecific structure, includes many pathotypes and races, which should be taken into account when breeding for resistance. The main method of creating resistant forms of table beet to C. beticola is the selection of cercospore-resistant lines in the natural manifestation of the disease and on artificial backgrounds. In open ground conditions, it is not always possible to assess the resistance of table beet to cercosporosis, since cercosporosis is weak in some hot and dry years. Therefore, laboratory assessment methods are important to accelerate the breeding process. The purpose of the research is to carry out an immunological analysis of beet lines in the field and laboratory conditions for the selection of sustainable material.
Текст научной статьи Оценка устойчивости инбредных линий свеклы столовой к церкоспорозу (Cercospora beticola sacc.) в полевых и лабораторных условиях
Оригинальная статья / Original article
Церкоспорозная пятнистость листьев (церкоспо-роз)- повсеместно распространенное заболевание свеклы столовой, снижающее урожайность корне- плодов во многих регионах свеклосеяния. Ежегодные потери от церкоспороза составляют до 30-40%, а в годы эпифитотий – 50% и более [1]. Усиление вредо- носности церкоспороза свеклы столовой за последние годы в различных регионах России связано как с изменением климата, так и с широким использованием гибридов западной селекции, которые характеризуются восприимчивостью к болезням и не пригодны для длительного хранения [2, 3, 4].
Симптомы церкоспороза проявляются в виде обра- зования на листьях нижнего и среднего яруса розетки характерных некротических пятен округлой формы 2-6 мм в диаметре с характерной каймой темно-красного или бурого цвета (рис. 1). По мере развития болезни число пятен на поверхности листовых пластин быстро увеличивается, сильно пораженные листья усыхают и отмирают. У больных растений сокращается площадь ассимиляционной поверхности, снижается интенсивность фотосинтеза, нарушаются процессы формирования корнеплодов, что приводит к недобору товарной части урожая, вызыва- ет снижение качества корнеплодов и их сохраняемости [5,6,7].

Рис. 1. Церкоспорозная пятнистость листьев свеклы столовой (автор фото: Тимакова Л.Н.)
Fig. 1. Cercospora leafspot ofred beet (photo by Timakova L.N.)
Возбудитель церкоспороза – фитопатогенный гриб Сercospora beticola Sасс ., в цикле развития имеет только бесполое конидиальное спороношение. Конидии нитевидной или игловидной формы с перегородками, размером 3-5х27-250 мкм (рис. 2), переносятся на здоровые растения аэрогенным путем, вызывая их заражение [8].
Обильному спороношению С. beticola и быстрому распространению болезни в посевах свеклы столовой способствует теплая и влажная погода и увлажнение листовой розетки. При оптимальных условиях для прорастания конидий и внедрения инфекции – (температура воздуха +20…+25oС, относительная влажность воздуха 90%) инкубационный период
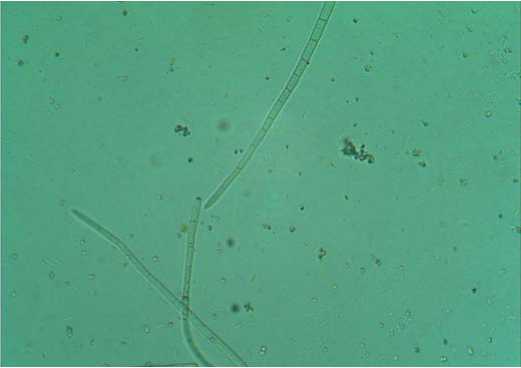
Рис. 2. Игловидные конидии С. beticola в поле зрения светового микроскопа при увеличении 16 х 40 (автор фото: Соколова Л.М.) Fig. 2. Needle-shaped conidia ofC. beticola in the field ofview ofa lightmicroscope ata magnification of16 x 40 (photo by L.M. Sokolova)
составляет 3 дня. Возбудитель церкоспороза С. beticola поражает, не только столовую свеклу, но и сахарную, свеклу кормовую, а также мангольд, шпинат и многие виды сорных растений семейства Маревые [7, 9, 10]. Зимует гриб в виде мицелия и стромовидных образований на сохраняющихся растительных остатках
Гриб имеет сложную внутривидовую структуру, включает множество патотипов и рас, что следует учитывать при селекции на устойчивость [11,12,13]. Основным методом создания устойчивых форм свеклы столовой к С. beticola является отбор церкоспороустойчивых линий при естественном проявлении болезни и на искусственных фонах. В условиях открытого грунта проведение оценки устойчивости линий свеклы столовой к церкоспорозу не всегда возможно, так как в отдельные жаркие и засушливые годы церкоспороз проявляется слабо. Поэтому для ускорения селекционного процесса важное значение имеют лабораторные методы оценки селекционного материала на устойчивость к патогену [14, 15]. Описание этих методов для свеклы столовой в литературе отсутствует, поэтому их разработка имеет важное значение.
Цель исследований – провести иммунологический анализ линий свеклы столовой в полевых и лабораторных условиях для отбора устойчивого материала и включения его в дальнейший селекционный процесс создания межлинейных гибридов F 1 , устойчивых к церкоспорозу,
Условия, материалы и методы исследований
Оценка сортообразцов свеклы столовой на устойчивость к церкоспорозу проводилась в полевых условиях в 2018-2023 годах на базе Всероссийского научно-исследовательского института овощеводства – филиале ФГБНУ ФНЦО (Московская обл.). Почва опытного участка относится к типу аллювиальных луговых, среднесуглинистая, насыщенная, влагоем- кая. Глубина пахотного слоя – 27 см, глубина залегания грунтовых вод – более 2м.Отличается высоким содержанием гумуса – 3,5–3,8%, близким к нейтральной реакцией солевой вытяжки – 5,5–6,1, общего азота – 0,19–0,24%, нитратного азота – 2,0–2,8 мг/100 г, содержание подвижных форм фосфора – 17,6–19,1 мг/100 г, калия – 7,0–8,2 мг/100 г соответственно.
Агроклиматические условия в годы проведения исследований были различными. В 2018 году все летние месяца были теплыми и солнечными с неравномерным выпадением осадков.Средняя температура июля и августа составляла +20…+.25 oС. Первые симптомы церкоспороза были отмечены в посевах свеклы столовой в первой декаде июля. К концу вегетационного периода распространенность болезни достигала 100%.
Погодные условия в 2020 году в целом были также благоприятными для развития болезни. Показатели атмосферных осадков в мае-июле существенно превышали среднемноголетние показатели, и первые симптомы церкоспороза были отмечены в посевах свеклы столовой во второй декаде июня. В августе осадков выпало на 30-60% меньше среднемноголетних значений, что замедлило распространение болезни во второй половине вегетационного периода.
В 2022 году преобладала жаркая и сухая погода. Количество выпавших осадков было значительно ниже нормы и составило в июне, июле, августе соответственно 50,8%, 87,8% и 19,9% от среднемноголетних значений. Среднесуточная температура воздуха со 2-ой декады июня по 3-ю декаду августа превышала многолетнюю норму. В этих условиях развитие болезни имело депрессивный характер.
Объектом исследований явились одноростковые инцухт линии 1-6 поколений, источниками которых стали образцы Хавская, Креолка, Монополи, Модана, 594 (табл. 1).

А – Отделенная листовая пластина
(1 способ – опрыскивание суспензией спор C. вeticola )
Таблица 1. Перечень сортообразцов инцухт линии Table 1. List of varieties of breeding line
|
№ образца |
Источник – сорт, гибрид |
Поколение |
|
708 |
Хавская |
2 |
|
713 |
Хавская |
2 |
|
714 |
Креолка односемянная |
1 |
|
715 |
Креолка односемянная |
1 |
|
734 |
Монополи |
2 |
|
736 |
Монополи |
2 |
|
739 |
594-1-3 |
6 |
|
790 |
594-1-1 |
6 |
|
805 |
Модана |
1 |

Б – Отделенные листья
(2 способ – опрыскивание суспензией спор C. вeticola )
Рис. 3. Способы заражения отделенных листьев свеклы столовой Fig. 3. Methods forinfecting separated beetleaves

Рис. 4. Приготовление суспензии спор C. beticola Fig. 4. Preparation ofC. beticola spore suspension
Семена высевали в третьей декаде мая.Оценку поражения листовой розетки растений церкоспоро-зом проводили методом визуальной диагностики в фазу технической спелости корнеплодов.В работе использовали стандартную 5-балльную шкалу поражения (по Салунской (1959) [16].
При выполнении лабораторных исследований за основу была принята методика искусственного инфицирования отделенных листовых пластин. Выборку листьев проводили в полевых условиях рендомизировано,с каждого сортообразца отбирали по 30 листьев без признаков поражения.
Материал в лабораторных условиях,отмывали от почвенных частиц и просушивали на стерильной фильтровальной бумаге в течение 3 часов до полного высыхания.
В опытах использовали два способа поддержания жизнеспособности отделенных листовых пластин.
Первый способ – раскладка листьев в лабораторные кюветы на фильтровальную бумагу (рис.3 А). Перед закладкой опыта кюветы и пленку дезинфицировали спиртом,фильтровальную бумагу стерилизовали при температуре 150oС, 2 часа. В кюветы укладывали фильтровальную бумагу, увлажняли её дистиллированной стерильной водой, затем черешок листа обматывали мокрой ватой (для предотвращения потери тургора) и раскладывали в кюветы.
Второй способ – размещение листовых пластин в лабораторных пробирках на гидрогеле (рис. 3 Б). Перед закладкой опыта в пробирки насыпали гидрогель по 0,1 г, затем заливали дистиллированную стерильную воду и оставляли на сутки для набухания. По истечении времени в пробирки с гелем помещали листовые пластины.
Для приготовления суспензии спор C. beticola использовали листья свеклы столовой, сильно пораженные церкоспорозом. Идентификацию гриба проводили в поле зрения светового микро-скопа.Пораженные листья резали на мелкие фрак-ции,помещали в лабораторный стакан с дистиллированной стерильной водой,встряхивали на качалке в течение 1 часа,после чего центрифугированием отделяли надосадочную жидкость, содержащую споры патогена (рис. 4).
Концентрацию спор в суспензии подсчитывали в камере Горяева. Опрыскивание листовых пластин суспензией спор патогена (титр 106 спор/мл) проводили ручным пульверизатором. В контроле листья опрыскивали дистиллированной стерильной водой. Затем листовые пластины в кюветах или пробирках с гидрогелем накрывали полиэтиленовой пленкой для поддержания влажности и ставили на инкубацию в световую комнату, где поддерживалась температура воздуха +25oС.
Полевые и лабораторные учеты проводили в баллах по следующей шкале: 0 до 0,8 – практически устойчивые; 0,9 –1,5 – слабовосприимчивые; 1,6–2,4 – средневосприимчивые; 2,5–3,2 – восприимчивые; 3,3– 4,0 – сильновосприимчивые.
Результаты исследований
Первичную оценку инбредных линий (I 1 -I 6 ) свеклы столовой на поражаемость церкоспорозом проводили в 2018 году (табл. 2).
Как показали проведенные учеты, в 2018 году все образцы свеклы столовой поражались церкоспоро-зом. Распространённость болезни варьировала от 30% (№79 0) до 100% (№708, 713, 714, 715, 7 34). Наиболее восприимчивой к поражению церкоспо-розом оказалась линия 7 08 со средним баллом поражения 2,5 и распространенностью болезни 100%. Ещё у 4-х образцов отмечен балл поражения 1,0-1,5 со 100% распространённостью болезни. Незначительное поражение листовой розетки цер-коспорозом отмечено у номера 790 (табл. 2).
Расчет среднеарифметического значения распространенности болезни по всем изучаемым образцам, показал, что в условиях 2018 года балл поражения церкоспорозом составил 1,1.
Отбор генотипов, устойчивых к церкоспорозу в 2018 году позволил снизить средний балл поражения растений в 2020 году, в среднем по образцам до 0,3. Устойчивым к C. beticola оказался номер 713, у которого не выявлено признаков поражения возбудителем. Единичные пятна церкоспороза на листовой пластинке были отмечены у № 7 39, 79 0, 805 (балл поражения 0,1). Наибольший балл поражения отмечен у линий 7 14 (0,8) и 7 15 1,0), полученные на основе сортопопуляции Креолка.
В 2022 году количество линий в номерах увеличилось и составляло от 2 (№7 34, №805) до 13 шт. (№715).
В результате оценки отмечено,что у линий произошло расщепление на устойчивые и восприимчивые к церкоспорозу формы. Если рассматривать
Таблица 2. Средний балл поражения листовой розетки свеклы столовой во время вегетации растений (2018, 2020, 2022 годы) Table 2. Average score of damage to the leaf rosette of red beets during the plant growing season (2018, 2020, 2022)
Проведенная иммунологическая оценка не выявила невосприимчивых сортообразцов свеклы столовой. Установлено, что при отборе в полевых условиях повышается устойчивость образцов к цер-коспорозу. Средний балл поражения снизился к 2020 году с 1,1 до 0,3. Но потомства линий без признаков поражения в дальнейшем не всегда полностью устойчивы к поражению патогеном. Например, линия 713, которая в 2020 году выделилась как невосприимчивая,расщепилась на невосприимчивую (балл поражения 0)и слабовосприимчивую (балл поражения от 0,5 до 1,0). В связи с этим, для практической селекции необходимо постоянно и строго вести отбор по признаку устойчивости к церкоспорозу.
В лабораторных условиях иммунологическую оценку проводили по линиям из номеров 708, 714, 715, 734. В полевых условиях линии 708-2, 714-1, 734-4 характеризовались как слабовосприимчивые к поражению церкоспорозом с баллом поражения от 0,5 до 0,9, линия 7 15-2 характеризовалась как средневосприимчивая с баллом поражения церкос-порозом 1,7 . В лабораторных условиях первые симптомы поражения были отмечены на 5-е сутки после инфицирования листьев в виде единичных некротических пятен (рис 5а). На 7 -е сутки от момента закладки опыта, было выявлено, что на образце 734-4 некротические пятна покрывали менее 20% поверхности листовой пластины. Балл поражения этого образца составил 1,4, что позволяет считать его слабовосприимчивыми (табл. 3).
У образцов 7 08-2 и 7 14-1 наблюдалось обесцвечивание листьев,некротические пятна покрывали от 21% до 40% листовой пластины. Балл поражения у этих образцов составил 1,6-1,8, что свидетельствует об их средней восприимчивости к пато-гену.В лабораторных условиях наблюдали побурение листовых пластинок у номера 7 15-2 (рис. 5). Балл поражения у этого образца составил 2,8.
При искусственном заражении листовой пластинки балл поражения выше,по сравнению с оцен-
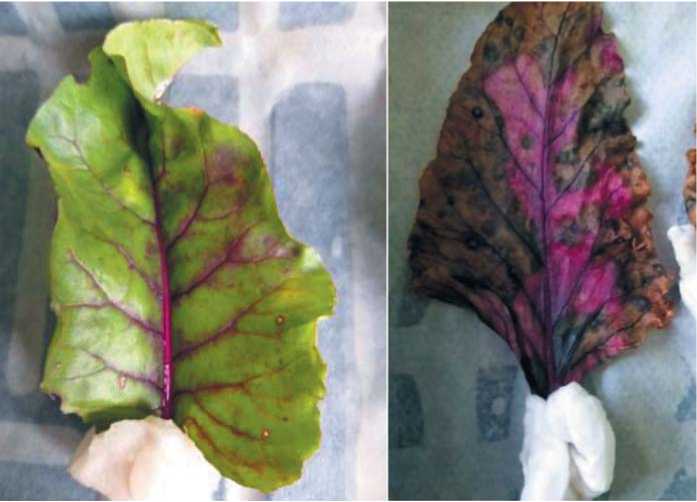
А
Б
Рис. 5. Симптомы церкоспороза на инфицированных листовых пластинках (А – единичные некрозы; Б – сильная степень некротизации)
Fig. 5. Symptoms ofCercospora beticola on infected leafblades (A – single necrosis; B – severe degree ofnecrosis)
Таблица 3. Оценка восприимчивости сортообразцов свеклы столовой к церкоспорозу методом отделенных листьев Table 3. Assessment of the susceptibility of beet varieties to Cercospora beticola using the separated leaf method
|
Наименование образца |
Балл поражения |
Степень восприимчивости |
Симптомы |
|
734-4 |
1,4 |
слабовосприимчивый |
Листья сохраняют зеленую окраску, некротические пятна, мелкие 2-3 мм в диаметре, покрывают менее 20% поверхности листовой пластины. |
|
708-2 |
1,8 |
средневосприимчивый |
Листья приобретают светло-зеленую и желтую окраску, некротические пятна 3-5 мм в диаметре, покрывают от 21% до 40% листовой пластины |
|
714-1 |
1,6 |
средневосприимчивый |
-----------«»-------- |
|
715-2 |
2,8 |
восприимчивый |
Некроз покрывает более 40% поверхности листовой пластинки и придает ей бордово-бурую окраску |
|
кой в полевых условиях. Это связано с тем, что в свеклы столовой на устойчивость к церкоспорозу лабораторных условиях (межсезонный период) Метод инфицирования отделенных листьев свеклы делается принудительное заражение агрессивным столовой суспензией спор Cercospora (с примене штаммом, который поражал свеклу столовую в нием гидрогеля) может быть рекомендован для период вегетации. Заражение в лаборатории про- первичной оценки устойчивости селекционного водилось при контролируемом уровне температуры материала, а также новых сортов и гибридов свек и влажности. На естественном фоне сдерживаю- лы столовой. щим фактором дальнейшего развития болезни могли стать погодные условия, а именно повыше- Выводы ние температуры и снижение влажности воздуха, Определены сортообразцы свеклы столовой с которые позволили снизить порог вредоносности. повышенной устойчивостью и отобран линейный Результаты иммунологической оценки сортообраз- материал для ведения дальнейшей селекции на цов свеклы столовой в лабораторных условиях устойчивость к церкоспорозу. Установлено, что для согласуются с данными полевых испытаний на практической селекции необходимо постоянно и естественном инфекционном фоне. Разработанный строго вести отбор по данному признаку. Для уско метод искусственного заражения отделенных рения селекционного процесса создания сортов и листовых пластин в лабораторных условия позво- гибридов с повышенной устойчивостью к болезни ляет в короткие сроки проводить предварительную предложен лабораторный экспресс метод оценки оценку большого числа исходных сортообразцов устойчивости селекционного материала ISSN 2618-7132 (Online) Овощи России №4 2024 [ 33 ] Vegetable crops of Russia №4 2024 ISSN 2072-9146 (Print) |
|||
Об авторах:
Aboutthe Authors:
Lyubov N. Timakova – Cand. Sci. (Agriculture),
Senior Researcher, SPIN-code:9553-8830, ,
Ksenia L. Alekseeva – Dr. Sci. (Agriculture),
Chief Researcher, SPIN-code: 8212-0261, ,
Lyubov M. Sokolova – Dr. Sci. (Agriculture),
Leading Researcher, , SPIN-code: 2187-0416,
ISSN 2618-7132 (Online) Овощи России №4 2024
[ 34 ] Vegetable crops of Russia №4 2024 ISSN 2072-9146 (Print)
Список литературы Оценка устойчивости инбредных линий свеклы столовой к церкоспорозу (Cercospora beticola sacc.) в полевых и лабораторных условиях
- Ахатов А.К, Ганнибал Ф.Б., Мешков Ю.И., Джалилов Ф.С., Чижов В.Н., Игнатов А.Н., Полищук В.П., Шевченко Т.П., Борисов Б.А., Стройков Ю.М., Белошапкина О.О. Болезни и вредители овощных культур и картофеля. Москва, Товарищество научных изданий КМК, 2013. 463 с. ISBN 978-5-87317-918-3. https://elibrary.ru/ubbgid
- Апасов И.В., Смирнов М.А. Производственно-техническая база свекловодства России. Сахар. 2020;(10):26-31. https://elibrary.ru/boeeql
- Малько А.М. Потребность Российской Федерации в семенах сахарной свеклы - наличие и качество. Сахарная свекла. 2016;(3):17-19. https://elibrary.ru/wzsudb
- Тимакова Л.Н., Борисов В.А., Фильрозе Н.А., Успенская О.Н., Соколова Л.М. Оценка качества сортов свеклы столовой в условиях Московской области. Картофель и овощи. 2020;(7):28-32. https://doi.org/10.25630/PAV.2020.83.92.004 https://elibrary.ru/jytroo
- Pethybridge S.J., Sharma S., Hansen Z., Vaghefi N., Hanson L. Improving fungicide-based management of Cercospora leaf spot in table beet in New York, USA. Canadian Journal of Plant Pathology. 2019;42(3):353-366.
- Sharma S., Heck D.W., Branch E., Kikkert J.R., Sarah J. Cercospora Leaf Spot of Table Beet. Plant Pathology. 2022;(22). https://doi.org/10.1094/PHI-P-2022-02-0101
- Pethybridge S.J., Sharma S., Hansen Z., Kikkert J.R., Olmstead D.L., Hanson L.E. Optimizing Cercospora leaf spot control in table beet using action thresholds and disease forecasting. Plant Disease. 2020;104(6):1831-1840. https://doi.org/10.1094/pdis-02-20-0246-re
- Knight N.L., Koenick L.B., Sharma S., Pethybridge S.J. Detection of Cercospora beticola and Phoma betae on Table Beet Seed using Quantitative PCR. Phytopathology. 2020;110(4):943-951. https://doi.org/10.1094/phyto-11-19-0412-r
- Pethybridge S.J., Vaghefi N., Kikkert J. Management of Cercospora Leaf Spot in Conventional and Organic Table Beet Production. Plant Disease. 2017;101(9):1642-1651. https://doi.org/10.1094/pdis-04-17- 0528-re
- Heck D.W., Kikkert J.R., Hanson L., Pethybridge S.J. Development of a Sequential Sampling Plan using Spatial Attributes of Cercospora Leaf Spot Epidemics of Table Beet in New York. Plant Disease. 2021;(105):2453-2465.
- Pethybridge S.J., Vaghefi N., Kikkert J. Horticultural Characteristics and Susceptibility of Table Beet Cultivars to Cercospora Leaf Spot in New York. HortTechnology. 2017;27(4):530-538.
- Козарь Е.Г., Ветрова С.А., Енгалычева И.А., Федорова М.И. Оценка устойчивости селекционного материала свеклы столовой к церкоспорозу на фоне эпифитотии в условиях защищенного грунта Московской области. Овощи России. 2019;(6):124-132. https://doi.org/10.18619/2072-9146-2019-6-124-132 https://elibrary.ru/xxchhd
- Vaghefi N., Kikkert J.R., Hay F.S., Carver G.D., Koenick L.R., Bolton M.D., Hanson L.E, Secor G.A., Pethybridge S.J. Cryptic diversity, pathogenicity, and evolutionary species boundaries in Cercospora populations associated with Cercospora leaf spot of Beta vulgaris. Fungal Biol. 2018;122(4):264-282. https://doi.org/10.1016/j.funbio.2018.01.008
- Демидова Е.С., Садыкина, Е.И., Сайчук А.И. Методы селекции томата на устойчивость к альтернариозу. Приднестровский НИИСХ, Тирасполь, 2006. 100 с.
- Стогниенко О.И., Мелькумова Е.А., Корниенко А.В. Экспресс метод лабораторного скрининга устойчивости селекционного материала сахарной свеклы к церкоспорозу // Мат-лы Всероссийской научно-практической конференции «Индуцированный иммунитет сельскохозяйственных культур - важное направление в защите растений»- Большие Вяземы, Московской области, 2006. С.113-115.
- Салунская Н.И. Пятнистость листьев, или церкоспороз. Свекловодство. Под. ред. Савченко Е.Н. Киев: ВНИС. 1959. 431 с.


