Оценка влияния блокатора АТ1-рецепторов ангиотензина II валсартана на регресс постинфарктного ремоделирования левого желудочка, нарушение микроциркуляции и инсулинорезистентности у больных ИБС, отягощенной сахарным диабетом 2-го типа
Автор: Нижегородцев М.Ю., Тепляков А.Т., Кузнецова А.В., Лукинов А.В., Горюцкий В.Н.
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: Клинические исследования
Статья в выпуске: 1 т.24, 2009 года.
Бесплатный доступ
Изучались антиишемические, кардиопротективные, гемодинамические и метаболические эффекты, а также влияние на регресс нарушений микроциркуляции инсулинорезистентности блокатора АТ1-рецепторов ангиотензина II валсартана в комбинации с тиазидным диуретиком гидрохлортиазидом во вторичной профилактике хронической сердечной недостаточности у больных с постинфарктным ремоделированием левого желудочка, ишемической дисфункцией сердца, отягощенной СД 2-го типа. В исследование включено 25 пациентов в среднем возрасте 59,2±5,8 лет. В ходе 3-месячной курсовой терапии блокатором АТ1-рецепторов А II валсартаном в индивидуально подобранной дозе 106,0±36,3 мг/сут в комбинации с гидрохлортиазидом в дозе 18,7±6,2 мг/сут отмечена высокая антиишемическая и кардиопротективная эффективность, а также положительное влияние на углеводный обмен и липидный спектр крови. По результатам исследования установлен существенный рост физической толерантности на 42,6%. Дистанция 6-минутной ходьбы возросла на 43,3%. Это сопутствовало регрессу коронарной недостаточности. Качество жизни улучшилось на 13,7%. В ходе исследования произошел регресс массы миокарда ЛЖ на 10,9%, а также улучшение диастолической функции ЛЖ. Показатели микроциркуляторного русла (МЦР) претерпевали положительные изменения, выражающиеся увеличением резервного кровотока на фоне уменьшения влияния атерогенной дислипопротеидемии, а также снижения степени инсулинорезистентности на 41,2%, базальной гипергликемии на 25,3% и постпрандиальной гликемии на 15,6%, косвенно отражающих пропорциональный регресс тканевой инсулинорезистентности.
Ибс, сд 2-го типа, валсартан, постинфарктное ремоделирование, инсулинорезистентность, антиишемические эффекты, микроциркуляция
Короткий адрес: https://sciup.org/14919005
IDR: 14919005 | УДК: 615.217.03:616-005.4-06:616.379-008-64
The assessment of the influence of angiotensin II AT1-receptors blocker valtarsan on regress of left ventricular postinfarction remodelling and insulin resistance in coronary artery disease patients having diabetes mellitus of the 2nd type
Anti-ischemic, cardioprotective, hemodynamic and metabolic affects as well as influence on regress of insulin resistance microcirculation injuries of valtarsan which was used in combination with tiasid diuretics hydrochlortiasid were studied in the secondary prevention of chronic heart failure in patients with left ventricular postinfarction remodeling, ischemic cardiac dysfunction aggravated with the diabetes mellitus of the 2-nd type. The study included 25 patients aged 59,2±5,8 years. Results of 3-months treatment with these drugs revealed their high anti-ischemic and cardioprotective efficacy. The study results showed markedly increased physical tolerance and quality of life of such patients.
Текст научной статьи Оценка влияния блокатора АТ1-рецепторов ангиотензина II валсартана на регресс постинфарктного ремоделирования левого желудочка, нарушение микроциркуляции и инсулинорезистентности у больных ИБС, отягощенной сахарным диабетом 2-го типа
Блокаторы АТ1-рецепторов ангиотензина II (БРА II) относятся к относительно новому классу лекарственных препаратов, обеспечивающих снижение активности ренин-ангиотензин-альдостероно-вой системы (РААС). Они вносят важный вклад в современное лечение сердечно-сосудистой патологии и ассоциированных заболеваний, открывают новые возможности профилактики сердечно-сосудистых осложнений [1, 2, 3]. Несмотря на то, что ингибиторы ангиотензинпревращающего фермента (иАПФ) являются препаратами «первой линии» и своеобразным «стандартом» в лечении дисфункции левого желудочка (ЛЖ), артериальной гипертонии (АГ) и хронической сердечной недостаточности (ХСН), БРА II обеспечивают более полную и более селективную блокаду РААС, не влияя на активность других нейрогуморальных систем, являются метаболически нейтральными, хорошо переносятся пациентами, что делает их более перспективными и привлекательными для лечения больных с ХСН [2, 3, 4].
Согласно современным представлениям, одним из путей снижения летальности больных с ХСН, возникшей в результате ишемического и/или пост-6
инфарктного ремоделирования ЛЖ, является медикаментозная антиишемическая цитокардиопротекция с предотвращением метаболических расстройств. Внедрение в широкую клиническую практику препаратов, способных активизировать гибернированный миокард и тем самым предотвращать ишемическое ремоделирование ЛЖ и МЦР, коронарную и сердечную недостаточность, представляется исключительно важным. Перспективным в этом отношении представляется блокатор АТ1-рецепторов А II валсартан.
В последнее время большое внимание уделяется изучению РААС, точнее ее компонентов, участвующих в патогенезе сахарного диабета (СД) 2-го типа. Согласно современным представлениям, ангиотензин II блокирует основной метаболический эффект инсулина – транспорт глюкозы в клетки, усиливает его пролиферативное и атерогенное действие и способствует инсулинорезистентности [5]. В связи с этим блокада РААС может оказывать профилактическое влияние в отношении нарушений углеводного обмена и инсулинорезистентности. Интерес к БРА II для потенциальной профилактики при СД 2-го типа, а также снижения частоты последствий его развития в настоящее время весьма актуален. Вместе с тем доказательства их клинической эффективности и влияния на предотвращение инсулинорезистентности у больных ИБС с СД 2-го типа еще предстоит получить в хорошо спланированных, рандомизированных, клинически контролируемых исследованиях.
Цель исследования – изучить антиишемические, кардиопротективные, гемодинамические и метаболические эффекты, а также влияние на регресс постинфарктного ремоделирования ЛЖ, коронарной сердечной недостаточности, инсулинорезистентнос-ти и нарушений МЦ блокатора АТ1-рецепторов А II валсартана во вторичной профилактике ХСН у больных с ишемической дисфункцией сердца, ассоциированной с СД 2-го типа.
МАТЕРИАЛ И МЕТОДЫ
Проведено открытое клинически контролируемое исследование клинической эффективности и безопасности терапии валсартаном в комбинации с тиазидным диуретиком гидрохлортиазидом у больных ишемической болезнью сердца с II-III ФК ХСН (по NYHA) в сочетании с СД 2-го типа.
В исследование включено 25 пациентов (13 мужчин, 12 женщин) в среднем возрасте 59,2±5,8 лет. К моменту обследования у 20 (80%) пациентов диагностировалась стабильная стенокардия напряжения II ФК, у 5 (20%) пациентов – III ФК. В среднем стаж ИБС составил 6,4±4,8 года. У всех обследованных регистрировался крупноочаговый ИМ давностью более 6 мес. По данным коронароангиографии выявлялся стенозирующий коронарный атеросклероз. У всех больных ИБС регистрировалась АГ II-III ст. и СД 2-го типа легкой и средней степени тяжести (стаж 10,5±5,6 лет).
В соответствии с протоколом в исследование не включали больных с мозговыми осложнениями АГ давностью менее 12 мес, крупноочаговым ИМ давностью менее 6 мес, тяжелой ХСН (IV ФК по NYHA), с брадиаритмией, нарушениями АВ-проводимости более II степени, сахарным диабетом 2-го типа в стадии декомпенсации, бронхиальной астмой и хроническим бронхообструктивным синдромом, перифе-
Таблица 1
Клинико-демографическая характеристика больных ИБС с СД 2-го типа
|
Показатель |
Количество пациентов |
% отношение |
|
Пол: мужчины/женщины |
13/12 |
52/48 |
|
Средний возраст, годы |
59,2±5,8 |
|
|
Стаж ИБС, годы |
6,4±4,8 |
|
|
Стаж СД 2-го типа, годы |
10,5±5,6 |
|
|
Стенокардия напряжения: II ФК III ФК |
5 20 |
20 80 |
|
ФК ХСН (по NYHA): II ФК III ФК |
20 5 |
80 20 |
|
Перенесенный первичный ИМ, в том числе Q-ИМ |
25 |
100 |
|
Повторный ИМ |
12 |
48 |
|
Постинфарктная аневризма ЛЖ |
2 |
8 |
|
Артериальная гипертензия II-III стадии |
25 |
100 |
|
ЖЭС высоких градаций (по Lown B. и Wolff W.) |
3 |
12 |
|
СД 2-го типа легкой и средней степени тяжести |
25 |
100 |
|
Гиперхолестеринемия > 5,5 ммоль/л |
25 |
100 |
|
Абдоминальное ожирение I-III cт. |
25 |
100 |
|
Курение |
3 |
12 |
|
АКШ+МКШ Стентирование КА |
6 6 |
24 24 |
|
Предшествующая терапия: |
||
|
аспирин пролонгированные нитраты ингибиторы АПФ З—адреноблокаторы антагонисты кальция |
25 20 25 25 5 |
100 80 100 100 20 |
Примечание. ФК – функциональный класс; ХСН – хроническая сердечная недостаточность; ИМ – инфаркт миокарда; КА – коронарные артерии; ФП – фибрилляция предсердий; СД – сахарный диабет; АКШ и МКШ – аорто-и маммарокоронарное шунтирование; АПФ – ангиотензин-превращающий фермент.
рическим атеросклерозом с синдромом Лериша, а также пациентов, имевших противопоказания к назначению блокаторов АТ1-рецепторов А II.
Пациенты, включенные в исследование, дали свое письменное информированное согласие на участие в нем. Клинико-демографическая характеристика пациентов представлена в табл. 1.
Препараты назначались после отмены предшествующего лечения (включавшего З-адреноблокаторы, антиаритмические средства, периферические вазодилататоры, антагонисты кальция, иАПФ) после 5дневного периода «отмывания». Допускался сублингвальный прием короткодействующих форм нитроглицерина и при подъемах АД – прием коринфара в дозе 10 мг.
В ходе исследования все пациенты получали вал-сартан в индивидуально подобранных дозах, методом титрования. Среднесуточная доза валсартана составила 106,0±6,3 мг и гидрохлортиазида 18,7±6,2 мг.
Длительность курсовой терапии составила 3 мес и предусматривала обеспечение удовлетворительной коррекции АГ до целевого уровня – 129,7± 14,3 мм рт. ст. и регресс симптомов ХСН не менее чем на I ФК. В итоге доза валсартана составила 106,0± 6,3 мг/сут, гидрохлортиазида – 18,7±6,2 мг/сут.
Профилактическая терапия оказалась эффективной у 25 (100%) пациентов. Базовая терапия предусматривала назначение сахароснижающих средств (метформин, диабетон), дезагреганты. До назначения валсартана и гидрохлортиазида все пациенты получали холестеринснижающую терапию (статины), которая не менялась в ходе исследования.
Влияние на антиишемические кардиопротектив-ные, гемодинамические и метаболические эффекты, а также на клиническое течение ХСН и безопасность 3-месячной курсовой комбинированной терапии валсартаном с гидрохлортиазидом оценивали по динамике клинических проявлений коронарной недостаточности, регрессу суточной частоты и тяжести стенокардии, суточной потребности в нитроглицерине, увеличению физической толерантности (ТФН), тесту 6-минутной ходьбы. Качество жизни оценивали с помощью Миннесотского опросника «Жизнь с сердечной недостаточностью» (Minnesota Living Heart Failure Questionnaire – MLHFQ). Метаболическую эффективность препарата оценивали по динамике в крови значений липидного спектра, уровня глюкозы натощак и постпрандиальной гликемии, инсулина. Определение индекса инсулинорезистентности (HOMA – IR) проводилось по формуле:
HOMA - IR = ИРИ (мкЕД/мл) х ГПН (моль/л) / 22,5;
где ИРИ –инсулин плазмы натощак, ГПН – глюкоза плазмы натощак [18].
Регистрация АД проводилась с использованием откалиброванного сфигмоманометра с учетом трех усредненных измерений. Определялись значения систолического (САД) и диастолического (ДАД) АД. Посредством ЭхоКГ оценивали параметры, отражающие показатели сократимости и внутрисердечной гемодинамики: фракцию выброса (ФВ) левого желудочка (ЛЖ), конечный систолический и конечный диастолические объемы (КДО, КСО), конечный диастолический размер (КДР), массу миокарда (ММ) ЛЖ, индекс массы миокарда (ИММ) ЛЖ, максимальную скорость раннего пика диастолического наполнения (пик Е, см/с), максимальную скорость трансмитрального кровотока во время систолы левого предсердия (пик А, см/с), отношение максимальных скоростей раннего и позднего наполнения (Е/А), время изоволюмического расслабления ЛЖ (ВИР, мс).
Физическая толерантность оценивалась в исходном контрольном периоде, затем по окончанию 3-месячной курсовой терапии. Велоэргометрия проводилась на эргометре «Siemens-Elema». Использовалась непрерывно ступенчато возраставшая пороговая нагрузка. Пробу начинали с нагрузки 25 Вт, которую увеличивали на 25 Вт каждые 5 минут. Эхокардиографическое исследование выполняли на аппарате «Aloka SSD-5500 SV» (Япония), Ultramark. 9 (ATL, США).
Микроциркуляция исследовалась посредством лазерной допплеровской флуо-метрии (ЛДФ) на аппарате фирмы «Tran-sonic System Inc.» (США). Исследование проводилось в положении сидя с расположением предплечья на уровне сердца. Датчик располагался в области наружной поверхности правого предплечья в точке, находящейся по срединной линии на 3-4 см выше основания шиловидных отростков локтевой и лучевой костей. Температура воздуха в помещении при проведении измерений варьировала в пределах 20-22°С. В исследовании анализировались данные исходной регистрации ЛДФ, показатели окклюзионной пробы. ЛДФ-граммы подвергались компьютерной обработке с вычислением среднего показателя МЦ (ПМ) за 3 мин. В норме у лиц без нарушений МЦ он варьирует в пределах 3,5-6 перф. ед. [3]. При выполнении окклюзионной пробы оценивались показатели максимального постокклюзионного кровотока (МПК), резерва капиллярного кровотока (РКК), прироста капиллярного кровотока (ПКК) и время восстановления (ВВ) показателей до исходных значений.
Статистическая обработка данных осуществлялась с помощью пакета прикладных программ Statistica 6.0 с представлением данных в виде средней величины и ее стандартной ошибки (M±m). Для сравнения показателей до и после курсового лечения использовался непараметричес-8
кий критерий Вилкоксона. Различия считали статистически значимыми при р<0,05.
ПОЛУЧЕННЫЕ РЕЗУЛЬТАТЫ
В результате 3-месячной курсовой комбинированной терапии валсартаном и гидрохлортиазидом частота стенокардии статистически значимо уменьшилась на 84,6% (р<0,001). Потребность в нитроглицерине также статистически значимо (p<0,001) сократилась на 86,4%. При этом физическая толерантность по результатам велоэргометрии существенно (р<0,001) возросла на 42,6% (с 49,2±27,2 Вт до 70,2±29,8 Вт), сопровождаясь улучшением качества жизни на 13,7% (табл. 2).
Показатели системной гемодинамики под влиянием курсовой терапии характеризовались снижением САД на 13% (p<0,0001) от исходного, достигнув 129,7±14,3 мм рт. ст., и среднего уровня ДАД на 14,6% от исходного, достигнув 80±6,1 мм рт. ст. Пульсовое давление на фоне приема валсартана уменьшилось на 11,7%, составив 48,5±2,0 мм рт. ст. Норма-
Таблица 2
Динамика показателей коронарной недостаточности, физической толерантности, качества жизни на фоне 3-месячной терапии валсартаном в дозе 106,0±6,3 мг/сут в комбинации с гидрохлортиазидом в дозе 18,7±6,2 мг/сут (M±m)
|
Показатель |
До лечения (n=25) |
После лечения (n=25) |
∆, % |
р |
|
Частота стенокардии, сут |
2,8±0,3 |
2,3±0,6 |
-84,6 |
0,001 |
|
Потребность в НТГ, таб. сут |
2,6±1,3 |
0,4±0,5 |
-86,6 |
0,00 |
|
Мощность ВЭМ нагрузки, Вт |
49,2±2,7 |
70,2±2,8 |
42,6 |
0,00 |
|
L, м |
270,6±6,7 |
391,9±10,3 |
43,3 |
0,05 |
|
КЖ, баллы |
62,8±14,4 |
50,6±14,2 |
-13,7 |
0,05 |
Примечание. НТГ – табл. нитроглицерина; ВЭМ – велоэргометрический тест; L – тест 6-минутной ходьбы; КЖ – качество жизни.
Таблица 3
Антигипертензивные эффекты 3-месячной терапии валсартаном в дозе 106,0±36,3 мг/сут в комбинации с гидрохлортиазидом в дозе 18,7±6,2 мг/сут (M±m)
|
Показатель |
До лечения (n=25) |
После лечения (n=25) |
∆, % |
Р |
|
САД, мм рт. ст. |
148,9±1,9 |
129,7±1,4 |
-13 |
0,001 |
|
ДАД, мм рт. ст. |
92,7±7,4 |
80,0±6,1 |
-14,6 |
0,00 |
|
ЧСС, уд. в мин |
81,3±6,0 |
69,5±9,7 |
-11,4 |
0,003 |
|
Пульсовое АД, мм рт. ст. |
54,9±2,3 |
48,5±2,0 |
-11,7 |
0,05 |
Примечание. САД – систолическое артериальное давление, ДАД – диастолическое артериальное давление, ЧСС – частота сердечных сокращений.
Таблица 4
Динамика показателей внутрисердечной гемодинамики на фоне 3-месячной терапии валсартаном в дозе 106,0±36,3 мг/сут в комбинации с гидрохлортиазидом в дозе 18,7±6,2 мг/сут (M±m)
|
Показатель |
Исход (n=25) |
Курс (n=25) |
А,1 (%) |
Валсартан |
А,2 (%) |
|
|
Исход (n=25) |
Курс (n=25) |
|||||
|
ЛП, мм |
42,3±6,1 |
43,7±5,2 |
3,5 |
44,2±4,7 |
43,1±4,5 |
-0,4 |
|
КДО, мл |
123,2±22,7 |
120,8±21,7 |
-1,9 |
155,2±28,0 |
142,0±28,9* |
4,4 |
|
КДР, мм |
50,7±3,8 |
50,5±4,1 |
-0,5 |
57,9±13,4 |
53,1±4,0 |
-8,1 |
|
КСО, мл |
47,2±13,1 |
44,2±14,6* |
-6,5 |
91,3,2±37,7 |
68,0±12,5* |
-11,2 |
|
ФВ,% |
63,8±4,7 |
64,2±5,5 |
0,7 |
53,0±8,7 |
57,5±6,7* |
3,0 |
|
ЗС ЛЖ, мм |
11,1±1,8 |
10,7±1,2* |
-3,6 |
10,8±0,6 |
10,6±0,9 |
-0,7 |
|
ММЛЖ, г |
273,2±68,3 |
264,9±55,0 |
-3,02 |
254,4±61,5 |
224,7±36,2* |
-11,6 |
|
ИММЛЖ г/м2 |
134,9±25,3 |
131,8±22,2* |
-2,3 |
135,8±24,4 |
114,8±19,7** |
-10,9 |
|
Е/А |
1,05±0,25 |
0,96±0,23 |
-8,7 |
1,05±0,06 |
0,95±0,05 |
-8,1 |
|
ВИР, с |
115,8±15,3 |
104,4±11,0 |
-9,8 |
123,3±16,4 |
109,9±21,9** |
-9,1 |
|
СИ, л/м 2 |
2,6±0,3 |
2,8±0,1* |
7,1 |
2,5±0,1 |
2,8±0,1* |
7,4 |
Примечание. ЛП – левое предсердие; КСО – конечный систолический объем; КДО – конечный диастолический объем; КДР – конечный диастолический размер; ФВ – фракция выброса; ЗСЛЖ – задняя стенка левого желудочка; ММЛЖ – масса миокарда левого желудочка; ИММЛЖ – индекс массы миокарда ЛЖ; Е/А – отношение быстрого наполнения левого желудочка к ускорению трансмитрального кровотока вследствие сокращения левого предсердия; ВИР – время изоволюмического расслабления; СИ – сердечный индекс; * – р<0,05; ** – р<0,001 (различия с исходными данными статистически значимы).
лизации гемодинамики сопутствовало увеличение в 2 раза числа пациентов с уровнем ДАД<90 мм рт. ст. (табл. 3). Следовательно, использованная комбинация препаратов оказалась эффективной, обеспечивая у 75% пациентов целевой уровень ДАД.
Регистрировались показатели внутрисердечной гемодинамики исходно и на фоне курсовой терапии (табл. 4). Группу сравнения составили пациенты с
ИБС в ассоциации с СД 2-го типа, не получавшие БРА II.
Так, по данным исследования имели место определенные признаки ремоделирования ЛЖ, которые проявились значимым снижением ИММ ЛЖ (р<0,00), ММ ЛЖ (р<0,01). Уменьшились показатели КСО и КДО (р<0,01). Значимо уменьшилось ВИР (р<0,00). ФВ увеличилась на 3% (р<0,03).
Таблица 5
Динамика показателей липидного и углеводного обмена на фоне 3-месячной терапии валсартаном в дозе 106,0±36,3 мг/сут в комбинации с гидрохлортиазидом в дозе 18,7±6,2 мг/сут (M±m)
|
Показатель |
Исход (n=25) |
Курс (n=25) |
А,1% |
Валсартан |
А,2% |
|
|
Исход (n=25) |
Курс (n=25) |
|||||
|
ОХС, ммоль/л |
6,027±1,32 |
5,24±0,82* |
-13,1 |
6,3±0,8 |
5,6±1,2* |
-10,7 |
|
ТГ, ммоль/л |
1,9±0,75 |
1,7±0,34 |
-12,2 |
2,7±1,2 |
2,5±1,4 |
-7,1 |
|
ЛПНП, ммоль/л |
4,05±1,06 |
3,5±0,69* |
-13,4 |
3,7±0,7 |
2,9±0,8* |
-12,9 |
|
ЛПВП, ммоль/л |
1,08±0,26 |
1,04±0,09 |
-3,8 |
0,9±0,2 |
1,1±0,4* |
1,6 |
|
ИА, у.е. |
3,85±1,14 |
3,4±0,91 |
-11,1 |
4,0±1,6 |
3,1±1,2** |
-14,1 |
|
Глюкоза натощак, ммоль/л |
7,78±2,4 |
6,6±1,26* |
-15,3 |
9,2±2,2 |
6,8±1,8** |
-15,3 |
|
Постпрандиальная гликемия, ммоль/л |
8,06±0,37 |
5,7±2,5 |
-28,9 |
11,1±2,3 |
9,4±2,1** |
-15,6 |
|
Инсулин, мкЕД/мл |
26,9±2,6 |
19,7±1,8** |
-26,9 |
|||
|
HOMA-IR, у.е. |
10,2±0,7 |
6,0±5,7** |
-41,2 |
|||
Примечание. ОХС – общий холестерин; ТГ – триглицериды; ЛПНП – липопротеиды низкой плотности; ЛПВП – липопротеиды высокой плотности; ИА – индекс атерогенности; HOMA-IR – индекс инсулинорезистентности; * – р<0,05; ** – р<0,001 (различия с исходными данными статистически значимы).
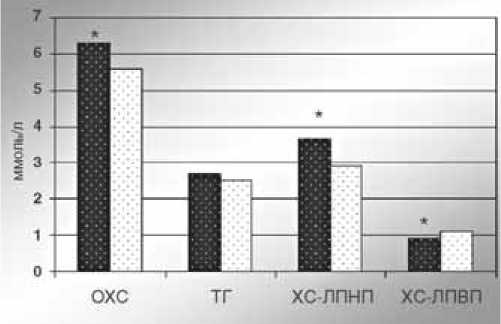
Рис. 1. Динамика показателей липидного спектра после курсовой терапии валсартаном с гидрохлортиазидом, * – р<0,001
Действительно, на фоне терапии валсартаном уровень ОХС уменьшился (р<0,02) на 10,7%, составив 5,6±1,2 ммоль/л, уровень атерогенного холестерина ЛПНП уменьшился на 12,9%, составив 2,9± 0,8 ммоль/л, ТГ – на 7,1%, уровень антиатерогенного ЛПВП возрос на 1,6% (табл. 5, рис. 1).
Исходно повышенный базальный уровень гликемии уменьшился (р<0,000) на 15,3%, составив 6,8± 1,8 ммоль/л (табл. 5, рис. 2). Этому сопутствовало статистически значимое снижение постпрандиаль-ной гликемии с 11,1±2,3 ммоль/л до 9,4±2,1 ммоль/л (р<0,000). Наряду с этим снизился показатель свободного инсулина плазмы на 26,9% (р<0,001).
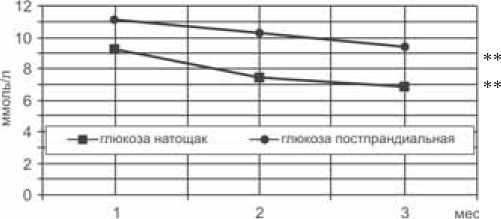
Рис. 2. Динамика показателей глюкозы на фоне курсовой терапии валсартаном с гидрохлортиазидом, ** – р<0,001
Оценка состояния МЦ показала: в исходном состоянии у больных СД 2-го типа диагностированы гетерогенные изменения микроциркуляции с преобладанием патологических гемодинамических типов микроциркуляции (ГТМ): гиперемический ГТМ – у 18,5% и спастический – у 81,5%, обусловленных структурно-функциональными изменениями микро-циркуляторного сосудистого русла. К окончанию курсовой комбинированной терапии валсартаном и гидрохлортиазидом регистрировался прирост показателей МЦ. Отмечалось статистически значимое (р<0,001) увеличение на 16,7% значений максимального постокклюзионного кровотока (МПК) с 7,5±3,4 до 8,7±3,2 перф. ед. При этом прирост (р<0,004) капиллярного кровотока (ПКК) составил 13,4% (с 4,8±3,4 до 5,5±3,1 перф. ед.). Время восстановления тканевой перфузии до исходного уровня уменьшилось на 16,2% (табл. 6). Эти изменения были обусловлены улучшением сосудистой реактивности на фоне проводимой терапии за счет снижения влияния симпатической нервной системы, а также уменьшения тканевой активности РААС у данной категории больных.
ОБСУЖДЕНИЕ
Активация РААС считается одним из основных факторов в патогенезе коронарной и сердечной недостаточности, ответственным за ремоделирование сердца у больных ИБС. Как известно, ангиотензин II играет важную роль в инициации и развитии миокардиофиброза, ишемического ремоделирования сердца и сосудов, левожелудочковой сердечной недостаточности. Имеющийся сравнительно небольшой опыт клинического применения блокаторов АТ1-рецепторов А II определил новые перспективы кардиопротективной терапии у больных ХСН. Вместе с тем вопрос об эффективности этого нового класса препаратов в сравнении с иАПФ остается открытым. Долгое время дискутировался вопрос о применении БРА II при ХСН. Так, в первом крупномасштабном исследовании ELITE II сравнивалась эффективность
Таблица 6
Динамика основных показателей микроциркуляции на фоне 3-месячной терапии валсартаном в дозе 106,0±36,3 мг/сут в комбинации с гидрохлортиазидом в дозе 18,7±6,2 мг/сут (M±m)
|
Показатели |
Здоровые лица (n=25) |
До лечения (n=25) |
После лечения (n=25) |
∆, % |
Р |
|
ПМ, перф. ед. |
3,8±0,3 |
2,1±0,6 |
2,8±0,6 |
34,5 |
0,00 |
|
Окклюзионная проба |
|||||
|
МПК, перф. ед. |
10,1±2,8 |
7,5±3,4 |
8,7±3,2 |
16,7 |
0,00 |
|
РКК, % |
354,8±88,7 |
271±48,6 |
325,3±98,5 |
16,4 |
0,01 |
|
ПКК, перф.ед. |
8,6±1,8 |
4,8±3,4 |
5,5±3,1 |
13,4 |
0,004 |
|
ВВ, с |
96,4±23,2 |
128,2±28,9 |
108,8±27,7 |
-16,2 |
0,001 |
Примечание. ПМ – показатель микроциркуляции; МПК – максимальный постокклюзионный кровоток; РКК – резерв капиллярного кровотока; ПКК – прирост капиллярного кровотока; ВВ – время восстановления.
БРА II лозартана и иАПФ каптоприла у больных ХСН, по результатам которого применение лозарта-на при ХСН представилась вполне перспективным и оправданным [6-11].
В другом крупном исследовании под названием Val-HeFT, в которое были включены 5010 больных с застойной сердечной недостаточностью, изучали возможность улучшения эффективности терапии ХСН. Так, на фоне курсовой терапии валсартаном в средней дозе 254 мг/сут было установлено статистически значимое увеличение ФВ ЛЖ, а также регресс симптомов ХСН. Кроме этого в исследовании CHARM на фоне терапии кандесартаном продолжается изучение возможности улучшения диастолической функции миокарда [7].
Опыт применения БРА II в клинической практике России весьма ограничен. В то же время БРА II в мировой кардиологической практике является наиболее динамично развивающимся классом препаратов. Упомянутые результаты клинических исследований представляют большую ценность этого класса препаратов, обладающих не только антигипертензивными, но и доказанными органопротективными свойствами.
Результаты настоящего исследования подтверждают высокую антиишемическую и антигипертензивную эффективность комбинированной терапии блокатора АТ1-рецепторов А II валсартана в дозе 106,0± 6,3 мг/сут в комбинации с гидрохлортиазидом 18,7± 6,2 мг/сут в процессе 3-месячной курсовой терапии у больных ИБС, отягощенной СД 2-го типа. Целевой уровень АД достигался у 85% пациентов на фоне такой терапии. Хороший антигипертензивный эффект валсартана с сопоставимой динамикой САД и ДАД (р<0,01-0,01) сопровождался регрессом коронарной недостаточности на 84,6%, повышением физической толерантности на 42,6% и улучшения качества жизни на 13,7% [8-13].
В ходе исследования установлены данные, свидетельствующие о явном регрессе гипертрофии ЛЖ даже на фоне сравнительно непродолжительной 3-месячной комбинированной терапии валсартаном с гидрохлортиазидом. Причем уменьшение ММЛЖ, ИММЛЖ, а также улучшение диастолической функции ЛЖ (по ВИР) и регресс дисфункции эндотелия произошли на фоне уменьшения влияния атерогенной дислипидемии (в частности снижения уровня атерогенного ХС ЛПНП с параллельным возрастанием антиатерогенного ХС ЛПВП), а также снижения уровня базальной гипергликемии на 15,3% и постпрандиальной гликемии – на 15,6%, косвенно отражающих пропорциональный регресс тканевой инсулинорезистентности. Статистически значимое снижение показателя инсулинорезистентности на 41,2%, свободного инсулина плазмы на 26,9%, по всей вероятности, свидетельствовало о снижении активности компонентов РАС, тем самым улучшался тканевой обмен, следовательно, уменьшалась ИР в периферических тканях. Это вселяет надежду предотвратить риск развития метаболических нарушений у больных АГ, а также осуществить своевременную профилактику нависшей эпидемии СД. В новом исследовании NAVIGATOR впервые в качестве первостепенной ставится задача оценить эффективность валсартана в профилактике СД 2-го типа у больных в состоянии преддиабета, то есть нарушенной толерантности к глюкозе. В исследовании VALUE, длившемся 4 года и включавшем более 15 000 больных артериальной гипертензией, применение валсартана в дозе 80-160 мг/сут привело к статистически значимому снижению риска развития СД 2-го типа в среднем на 23% по сравнению с применением амлодипина в дозе 5-10 мг/сут. Это еще раз доказывает особую важность и эффективность применения БАР II у больных с СД [12-21].
Согласно современным представлениям, блокада АТ1-рецепторов А II, уменьшая вазоконстрикцию, создает предпосылки и возможность стимуляции тканевых АТ2-рецепторов А II, сопровождающейся мощным вазодилататорным эффектом, подавлением тканевой пролиферации за счет повышения синтеза NO (оксида азота), брадикинина и простагландина Е2 [18].
Таким образом, комбинированная терапия вал-сартаном в комбинации с тиазидовым диуретиком гидрохлортиазидом в индивидуально подобранных дозах у больных ИБС в ассоциации с СД 2-го типа эффективно предупреждает прогрессирование нарушений микрогемоциркуляции, обеспечивает регресс процессов патологического ишемического ремоделирования терминального звена кровообращения у больных с постинфарктной дисфункцией ЛЖ, клиническими проявлениями умеренной ХСН. Результаты настоящего исследования показали также, что валсартан обладает дополнительными метаболическими эффектами, проявляющимися улучшением углеводного и липидного обмена, снижением ИР.
Список литературы Оценка влияния блокатора АТ1-рецепторов ангиотензина II валсартана на регресс постинфарктного ремоделирования левого желудочка, нарушение микроциркуляции и инсулинорезистентности у больных ИБС, отягощенной сахарным диабетом 2-го типа
- Мареев В.Ю. Лечение сердечной недостаточности на рубеже веков. Становятся ли положения доказательной медицины доказательными для практикующих врачей. Кардиология 2000; 12: 4-11.
- Преображенский Д.В., Сидоренко Б.А. Успехи и неуда чи разработки новых подходов к медикаментозной терапии ХСН (обзор результатов рандомизированных исследований, выполненных в 90-е годы). Часть II. Кардиология 2000; 4: 67-76.
- Маколкин В.И., Подзолков В.И., Павлов В.И. и др. Состояние микроциркуляции при гипертонической болезни. Кардиология 2002; 7: 36-40.
- Маколкин В.И., Подзолков Т.В., Ренскова Т.В. Оценка влияния периндоприла на величину АД, ремоделирование сосудов и микроциркуляцию при гипертонической болезни. Кардиология 2001; 6: 17.
- Carlsson P.O., Berne C., Jansson L. Angiotensin II and the endocrine pancreas: effects on islet blood flow and insulin secretion in rats. Diabetologia 1998; 41: 127-33.
- Folli F., Saad M.A., Velloso L. et al. Crosstalk between insulin and angiotensin II signaling systems. Exp Clin Endocrinol Diabetes 1999; 107: 133-9. Konstam MA. Val-HeFT and angiotensin-receptor blockers in perspective: A tale of the blind man and the elephant. J Card Fail 2002;8:56-58.
- Yusuf S., Pfeffer M.A., Swedberg K., et al. Effects of candesartan in patients with chronic heart failure and preserved left-ventricular ejection fraction: the CHARM-Preserved Trial. Lancet 2003;362:777-81.
- Тигай Ж.Г., Котовская Ю.В., Лобжанидзе Т.В., Кобалава Ж.Д. Влияние антагониста АТ1-рецепторов ангиотензина II эпросартана на состояние микроциркуляторного русла и показатели углеводного обмена у больных артериальной гипертензией с метаболическим синдромом. Кардиология СНГ 2006; т. 4: 17-26.
- Тепляков А.Т., Гарганеева А.А. Расстройства микроциркуляции при ишемической болезни сердца. Изд-во Томского ун-та 2001. -339 с.
- Оганов Р.Г., Небиеридзе А.В. Метаболические эффекты блокаторов рецепторов ангиотензина II. Кардиология 2002; 4: 35-39.
- Сидоренко Б.А., Иосава И.К., Киктев В.Г., Преображенский Д.В. Блокаторы АТ1-ангиотензиновых рецепторов как новая группа антигипертензивных препаратов//Клиническая фармакология и терапия. 1999. -Т. 8. -№ 6. -С. 38-45.
- Timmermans РВ, Smith RD. Angiotensinll receptor subtypes: selective antagonists and functional correlates. EurHear J 1994; 15 (suppl.D):79-87.
- Lucius R., Galliant S., Busche S. Et al. Beyond blood pressure: new roles for angiotensin II. Cell Mol Life Sci vol. 56, 1999, Р. 1008-1019.
- Unger T. Blood pressure lowering and rennin angiotensin system blockade. J.Hypertens, Vol.21, suppl. 6, 2003, Р. S3-7.
- Ивлева А.Я. Клиническое применение ингибиторов ангиотензинпревращающего фермента и антагонистов ангиотензина II Изд. «Миклош», М., 1998.
- Willenheimeir R., Dahluf B., Rydberg E. et al. AT1-receptor blockers in hypertension and heart failure: clinical experience and future directions. Eur., Heart J., 1999; 20: 997-1008.
- Кannel W. Epidemiological implications of left ventricular hypertrophy. Left ventricular hypertrophy and its regression. Eds. By J.M.Cruickshank, F.H.Messerli. London: Science Press, 1992; 1-13.
- Арутюнов Г.П. Перспективы применения антагонистов ангиотензина II//Consilium Medicum. -3. -Т. 2. -2000. -С. 9-12.
- Беленков Ю.Н., Мареев В.Ю. Тройная комбинация не имеет преимуществ перед beta-адреноблокатором бисопрололом в сочетании с блокатором рецепторов ангиотензинa II валсартаном во влиянии на параметры ремоделирования левого желудочка у больных с умеренной хронической сердечной недостаточностью//Consilium Medicum -1. -Т. 13. -2006. -С. 24-26.
- Yoriuchi M., Akishita M., Dzau V. Recent progress in angiotensin II type 2 receptor research in cardiovascular system. Hypertension 1999; 33: 613-621.
- Julius S, Kjeldsen SE, Weber M. The Value trial group. Outcomes in hypertensive patients at high cardiovascular risk treated with regimens based on valsartan or amlodipine: the VAL UE randomized trial. Lancet 2004; 363: 2022-31.


