Оценка защиты миокарда методом лазерно-индуцированной флуоресценции на этапах коррекции врожденных пороков сердца у детей первого года жизни при применении раствора "Custodiol"
Автор: Углова Елена Владимировна, Ларионов Петр Михайлович, Ломиворотов Владимир Николаевич, Горбатых Юрий Николаевич, Синельников Юрий Семенович, Афанасьев Иван Сергеевич, Мандрик Мария Михайловна
Журнал: Патология кровообращения и кардиохирургия @journal-meshalkin
Рубрика: Анестезиология, реаниматология и перфузиология
Статья в выпуске: 1 т.13, 2009 года.
Бесплатный доступ
Впервые в кардиохирургии проведена оценка защиты сердца методом лазерно-индуцированной флуоресценции. Изучены также процессы интраоперационного повреждения ДНК кардиоцитов на аноксическом и реперфузионном этапах при наблюдении за 12 детьми раннего возраста с врожденными пороками сердца (ВПС), оперированных в условиях искусственного кровообращения, миокард которых был защищен раствором «Кустодиол».
Защита миокарда, метод лазерно-индуцированной флуоресценции, повреждения днк, коррекция врожденных пороков сердца, дети первого года жизни
Короткий адрес: https://sciup.org/142233491
IDR: 142233491 | УДК: 616.12-007.1-053.3-089:616.127-076
Evaluation of myiocardium protection by using laser-induced fluorescence when repairing chd in infants and applying "Custodiol" solution
Carried out for the first time in cardiac surgery is the evaluation of cardiac protection by using a laser-induced fluorescence method. The processes of intraoperative damage of cardiocyte DNA at anoxic and reperfusion stages are also studied while observing 12 infants with congenital heart diseases (CHD) operated under extracorporeal circulation, with their myocardium protected by «Custodiol» solution.
Текст научной статьи Оценка защиты миокарда методом лазерно-индуцированной флуоресценции на этапах коррекции врожденных пороков сердца у детей первого года жизни при применении раствора "Custodiol"
Изучение вопросов адекватности защиты миокарда у детей первого года жизни с использованием современных лабораторных методов крайне актуально и способствует профилактике послеоперационных осложнений. C целью оценки эффективности кардиопротекции до настоящего времени использовался анализ ультраструктуры кардиомиоцитов методом электронной микроскопии при операциях АКШ [4, 6], а также при коррекции ВПС [5, 8]. Проблема оценки состояния миокарда с использованием расширенного арсенала методик и введением новых морфологических характеристик по-прежнему актуальна [2, 3]. Апоптоз клеток миокарда при экспериментальном стенозе коронарных артерий регистрировался иммуногистохимическими методами [10, 11]. В нашем институте метод лазерно-индуцированной флуоресценции использовался в экспериментальных моделях для оценки жизнеспособности миокарда изолированного сердца как критерий подготовленности к трансплантации [7]. Для визуализации ДНК использовался этидиум бромид. Установлено, что снижение интенсивности флуоресценции скорее всего связано с потерей ядерного материала, так как динамика этого показателя носила однонаправленный характер по мере нарастания гипоксии [7]. Повреждение ДНК кар-диоцитов происходит и в результате действия эндонуклеаз, которые активируются при повышении концентрации внутриклеточного Ca2+, наблюдаемом в ходе окислительного стресса [7]. Активные формы кислорода (АФК) вызывают повреждения ДНК - происходят разрывы цепей, повреждения хромосом [1]. В экспериментальных моделях хронической ишемии миокарда при оценке структуры кардиоцитов методом лазерно-индуцированной флуоресценции наблюдалась фрагментация ДНК, что авторами ассоции ровалось с апоптозом [9,12] и не расценивалось как гибель кардиоцитов [12]. Участки фрагментированного ДНК, по видимому, далее подвергаются фагоцитозу [12]. В доступных нам информационных источниках работ по вопросам оценки адекватности защиты миокарда на этапах коррекции ВПС методом лазерно-индуцированной флуоресценции с анализом степени интраоперационного повреждения ДНК на аноксическом и реперфузионном этапах нами не найдено.
МАТЕРИАЛ И МЕТОДЫ
Обследовано 12 пациентов с ВПС (ДМЖП+ЛГ - 5, АВК - 4, ТФ - 2, ДОМС от ПЖ - 1). Средний возраст -11±0,7 месяцев. Исследования проводились на следующих этапах: до окклюзии аорты (Ао) - первый, во время пережатия Ао - второй, 20-30-я минута реперфузии - третий. Для защиты миокарда использовался раствор «Custodiol», средняя продолжительность окклюзии Ао - 60,0±3,8 мин; искусственного кровообращения (ИК) - 112,1±5,4 мин. Трое пациентов имели летальный исход.
Забор биопсии из ушка правого предсердия производили на следующих этапах операции: 1) непосредственно перед пережатием Ао, 2) после открытия Ао, 3) на 20-30-й минуте реперфузии. Изготавливали криостатные срезы и фиксировали этидиумом бромидом.
Оценка результатов проводилась на люминесцентном компьютеризированном микроскопе с определением интенсивности флуоресценции и с последующим вычислением процентного соотношения фрагментированного ДНК в ядре и в цитоплазме кардиоцитов. Для точности измерения в биоптате выделяли от трех до пяти зон, включающих в общей сложности до 400 кардиоцитов. Мы наблюдали различную интенсив- ность флуоресценции в биоптатах различных пациентов и четкую однонаправленность динамики показателя относительно исследуемых этапов у каждого в отдельности. Учитывая возможность ошибки, которая возникает при покраске и хранении материала, мы нормировали оценку, применив показатель процентного соотношения содержания фрагментированной ДНК в ядре и цитоплазме кардиоцитов.
Статистическую обработку данных проводили с помощью пакета статистических программ Statistica 6.0. В качестве достоверных считали результаты при достижении уровня значимости р<0,05, для характеристики тенденции указывали уровень p<0,1. Методы статистики: непараметрический коэффициент корреляции Спирмана (rho), достоверность различия средних значений между двумя группами оценивали непараметрическим критериями Манна-Уитни, Уилкоксона. Если число сравниваемых групп превышало две, использовали непараметрический тест Краскелла-Уоллиса, для сравнения средних значений использовался критерий Стьюдента.
РЕЗУЛЬТАТЫ
Абсолютные показатели интенсивности флуоресценции кардиоцитов на 1,2 и 3 этапах коррекции ВПС представлены в табл. 1. Мы наблюдали наличие флуоресценции как в ядре, так и в цитоплазме кардиоцитов. При анализе динамики процентного соотношения интенсивности флуоресценции в цитоплазме кардиоцитов относительно ядра между 1 и 2, а также между 1 и 3 этапами операции достоверных различий не найдено (табл. 2). Корреляционной зависимости исследуемого показателя с длительностью окклюзии Ао не обнаружено (корреляционный анализ по Спирману). Вид сохранного миокарда при оценке структуры ДНК методом лазерно-индуцированной флуоресценции на 2 и 3 этапе операции представлен на рис. 1. Вид миокарда при частичном повреждении ДНК на этапе аноксии и реперфузии представлен на рис. 2.
У одного пациента с неблагоприятным исходом зарегистрировано соотношение показателя ядро-цитоплазма, приближающееся к 1:1 на 2 и 3 этапах операции (рис. 3).
Таблица 1
Средние значения интенсивности флюоресценции фрагментов ДНК в ядре и цитоплазме кардиоцитов на этапах коррекции ВПС при защите миокарда раствором «Custodiol»
|
Этап |
N |
Среднее значение |
Min |
Max |
Стандартное отклонение |
Ошибка среднего |
|
|
АО |
34 |
60,47 |
25,00 |
87,00 |
22,06 |
3,78 |
|
|
ИК |
34 |
112,09 |
53,00 |
157,00 |
31,36 |
5,38 |
|
|
1 |
ядро |
18 |
121,94 |
41,00 |
277,00 |
83,36 |
19,65 |
|
цитоплазма |
18 |
68,39 |
27,00 |
156,00 |
43,30 |
10,21 |
|
|
2 |
ядро |
23 |
168,65 |
49,00 |
307,00 |
93,83 |
19,56 |
|
цитоплазма |
23 |
104,26 |
26,00 |
215,00 |
63,96 |
13,34 |
|
|
3 |
ядро |
13 |
98,69 |
37,00 |
285,00 |
73,06 |
20,26 |
|
цитоплазма |
13 |
58,46 |
23,00 |
194,00 |
49,24 |
13,66 |
|
Таблица 2
Показатели процентного и относительного содержания фрагментированной ДНК в цитоплазме кардиоцитов относительно клеточного ядра на этапах коррекции ВПС при защите миокарда раствором «Custodiol»
|
Этап |
N |
Среднее |
Медиана |
Min |
Max |
Стандартное отклонение |
Ошибка среднего |
|
Ядро/цитоплазма 1 |
18 |
0,62 |
0,57 |
0,22 |
1,00 |
0,21 |
0,05 |
|
% |
18 |
62,04 |
56,82 |
22,13 |
100,00 |
21,32 |
5,02 |
|
Ядро/цитоплазма |
23 |
0,61 |
0,61 |
0,41 |
0,82 |
0,11 |
0,02 |
|
2 % |
23 |
61,14 |
60,51 |
40,74 |
82,00 |
10,73 |
2,24 |
|
Ядро/цитоплазма |
13 |
0,57 |
0,56 |
0,44 |
0,72 |
0,09 |
0,03 |
|
% |
13 |
57,20 |
55,56 |
43,86 |
72,31 |
9,35 |
2,59 |
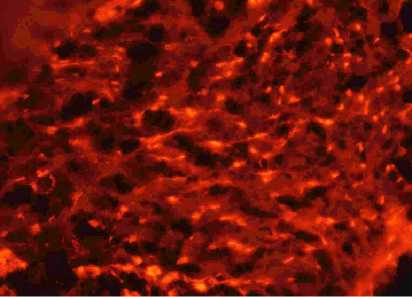
Рис. 1. Сохранный миокард.

Рис. 2. Миокард поврежден частично.
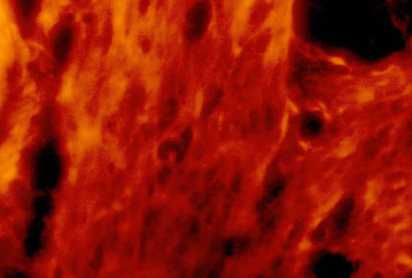
Рис. 3. Поврежденный миокард.
Клинический анализ течения ближайшего послеоперационного периода показал следующие особенности:
-
1. Тип восстановления сердечной деятельности - трое пациентов из 12 через атриовентрикулярный (A-V блок), двое - через дефибрилляцию с восстановлением синусового ритма.
-
2. Нарушения ритма - блокада правой ножки пучка Гиса - 5, транзиторный A-V блок - 1, полный A-V блок с асистолией желудочков (проводилась постоянная электрокардиостимуляция) -1.
-
3. Ухудшение метаболизма миокарда в ближайший послеоперационный период не зарегистрировано.
-
4. Инотропная поддержка у пациентов с благоприятным исходом - средние дозы двух кардиотоников до двух суток.
-
5. Нарушения сократимости миокарда не зарегистрировано.
-
6. Причины летальности: сердечная недостаточ-ность+ легочная гипертензия (ЛГ) III стадии -2, полная A-V блокада с асистолией желудочков - 1.
ОБСУЖДЕНИЕ
Исследования по разработке интраоперационных критериев адекватности защиты миокарда при коррекции ВПС у детей первого года жизни, а также по вопросам метаболизма незрелого миокарда, перенесшего состояние аноксии и реперфузии, обсуждаются в отечественных и зарубежных работах [5, 8]. В цитируемых источниках оценка ультраструктурных изменений при кардиопротекции проводилась по митохондриальному индексу и содержанию гликогена в кардиоцитах. Нами впервые использован метод лазерно-индуцированной флуоресценции для определения степени дефрагментации ДНК при защите миокарда раствором «Custodiol». Нами использован показатель процентного содержания фрагментированной ДНК в цитоплазме кардиоцитов относительно ядра. При использовании нами метода лазерно-индуцированной флуоресценции установлено, что при применении раствора «Custodiol» нет статистических различий в исследуемых показателях на этапах аноксии и реперфузии, что указывает на эффективность защиты миокарда. Это согласуется с данными исследования из НЦ ССХ РАМН им. А.Н. Бакулева, где констатировано отсутствие достоверных изменений показателей митохондриального индекса и запасов гликогена в период аноксии и реперфузии при кардиопротекции раствором «Custodiol» у детей первого года жизни [8]. В то же время обнаруженное нами наличие фрагментированной ДНК в цитоплазме клетки отражает повреждение ядерных мембран кардиоцитов и косвенно указывает на активизацию процессов свободно радикального окисления.
Немаловажен и факт, что в группу «Custodiol» вошли пациенты со сложными пороками, в том числе и с цианотическими, что требовало длительных сроков выключения сердца из кровообращения: окклюзия Ао 60±3,8 мин; ИК 112,1±5,4 мин. Клинические характеристики адекватности защиты миокарда у всех пациентов показали отсутствие ишемических изменений и локальных нарушений сократимости сердечной мышцы. Транзиторные нарушения A-V проводимости были кратковременны и гемодинамически незначимы. Экспериментальными работами нашего института методом лазерно-индуцированной флуоресценции доказано снижение устойчивости проводящих структур сердца к ишемии по сравнению с рабочими кардиомиоцитами [7]. У одного летального пациента на этапе аноксии и реперфузии зарегистрировано соотношение показателя, приближающееся 1:1 с одновременным снижением интенсивности флуоресценции, что ставит под сомнение адекватность кардиопротекции, в то же время клинику сердечной недостаточности необходимо соотносить со стадией порока (ЛГ) III ст. и кризовым течением послеоперационного периода.
ВЫВОДЫ
-
1. Метод лазерно-индуцированной флуоресценции с оценкой степени повреждения ДНК карди-оцитов может быть использован в клинической практике как критерий адекватности кардиопротекции и вносит перспективы в дальнейшее изучение ультраструктурных сдвигов кардиоцитов с комплексным морфологическим анализом.
-
2. При защите миокарда раствором «Custodiol» на этапах коррекции ВПС у детей первого года жизни определяется дефрагментация ДНК кардиоцитов с выходом фрагментов ДНК в цитоплазму.
-
3. При защите миокарда раствором «Custodiol» не зарегистрировано достоверных различий в степени фрагментации ДНК на этапах аноксии и реперфузии по сравнению с доокклюзионным периодом, что указывает на эффективность кардиопротекции и относительную сохранность ультраструктуры миокарда.
-
4. Отсутствие корреляционной зависимости процентного содержания фрагментированной ДНК в цитоплазме кардиоцитов с длительностью выключения сердца из кровообращения свидетельствует о надежности кардиопротекции раствором «Custodiol» при сроке выключения сердца из кровообращения до 60 мин.
-
5. Клинические характеристики адекватности защиты миокарда соответствовали лабораторным данным - у всех пациентов в ближайшем послеоперационном периоде отсутствовали ишемические изменения и локальные нарушения сократимости сердечной мышцы. Нарушения A-V проводимости были транзиторны и гемодинамически незначимы.
-
6. Нами, по-видимому, зарегистрирована сомнительная кардиопротекция у одного летального пациента, но в данном случае этот факт необходимо соотносить со стадией порока (ЛГ)
III ст. и кризовым течением послеоперационного периода.
Список литературы Оценка защиты миокарда методом лазерно-индуцированной флуоресценции на этапах коррекции врожденных пороков сердца у детей первого года жизни при применении раствора "Custodiol"
- Кулинскии В.И., Колесниченко Л.С.//Успехи современной биологии. 1993. Т. 113, Вып. 1. С. 107-122.
- EDN: RTSBOK
- Ларионов П.М., Литасова Е.Е., Мандрик М.М.//Патология кровообращения и кардиохирургия. 2002. № 2. С. 61-66.
- EDN: VZLLZU
- Ларионов П.М., Мандрик М.М.//Журнал прикл. спектроскоп. 2003. Т. 70, № 1. С. 38-42.
- EDN: HMRRRJ
- Пушкин А. В. Использование кардиоплегического раствора «Custodiol» у больных ишемической болезнью сердца: автореф. дис... канд. мед. наук. М., 2000.
- Мазур А.П.: Захист мюкарду при операциях з штучним кровооб\гом у новонароджених i детей першого року життя: автореф. дис.... канд. мед. наук. Киев, 2001.


