Одноэтапное замещение дефекта пястной кости при остеобластокластоме (клинический случай)
Автор: Ходжамурадов Г.М., Хусейнов З.Х., Исмоилов М.М., Саидов М.С., Шаймонов А.Х., Шарипов Г.Н.
Журнал: Саратовский научно-медицинский журнал @ssmj
Рубрика: Хирургия
Статья в выпуске: 1 т.16, 2020 года.
Бесплатный доступ
Представленный клинический случай демонстрирует преимущества одноэтапного замещения дефекта пястной кости (при остеобластокластоме) с вовлечением суставной головки при помощи костно-суставного аваскулярного аутотрансплантата третьей плюсневой кости. Использование костно-суставного аваскулярного трансплантата третьей плюсневой кости позволило практически идеально возместить дефект пястной кости. Получены оптимальные функциональные и эстетические результаты с полным восстановлением утраченной анатомии. Длительность операции составила 1 час 45 минут. Осложнений в ближайшем послеоперационном периоде не отмечалось.
Аваскулярный костно-суставной аутотрансплантат, остеобластокластома, пястная кость, реконструкция костного дефекта пястной кости
Короткий адрес: https://sciup.org/149135544
IDR: 149135544 | УДК: 616-006.34
One-stage replacement of metacarpal bone due to osteoblastoma lesion
The presented clinical case demonstrates the advantages of one-stage replacement of the metacarpal defect (in osteoblastoclastoma) with the involvement of the distal articular head with the help of bone-articular avascular auto-transplant of the third metatarsal bone. The use of bone-articular avascular graft of the third metatarsal bone allowed almost perfectly compensate for the defect of the metacarpal bone. Optimal functional and aesthetic results with complete restoration of the lost anatomy were obtained. The duration of the operation was 1 hour 45 minutes. There were no complications in the immediate postoperative period.
Текст научной статьи Одноэтапное замещение дефекта пястной кости при остеобластокластоме (клинический случай)
сивным течением [1]. Опухоль редко локализуется в пястных костях с частотой в пределах от 1 до 5,5% случаев [2].
В тех случаях, когда патологический процесс поражает пястные кости, поражение сопровождается чрезмерной деструкцией костной ткани. Данный вид опухоли чаще встречается у молодых лиц, в то вре- мя как другие локализации поражают людей старшего возраста [1, 2]. Опухоль может поражать любую пястную кость и, как правило, не выходит за ее костно-суставные пределы. Пациенты чаще обращаются в период, когда опухоль распространяется за пределы 3–6 см по длине пястной кости, представляя собой объемное образование с шаровидным или эллипсовидным контуром без периостальной реакции [3, 4]. Местные рецидивы после кюретажа опухоли с последующей или без костной пластики имеют тенденцию к рецидиву с вероятностью до 90%. В связи с этим блочная радикальная резекция опухоли в пределах здоровой костной ткани является общепринятым стандартом лечения [3–6]. После радикальной резекции пораженного блока пястной кости возникает проблема замещения образовавшегося дефекта. Вовлечение в процесс одной или обеих суставных головок пястной кости ставит перед хирургом сложную задачу в выборе оптимального трансплантата для реабилитации функции кисти. В настоящее время в подобных случаях используются ауто-, алло-или ксенотрансплантаты [5–15].
Цель: на клиническом примере оценить преимущества одноэтапного замещения дефекта третьей пястной кости (остеобластокластомы) с вовлечением суставной головки при помощи костно-суставного аваскулярного аутотрансплантата третьей плюсневой кости.
Описание клинического случая. В клинику восстановительной хирургии Республиканского научного центра сердечно-сосудистой хирургии (РНЦССХ) поступила молодая пациентка в возрасте 21 года с жалобами на наличие образования в области третьей пястной кости правой кисти.
С целью диагностики выполнены рентгеновские снимки, магнитно-резонансная томография, пункционная биопсия. Установлено наличие субтотальной деструкции третьей пястной кости с вовлечением суставной головки.
Тактика лечения обсуждена консилиумом сотрудников Республиканского онкологического диспансера вместе со специалистами отделения восстановительной хирургии РНЦССХ.
Местно определяется неподвижное опухолевидное образование шаровидно-эпилептоидной формы твердой консистенции около 3,5 см в диаметре.
На послойных рентгенологических снимках установлена почти полная деструкция суставной головки третьей пястной кости правой кисти с поражением диафиза, с распространением опухоли на протяжении 3,5 см (рис. 1).
После тщательного определения объема поражения третьей пястной кости консилиумом врачей запланирована операция, включающая следующие компоненты:
-
— субтотальную резекцию третьей пястной кости вместе с суставной головкой;
-
— одномоментное замещение дефекта костносуставным аутотрансплантатом третьей плюсневой кости с правой стопы;
-
— фиксацию костного трансплантата к проксимальной части третьей пястной кости спицей Киршнера;
— фиксацию третьего пальца донорской зоны стопы.
Под эндотрахеальным наркозом выполнена операция с привлечением двух бригад хирургов. В донорской зоне бригада онкологов зигзагообразным послойным разрезом длиной 7 см приступила к выделению блока пораженной пястной кости правой
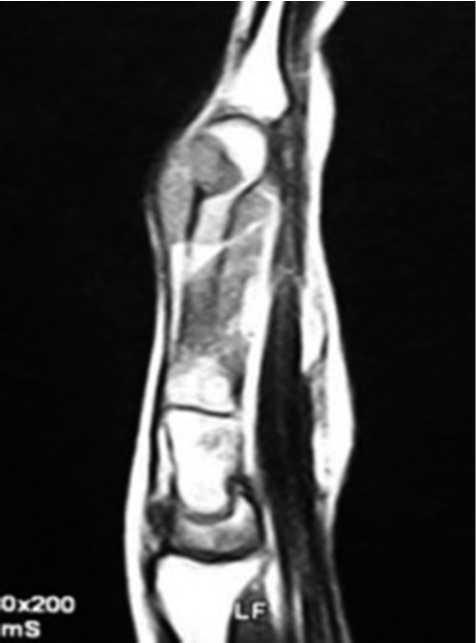
Рис. 1. Субтотальная деструкция пястной кости с преимущественным поражением суставной головки
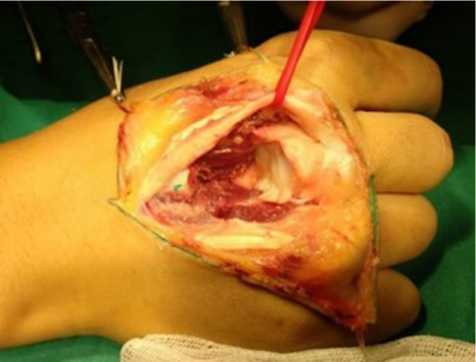
Рис. 2. Вид ложа после удаления блока пораженного сегмента третьей пястной кости кисти. После полной мобилизации пястной кости с рассечением капсулы пястно-фалангового сустава и мобилизацией проксимальной суставной головки с отступом на 1,5 см от края опухоли при помощи пилы Джигли пораженная кость была резецирована. На культе основания пястной кости определялась здоровая ткань с непораженным костным мозгом. Длина резецированного блока пястной кости вместе с суставной головкой составила 41 мм. Резецированный участок представлен в виде макропрепарата округлой формы с псевдокапсулой, диаметром 3,5 см. На разрезе отмечается почти полная деструкция суставной головки с субтотальным поражением кости на всем протяжении (рис. 2).
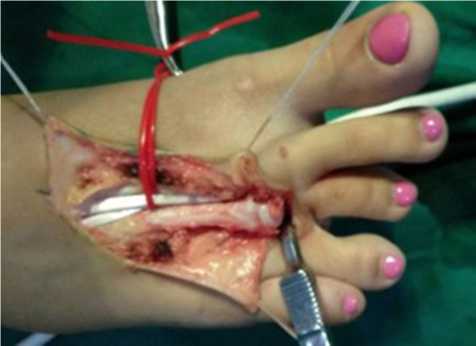
Рис. 3. Подготовка донорского аваскулярного аутотрансплантата третьей плюсневой кости до и после его выделения
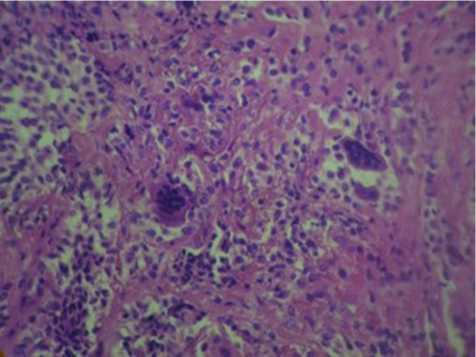
Рис. 5. Вид биопсийного материала (гигантоклеточные образования имеют более темную окраску)
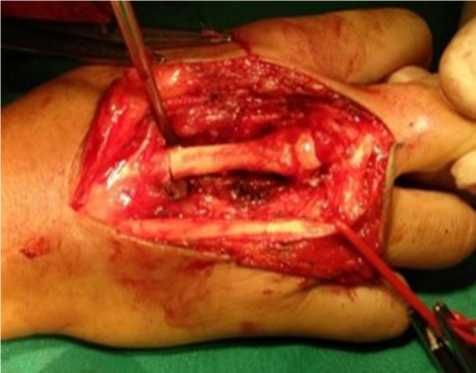
Рис. 4. Вид трансплантата после укладки в донорское ложе
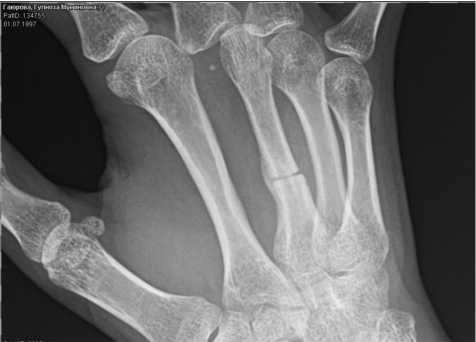
Рис. 6. Рентгенографическая картина костей правой кисти через месяц после оперативного вмешательства и контроль через три месяца: видны признаки омозоления
Одновременно другая бригада реконструктивных хирургов приступила к мобилизации донорского трансплантата. Аналогичным разрезом над проекцией расположения третьей плюсневой кости правой стопы послойно выделена и мобилизована суставная головка (рис. 3). Длина донорского трансплантата составила также 41 мм.
После переноса трансплантата на донорскую область основание основной фаланги третьего пальца стопы фиксировано путем подшивания капсулы и коллатеральных связок к соседним плюснефалан-говым суставам второго и четвертого пальцев.
Аваскулярный трансплантат третьей плюсневой кости правой стопы фиксирован к основанию остатка третьей пястной кости при помощи спицы Киршнера. Капсула сустава ушита в циркулярном направлении при помощи атравматических нитей (рис. 4).
Длительность операции составила 1 час 45 минут. Осложнений в ближайшем послеоперационном периоде не отмечалось. Ближайший послеоперационный период протекал гладко, признаков отторжения пересаженного трансплантата не наблюдалось, все раны зажили первичным натяжением.
Госпитальный период составил 3 дня. Швы были сняты на 14-е сутки; спица Киршнера, расположенная для фиксации третьего пальца правой кисти с целью выпрямления пальца, была удалена на 55-е сутки.
Гистологическое заключение: гигантоклеточная остеокластома (рис. 5).
При контрольном осмотре, спустя месяц после проведения хирургического вмешательства, была выполнена рентгенография правой кисти (рис. 6).
Функциональная активность пальцев кисти восстановлена практически в полном объеме. Спица, расположенная для фиксации трансплантата, оставлена на более длительный срок, так как трансплантат изначально был лишен кровоснабжения. Со стороны донорской зоны (правой стопы) значительного функционального снижения не наблюдается.
Обсуждение клинического случая. Как уже отмечено, гигантоклеточная остеокластома третьей пястной кости является редкой локализацией опухоли. До сих пор вопрос о выборе оптимального способа хирургического лечения не нашел своего окончательного решения.
В настоящее время наряду с вариантом радикальной резекции пораженного сегмента кости сохраняется практика кюретажа с заполнением дефекта аваскулярными аутотрансплантатами костей, взятых из кортикальной пластинки большеберцовой и из гребня подвздошной костей [7–9]. Однако радикальная резекция опухоли в виде блока пораженного участка с одномоментным замещением костно-суставного дефекта является общепринятым стандартом, и направлена она на устранение риска развития местного рецидива [3, 5, 12, 14, 15].
В качестве донорского трансплантата предлагается использовать цельные аутотрансплантаты малоберцовой кости [12], третьей плюсневой кости нижней конечности [14, 15], реже — аллотрансплантаты, титановые пластины и прочие материалы [6, 10, 11]. После обширных радикальных резекций целой пястной кости вместе с пястно-фаланговым сочленением по поводу рецидивов опухоли рекомендуется применение свободных васкуляризированных трансплантатов третьей плюсневой кости [15].
Комбинированное лечение с хирургической санацией очага остеобластокластомы пястной кости в сочетании с пред- или послеоперационным облучением является спорным и не нашло полного одобрения [7, 9].
В условиях Республики Таджикистан ранее широко применялся кюретаж костной ткани с заполнением размельченных фрагментов аутологической костной ткани, а после радикальной резекции пястной кости пластическое возмещение оставлялось на второй этап, судьба которого оставалась неизвестной.
Данная операция стала возможной благодаря совместной работе онкологов и реконструктивно-пластических хирургов. Выбор трансплантата продиктован обобщением литературных данных результатов исследований по применению различных трансплантатов, простотой технического исполнения, минимальным донорским ущербом.
Заключение. При локализации гигантоклеточной опухоли в пястных костях радикальное блоковидное иссечение является оптимальным подходом с целью предупреждения местных рецидивов. Использование костно-суставного аваскулярного трансплантата третьей плюсневой кости позволяет практически идеально возместить аналогичный дефект пястной кости. Донорский дефект после забора трансплантата сопровождается минимальными донорскими потерями и не приводит к нарушению функции стопы. Получены оптимальные функциональные и эстетические результаты с полным восстановлением утраченной анатомии.
Список литературы Одноэтапное замещение дефекта пястной кости при остеобластокластоме (клинический случай)
- Kabul CS, Sanjeev KB, Firoz A, Debashish Ch. Giant cell tumor of the metacarpal bones. Indian Journal Orthopedics 2011; 45 (5): 475-8. DOI: 10.4103/0019-5413.83957.
- Averill RM, Smith RJ, Campbell CJ. Giant cell tumours of the bones of the hand. Journal of Hand Surgery 1980; 5: 3950.
- Williams J, Hodari A, Janevski P, Siddiqui A. Recurrence of giant cell tumor in the hand: A prospective study. Journal of Hand Surgery 2010; 35: 451-6. [PubMed].
- Slesarencko YA, Sampson SP, Gould ES. Giant cell tumour of the distal phalanx of hand. Journal of Hand Surgery 2005; 10: 289-91.
- Ozalp T, Yercan H, Okpu G, et al. Giant cell tumour of hand: Midterm results in five patients. Rev Chir Orthopedics Reparatrice Appar Mot 2007; 93: 842-7.
- Smith RJ, Brushart TM. Allograft bone for metacarpal reconstruction. Journal of Hand Surgery 1985; 10 (3): 325-34.
- Shlyakhtunov EA, Lud NG, Fedorenko II, Valshonok ON. Osteoblastoclastoma of the third metacarpal bone in a patient with secondary lymphedema of the upper limb: A case from practice. Surgery news 2013; 21 (2): 105-10. Russian (Шляхту-нов Е. А., Луд Н. Г., Федоренко И. И., Вальшонок О. Н. Остео-бластокластома третьей пястной кости у пациентки с вторичной лимфедемой верхней конечности: Случай из практики. Новости хирургии 2013; 21 (2): 105-10).
- Kuftyrev LM. Autoplasty of post-resection defects of the tubular bones of the hand in the treatment of benign tumors and tumor-like diseases using transostealosteses. The genius of orthopedics 2004; 2: 20-5. Russian (Куфтырев Л. М. Аутопластика пострезекционных дефектов трубчатых костей кисти при лечении доброкачественных опухолей и опухолеподоб-ных заболеваний с использованием чрескостного остеосин-теза. Гений ортопедии 2004; 2: 20-5).
- Deykalo VP, Tolstik AN. Hand surgery: history, modern achievements, problems and development prospects. Surgery news 2006; 14 (4): 26-36. Russian (Дейкало В. П, Тол-стик А. Н. Хирургия кисти: история, современные достижения, проблемы и перспективы развития. Новости хирургии 2006; 14 (4): 26-36).
- Patradul A, et al. Allograft replacement in giant cell tumour of the hand. Hand Surgery 2001; 6 (1): 59-5.
- Punyaratabandhu T, Lohwongwatana B, Puncreobutr C, et al. A Patient-Matched Entire First Metacarpal Prosthesis in Treatment of Giant Cell Tumor of Bone. Case Reports in Orthopedics 2017; 7 (1-6): 3. DOI: 10.1155/2017/4101346.
- Jones NF, Dickinson BP, Hansen SL. Reconstruction of an entire metacarpal and metacarpophalangeal joint using a fibular osteocutaneous free flap and silicone arthroplasty. Journal of Hand Surgery 2012; 37 (2): 310-5.
- Mendenhall WM, Zlotecki RA, Scarborough MT, et al. Giant cell tumor of bone. Journal of Clinical Oncology 2006; 29 (1): 96-9.
- Saikat S. Reconstruction of metacarpal bone giant cell tumor by metatarsal bone. Journal of Orthopaedic Surgery and Research 2016; 2 (1): 23-35.
- Kotwal PP, Nagaraj C, Gupta V. Vascularised joint transfer in the management of recurrent giant cell tumour of the second metacarpal. Journal of Hand Surgery-European 2008; 33 (3): 314-6.


