Одномоментная субтотальная эзофагэктомия и верхняя лобэктомия справа с резекцией главного и промежуточного бронхов при синхронном раке пищевода и легкого
Автор: Рябов Андрей Борисович, Черемисов Вадим Владимирович, Хомяков Владимир Михайлович, Пикин Олег Валентинович, Шеметова Мария Михайловна, Телегина Лариса Валентиновна, Волченко Надежда Николаевна, Колобаев Илья Владимирович, Чайка Анна Валентиновна, Кострыгин Александр Константинович
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Случай из клинической практики
Статья в выпуске: 2 (68), 2015 года.
Бесплатный доступ
Приводится редкое клиническое наблюдение успешной симультанной операции - эзофагэктомии и верхней лобэктомии с резекцией главного и промежуточного бронхов при первично-множественной синхронной опухолевой патологии: рак грудного отдела пищевода и центральный рак правого легкого. Подробно представлены диагностический комплекс и особенности морфологической диагностики в плане дифференциального диагноза синхронной неоплазии и метастатического процесса. Данное клиническое наблюдение демонстрирует возможность успешного одномоментного хирургического лечения при тяжелой конкурирующей по прогнозу опухолевой патологии, при условии корректной оценки распространенности заболевания и функционального статуса пациента.
Первично-множественный рак пищевода и легкого, радикальное оперативное лечение, бронхопластика
Короткий адрес: https://sciup.org/14056535
IDR: 14056535 | УДК: 616.329+616.24]-006.6-089.87
One-stage subtotal esophagectomy and right upper lobectomy with resection of main and intermediate bronchi in synchronous esophageal and lung cancer
We report a rare case of successful surgical management (simultaneous esophagectomy and upper lobectomy with resection of the main and intermediate bronchi) of synchronous multiple primary cancer of the thoracic esophagus and central cancer of the right lung. The role of morphological characteristics in differential diagnosis between synchronous neoplasia and metastasis has been described. This clinical case demonstrates successful one-stage surgical management of this disease provided a correct assessment of the extent of cancer involvement and the patient’s functional status.
Текст научной статьи Одномоментная субтотальная эзофагэктомия и верхняя лобэктомия справа с резекцией главного и промежуточного бронхов при синхронном раке пищевода и легкого
Сочетание рака пищевода и рака легкого наблюдается редко [1]. При этом в структуре первично-множественных злокачественных новообразований, по данным МНИOИ им. П.А. Герцена, рак пищевода наиболее часто сочетается с синхронными и метахронными опухолями легкого – 35,06 %, а синхронный и метахронный рак легкого в сочетании с новообразованиями пищевода встречается в 13,25 % [1, 2] . В литературе описаны единичные случаи выполнения одномоментных радикальных операции при синхронных новообразованиях пищевода и легкого [6].
Приводим клиническое наблюдение выполнения успешной одномоментной операции у пациента с первично-множественным синхронным раком пищевода и центральным раком верхней доли правого легкого с одномоментной эзофаго- и бронхопластикой.
Пациент Р., 57 лет, обратился в МНИОИ им. П.А. Герцена в марте 2014 г. с жалобами на затруднение при глотании твердой и полутвердой пищи (дисфагия II степени), потерю массы тела на 5 кг за 2 мес, общую слабость. Индекс по шкале Карновского составил 80 %, активность по шкале
ECOG – 1 балл. Пациент считает себя больным с января 2014 г., когда впервые появились симптомы дисфагии.
По данным комплексного обследования, в средне-грудном отделе пищевода выявлена опухоль, протяженностью 4,0 см (уровень 33–37 см от резцов) с утолщением стенок до 2,0 см, без признаков инвазии параэзофагеальной клетчатки с единичным увеличенным лимфатическим узлом бифуркационной группы (19×16 мм) (рис. 1а). В корне верхней доли правого легкого выявлена опухоль размером 24×24×34 мм, распространяющаяся от устья верхнедолевого и по ходу сегментарных бронхов с метастатическим поражением бронхопульмональных лимфатических узлов (рис. 1б).
При бронхоскопии и эзофагогастроскопии были взяты биопсии. При морфологическом исследовании в пищеводе на фоне тяжелой дисплазии покровного многослойного плоского эпителия и очагов тяжелой дисплазии имеется инфильтративный рост плоскоклеточного высокодифференцированного рака. В биопсии из устья верхнедолевого бронха выявлен умереннодифференцированный плоскоклеточный рак на фоне
карциномы in situ метаплазированного плоского эпителия покрова (рис. 2).
По данным позитронно-эмиссионной томографии, в режиме «все тело» отмечались очаги патологической гиперфиксации 18F-фтордезоксиглюкозы в области опухоли пищевода (SUV max=9,0), в области корня правого легкого (SUV max=5,2), а также дополнительный очаг «свечения» в паренхиме верхней доли правого легкого (SUV max=5,96) – метастаз?(рис. 3).
Был сформулирован следующий клинический диагноз: Первично-множественные злокачественные новообразования: рак пищевода IIIA стадии (eT 3 N1M0) и рак легкого IIA стадия (сТ2а N 1 M 0 ), согласно классификации TNM 7-го пересмотра.
Пациент был обследован по соматическому статусу, проведено комплексное обследование состояния кардиореспираторной системы (ЭКГ, ЭХО-КГ, xолтеровское мониторирование, пробы с нагрузкой, функция внешнего дыхания) и оценка нутритивного статуса. Из сопутствующих заболеваний выявлена выраженная обструктивная болезнь легких, хронический бронхит курильщика (40-летний анамнез курильщика, с потреблением 3 пачек сигарет в сутки). По данным исследования функции внешнего дыхания FEV1 – 65 %, FVC – 82 %, расчетный послеоперационный объем форсированного выдоха за 1 сек (ppoFEV1) – 49,5 %.
Тактика лечения пациента была обсуждена на мультидисциплинарном консилиуме. С учетом диагностических данных о распространенности патологического процесса оба заболевания представлялись локализованными и резектабельными. Принимая во внимание относительно сохранное общее состояние пациента, решено было выполнить одномоментную операцию.
В стационаре пациенту в течение 2 нед проведена поликомпонентная предоперационная подготовка, включающая инфузионную терапию в режиме частичного парэнтерального питания, кардиотропную, респираторную терапию (муколитики, бронхолитики, отказ от курения), антибактериальную терапию, нутритивную поддержку и ЛФК.
Торакальный этап операции произведен через правостороннюю боковую торакотомию в V межреберье. В плевральной полости признаков диссеминации не выявлено. В пищеводе на уровне бронхиального сегмента отмечалось уплотнение стенки, протяженностью 4 см. На уровне опухоли определялся увеличенный до 2,0×1,0 см плотный лимфатический узел. Произведена эзофагэктомия с лимфодиссекцией в объеме 2F и формированием двухрядного эзофагогастроанастомоза по типу «конец в бок» в куполе гемиторакса. В проекции устья верхнедолевого бронха правого легкого определялась опухоль, размером 3,5×4,0 см, с увеличенными лимфатическим узлами корня верхней доли. В связи с распространением на шпору верхнедолевого бронха была выполнена верхняя лобэктомия с циркулярной резекцией главного и промежуточного бронхов в пределах здоровых тканей (подтверждено данными срочного морфологического исследования) с формированием непрерывного межбронхиального анастомоза нитью PDS 3,0. Линия анастомоза укрыта перикардиальным лоскутом на сосудистой ножке.
Во время операции гемодинамических нарушений не отмечалось и вазопрессорная поддержка не осуществлялась. Объем кровопотери составил 500 мл. Время операции – 600 мин. Гемотрансфузия не проводилась.
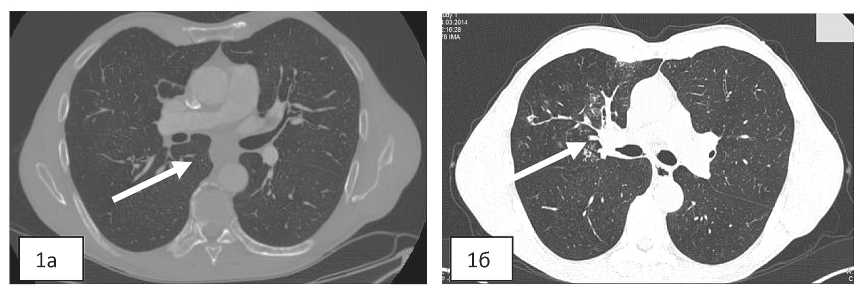
Рис. 1. КТ органов средостения: а) опухоль средне-грудного отдела пищевода (обозначена стрелкой); б) опухоль в корне верхней доли правого легкого с прилежащими лимфатическими узлами (обозначена стрелкой)
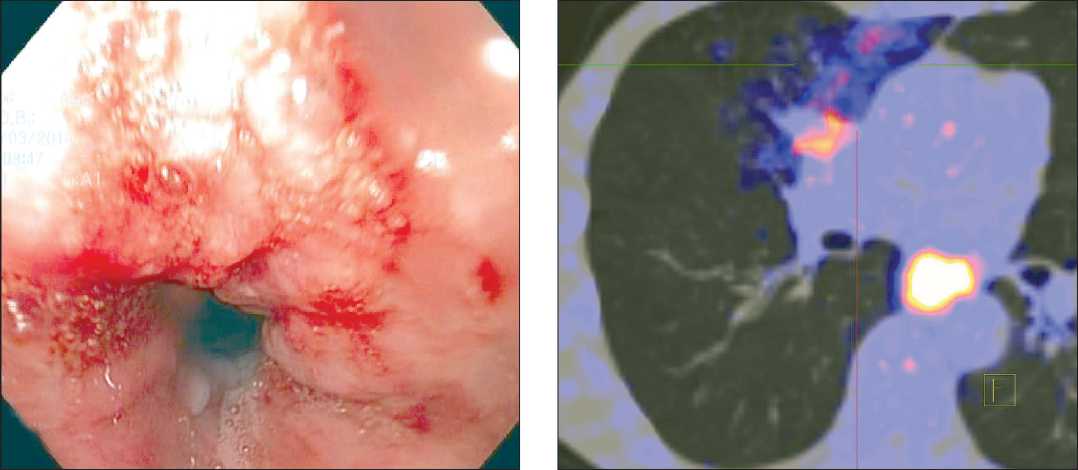
Рис. 2. Эндофото. Опухоль пищевода
Рис. 3. Позитронно-эмиссионная томография. Очаги патологического накопления радиофармпрепарата в проекции грудного отдела пищевода и корня правого легкого
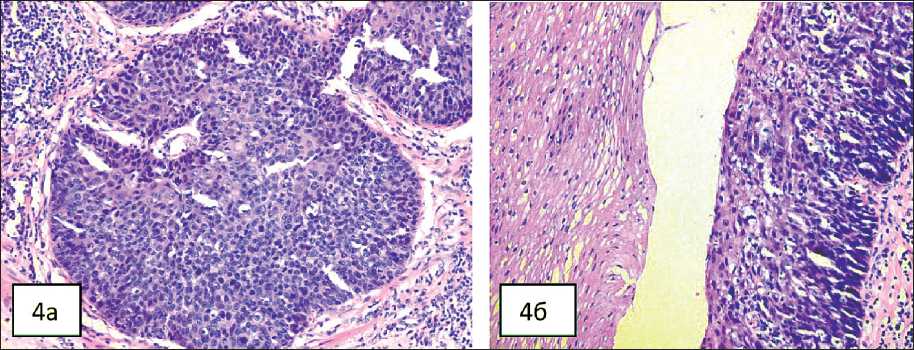
Рис. 4. Микрофото: а) инфильтративный рост плоскоклеточного умереннодифференцированного рака пищевода, окраска гематоксилином и эозином, ×40; б) внутриэпителиальный (carcinoma in situ) плоскоклеточный рак опухоли пищевода, окраска гематоксилином и эозином, ×100
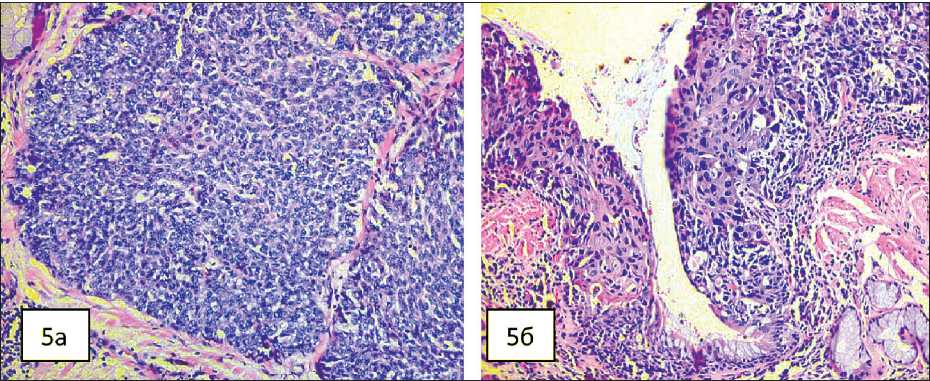
Рис. 5. Микрофото. а) инвазивный рост плоскоклеточного умереннодифференцированного рака бронха, окраска гематоксилином и эозином, ×40; б) carcinoma in situ плоскоклеточного типа слизистой бронха, окраска гематоксилином и эозином, ×10
Течение послеоперационного периода в целом расценивалось как неосложненное. Проводилась комплексная послеоперационная реабилитационная терапия: лечебная физкультура, инфузионная, антибактериальная и раннее энтеральное питание через еюностому.
При бронхоскопии отмечались признаки нарушения трофики в области межбронхиального анастомоза. В этой связи во время фибробронхоскопий проводились сеансы низкоинтенсивной лазерной терапии на зону межбронхиального анастомоза.
Через 7 дней пациент был повторно госпитализирован с жалобами на повышение температуры тела до 39°С. При обследовании выявлена картина правосторонней нижнедолевой пневмонии. Проведена терапия с положительным результатом.
С учетом морфологического заключения был сформулирован послеоперационный диагноз: Первично-множественные злокачественные опухоли. Рак среднегрудного отдела пищевода IIIA стадия (рТ3Ы 1 М 0 ). Рак верхней доли правого легкого IIA стадия (рТ^НМфТаким образом, клинический и заключительный (патоморфологи-ческий) диагнозы совпали.
Обсуждение
В литературе имеются единичные публикации, сообщающие о выполнении одномоментной эзофагэктомии и лобэктомии с бронхопластикой [6]. В МНИОИ им. П.А. Герцена подобная операция была произведена впервые. В нашей клинике уже имелся опыт успешного одномоментного выпол- нения операции Льюиса и лобэктомии в связи с первично-множественными злокачественными опухолями. Редкая встречаемость таких операций обусловлена, с одной стороны, низкой операбельностью рака пищевода и легкого, так как чаще всего диагностируются распространенные опухоли данной локализации, с другой, тяжелым коморбидным статусом подобных пациентов. В связи с последним обстоятельством в работе F. Fekete et al. [3] приведены данные о том, что из 39 пациентов с синхронными и метахронными опухолями легкого и пищевода оперирован лишь 21 (54 %) больной. В нашем наблюдении пациент имел длительный анамнез курения и употребления алкоголя, страдал хронической обструктивной болезнью легких. Однако резервы дыхания были снижены незначительно.
Планируя подобное хирургическое вмешательство, важно корректно оценить распространенность опухолевого процесса. Поэтому предоперационной диагностике уделяется большое внимание. В нашем случае пациенту, помимо КТ грудной клетки и брюшной полости, МРТ головного мозга, бронхоскопии и остеосцинтиграфии, была выполнена позитронно-эмиссионная томография. Скрупулёзность анализа данных обследования позволила выставить клинические стадии патологических процессов, которые в итоге не отличались от заключительного диагноза. Считаем важным проведение предоперационной подготовки к операции, так как в плане профилактики легочных осложнений именно дооперационная подготовка имеет большее значение, нежели реабилитационные мероприятия в послеоперационном периоде [8].
Учитывая большой объем хирургического вмешательства и отягощенный фон сопутствующей патологии у данной категории пациентов, ряд авторов не исключает выполнения подобных хирургических вмешательств в два этапа (в представленных статьях хирургические вмешательства по поводу рака легкого ограничивались выполнением лобэктомий) [5, 7]. Двухэтапные операции чаще выполняются при поражении левого легкого: при первой операции выполняют эзофагэктомию правосторонним доступом, а через месяц производят лобэктомию слева [9]. Другой вариант применил И.С. Стилиди в 2007 г. в РОНЦ им. Н.Н. Блохина, выполнив одномоментно верхнюю лобэктомию слева и субтотальную эзофагэктомию из левого трансторакального доступа в V межреберье с формированием пищеводно-желудочного анастомоза выше дуги аорты. Как отмечают большинство авторов, несмотря на обширность хирургического вмешательства при синхронном раке пищевода и легкого, все оперированные пациенты были выписаны из стационара, что говорит о переносимости подобного хирургического вмешательства [4, 9].
В своих обзорах авторы уделяют мало внимания отдаленным результатам лечения, объясняя это
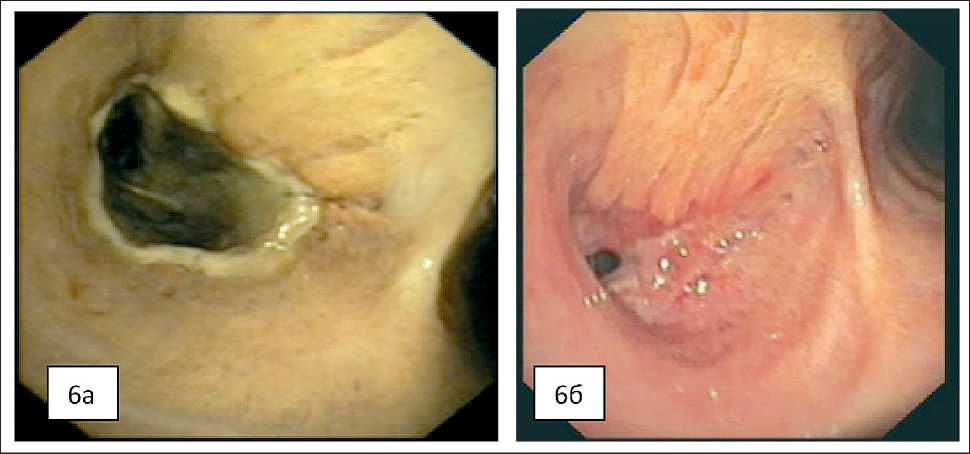
Рис. 6. Эндофото: а) бронхоскопия на 10-е сут после операции; б) бронхоскопия на 58-е сут после операции
незначительным числом наблюдений. В работах H. Ishii et al. (2008) [5] и K. Kuhn et al. (2000) [6] срок наблюдения за тремя оперированными пациентами составил 10 мес, признаков прогрессирования заболевания не отмечено. F. Fekete et al. (1994) [3] приводят данные о 3 пациентах после радикального хирургического лечения, которые пережили двухлетний срок наблюдения без признаков рецидива заболевания (5-летняя выживаемость при синхронном поражении составила 11 %). Наш пациент находился под наблюдением 5 мес.
Сама методика операции не имеет существенных особенностей, так как складывается из двух стандартных, хорошо освоенных в специализированных клиниках хирургических вмешательств: операции Льюиса и лобэктомии с резекцией главного и промежуточного бронхов. Особенностью является то, что условия для заживления бронхиального анастомоза неблагоприятны, так как в процессе лимфодиссекции производится лигирование бронхиальных артерий, в то же время удаление пищевода также нарушает артериальное кровоснабжение трахеобронхеального дерева. Мы наблюдали у нашего пациента изменение цвета слизистой бронхов в зоне бронхиального анастомоза как следствие компрометированной трофики. К концу 2-го мес после операции цвет слизистой бронха приобрел нормальную окраску (рис. 6а, б). В этой связи считаем оправданным дополнительно укрывать зону бронхиального анастомоза тканевыми лоскутами.
Насколько важна последовательность выполнения легочного и пищеводного этапов операции? K. Kuhn et al. [6] произвели вначале лобэктомию с бронхопластикой, а затем приступили к резекции и пластике пищевода с тем, чтобы не произошло инфицирования трахеобронхеального дерева из просвета желудочно-кишечного тракта. Мы счита- ем, что риск инфицирования трахеобронхеального дерева преувеличен, и придерживаемся обратной последовательности хирургических вмешательств. По функциональным соображениям легочный этап должен быть последним, за исключением случаев легочного кровотечения или ателектазирования. Кроме того, после бронхопластики желательно не осуществлять тракцию легкого, что возможно при выполнении пищеводного этапа вмешательства.
Другим сложным моментом является интерпретация очага в легочной паренхиме при одинаковом гистологическом строении опухолей пищевода и легкого: следует ли его рассматривать как первично-множественный процесс или метастатическое поражение. Метастазирование рака пищевода в легкое исключает возможность попытки радикального хирургического вмешательства. Надо понимать, что диагноз до операции всегда клинико-морфологический. Биопсийный материал часто недостаточен в плане постановки диагноза. Помимо гистологической формы, важны фоновые изменения, наличие раковых эмболов в лимфатических и кровеносных сосудах, степень дифференцировки опухолевых клеток, наличие метастазов в регионарных лимфатических узлах. В представленном наблюдении в легком и пищеводе плоскоклеточный рак развился на фоне карциномы in situ метаплазированного эпителия, что подтверждает первичную множественность опухолевого процесса.
Таким образом, данное клиническое наблюдение демонстрирует возможность успешного одномоментного хирургического лечения при тяжелой конкурирующей по прогнозу опухолевой патологии при условии корректной оценки распространенности заболевания и функционального статуса пациента.
Список литературы Одномоментная субтотальная эзофагэктомия и верхняя лобэктомия справа с резекцией главного и промежуточного бронхов при синхронном раке пищевода и легкого
- Мамонтов А.С., Шляков С.Л. Рак пищевода при первично-множественных злокачественных опухолях//Первично-множественные злокачественные опухоли: Руководство для врачей/Под ред. В.И. Чиссова, А.Х. Трахтенберга. М.: Медицина, 2000. С. 220.
- Трахтенберг А.Х., Колбанов К.И., Сомратов Д.У. Рак легкого при первично-множественных злокачественных опухолях//Первично-множественные злокачественные опухоли: Руководство для врачей/Под ред. В.И. Чиссова, А.Х. Трахтенберга. М.: Медицина, 2000, С. 120.
- Fekete F., Sauvanet A., Kaisserian G., Jauffret B., Zouari K., Berthoux L., Flejou J.F. Associated primary esophageal cancer and lung carcinoma: a study of 39 patients//Ann. Thorac. Surg. 1994. Vol. 58 (3). P. 837-842.
- Fukuda H., Ogino N., Takao T., Kobayashi S., Kido T. A case report of synchronous double cancer of the lung and esophagus//Nippon Kyobu Gekka Gakkai Zasshi. 1990. Vol. 38(6). P. 1053-1058.
- Ishii H., Sato H., Tsubosa Y., Kondo H. Treatment of double carcinoma of the esophagus and lung//Gen. Thorac. Cardiovasc. Surg. 2008. Vol. 56 (3). P. 126-130 DOI: 10.1007/s11748-007-0200-0
- Kuhn K., Pasch S., Woiciechowski W., Macchiarini P. Combined sleeve lobectomy and Ivor Lеwis esophagectomy for synchronous primary carcinoma of the lung and Barret esophagus//J. Thorac. Cardiovasc Surg. 2000. Vol. 119 (6). P. 1289-1290.
- Morimoto M., Ohno T., Yamashita Y., Honda M., Asada S. Two surgical cases of synchronous double carcinoma of the lung and esophagus and review of 10 documented cases in Japan//Nippon Kyobu Gekka Gakkai Zasshi. 1991. Vol. 3 (2). P. 245-250.
- Rodrigues-Larrad A., Lascarian-Augirrebena I., Abecia-Inchaurregui L.C., Seco J. Perioperative physiotherapy in patients undergoing lung cancer resection//Interact. Cardiovasc. Thorac. Surg. 2014. Vol. 19 (2). P. 269-281 DOI: 10.1093/icvts/ivu126
- Takeo M., Yamamoto M. Synchronous double carcinoma of the left lung and esophagus; report of a case//Kyobu Geka. 2008. Vol. 61 (9). P. 808-801.


