Окисление трис(2-метоксифенил)сурьмы трет-бутилгидропероксидом в присутствии карбоновой кислоты
Автор: Шарутин В.В., Шарутина О.К., Палилова В.В.
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Химия элементоорганических соединений
Статья в выпуске: 2 т.17, 2025 года.
Бесплатный доступ
Окисление трис(2-метоксифенил)сурьмы трет-бутилгидропероксидом в присутствии карбоновой кислоты в тетрагидрофуране или диэтиловом эфире приводит к образованию бис(хлорацетата) трис(2-метоксифенил)сурьмы (2-MeOC6H4)3Sb[OC(O)CH2Cl]2 (1), бис(2-метоксибензоата) трис(2-метоксифенил)сурьмы (2-MeOC6H4)3Sb[OC(O)C6H4(OMe-2)]2 (2), бис(2,3-дифторбензоата) трис(2-метоксифенил)сурьмы [(2-MeOC6H4]3Sb[OС(O)C6H3F2-2,3]2 (3) и сольвата бис(пентафторбензоата) трис(2-метоксифенил)сурьмы с бензолом [(2-MeOC6H4]3Sb[OС(O)C6F5]2 ∙ ½ PhH (4). Соединения 1-4, выделенные после перекристаллизации из смеси бензол-октан в виде монокристаллов, охарактеризованы методами ИК-спектроскопии и рентгеноструктурного анализа (РСА). В ИК-спектрах присутствуют полосы, характеризующие колебания карбонильных груп (1697, 1624, 1655, 1668 см-1), фрагмента SbC3 (440-447 см-1), связей Sb-O (575-536 см-1) соответственно. По данным РСА, кристаллы 1 и 4 принадлежат триклинной сингонии, группа симметрии Р-1; кристаллы 2 и 3 - моноклинной сингонии, группа симметрии P21/n. Факторы недостоверности уточнения структурных данных соствляют R1 = 0,0502 (1), R1 = 0,0437 (2), R1 = 0,0409 (3), R1 = 0,0333 (4). В тригонально-бипирамидальных молекулах с электроотрицательными лигандами в аксиальных положениях расстояния Sb-C составляют для 1 2,0966(17)-2,1194(18) Å, для 2 2,104(2)-2,126(2) Å, для 3 2,0889(19)-2,1134(19) Å и для 4 2,109(2)-2,123(2) Å; валентные углы OSbO принимают значения 175,15(5)° (1), 171,42(6)° (2), 176,97(6)° (3) и 164,47(6)° (4). Расстояния Sb-О в 1 [2,1088(15) и 2,1269(15) Å] сопоставимы с наблюдаемыми в 2 [2,1137(17) и 2,1232(18) Å], в 3 [2,0880(14) и 2,1063(14) Å] и несколько отличными для 4 [2,1035(17) и 2,1460(17) Å]. Сольватные молекулы бензола в 4 связывают собой соседние молекулы дикарбоксилатов [расстояния С∙∙∙H и Сl∙∙∙H равны 2,84 Å и 3,06 Å, что меньше суммы ковалентных радиусов атомов-партнеров. Атом сурьмы координирует карбонильные атомы кислорода со стороны малых экваториальных углов (115,31(9)° и 119,59(9)°), при этом внутримолекулярные контакты Sb∙∙∙O=C составляют 3,374(3) и 3,296(3) Å, что больше внутримолекулярных контактов Sb∙∙∙OMe (3,079-3,172 Å). Отметим, что подобное различие внутримолекулярных контактов Sb∙∙∙O и Sb∙∙∙OMe наблюдается и в первых трех молекулах комплексов [3,296(3), 3,374(3) Å и 3,102-3,167 Å для 1, 3,010(3), 3,164(3) Å и 3,058-3,202 Å для 2 и 3,190(3), 3,233(3) Å и 3,056-3,120 Å для 3]. Внутримолекулярные контакты Sb∙∙∙O=С между центральным атомом металла и карбонильным атомом кислорода наибольшие в 1 и 4, что можно объяснить присутствием электроакцепторных карбоксилатных лигандов. Полные таблицы координат атомов, длин связей и валентных углов для структур депонированы в Кембриджском банке структурных данных (№ 2416266 (1), № 2415652 (2), № 2415732 (3), № 2415648 (4), deposit@ccdc.cam.ac.uk; http://www.ccdc. cam.ac.uk).
Трис(2-метоксифенил)сурьма, трет-бутилгидропероксид, хлоруксусная, 2-метоксибензойная, 2, 3-дифторбензойная, пентафторбензойная, кислота, синтез, карбоксилаты трис(2-метоксифенил)сурьмы, рентгеноструктурный анализ
Короткий адрес: https://sciup.org/147248076
IDR: 147248076 | УДК: 546.865+547.53.024+548.312.5 | DOI: 10.14529/chem250204
Oxidation of tris(2-methoxyphenyl)antimony with tert-butyl hydroperoxide in the presence of carboxylic acid
Oxidation of tris(2-methoxyphenyl)antimony with tert-butyl hydroperoxide in the presence of a carboxylic acid in tetrahydrofuran or diethyl ether leads to formation of tris(2-methoxyphenyl)antimony bis(chloroacetate) (2-MeOC6H4)3Sb[OC(O)CH2Cl]2 (1), tris(2-methoxyphenyl)antimony bis(2-methoxybenzoate) (2-MeOC6H4)3Sb[OC(O)C6H4(OMe-2)]2 (2), tris(2-methoxyphenyl)antimony bis(2,3-difluorobenzoate) [(2-MeOC6H4]3Sb[OC(O)C6H3F2-2,3]2 (3) and tris(2-methoxyphenyl)antimony bis(pentafluorobenzoate) solvate with benzene [(2-MeOC6H4]3Sb[OC(O)C6F5]2 ∙ ½ PhH (4). Compounds 1-4 isolated after recrystallization from a benzene-octane mixture in the form of single crystals, were characterized by IR spectroscopy and X-ray diffraction (XRD) analysis. The IR spectra contain bands characterizing vibrations of carbonyl groups (1697, 1624, 1655, 1668 cm-1), the SbC3 fragment (440-447 cm-1), the Sb-O bonds (575-536 cm-1), respectively. According to the XRD data, crystals 1 and 4 belong to the triclinic syngony, symmetry group P-1; crystals 2 and 3 belong to the monoclinic syngony, symmetry group P21/n. The uncertainty factors for refinement of the structural data are R1 = 0.0502 (1), R1 = 0.0437 (2), R1 = 0.0409 (3), R1 = 0.0333 (4). In trigonal bipyramidal molecules with electronegative ligands in axial positions, the Sb-C distances are 2.0966(17)-2.1194(18) Å for 1, 2.104(2)-2.126(2) Å for 2, 2.0889(19)-2.1134(19) Å for 3, and 2.109(2)-2.123(2) Å for 4; the OSbO bond angles take the values of 175.15(5)° (1), 171.42(6)° (2), 176.97(6)° (3), and 164.47(6)° (4). The Sb-O distances in 1 [2.1088(15) and 2.1269(15) Å] are comparable with those observed in 2 [2.1137(17) and 2.1232(18) Å], in 3 [2.0880(14) and 2.1063(14) Å] and are slightly different for 4 [2.1035(17) and 2.1460(17) Å]. The solvate molecules of benzene in 4 bind neighboring dicarboxylate molecules [the C∙∙∙H and Cl∙∙∙H distances are 2.84 Å and 3.06 Å, which is less than the sum of the covalent radii of the partner atoms. The antimony atom coordinates the carbonyl oxygen atoms from the side of small equatorial angles (115.31(9)° and 119.59(9)°), while the Sb∙∙∙O=C intramolecular contacts are 3.374(3) and 3.296(3) Å, which is greater than the Sb∙∙∙OMe intramolecular contacts (3.079-3.172 Å). It should be noted that a similar difference in the Sb∙∙∙O and Sb∙∙∙OMe intramolecular contacts is also observed in the first three molecules of the complexes [3.296(3), 3.374(3) Å and 3.102-3.167 Å for 1, 3.010(3), 3.164(3) Å and 3.058-3.202 Å for 2 and 3.190(3), 3.233(3) Å and 3.056-3.120 Å for 3]. The Sb∙∙∙O=C intramolecular contacts between the central metal atom and carbonyl oxygen atom are the largest in 1 and 4, which can be explained by the presence of electroacceptor carboxylate ligands. Complete tables of atomic coordinates, bond lengths and bond angles for the structures have been deposited with the Cambridge Crystallographic Data Centre (No. 2416266 (1), No. 2415652 (2), No. 2415732 (3), No. 2415648 (4), deposit@ccdc.cam.ac.uk; http://www.ccdc.cam.ac.uk).
Текст научной статьи Окисление трис(2-метоксифенил)сурьмы трет-бутилгидропероксидом в присутствии карбоновой кислоты
Аннотация. Окисление трис(2-метоксифенил)сурьмы трет-бутилгидропероксидом в присутствии карбоновой кислоты в тетрагидрофуране или диэтиловом эфире приводит к образованию бис(хлорацетата) трис(2-метоксифенил)сурьмы (2-MeOC6H4)3Sb[OC(O)CH2Cl]2 (1), бис(2-метоксибензоата) трис(2-метоксифенил)сурьмы (2-MeOC6H4)3Sb[OC(O)C6H4(OMe-2)]2 (2), бис(2,3-дифторбензоата) трис(2-метоксифенил)сурьмы [(2-MeOC6H4]3Sb[OС(O)C6H3F2-2,3]2 (3) и сольвата бис(пентафторбензоата) трис(2-метоксифенил)сурьмы с бензолом [(2-MeOC6H4]3Sb[OС(O)C6F5]2 ∙ ½ PhH (4). Соединения 1-4, выделенные после перекристаллизации из смеси бензол-октан в виде монокристаллов, охарактеризованы методами ИК-спектроскопии и рентгеноструктурного анализа (РСА). В ИК-спектрах присутствуют полосы, характеризующие колебания карбонильных груп (1697, 1624, 1655, 1668 см–1), фрагмента SbC3 (440–447 см–1), связей Sb–O (575–536 см–1) соответственно. По данным РСА, кристаллы 1 и 4 принадлежат триклинной сингонии, группа симметрии Р–1; кристаллы 2 и 3 - моноклинной сингонии, группа симметрии P2 1/n. Факторы недостоверности уточнения структурных данных соствляют R1 = 0,0502 (1), R1 = 0,0437 (2), R1 = 0,0409 (3), R1 = 0,0333 (4). В три-гонально-бипирамидальных молекулах с электроотрицательными лигандами в аксиальных положениях расстояния Sb-C составляют для 1 2,0966(17)-2,1194(18) Å, для 2 2,104(2)-2,126(2) Å, для 3 2,0889(19)-2,1134(19) Å и для 4 2,109(2)-2,123(2) Å; валентные углы OSbO принимают значения 175,15(5)° (1), 171,42(6)° (2), 176,97(6)° (3) и 164,47(6)° (4). Расстояния Sb-О в 1 [2,1088(15) и 2,1269(15) Å] сопоставимы с наблюдаемыми в 2 [2,1137(17) и 2,1232(18) Å], в 3 [2,0880(14) и 2,1063(14) Å] и несколько отличными для 4 [2,1035(17) и 2,1460(17) Å]. Сольватные молекулы бензола в 4 связывают собой соседние молекулы дикарбоксилатов [расстояния С∙∙∙H и Сl∙∙∙H равны 2,84 Å и 3,06 Å, что меньше суммы ковалентных радиусов атомов-партнеров. Атом сурьмы координирует карбонильные атомы кислорода со стороны малых экваториальных углов (115,31(9)° и 119,59(9)°), при этом внутримолекулярные контакты Sb∙∙∙O=C составляют 3,374(3) и 3,296(3) Å, что больше внутримолекулярных контактов Sb—OMe (3,079-3,172 А). Отметим, что подобное различие внутримолекулярных контактов Sb∙∙∙O и Sb∙∙∙OMe наблюдается и в первых трех молекулах комплексов [3,296(3), 3,374(3) А и 3,102-3,167 А для 1, 3,010(3), 3,164(3) А и 3,058-3,202 А для 2 и 3,190(3), 3,233(3) А и 3,056-3,120 А для 3]. Внутримолекулярные контакты Sb—О=С между центральным атомом металла и карбонильным атомом кислорода наибольшие в 1 и 4, что можно объяснить присутствием электроак-цепторных карбоксилатных лигандов. Полные таблицы координат атомов, длин связей и валентных углов для структур депонированы в Кембриджском банке структурных данных (№ 2416266 (1), № 2415652 (2), № 2415732 (3), № 2415648 (4), ; .
Органические соединения Sb(V) применяются в различных областях. Так, хорошо изучены полезные свойства дикарбоксилатов триарилсурьмы, которые представлены многочисленным рядом [1]. Например, установлена их способность выступать арилирующими агентам в реакциях кросс-сочетания, катализируемых палладием, для образования как новых углерод-углеродных связей [2–8], так и связей углерода с гетероатомами (C–B [9] и C–P [10]). Установлена биологическая активность некоторых дикарбоксилатов триарилсурьмы [11], например, противоопухоле- вое [12] или антилейшманиозное действие [13]. Опубликованы примеры использования сурьма-органических производных непредельных карбоновых кислот, способных к полимеризации, в фотолитографии в качестве высокочувствительных УФ-резистов [14] и для получения прозрачных металлосодержащих органических стекол и полимеров [15]. Исследована возможность использования дикарбоксилатов триарилсурьмы в качестве фотокатализаторов при разложении красителей [16].
Особенности строения дикарбоксилатов триорганилсурьмы описаны многократно [17 - 27]; в большей мере, безусловно, это касается фенильных производных c карбоксилатными лигандами разнообразного строения. Тем не менее, из имеющихся публикаций следует, что искажение три-гонально-бипирамидальной конфигурации молекул дикарбоксилатов в значительной степени определяется природой карбоксилатных остатков и заместителей в арильных группах [28 - 32].
Соединения сурьмы общей формулы Ar 3 Sb[OC(O)R] 2 , содержащие в арильных лигандах при атоме сурьмы различные функциональные группы, изучены в меньшей степени, хотя именно в строении этих соединений чаще всего встречаются интересные особенности [31 - 32].
Целью настоящей работы явился синтез и установление особенностей строения дикарбоксилатов трис (2-метоксифенил)сурьмы, которые в настоящий момент практически не изучены и описаны на единственном примере [33].
Экспериментальная часть
К раствору 0,100 г (0,23 ммоль) трис (2-метоксифенил)сурьмы и 0,069 г (0,45 ммоль) хлоруксусной кислоты в 25 мл тетрагидрофурана прибавляли 0,040 г (0,23 ммоль) трет бутилгидропероксида и выдерживали 24 ч при комнатной температуре. Удаляли растворитель, остаток перекристаллизовали из смеси бензол - октан (3:1 объем.). Масса образовавшихся бесцветных кристаллов бис (2-хлорацетат) трис (2-метоксифенил)сурьмы ( 1 ) с т. пл. 174 ° С составила 0,12 г (85%). ИК-спектр, v , см - 1: 3001, 2951, 1697, 1659, 1582, 1481, 1464, 1435, 1408, 1377, 1327, 1285, 1257, 1215, 1184, 1185, 1126, 1059, 1020, 931, 795, 754, 694, 575, 519, 482, 447. Найдено, %: С 47,52; Н 4,17. C 25 H 25 O 7 Cl 2 Sb. Вычислено, %: С 47,61; Н 3,97.
Аналогично получали бис (2-метоксибензоат) трис (2-метоксифенил)сурьмы ( 2 ) (т.пл. 136 ° С, 83 %, ИК-спектр, v , см - 1: 3109, 3067, 2957, 2833, 1624, 1597, 1580, 1481, 1468, 1435, 1327, 1254, 1180, 1165, 1143, 1138, 1097, 1053, 1020, 997, 849, 795, 748, 702, 684, 565, 536, 480, 440. Найдено, %: С 50,38; Н 4,82. C 37 H 35 O 9 Sb. Вычислено, %: С 50,56; Н 4,70).
Бис (2,3-дифторбензоат) трис (2-метоксифенил)сурьмы ( 3 ) (растворитель - диэтиловый эфир, т.пл. 179 ° С, 76 %, ИК-спектр, v , см - 1: 3084, 2963, 2837, 1655, 1581, 1481, 1431, 1335, 1312, 1269, 1250, 1225, 1182, 1151, 1123, 1061, 951, 833, 783, 758, 631, 571, 517, 482, 459, 442. Найдено, %: С 55,37; Н 3,63. C 35 H 27 O 7 F 4 Sb. Вычислено, %: С 55,46; Н 3,57).
Сольват бис (пентафторбензоата) трис (2-метоксифенил)сурьмы с бензолом ( 4 ) (т.пл. 115 ° С, 86 %, ИК-спектр, v , см - 1: 3065, 2941, 2837, 1688, 1649, 1582, 1522, 1499, 1479, 1435, 1329, 1279, 1252, 1180, 1163, 1126, 1105, 1057, 1015, 995, 922, 862, 825, 795, 746, 694, 573, 519, 484, 445. Найдено, %: С 50,39; Н 2,73. C 38 H 24 O 7 F 10 Sb. Вычислено, %: С 50,42; Н 2,65).
Элементный анализ проводили на анализаторе Euro EA3028-НТ.
Рентгеноструктурный анализ проводили на автоматическом четырехкружном дифрактометре Bruker D8 QUEST (Mo [С.-излучение. X = 0,71073 А, графитовый монохроматор). Сбор, редактирование данных и уточнение параметров элементарной ячейки, а также учет поглощения проведены по программам SMART и SAINT-Plus [34]. Все расчеты по определению и уточнению структуры выполнены по программам SHELXL/PC [35] и OLEX2 [36]. Структуры определены прямым методом и уточнены методом наименьших квадратов в анизотропном приближении для неводородных атомов. Кристаллографические данные и результаты уточнения структур приведены в табл. 1, длины связей и валентные углы – в табл. 2. Полные таблицы координат атомов, длин связей и валентных углов для структур депонированы в Кембриджском банке структурных данных (№ 2416266 (1), № 2415652 (2), № 2415732 (3), № 2415648 (4), ; .
Таблица 1
|
Параметр |
1 |
2 |
3 |
4 |
|
Формула |
C 25 H 25 O 7 Cl 2 Sb |
C 37 H 35 O 9 Sb |
C 35 H 27 O 7 SbF 4 |
C 38 H 24 O 7 F 10 Sb |
|
М |
630,10 |
745,40 |
757,32 |
904,32 |
|
Сингония |
Триклинная |
Моноклинная |
Моноклинная |
Триклинная |
|
Пр. группа |
P -1 |
P 2 1 / n |
P 2 1 / n |
P -1 |
|
a , Å |
9,561(4) |
19,241(8) |
12,179(9) |
11,323(7) |
|
b, Å |
10,465(6) |
8,975(4) |
16,878(8) |
13,101(4) |
|
c, Å |
15,315(6) |
20,725(11) |
15,673(9) |
13,624(5) |
|
α, град. |
101,28(2) |
90,00 |
90,00 |
112,437(12) |
|
β, град. |
102,982(19) |
113,485(16) |
99,985(15) |
101,948(19) |
|
γ, град. |
108,150(19) |
90,00 |
90,00 |
91,20(2) |
|
V , Å3 |
1359,3(11) |
3292(3) |
3172,9(11) |
1816,3(14) |
|
Z |
2 |
4 |
4 |
2 |
|
ρ (выч.), г/см3 |
1,539 |
1,508 |
1,585 |
1,653 |
|
µ , мм–1 |
1,252 |
0,897 |
0,942 |
0,860 |
|
F (000) |
632,0 |
1520,0 |
1520,0 |
898,0 |
|
Размер кристалла (мм) |
0,43 × 0,31 × 0,24 |
0,5 × 0,35 × 0,32 |
0,53 × 0,36 × 0,17 |
0,5 × 0,47 × 0,07 |
|
Область сбора данных по 2 θ , град. |
5,7–93,66 |
5,88–65,36 |
5,8–73,02 |
6,06–60,38 |
|
Интервалы индексов отражений |
- 19 ≤ h ≤ 19, - 21 ≤ k ≤ 21, - 31 ≤ l ≤ 31 |
- 29 ≤ h ≤ 29, - 13 ≤ k ≤ 13, - 31 ≤ l ≤ 31 |
- 20 ≤ h ≤ 20, - 28 ≤ k ≤ 28, - 16 ≤ l ≤ 26 |
- 15 ≤ h ≤ 15, - 17 ≤ k ≤ 17, - 18 ≤ l ≤ 17 |
|
Измерено отражений |
103548 |
71613 |
64893 |
24210 |
|
Независимых отражений |
24228 |
11982 |
15486 |
9369 |
|
Переменных уточнения |
319 |
429 |
427 |
508 |
|
GOOF |
1,033 |
1,064 |
1,002 |
1,084 |
|
R -факторы по F 2 > 2 σ ( F 2) |
R 1 = 0,0502, wR 2 = 0,1052 |
R 1 = 0,0437, wR 2 = 0,0759 |
R 1 = 0,0409, wR 2 = 0,0783 |
R 1 = 0,0333, wR 2 = 0,0652 |
|
R -факторы по всем отражениям |
R 1 = 0,1061, wR 2 = 0,1262 |
R 1 = 0,0795, wR 2 = 0,0870 |
R 1 = 0,0982, wR 2 = 0,0973 |
R 1 = 0,0456, wR 2 = 0,0698 |
|
Остаточная электронная плотность (min/max), e /Å3 |
1,18/ - 1,08 |
0,65/ - 0,79 |
1,07/ - 0,63 |
0,43/ - 0,62 |
Таблица 2
|
Связь d , Å \ |
Угол ω , град. |
||
|
1 |
|||
|
Sb(1)–O(5) |
2,1269(15) |
O(7)Sb(1)O(5) |
175,15(5) |
|
Sb(1)–O(7) |
2,1088(15) |
C(1)Sb(1)C(11) |
111,15(7) |
|
Sb(1)–C(1) |
2,0966(17) |
C(1)Sb(1)C(21) |
125,87(7) |
|
Sb(1)–C(11) |
2,1194(18) |
C(11)Sb(1)C(21) |
122,95(7) |
|
Sb(1)–C(21) |
2,1181(18) |
O(5)Sb(1)С(1) |
88,35(7) |
|
O(4) - С(31) |
1,212(3) |
O(5)Sb(1)С(11) |
83,12(7) |
|
O(5) - С(31) |
1,295(2) |
O(5)Sb(1)С(21) |
96,06(7) |
|
O(6) - С(33) |
1,206(2) |
O(7)Sb(1)С(1) |
86,91(6) |
|
O(7) - С(33) |
1,298(2) |
O(7)Sb(1)С(11) |
97,68(7) |
|
Sb(1)∙∙∙O(1) |
3,113(5) |
O(7)Sb(1)С(21) |
87,53(7) |
|
Sb(1)∙∙∙O(2) |
3,103(5) |
О(4)С(31)О(5) |
125,68(19) |
Окончание табл. 2
|
Связь d , Å |
Угол ω , град. |
||
|
Sb(1)∙∙∙O(3) |
3,127(6) |
О(6)С(33)О(7) |
124,96(19) |
|
Sb(1)∙∙∙O(4) |
3,167(5) |
||
|
Sb(1)∙∙∙O(6) |
3,102(5) |
||
|
2 |
|||
|
Sb(1)–O(5) |
2,1232(18) |
O(7)Sb(1)O(5) |
171,42(6) |
|
Sb(1)–O(7) |
2,1137(17) |
C(1)Sb(1)C(11) |
131,29(10) |
|
Sb(1)–C(1) |
2,115(2) |
C(1)Sb(1)C(21) |
119,48(9) |
|
Sb(1)–C(11) |
2,104(2) |
C(11)Sb(1)C(21) |
108,99(10) |
|
Sb(1)–C(21) |
2,126(2) |
O(5)Sb(1)C(1) |
91,05(8) |
|
O(4)–C(48) |
1,218(3) |
O(5)Sb(1)C(21) |
85,61(9) |
|
O(5)–C(48) |
1,301(3) |
O(5) Sb(1) C(11) |
87,90(9) |
|
O(8)–C(58) |
1,218(3) |
O(7)Sb(1)C(1) |
87,99(8) |
|
O(7)–C(58) |
1,294(3) |
C(11)Sb(1)O(7) |
86,34(8) |
|
Sb(1)∙∙∙O(4) |
3,058(5) |
O(7)Sb(1)C(21) |
102,28(9) |
|
Sb(1)∙∙∙O(8) |
3,010(5) |
О(4)С(48)О(5) |
123,3(2) |
|
Sb(1)∙∙∙O(1) |
3,058(5) |
O(7)С(58)О(8) |
122,7(2) |
|
Sb(1)∙∙∙O(2) |
3,164(5) |
||
|
Sb(1)∙∙∙O(3) |
3,202(6) |
||
|
3 |
|||
|
Sb(1)–O(4) |
2,1063(14) |
O(4)Sb(1)O(6) |
176,97(6) |
|
Sb(1)–O(6) |
2,0880(14) |
C(1)Sb(1)C(11) |
128,22(8) |
|
Sb(1)–C(1) |
2,11134(19) |
C(1)Sb(1)C(21) |
114,46(7) |
|
Sb(1)–C(21) |
2,0889(19) |
C(11)Sb(1)C(21) |
117,32(8) |
|
Sb(1)–C(11) |
2,105(2) |
O(4)Sb(1)С(1) |
88,93(7) |
|
O(4)–C(37) |
1,287(2) |
O(4)Sb(1)C(11) |
96,23(7) |
|
O(5)–C(37) |
1,204(3) |
O(4)Sb(1) C(21) |
84,16(7) |
|
O(6)–C(47) |
1,295(3) |
O(6)Sb(1)C(1) |
88,32(7) |
|
O(7)–C(47) |
1,204(3) |
O(6)S(1)C(11) |
84,48(7) |
|
Sb(1)∙∙∙O(5) |
3,190(5) |
O(6)Sb(1)C(21) |
98,14(7) |
|
Sb(1)∙∙∙O(7) |
3,233(6) |
O(4)C(37)O(5) |
124,5(2) |
|
Sb(1)∙∙∙O(1) |
3,056(5) |
O(6)C(47)O(7) |
125,5(2) |
|
Sb(1)∙∙∙O(2) |
3,019(5) |
||
|
Sb(1)∙∙∙O(3) |
3,120(6) |
||
|
4 |
|||
|
Sb(1)–O(4) |
2,1460(17) |
O(6)Sb(1)O(4) |
164,47(6) |
|
Sb(1)–O(6) |
2,1035(17) |
C(1)Sb(1)C(11) |
115,31(9) |
|
Sb(1)–C(1) |
2,109(2) |
C(1)Sb(1)C(21) |
125,10(9) |
|
Sb(1)–C(11) |
2,119(2) |
C(11)Sb(1)C(21) |
119,59(9) |
|
Sb(1)–C(21) |
2,123(2) |
O(4)Sb(1)C(1) |
83,40(8) |
|
O(4)–C(37) |
1,293(3) |
O(4)Sb(1)C(11) |
100,46(9) |
|
O(5)–C(37) |
1,208(3) |
O(4)Sb(1)C(21) |
86,70(8) |
|
O(6)–C(47) |
1,308(3) |
O(6)Sb(1)C(1) |
90,06(8) |
|
O(7)–C(47) |
1,208(3) |
O(6)Sb(1)C(11) |
95,07(0) |
|
Sb(1)∙∙∙O(5) |
3,296(5) |
O(6)Sb(1)C(21) |
85,58(8) |
|
Sb(1)∙∙∙O(7) |
3,374(6) |
O(4)C(37)O(5) |
126,7(2) |
|
Sb(1)∙∙∙O(1) |
3,079(5) |
O(6)C(47)O(7) |
127,0(2) |
|
Sb(1)∙∙∙O(2) |
3,172(5) |
||
|
Sb(1)∙∙∙O(3) |
3,126(6) |
||
Обсуждение результатов
Дикарбоксилаты триарилсурьмы получают, как правило, или по реакциям замещения, действуя на дигалогениды или дигидроксиды триарилсурьмы солями карбоновых кислот [22, 30, 37], или по реакции окислительного присоединения из триарильных соединений сурьмы, карбоновой кислоты и пероксида как окислителя [38].
Для синтеза карбоксилатов трис (2-метоксифенил)сурьмы нами был выбран окислительный метод как наиболее эффективный и менее трудоемкий, поскольку протекает в одну стадию и позволяет получить достаточно чистый продукт. В качестве окислителя был испльзован трет бутилгидропероксид, растворителем служили тетрагидрофуран или диэтиловый эфир. Нами получены бис (2-хлорацетат) трис (2-метоксифенил)сурьмы ( 1 ), бис (2-метоксибензоат) трис (2-метоксифенил)сурьмы ( 2 ), бис (2,3-дифторбензоат) трис (2-метоксифенил)сурьмы ( 3 ) и бис (пентафторбензоата) трис (2-метоксифенил)сурьмы, который был выделен в форме сольвата с бензолом ( 4 ).
(2-MeOC 6 H 4 ) 3 Sb + 2 HOC(O)R + t -BuOOH → (2-MeOC 6 H 4 ) 3 Sb[OC(O)R] 2 + t -BuOH + H 2 O
CH 2 Cl ( 1 ), C 6 H 4 (OMe-2) ( 2 ), C 6 H 3 F 2 -2,3 ( 3 ), C 6 F 5 ( 4 )
Целевые соединения после перекристаллизации из смеси бензол - октан выделяли с выходами 76 - 89 % в виде бесцветных кристаллических веществ, растворимых в ароматических углеводородах и нерастворимых в алканах.
Соединения 1 - 4 были охарактеризованы методами ИК-спектроскопии и рентгеноструктурного анализа.
Найдено, что в молекулах 1 - 4 атомы сурьмы имеют координацию искаженной тригональной бипирамиды, в аксиальных положениях которой находятся карбоксилатные лиганды (рис. 1 - 4).
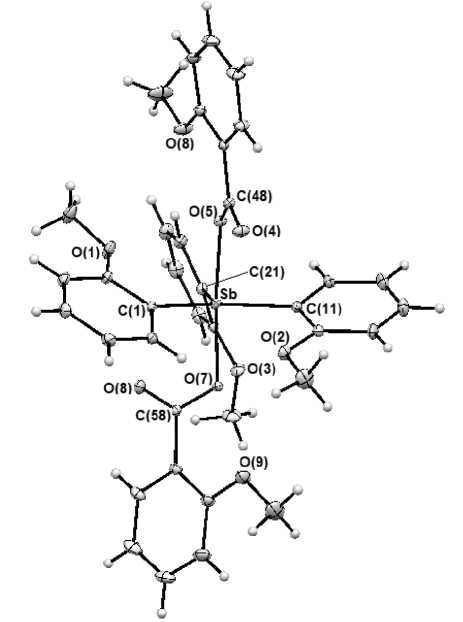
Рис. 2. Строение молекулы (2-MeOC 6 H 4 ) 3 Sb[OC(O)C 6 H 4 (OMe-2)] 2 (2)
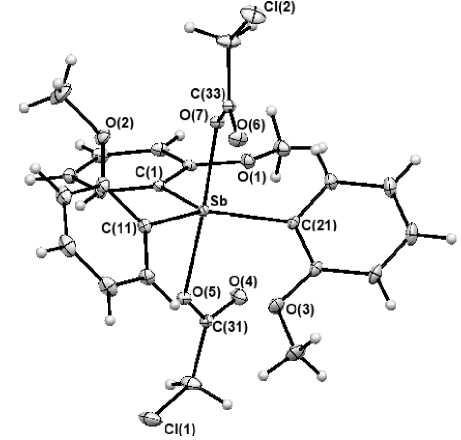
Рис. 1. Строение молекулы (2-MeOC 6 H 4 ) 3 Sb[OC(O)CH 2 Cl] 2 (1)
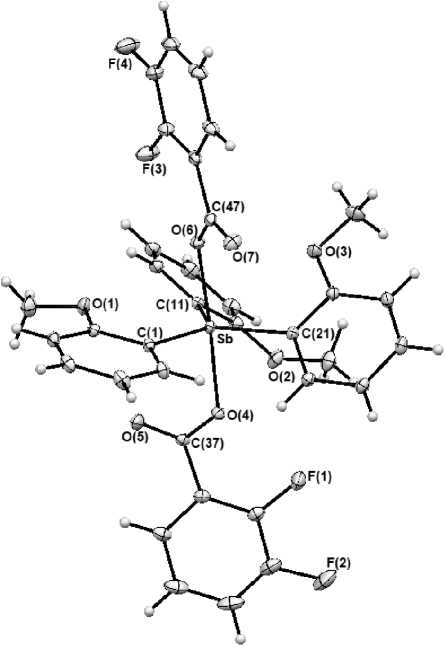
Рис. 3. Строение комплекса (2-MeOC 6 H 4 ) 3 Sb[OC(O)C 6 H 3 F 2 -2,3] 2 (3)
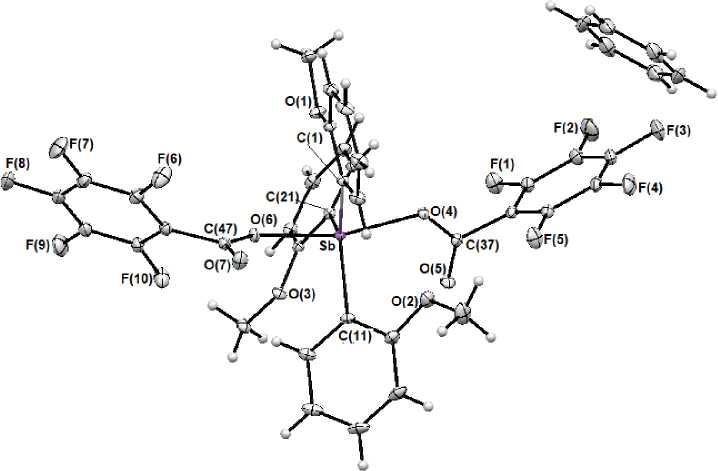
Рис. 4. Строение сольвата (2-MeOC 6 H 4 ) 3 Sb[OC(O)C 6 F 5 ] 2 ∙ ½PhH (4)
Аксиальные углы OSbO отличаются от линейного угла и составляют 175,15(5)°, 171,42(6)°, 176,97(6)°, 164,47(6)° в 1-4 соответственно. Валентные углы СSbС в экваториальной плоскости изменяются в интервалах 111,15(7)°-125,87(7)° (1), 108,99(10)°-131,29(10)° (2), 114,46(7)°-128,22(8)° (3), 115,31(9)°-125,10(9)° (4), а их суммы практически равны 360°. Выходы атомов сурьмы из экваториальной плоскости характеризуются малыми значениями: 0,019 Å, 0,059 А, 0,002 А, 0,003 А (в 1-4 соответственно). Интервалы изменения углов OSbC между эква- ториальными и аксиальными связями составляют 83,12(7)°-97,68(7)° (1), 85,61(9)°-102,28(9)° (2), 84,16(7)°-98,14(7)° (3), 83,40(8)°-100,46(9)° (4).
Расположение арильных колец относительно экваториальной плоскости во всех молекулах похоже: одно из арильных колец отклоняется от плоскости [C(1)C(11)C(21)] на угол чуть больше 10 ° (11,51 ° ( 1 ), 14,13 ° ( 3 ), 9,79 ° ( 4 ), за исключением 2 , где этот угол равен 23,71 ° ), два других арильных кольца составляют с экваториальной плоскостью большие углы (42,01 ° , 49,55 ° ( 1 ), 32,29 ° , 66,07 ° ( 2 ), 39,01 ° , 43,81 ° ( 3 ), (35,85 ° , 56,10 ° ( 4 )).
Известно, что для соединений с пентакоординированным центральным атомом возможны две конфигурации молекул: квадратная пирамида а и тригональная бипирамида б (рис. 5), энергии которых часто близки между собой, однако вторая оказывается энергетически немногим более стабильной, чем первая [39].
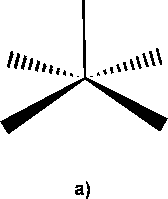
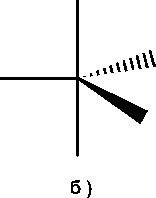
Рис. 5. Конфигурации квадратной пирамиды (а) и тригональной бипирамиды (б)
Для производных сурьмы общей формулы Ar3SbX2, где Х - электротрицательная группа, характерна, как правило, искаженная тригонально-бипирамидальная конфигурация [28]. Оценить степень искажения тригонально-бипирамидальной конфигурации и вклад в нее конфигурации квадратной пирамиды позволяет структурный параметр т, предложенный в работе [40], который определяется как отношение (а - в)/60, где а и в — величины двух наибольших углов между связями при атоме Sb (а > в). Для идеальной тетрагональной пирамиды т = 0 (а = в = 90 ° ), а в случае идеальной тригональной бипирамиды τ = 1 (аксиальный угол α = 180°, экваториальный β = 120°). Значения параметра т для исследуемых соединений 1 - 4 приведены в табл. 3.
Таблица 3
Валентные углы (град) в молекулах (2-MeOC 6 H 4 ) 3 Sb[OC(O)R] 2 и значение структурного параметра т
|
Соединение |
OSbO |
C(1)SbC(11) |
C(1)SbC(21) |
C(11)SbC(21) |
т |
|
1 |
175,15(5) |
111,15(7) |
125,87(7) |
122,95(7) |
0,82 |
|
2 |
171,42(6) |
131,29(10) |
119,48(9) |
108,99(10) |
0,67 |
|
3 |
176,97(6) |
128,22(8) |
114,46(7) |
117,32(8) |
0,76 |
|
4 |
164,47(6) |
115,31(9) |
125,10(9) |
119,59(9) |
0,65 |
В соответствии с рассчитанными значениями т , вклады тетрагонально-пирамидальной конфигурации в координационное окружение атома сурьмы в 1 - 4 составляют 18 - 35%.
Расстояния Sb-C, как и следовало ожидать, в молекулах 1 - 4 мало отличаются: 2,0966(17)-2,1194(18) А, среднее значение 2,111 А ( 1 ), 2,104(2)-2,126(2) А, 2,115 А ( 2 ), 2,0889(19)-2,1134(19) А, 2,102 А ( 3 ) и 2,109(2)-2,123(2) А, 2,117 А ( 4 ). Средние значения длин связей Sb-О в 1 - 4 равны 2,118(2) А (2,1088(15) и 2,1269(15) А), 2,118(2) А (2,1137(17) и 2,1232(18) А), 2,097(1) А (2,0880(14) и 2,1063(14) А), 2,125(2) А (2,1035(17) и 2,1460(17) А).
Известно, что карбоксилатные лиганды склонны к бидентатной координации на атом металла [28]. При этом в дикарбоксилатах триарилсурьмы лиганды, как правило, проявляют анизоби-дентатный характер связывания с высококой асимметрией координации. Лишь в редких случаях два расстояния М - О близки друг другу [7, 41, 42].
В молекулах 1-4 карбоксилатныые лиганды координированы асимметрично. В ряду 1-4 расстояния между атомом сурьмы и атомами кислорода карбонильных групп Sb---O=C увеличиваются 3,102 и 3,167 Å, 3,010 и 3,058 Å, 3,190 и 3,123 Å, 3,296 и 3,374 Å, что согласуется с возрас- танием электроноакцепторных свойств групп R в кислотах, уменьшающих донорные способности карбонильного атома кислорода.
Особеностью строения молекул 1 - 4 можно считать ориентацию карбоксильных групп относительно экваториальной плоскости. Так, в подавляющем большинстве дикарбоксилатов трифе-нилсурьмы углы между плоскостями карбоксильных групп ОСО не превышают 10 ° [28]. В 1 - 4 такие углы составляют 49,19 ° , 52,36 ° , 40,94 ° , 79,20 ° соответственно. Аналогичные большие значения указанных углов наблюдали в молекулах дикарбоксилатов трис (5-бром-2-метоксифенил)сурьмы [31 - 32], что, очевидно, обусловлено наличием метокси-групп в орто -положениях ароматических колец, которые создают стерические затруднения при ориентации карбоксилатных лигандов. Отметим, что расстояния Sb-OMe (3,103(2) - 3,127(2) А 1 , 3,058(2) - 3,202(2) А 2 , 3,019(2) - 3,120(2) А 3 , 3,079(2) - 3,172(3) А 4 ) меньше суммы ван-дер-ваальсовых радиусов атомов сурьмы и кислорода (3,58 Å [43]).
Основными межмолекулярными взаимодействиями в кристаллах 1 - 4 являются слабые водородные связи типа С - H- ' O и С - H- ' F. В кристалле 4 молекулы бензола участвуют в С - Н---Л-взаимодействиях типа «торец к плоскости», при этом расстояния между центроидами ароматических колец бензола и [С(21) - С(26)] молекулы бис (пентафторбензоата) трис (2-метоксифенил)сурьмы равны 4,89 А, а углы между плоскостями - 88,24 ° .
В ИК-спектрах дикарбоксилатов трис (2-метоксифенил)сурьмы 1 - 4 присутствуют интенсивные полосы поглощения, относящиеся к валентным колебаниям связи С=О: 1697, 1624, 1655, 1668 см–1 соответственно. По сравнению с колебаниями связи С=О в соответствующих карбоновых кислотах (1734, 1697, 1695, 1721 см-1) полоса поглощения в спектрах 1 - 4 смещена в низкочастотную область. Наличие фрагмента SbC 3 характеризуется присутствием в спектрах полос поглощения, находящихся в интервале 440–447 см–1. Наличие связей Sb–O подтверждается полосой поглощения в области 575–536 см–1.
Выводы
Окисление трис (2-метоксифенил)сурьмы трет -бутилгидропероксидом в присутствии хлоруксусной, 2-метоксибензойной, 2,3-дифторбензойной и пентафторбензойной кислот приводит к образованию дикарбоксилатов трис (2-метоксифенил)сурьмы с высокими выходами. В ИК-спектрах дикарбоксилатов трис (2-метоксифенил)сурьмы имеет место смещение полосы поглощения карбонильной группы по сравнению с аналогичной полосой в спектрах соответствующих кислот на 37 - 73 см-1. Атомы сурьмы в молекулах 1 - 4 имеют тригонально-бипирамидальную конфигурацию, искажение которой обусловлено вкладом тетрагонально-пирамидальной конфигурации (18 - 35 %). Карбоксилатные лиганды проявляют анизобидентатный характер связывания с атомом сурьмы (разница расстояний Sb - O и Sb—O=C составляет от 0,896 до 1,270 А). Особенностью строения молекул дикарбоксилатов трис (2-метоксифенил)сурьмы можно считать необычные для дикарбоксилатов триарилсурьмы большие значения углов между плоскостями карбоксильных групп, которые составляют 40,94 °- 79,20 ° . Кроме того, наличие коротких внутримолекулярных расстояний Sb—O=C и Sb-OMe позволяет записать координационное число атомов сурьмы как сумму двух координационных сфер 5+5.


