Окисление трис(2-метоксифенил)сурьмы трет-бутилгидропероксидом в присутствии 2-хлор-4-фторфенола
Автор: Шарутин В.В., Шарутина О.К., Бянкина М.Р., Кудряшов М.В., Сомов Н.В.
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Химия элементоорганических соединений
Статья в выпуске: 1 т.18, 2026 года.
Бесплатный доступ
Окисление трис(2-метоксифенил)сурьмы трет-бутилгидропероксидом в присутствии 2-хлор-4-фторфенола в тетрагидрофуране или диэтиловом эфире приводит к образованию бис(2-хлор-4-фторфенолята) трис(2-метоксифенил)сурьмы (2-MeOC6H4)3Sb(OC6H3Cl-2-F-4)2 (1) которая, после перекристаллизации из смеси бензол октан, была охарактеризована методами ИК-спектроскопии и рентгеноструктурного анализа (РСА). В ИК-спектре 1 присутствуют полосы, характеризующие колебания фрагмента SbC3 (434 см–1) и связей Sb–O (536 см–1). Кристаллографические характеристики 1 [C33H27Cl2F2O5Sb, M = 734,19; триклинная сингония, пр. гр. Р-1; параметры ячейки: a = 8,41080(10) Å, b = 9,3964(2) Å, c = 19,6967(2) Å; = 83,7850(10)°, β = 88,4990(10)°, = 81,8700(10)°; V = 1531,86(4) Å3, Z = 2; выч = 1,592 г/см3; = 1,128 мм–1; F(000) = 736; обл. сбора по : 2,648–30,505°; –11 ≤ h ≤ 12, –13 ≤ k ≤ 13, –28 ≤ l ≤ 28; всего отражений 41617; независимых отражений 8942 (Rint = 0,0426); GOOF = 1,035; R-фактор = 0,0215]. Из данных РСА в тригонально-бипирамидальных молекулах 1 с электроотрицательными лигандами в аксиальных положениях расстояния Sb−C составляют для 2,0973(12)−2,0996(13) Å; валентный угол OSbO равен 169,00(4)°. Расстояния Sb−О в [2,0686(9) и 2,0850(10) Å] сопоставимы с наблюдаемыми в подобных диароксидах триарилсурьмы. Экваториальные углы CSbC равны 109,56(5)°, 124,53(5)°, 125,87(5)°, сумма которых близка к 360°. Столь большое неравенство в экваториальных углах обусловлено присутствием внутримолекулярных контактов Sb∙∙∙OMe [3,000(3), 3,092(3) и 3,124 Å]. Полные таблицы координат атомов, длин связей и валентных углов для структуры 1 депонированы в Кембриджском банке структурных данных (№ 2478179 (1); deposit@ccdc.cam.ac.uk; http://www.ccdc. cam.ac.uk).
Трис(2-метоксифенил)сурьма, трет-бутилгидропероксид, 2-хлор-4-фторфенол, диароксид трис(2-метоксифенил)сурьмы, синтез, рентгеноструктурный анализ
Короткий адрес: https://sciup.org/147253372
IDR: 147253372 | УДК: 546.865+547.53.024+548.312.5 + 548.73 | DOI: 10.14529/chem260106
Oxidation of tris(2-methoxyphenyl)antimony by tert-butyl hydroperoxide in the presence of 2-chloro-4-fluorophenol
Oxidation of tris(2-methoxyphenyl)antimony by tert-butyl hydroperoxide in the presence of 2-chloro-4-fluorophenol in tetrahydrofuran or diethyl ether led to formation of tris(2-methoxyphenyl)antimony bis(2-chloro,4-fluorophenolate) (2-MeOC6H4)3Sb[OC6H3(Cl-2)(F-4)]2 (1), which, after recrystallization from a benzene-octane mixture, was characterized by IR spectroscopy and X-ray dif-fraction analysis. The IR spectrum of 1 contains bands characterizing vibrations of the SbC3 fragment (434 cm–1) and Sb–O bonds (536 cm–1), respectively. Crystallographic characteristics of 1 [C33H27Cl2F2O5Sb, M = 734.19; triclinic syngony, space group P-1; cell parameters: a = 8.41080(10) Å, b = 9.3964(2) Å, c = 19.6967(2) Å; = 83.7850(10)°, β = 88.4990(10)°, = 81.8700(10)°; V = 1531.86(4) Å3, Z = 2; calc = 1.592 g/cm3; = 1.128 mm–1; F(000) = 736; collection area by 2: 2.648–30.505°; –11 ≤ h ≤ 12, –13 ≤ k ≤ 13, –28 ≤ l ≤ 28; total reflections 41617; independent reflections 8942 (Rint = 0.0426); GOOF = 1.035; R-factor = 0.0215]. According to the X-ray diffraction data, the Sb−C distances in trigonal bipyramidal molecules 1 with electronegative ligands in axial positions are 2.0973(12)−2.0996(13) Å; the OSbO bond angle is 169.00(4)°. The Sb−O distances [2.0686(9) and 2.0850(10) Å] are comparable with those observed in similar triarylantimony diaroxides. The CSbC equatorial angles are 109.56(5)°, 124.53(5)°, 125.87(5)°, the sum of which is close to 360°. Such a large inequality in the equatorial angles is due to the presence of intramolecular contacts Sb∙∙∙OMe [3.000(3), 3.092(3), and 3.124 Å]. Complete tables of atomic coordinates, bond lengths and bond angles for structure 1 have been deposited with the Cam-bridge Crystallographic Data Centre (no. 2478179; deposit@ccdc.cam.ac.uk; http://www.ccdc.cam.ac.uk).
Текст научной статьи Окисление трис(2-метоксифенил)сурьмы трет-бутилгидропероксидом в присутствии 2-хлор-4-фторфенола
Известно, что среди многочисленных известных арильных соединений сурьмы общей формулы Ar3SbX2 (X – остаток различных органических НО-кислот) бόльшую часть составляют производные карбоновых кислот (более 150); в меньшей степени представлены производные оксимов, сульфоновых кислот и фенолов [1]. Первые диароксиды трифенилсурьмы получали по реакциям замещения из дигалогенида трифенилсурьмы и соответствующего фенола. Таким методом синтезировали бис (2,4,6-трибромфенокси)трифенилсурьму Ph 3 Sb(OC 6 H 2 Br 3 -2,4,6) 2 с выходом 80 %, которая, как оказалось, является ингибитором воспламенения полиэтилена [2]. Установлено, что дихлорид трифенилсурьмы также реагирует с дигидроксибензолом - пирокатехином и его производными в присутствии сухого аммиака или другого акцептора хлороводорода с образованием хелатных комлексов [3 - 5]. В работе [6] приводится оригинальный метод синтеза диа-роксидов трифенилсурьмы с выходами 80 - 93 % из трифенилстибазосульфониларила Рh 3 Sb=NS(O) 2 Ar и фенола HOAr (Ar = C 6 H 5 , 4-ClC 6 H 4 , 4-BrC 6 H 4 , 4-NO 2 C 6 H 4 , 2,4-Br 2 C 6 H 3 , C 6 Cl 5 ).
Существует достаточно много публикаций, в которых описаны реакции окисления триарил-сурьмы замещенными орто- хинонами, продуктами которых являются катехолаты триарилсурь-мы, содержащие металлоцикл [SbO 2 C 2 ] [7 - 11].
Впервые окислительный метод синтеза, который заключается в окислении триарилсурьмы окислителем с одновременным введением в реакционную смесь органической НО-кислоты с использованием фенолов был осуществлен на примере дигидроксибензолов [12]. Авторами установлено, что строение продуктов реакции определяется расположением гидроксигрупп в ароматическом кольце: с пирокатехином образуется 5-членный орто -фенилендиоксид трифенилсурь-мы, с резорцином – макроциклическое соединение, при взаимодействии с гидрохиноном получается полимерный гидрохинолят трифенилсурьмы.
По реакции окислительного присоединения из трифенилсурьмы, фенола и пероксида водорода (мольное соотношение реагентов 1:2:1) были синтезированы три диароксида трифенил-сурьмы Ph 3 Sb(OAr) 2 , где Ar – C 6 H 5 , C 6 H 4 (NO 2 )-4, C 6 H 2 (NO 2 ) 3 -2,4,6 [13]. Автор отмечает, что получить диароксиды трифенилсурьмы с фенолами, имеющими электронодонорные заместители в кольце, не удалось.
В работе [14] описаны реакции трифенил- и три( пара -толил)сурьмы с полифункциональны-ми фенолами: 2,4,6-трибромфенолом, 4-ацетил-3-оксифенолом, 2-формил-4-бромфенолом в присутствии пероксида водорода. Показано, что наряду с диароксидами триарилсурьмы из реакционной смеси (соотношение исходных соединений 1:2:1 мольн.) выделяли µ -оксо бис [(ароксо)триарилсурьму], выход которой, например, в случае 2,4,6-трибромфенола достигал 44 %. Образование второго продукта - µ -оксо бис [(ароксо)триарилсурьмы] - авторы объяснили гидролитической неустойчивостью диароксидов триарилсурьмы, что подтвердили специальными экспериментами. Установлено, что при мольном соотношении реагентов в реакции триа-рилсурьмы, фенола и пероксида водорода 1:1:1 единственным сурьмаорганическим продуктом являлись биядерные соединения µ -оксо бис [(ароксо)триарилсурьмы] [Ar 3 Sb(OAr ′ )] 2 O, где Ar = Ph, p -Tol; Ar ′ = C 6 H 2 Br 3 -2,4,6, С 6 H 3 (CHO-2)(Br-4), С 6 H 3 (OH-3)(Ac-4), C 6 H 4 I-4.
Автор [15] детально исследовал реакции окислительного присоединения трис (4-метилфенил)-, трис (4-фторфенил)-, трис (3-фторфенил)- и трис (5-бром-2-метоксифенил)сурьмы и фенолов в присутствии трет- бутилгидропероксида. Установлено, что образование соединений Ar3Sb(OAr ′ )2 или [Ar3Sb(OAr ′ )]2O обусловлено влиянием совокупности ряда факторов: объем, природа, количество и расположение заместителей в ароксидном лиганде, а также природа функциональной группы в арильном радикале при атоме металла.
В настоящей работе впервые в реакции окислительного присоединения с фенолами использована трис (2-метоксифенил)сурьма и синтезирован бис (2-хлор-4-фтор-феноксид) трис (2-метоксифенил)сурьмы, строение которой доказано методами ИК-спектроскопии и рентгеноструктурного анализа.
Экспериментальная часть
Синтез бис (2-хлор-4-фтор-феноксида) трис (2-метоксифенил)сурьмы (1). К бензольному раствору 0,10 г (0,226 ммоль) трис (2-метоксифенил)сурьмы приливали раствор 0,066 г (0,451 ммоль) 2-хлор-4-фтор-фенола в бензоле и прибавляли 0,03 г 70%-ного водного раствора (0,226 ммоль) трет -бутилгидропероксида. Реакционную смесь выдерживали при комнатной температуре до испарения растворителя. Остаток промывали диэтиловым эфиром и после перекристаллизации из смеси бензол–октан (5:1 объемн.) выделяли бесцветные кристаллы бис (2-хлор-4-фтор-феноксида) трис (2-метоксифенил)сурьмы, выход 46 %, т. пл. 153 °C. Найдено, %: С 53,82; Н 3,70. C 33 H 27 Cl 2 F 2 O 5 Sb. Вычислено, %: С 53,94; Н 3,68. ИК-спектр ( ν , см–1): 3424, 3065, 3005, 2961, 2938, 2835, 1630, 1582, 1476, 1431, 1398, 1277, 1251, 1188, 1165, 1123, 1061, 1043, 1024, 907, 878, 864, 802, 750, 714, 681, 573, 536, 509, 478, 434.
Элементный анализ проводили на анализаторе Euro EA3028-НТ.
Рентгеноструктурный анализ кристаллов 1 проводили на автоматическом дифрактометре Rigaku XtaLab при 100 °К. Первичные фрагменты структур найдены методом двойного пространства в программных комплексах SHELX [16], ShelXle [17]. Параметры остальных атомов, включая атомы водорода, определены по разностному синтезу электронной плотности и уточнены по |F|2 методом наименьших квадратов. Положения водородных атомов уточнялись в основном цикле метода наименьших квадратов в изотропном приближении. Полные таблицы координат атомов, длин связей и валентных углов депонированы в Кембриджском банке структурных данных (ССDC 2478179); ; . Основные кристаллографические данные и результаты уточнения структуры 1 приведены в табл. 1, длины связей и валентные углы – в табл. 2.
Таблица 1
Кристаллографические данные, параметры эксперимента и уточнения структуры 1
|
Параметр |
1 |
|
Формула |
C 33 H 27 Cl 2 F 2 O 5 Sb |
|
М |
734,21 |
|
Сингония |
Триклинная |
|
Пр. группа |
гТ |
|
a , Å |
8,41080(10) |
|
b, Å |
9,3964(2) |
|
c, Å |
19,6067(2) |
Окончание табл. 1
|
Параметр |
1 |
|
α, град |
83,7850(10) |
|
β, град |
88,4990(10) |
|
γ, град |
81,8700(10) |
|
V , Å3 |
1531,86(4) |
|
Z |
2 |
|
ρ выч, г/см |
1,592 |
|
µ , мм–1 |
1,128 |
|
Поглощение Т/T max |
0,210 / 1,000 |
|
Учет поглощения |
Аналитический (Гаусс) |
|
F (000) |
736,0 |
|
Размер кристалла, мм |
0,719 × 0,392 × 0,128 |
|
Дифрактометр / Излучение / Монохроматор / тип сканирования |
Rigaku XtaLab, MM003, P200K / MoK α , λ = 0,71073 Å / MicroMax-003 / ω -сканирование |
|
Область сбора данных по θ , град. |
2,648–30,505 |
|
Интервалы индексов отражений |
- 11 ≤ h ≤ 12, - 13 ≤ k ≤ 13, - 28 ≤ l ≤ 28 |
|
Измерено отражений |
41617 |
|
Независимых отражений |
9327 |
|
R int |
0,0426 |
|
Переменных уточнения |
469 |
|
GOOF |
1,035 |
|
R -факторы по F 2 > 2 σ ( F 2) |
R 1 = 0,0215, wR 2 = 0,0575 |
|
R -факторы по всем отражениям |
R 1 = 0,0225, wR 2 = 0,0579 |
|
Остаточная электронная плотность (min/max), e /Å3 |
- 0,640/0,797 |
Таблица 2
Длины связей и валентные углы в структуре 1
|
Связь d , Å |
Угол ω , град |
||
|
Sb(1)–O(1) |
2,0686(9) |
С(20)Sb(1)C(27) |
109,56(5) |
|
Sb(1)–O(2) |
2,0850(10) |
C(27)Sb(1)C(13) |
124,53(5) |
|
Sb(1)–C(20) |
2,0973(12) |
C(20)Sb(1)C(13) |
125,87(5) |
|
Sb(1)–C(27) |
2,0983(12) |
O(1)Sb(1)O(2) |
169,00(4) |
|
Sb(1)–C(13) |
2,0996(13) |
O(1)Sb(1)С(20) |
89,68(5) |
|
С(1) - О(1) |
1,3377(16) |
O(1)Sb(1)С(27) |
86,52(4) |
|
C(7) - O(2) |
1,3228(17) |
O(1)Sb(1)С(13) |
91,50(4) |
|
C(33) - O(3) |
1,4238(18) |
O(2)Sb(1)С(20) |
96,00(5) |
|
C(19) - O(4) |
1,4226(17) |
O(2)Sb(1)С(27) |
82,70(4) |
|
C(26) - O(5) |
1,4193(18) |
O(2)Sb(1)С(13) |
92,78(5) |
|
C(32) - O(3) |
1,3630(17) |
С(1)O(1)Sb(1) |
130,40(8) |
|
C(18) - O(4) |
1,3615(16) |
С(7)O(2)Sb(1) |
134,61(9) |
|
C(25) - O(5) |
1,3622(17) |
||
Обсуждение результатов
Реакционная способность трис (2-метоксифенил)сурьмы в настоящее время изучена недостаточно. Например, ее реакции оксилительного присоединения с фенолами в литературе не описаны. Нами установлено, что взаимодействие 2-хлор-4-фторфенола с трис (2-метоксифенил)сурьмой в присутствии трет- бутилгидропероксида приводит к образованию бис (2-хлор-4-фторфеноксида) трис (2-метоксифенил)сурьмы ( 1 ) с выходом 46 % (после перекристаллизации из смеси бензол - октан). Для достижения гомогенности реакционной смеси в качестве растворителя был использован бензол, а не диэтиловый эфир, как обычно при проведении реакций окислительного присоединения с триарилсурьмой.
(2-MeOC 6 H 4 )3Sb + 2HOC 6 H 3 C1-2-F-4 + t -BuOOH ^ (2-MeOC6H4)3Sb(OC6H3Cl-2-F-4)2
Соединение 1 было выделено в виде бесцветных кристаллов с температурой плавления 153°С, растворимых в ароматических углеводородах и нерастворимых в алканах. Строение соединения 1 было охарактеризованы методами ИК-спектроскопии и рентгеноструктурного анализа.
В ИК-спектре наблюдались характерные полосы при 434 см–1 и 536 см–1, соответствующие валентным колебаниям связей Sb–С и Sb–О соответственно [18]. Колебания связи С Ar –О в фенолах находятся обычно при 1275–1150 см–1 [19]. В спектре соединения 1 обнаружены полосы 1251 и 1277 см-1, которые можно отнести к колебаниям связей С - О в ароксильных лигандах и арильных группах соответственно. Отметим, что в спектре трис (2-метоксифенил)сурьмы имеет место полоса 1269 см–1. Кроме того, в спектре имеют место полосы при 1024 см–1 и 1188 см–1, характеризующие колебания связей C - Cl и C-F соответственно [20].
По данным РСА, в молекулах 1 атомы сурьмы имеют координацию искаженной тригональной бипирамиды, в аксиальных положениях которой находятся более электроотрицательные арок-сильные лиганды (см. рисунок).
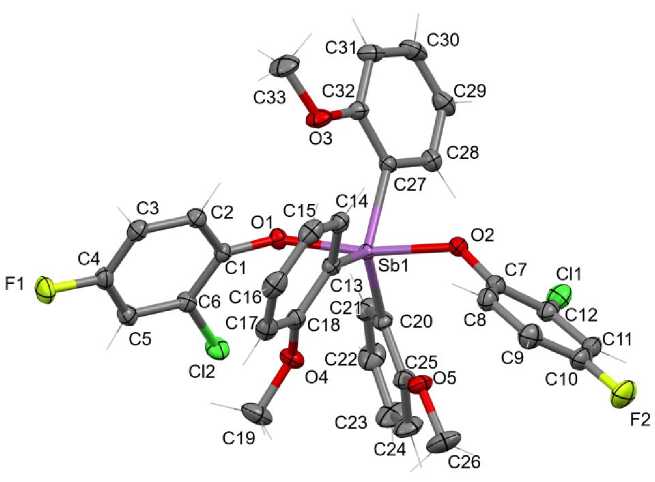
Строение молекулы (2-МеОС 6 Н 4 ) 3 Sb(OC 6 H 3 Cl-2-F-4) 2 (атомы водорода не показаны)
Аксиальный угол OSbO отличается от линейного угла и составляет 169,00(4) ° . Валентные углы CSbC в экваториальной плоскости равны 109,56(5); 124,53(5); 125,87(5) ° , а их сумма практически равна 360° (359,96(5)°). Выход атома сурьмы из экваториальной плоскости к атому О(2) характеризуются малым значением (0,024 Å), а интервал изменения углов OSbС между экваториальными и аксиальными связями составляет 82,70(4) - 96,00(5)°. Экваториальные связи Sb - C [2,0686(10)-2,0973(12) Å] меньше указанных расстояний в молекулах трис (2-метоксифенил)сурьмы (2,151(3) А [21]). Расстояния Sb - О [2,0686(9), 2,0850(10) А] несколько больше суммы ковалентных радиусов атомов-партнеров (2,05 Å [22]). Отметим, что наблюдаемые значения Sb - О попадают в интервал изменения указанных связей в молекулах Ar3Sb(OAr ' ) 2 , где Ar = Ph, 4-CH 3 C 6 H 4 , 4-FC 6 H 4 3-FC 6 H 4 ), а в группах Ar ' присутствуют один или два электроотрицательных заместителя [15].
Расстояния C A - О в арокси-группах равны 1,338(2) и 1,323(2) А, в арильных группах (1,362(2), 1,362(2), 1,363(2) Å) несколько больше.
Арильные кольца в экваториальной плоскости имеют пропеллерную конформацию, которая считается наиболее энергетически выгодной. Так, двугранные углы между экваториальной плос- костью [C(13)C(20)C(27)] и плоскостями [С(13)-С(18)], [С(20)-С(25)], [С(27)-С(32)] составляют 24,25; 37,77; 26,59°.
Обнаружено, что плоскость арильной группы [С(13) - С(18)] и плоскость арокси-группы [С(1) - С(6)] составляют угол 32,43°. Наблюдаемая конформация арильных заместителей при атоме сурьмы обеспечивает возможность взаимодействия ароматических систем ( π⋅⋅⋅π -стекинг). Согласно литературным данным, расстояние между центроидами ароматических π-систем при наличии π···π-стекинга варьирует в пределах 3,3–3,8 Å [23, 24], однако допускаются значения до 4 Å и более. В молекуле 1 расстояние между центрами π-систем арильного и ароксидного лигандов составляет 4,19 Å, а наименьшие расстояния С Ar ···C ArO [С(1) ⋅⋅⋅ С(13)] равно 3,21 Å. Косвенным доказательством взаимодействия можно считать уменьшение угла С(1)О(1)Sb (130,40(8)°) по сравнению с углом C(7)O(2)Sb (134,61(9)°). Наличие π⋅⋅⋅π -взаимодействия, вероятно, является причиной искажения экваториальных углов: углы С(13)SbC(20) и C(13)SbC(27) больше теоретического значения на ≈ 5 - 6°, а угол C(20)SbC(27) меньше на ≈ 10°.
Особенностью строения молекул 1 является присутствие внутримолекулярных контактов атомов кислорода метоксигрупп с центральным атомом (расстояния Sb∙∙∙OMe составляют 3,103(2) - 3,127(2) Å, что меньше суммы ван-дер-ваальсовых радиусов атомов сурьмы и кислорода [25]). В молекуле трис (2-метоксифенил)сурьмы аналогичные расстояния составляют 3,054(2) Å [21].
Основными межмолекулярными взаимодействиями в кристалле 1 являются слабые водородные связи типа С - Н ⋅⋅⋅ O и С - Н ⋅⋅⋅ F, количественные характеристики которых сведены в табл. 3.
Таблица 3
Параметры водородных связей в структуре 1
|
Атомы |
D–H, Å |
H···A, Å |
D···A, Å |
D–H···A, град. |
|
C(5)–H(5)···O(2)(I) |
0,94(2) |
2,46(2) |
3,3572(17) |
158,8(17) |
|
C(2)–H(2)···O(3) |
0,99(2) |
2,580(19) |
3,3961(17) |
139,4(15) |
|
C(26)–H(26A)···F(2)(II) |
0,97(3) |
2,55(3) |
3,414(2) |
148(2) |
|
C(3)–H(3)···F(1)(III) |
0,98(2) |
2,61(2) |
3,4939(17) |
149,1(16) |
Симметрично эквивалентные позиции: I) x, y+1, z; II) –x, –y+1, –z; III) –x, –y+2, –z+1.
Выводы
Окисление трис (2-метоксифенил)сурьмы трет -бутилгидропероксидом в присутствии 2-хлор-4-фторфенола приводит к образованию бис (2-хлор-4-фторфеноксида) трис (2-метоксифенил)сурьмы с выходом 46 %. Атомы сурьмы в молекулах 1 имеют тригонально-бипирамидальную конфигурацию c ароксильными лигандами в аксиальных положениях. Особенностью строения молекулы 1 является наличие π⋅⋅⋅π -взаимодействия между ароматическими системами, расположенными в экваториальном и аксиальном положениях, что приводит к искажению экваториальных углов. Кроме того, имеют место внутримолекулярные контакты Sb∙∙∙OMe.


