Олигонуклеотидные праймеры для детекции генов, кодирующих большую субъединицу бифенил 2,3-диоксигеназы, бактерий порядка Actinomycetales
Автор: Шумкова Екатерина Сергеевна, Плотникова Елена Генриховна
Журнал: Вестник Пермского университета. Серия: Биология @vestnik-psu-bio
Рубрика: Микробиология
Статья в выпуске: 1, 2012 года.
Бесплатный доступ
Бифенил 2,3-диоксигеназа (БДО) является ключевым ферментом, участвующим в разложении бифенила и полихлорированных бифенилов (ПХБ) у бактерий. Структура ее активного центра определяет спектр утилизируемых конгенеров ПХБ. Нами были подобраны вырожденные праймеры для скрининга бактерий-деструкторов порядка Actinomycetales на наличие генов bphA1, кодирующих большую субъединицу бифенил диоксигеназ.
Полихлорированные бифенилы (пхб), бифенил 2, 3-диоксигеназа, бактерии, порядок actinomycetales, вырожденные праймеры, гены bpha1
Короткий адрес: https://sciup.org/147204575
IDR: 147204575 | УДК: 579.25
Oligonucleotide primers for detection of biphenyl 2,3-dioxygenase large subunite encoding genes of bacteria belonging to the order Actinomycetales
Biphenyl 2,3-dioxygenase (BDO) is a key enzyme involved in bacterial degradation of biphenyl/polychlorinated biphenyl (PCB). The structure of the active site determines the range of recyclable PCB congeners. We have designed the degenerate PCR-primers to target a region, encoding the large subunit of biphenyl dioxygenase. The oligonucleotides will be applied to screen to BDO large subunit encoding genes of bacteria belonging to the order Actinomycetales
Текст научной статьи Олигонуклеотидные праймеры для детекции генов, кодирующих большую субъединицу бифенил 2,3-диоксигеназы, бактерий порядка Actinomycetales
Полихлорированные бифенилы (ПХБ) входят в число наиболее опасных абиотичесих веществ, созданных человеком. Это высокотоксичные соединения, мутагены, канцерогены. Благодаря исключительной стабильности, устойчивости к воздействию химических и физических факторов, ПХБ долго остаются в окружающей среде [Ross, 2004]. Несмотря на запрет производства ПХБ во многих странах, проблема их утилизации остается актуальной [Васильева, Стрижакова, 2007]. Всестороннее изучение микроорганизмов-деструкторов бифенила/ПХБ является перспективным для создания эффективных технологий очистки окружающей среды от данных соединений.
У ряда грамположительных и грамотрицатель-ных бактерий изучены ферментные системы, контролирующие разложение бифенила/ПХБ [Pieper, 2005]. Так, бифенил 2,3-диоксигеназа (БДО) является ферментом, катализирующим первую реакцию окисления одного из ароматических колец бифени-ла/ПХБ с образованием дигидродиольного производного. Изучению этого фермента уделяется особое внимание, так как он определяет спектр утилизируемых бактериями конгенеров ПХБ. Бифенил 2,3-диоксигеназа – мультикомпонентный фермент, состоящий из трех белков: терминальной оксигеназы (BphA1/BphA2), ферредоксина (BphA3) и ферредоксин редуктазы (BphA4). Терминальная оксигеназа содержит α- и β-субъединицы (кодируются генами bphA1 и bphA2 , соответственно) и является
α 3 β 3 гексамером [Seeger et al., 2001]. α-Субъединица БДО состоит из 458 – 468 АКО, которые образуют два домена [Zielinski et al., 2002]. N-концевой домен включает в себя железо-серный кластер Риске [2Fe-2S] (с 40 по 140 АКО у Spingobium yanoikyae B1). Два остатка гистидина и два цистеина координируют атомы железа и серы, входящие в этот кластер. С-концевой домен включает каталитический карман, в котором находится негемовое железо (II), координированное двумя остатками гистидина (His-207 и His-212) и одним остатком аспарагиновой кислоты (Asp-360) [Ferraro et al., 2007] (рис. 1). Предполагается, что размер и форма каталитического кармана напрямую влияют на спектр окисляемых ферментом субстратов и на эффективность взаимодействия [Jaconcic et al., 2007], а пространственная структура белка и, соответственно, структура активного центра, в свою очередь, определяется взаимодействием аминокислот. Известно, что замены определенных аминокислот, влекут за собой изменение структуры активного центра и, соответственно, спектра окисляемых субстратов [Kimura et al., 1997; Suenaga et al., 2002].
Большие субъединицы (α-субъединицы) негемовых железосодержащих диоксигеназ, способных осуществлять гидроксилирование бензольного кольца ароматических соединений, составляют большое семейство эволюционно родственных аминокислотных последовательностей, которые делятся на четыре подсемейства. Ферменты, осуществляющие гидроксилирование ароматического кольца бифенила/ПХБ, относятся к подсемейству бифе-
нил/толуол диоксигеназ (Б/Т ДО) [Gibson, Parales, 2000].
Однако есть данные о бифенил 2,3-диоксигена-зах бактерий родов Sphingomonas , Bacillus , Rhodo-coccus , существенно отличающихся от ферментов подсемейства Б/Т ДО и сходных с фенантрен- и нафталин диоксигеназами бактерий-деструкторов полициклических углеводородов [Romine et al., 1999; Mukerjee-Dhar et al., 2005; Taguchi et al., 2007; Yang et al., 2007]. Так, уровень сходства между недавно описанными генами, кодирующими БДО Rhodococcus sp. R04 и генами Rhodococcus sp. RHA1, БДО которого относится к ферментам подсемейства Б/Т ДО, составляет менее 44% [Yang et al., 2007].
Известно, что гены БДО грамположительных и грамотрицательных бактерий существенно отличаются. Так, по данным Е. Masai с соавторами [1995] БДО бактерий рода Rhodococcus более сходны с толуол диоксигеназами грамположительных бактерий, чем с бифенил диоксигеназами протеобакте-рий. Нами были выделены и охарактеризованы грамположительные бактерии порядка Actinomycetales , способные активно разлагать би-фенил/ПХБ [Плотникова и др., 1998; 2001; 2005;
Шумковa, 2009]. При изучении генетических систем деструкции данных соединений у ряда штаммов рода Rhodococcus , способных к активной деструкции бифенила/ПХБ, не были выявлены гены, присутствующие в геноме хорошо исследованных бактерий-деструкторов ПХБ. Так, отсутствовала специфическая амплификация гена bphA1 при использовании вырожденных праймеров, сконструированных на основе анализа известных последовательностей α-субъединиц гидроксилирующих диоксигеназ бифенила/толуола/бен-зола/изопропилбензола (подсемейство Б/Т ДО) [Witzig et al., 2006]. В то же время у ряда исследованных бактерий порядка Actinomycetales (рода Rhodococcus , Janibacter ), а также у грамотрицатель-ных бактерий-деструкторов рода Pseudomonas была амплифицирована область гена bphA1 , располагающаяся в районе 668–1152 п.н. Исходя из данных M. Zielinski с соавторами [2002], размер гена bphA1 у разных бактерий составляет 1374–1404 п.н.). Ам-плифицированный участок гена кодирует 222–384 АКО α-субъединицы БДО. Это АКО С-концевого домена, формирующие активный центр фермента (рис. 1) [Шумковa и др., 2008; Шумкова, 2009].
ll^T
II
N
[2Fe-2S]
и Кластер Риске
Активный центр
20 40 6
80 100 120 140 1 60 1 80 200 220 240 260 280
400 420 440 460
*
11^1_______________ у
Рис. 1 . Схема строения α-субъединицы бифенил 2,3-диоксигеназы [Zielinski et al., 2002] и исследуемые нами области:
заштрихованный и белый участки соответствуют каталитическому и Риске доменам, соответственно; короткие вертикальные линии, соединенные горизонтальной, показывают расположение лигандов железосерного кластера и мононуклеарного железа активного центра; I – исследованная нами ранее область, II – область, исследование которой планируется; длинными вертикальными линиями показано положение праймеров; внизу отображена нумерация АКО, соответствующая порядку их расположения в α-субъединице БДО Burkholderia xenovorans LB400
Таким образом, подбирая новые праймеры, мы ставили две цели:
-
1. Амплифицировать часть гена, кодирующую N-концевой домен α-субъединицы БДО, включающий железо-серный кластер Риске. Это позволит получить более полную информацию о генах тех бактерий, у которых ранее был амплифицирован участок гена bphA1 , кодирующий активный центр.
-
2. Получить ПЦР-продукт с другого участка гена тех бактерий, у которых ранее амплификации не наблюдалось. Это послужит основой для дальнейшего изучения полной нуклеотидной последо-
- вательности гена bphA1, а также позволит в дальнейшем проводить скрининг бактерий на присутствие генов, контролирующих деструкцию бифе-нила/ПХБ у бактерий порядка Actinomycetales.
Материалы и методы исследования
Программное обеспечение
Поиск генов bphA1 проводился с помощью программы BLAST в международной базе данных GenBank. Для выравнивания нуклеотидных последовательностей и поис- ка консервативных участков была использована программа VectorNTI 10 . Последовательности олигонуклеотидов подбирались вручную. Для анализа свойств праймеров использовалась программа OligoAnalyzer 3.1 (http:// com/analyzer/Applications/OligoAnalyzer/. Проверка комплементарности праймеров соответствующим генам проводилась с помощью программы Primer-BLAST
.
Результаты и обсуждение
Подбор праймеров
Поскольку bphA1 гены грамположительных и гра-мотрицательных бактерий имеют существенные отличия [Masai et al., 1995], подбор праймеров проводился на основе известных нуклеотидных последовательностей генов α-субъединиц БДО, депонированных в международной базе данных GenBank, грамположительных штаммов: Rhodo-coccus globerulus P6 [X80041], R. erythropolis TA421 [D88021], R. erythropolis TA421 [D88020], R. aetherivorans I24 cosmid 2G11 [AF452376], Rho-dococcus sp. RHA1 [D32142], Rhodococcus sp. R04 [DQ403247], Rhodococcus sp. HA99 [AB272986], R. erythropolis TA431 [AB272985], R. rhodochrous K37 [AB272984].
Было проведено множественное выравнивание нуклеотидных последовательностей (ген bphA1 и прилегающие к нему с краев участки длиной 230 п.н.) перечисленных выше бактерий. Найдено несколько консервативных областей без делеций, длина которых составляла 26–53 п.н., что достаточно для подбора праймера: 1) 377–430 п.н., 2) 452– 495 п.н., 3) 530–582 п.н., 4) 593–633 п.н., 5) 746–773 п.н., 6) 900–926 п.н., 7) 1410–1433 (рис. 2).
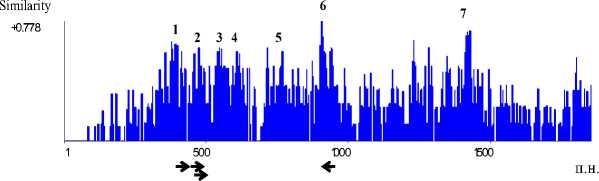
Рис. 2 . График сходства выравненных нуклеотидных последовательностей гена bphA1 :
по оси х – показатель сходства (Similarity) с консенсусной последовательностью – рассчитывался следующим образом: значения от 0 до 1, присвоенные каждому нуклеотиду (1 – идентичность, 0.5 – сходство, 0.2 – слабое сходство) суммированы и поделены на количество последовательностей в выравнивании; по оси у – порядковый номер нуклеотида от начала гена; стрелками показано положение праймеров; номерами (1–7) обозначены консервативные области
При подборе праймеров мы руководствовались рекомендациями [Kwok et al., 1994; Патрушев, 2004; Linhart, Shamir, 2005]. Кроме того, старались минимизировать вырожденность праймеров [Compton, 1990] и подобрать их таким образом, чтобы 3'-конец праймера не содержал нуклеотидных замен, т.е. максимально соответствовал участку, на который он будет отжигаться. На 5'-конце допускали несоответствия матрице. Необходимо было, чтобы амплифици-руемая область гена перекрывалась с ранее исследованным нами участком гена bphA1 , а положение прямого праймера было максимально близко к началу гена. С учетом поставленных задач для подбора праймеров подходили консервативные области № 1, 2 и 6. При соблюдении данных условий нам удалось подобрать несколько вариантов прямого, forvard(F) – праймера и один обратный revrse(R)-праймер (рис. 3): BphA1F409 5'-TTCTTGGCTGYTKHTSGSNCA-3', BphA1F450 5'-CCGGCGACTTYATSACSAMSTACAT-3', BphA1F462 5'-TGACCACGTACATGGGBGARGA-3', BphA1R900 5'-TCSGCDGCRAWYTTCCAGTT-3'.
Анализ термодинамических характерик и вторичной сруктуры подобранных праймеров
Далее мы провели анализ термодинамических параметров и вторичной структуры вышеперечисленных олигонуклеотидов (таблица). Forvard-праймер BphA1F409 позволяет амплифицировать максимально длинный участок гена bphA1, однако по сравнению с BphA1F450 и BphA1F462 обладает большой вырожденностью, худшими термодинамическими характеристиками. Вырожденный праймер – это смесь нуклеотидных последовательностей, каждая из которых представляет собой индивидуальный праймер. Чем выше «степень вырожденности» (число индивидуальных праймеров в смеси), тем сильнее падает эффективность ПЦР из-за снижения эффективной концентрации праймера. Рекомендуется, чтобы степень вырожденности не превышала 512 [Compton, 1990]. Также, в случае BphA1F409 разница между максимальной и минимальной температурой плавления индивидуальных вариантов праймера в общей смеси будет наибольшей: почти 11ºС по сравнению с 3.9ºC и 4.5ºC в случае BphA1F450 и BphA1F462, соответ- ственно (таблица), что может вызвать трудности при подборе температуры отжига в ПЦР.
AB 272985] _Rh о do с ос c us_eryt hro po lts_T A431 [DQ403247]_Rhodococcus_sp ,_R04 [D88021]_Rhodococcus_errthropois_TA421 [A F452376] _Rh о do с ос c us_ae t herivoran s_I24 [D 3 2142 ] _Rh od о co c cu s_sp ._RHA 1 [D8 80 20]_Rhodococcus_er>thropois_TA421 ГХ800411 Rjipdococcus oloberulus P6 [A В 27 29 8 6] _Rn о do с ос c us_sp, _H A 99 [A B2729 8 4] _Rh о do с ос c us_rh о do c hro us_K37

GTGGACC GAGATGTCTA C GA GCT CGAGС TC GA GO G CC ТС ТГС GC С АЛ ТА СC TG G CTGTTTCTC GG GСЛ GTGGACCGAGATGTCTACGAGCTCGAGCTCGAGCGCLTCTTCGCLA#TACCTGGCTGTTTCTCGGGC# i ACCGATCAGGCAATCTACGAGCGAGAGCTCGAGCAAGTTTTCGGGCC GAGTTGGCTGTTCCTCGCACJ I ACC^jACGAGGCGCTGTACGAACAGGAACTGGAGCGGATCTTCGGTC( CTCGTGGTTGCTGATGGGCCJ । ACCBACGAGGCGCTGTACGAACAGGAACTGGAGCGGATCTTCGGTC( CTCGTGGTTGCTGATGGGC CJ । A CgIaC GAGGCGCTTTACCAGCAGGAACTCGAGCTCATCTTCGGTCC GTCCTGGCTCCTGTTGGGGCJ ।
CGTGAGC CGTGAGC CGATTCG CGAGACG CGAGACG CGAGACG
GTGGACCGAGATGKTACC4GCTCGAGCTCGAGCGCCTCTTCGCCM TACCTGGCTGTTTCTCGGGCj CGTGAGC
(361) GTGGACCGAGATGTCTACGAGCTCGAGCTCGAGCGCCTCTTCGCCAj TACCTGGCTGTTTCTCGGGCj CGTGAGC
BphA1F409
[AB272985]_Rhodococcus_erythropolis_T A 431 (397) [DQ403247]_Rhod0CDCCUS_sp._R04 (385)
[D88021LRhodococcus_erythropolis_T A421 (331) [A F452376 ] _Rh od о co с c us_ae t herivoran s_I24 (401) [D32142]_Rhodococcus_sp ._RHA1 (363)
[D88020]_Rhodococcus_erythropolis_T A421 (380) [X 80041 ] _Rho d ос о cc и s_g Io be rulu s_P6 (380) [AB272986]_Rhodococcus_sp ,_HA99 (352) [AB272984]_Rhodococcus_rhodochrous_K37 (430)
GTGAGCLAGGTCGCCGlAtCGGGCGACTTTA
BTGAGCCAGGlCGCCGiAt CGGGCGACTTTA
TCACCACGTACAT
TCACCACGTACAT
GATTCGCAACTTCCGAAA( GCGGCAGCTTCGTGCAGACCTACAT
GAGAC GC AGArTC CGAAGlCC GGC GACTTCA GAGACGCAGATTC CGAAGt CCGGCGACTTCA GAGACGCAAATCCCGAAGt CCGGCGACTTCA gagacgIlaatcccgaagi CCGGCGACTTLA GTGAGCCAGGTCGCCGAAC CGGGCGACTTTA
ГGACGAAСТАCAT ГGACGAACTACAT ГGACCCAGTACAT ГGACCCAGTACAT TCACCACGTACAT
rGGTGAAGA [TCCGTTATCGTCTCCHCGGT rGGGGAAGA [TCCGTTATCGTCTCCCGCGGT jggtgagga :cctgtacttgttgtgcgacag rG G C GA GGA ГС С C GTG ATG GTC GTTC GT C A G rGG C GA GGA ГС С C GTG ATG GTC GTTC GT C A G rGGTGAGGA ^CCGGTTATCGTCTCGCGGCAG rG GT GA GGA JCCGGTTATCGTCTCGCGGCAG iGGTGAAC-A [TCCGTTATCGTCTCCCGCGGT
GTGAGCCAGGTCGCCGAAC CGGGCGACTTTA TZACCACGTACAT iGGTGAAGA'TCCGTTATCGTCTCCCGCGGT
BphA1F450
[AB272985]_Rhodococcus_e ryt hrupolis_T Д43 1 [DQ40 3 2 47]_Rhodococcus_sp._R]0 4 [D8 80 2 1 J_Rhodococcus_e ryt hropolis_T A42 1
[AF452376 ]_Rhodococcus_a et herivorans_I24 [D3 2 14 2 ]_R hodococcu s_s p ._RH Al
[D88020]_Rhodococcus_e ryt hropolis_T A421
ГХ800411 Rhodococcus doberulus P6 [ AB272986 ]_R hodococcu s_s p. _H A99 [AB272984]_Rhodococcus_rhodochrous_K37

BphA1F462
ACССТCGAGAС AACTGGAAGAT CGC C GCCGAGIAACTT CGCC-GCCGACATСТАCCACGTCGAАСАС TCGCACGC ACCGTCCAСАС( AACTGGAAGATCGCCGCCGAGAACTTCGCC-GCCGACATGTACCACGTCGAACACTCGCACGC GT TATC GACTG( AACTGGAДАТT T GCA TCCGAGCAGT-CTGCGAGCGACATGTA TCACGT GС-С TTТСTС СC
GT CAT T С C CT Gt ДАС T G GAAGT T C GC AG C GGAG CAAT T C TGC - A GC GA CAT GTA CCAC G C GG- G iZAC CA CAT С С C GTCATTССДТG( AACTGGAAGTTCGCAGCGGAGCAATTCTGC-AGCGACATGTAСCACGCGG-GCACCACATССC GTCAT CCAGTGiAACTGGAAGT TCGCAGCGGAGCAGTT CTGC-TCTGATATGTACCACGTCG-GCACGACGTCAC
GTCAT CCAGTG( AACTGGAAGT TCGCAGCGGAGCAGTTCTGC-TCTGATATGTACCACGTCG-GCACGACGTCAC ACC GT C GA CAC ( AAC T G GAAGATC GC C GC CGAG AAC T T C GC C - GCC GA CAT GTA CCAC G TCGAACAC TC GCAC G C ACC GT C GA CAC( AAC T G GAAGAT C GC C GC CGAG ДАС T T C GC C- GCC GA CAT GTA CCAC G TC GAACAC TC GCAC G C
BphA1R900
Рис. 3 . Фрагменты выравнивания нуклеотидных последовательностей генов bphA1 :
консервативные нуклеотиды выделены цветом, участки, комплементарные праймерам, выделены прямоугольниками и стрелками
Ни один из forvard-праймеров не образует тугоплавких шпилек (с ∆G меньше –7 kcal.mole -1 ). Однако для каждого из сконструированных праймеров имеются индивидуальные варианты, образующие тугоплавкие гомо- или гетеродимеры (таблица). Оптимальным в этом отношении является BphA1F462, который при степени вырожденности 6 образует 1 гетеродимер, характеризующийся свободной энергией Гиббса ∆G –10.13 kcal.mole -1 . BphA1F409 образует 11 вариантов (из 192) гомо- и гетеродимеров с ∆G меньше –7 kcal.mole -1 , что может вызвать затруднения на стадии отжига данных индивидуальных вариантов праймера. Однако BphA1F462, по сравнению с BphA1F450 и BphA1F462, позволяет амплифици-ровать наиболее короткий фрагмент гена bphA1 .
Проверка специфичности праймеров
В результате проверки комплементарности праймеров к имеющимся в базе GenBank генам bphA1 , было выявлено, что сконструированные нами олигонуклеотиды в разной степени специфичны генам, кодирующим α-субъединицы негемовых железосодержащих диоксигеназ.
Пара праймеров BphA1F409 и BphA1R900 в подавляющем большинстве случаев была компле- ментарна bphA1 генам грамположительных бактерий (рода Rhodococcus, Arthrobacter). Но среди найденных с их помощью нуклеотидных последовательностей, депонированных в GenBank, были соответствующие гены bphA1 грамотрицательных бактерий Comamonas testosteroni и Dyella ginsengi-soli, а также участок транспозона Tn4371, содержащего гены деструкции бифенила, грамотрица-тельной бактерии Ralstonia oxalatica. Длина ожидаемого ПЦР-продукта составляла 492 или 507 п.н.
Праймеры BphA1F450 и BphA1R900 также в большинстве случаев были комплементарны bphA1 генам грамположительных бактерий (рода Rhodococcus, Janibacter). Однако среди найденных в GenBank нуклеотидных последовательностей было несколько bphA1 генов грамотрицательных бактерий родов Pseudoxanthomonas и Dyella; гены α-субъединиц неизвестной гидроксилирующей диоксигеназы, фенилпропионат диоксигеназы и хлорбензол диоксигеназы грамотрицательных бактерий родов Rhizobium, Bordetella и Pseudomonas, соответственно. Размер ожидаемого ампликона составил 445 – 466 п.н. Вероятен также неспецифический отжиг на ДНК грамотрицательных бактерий рода Pirellula (с длиной ожидаемого про- дукта реакции 1432 п.н.), Starkeya (2691 п.н.) и ар- хей Methanocella (4614 п.н.).
Анализ термодинамических характеристик и вторичной структуры подобранных праймеров
|
Параметры |
BphA1F409 |
BphA1F450 |
BphA1F462 |
BphA1R900 |
|
Длина, п.н. |
21 |
25 |
22 |
20 |
|
Степень вырожденности |
192 |
32 |
6 |
48 |
|
Содержание GC, % |
51.6 |
52.0 |
55.3 |
51.7 |
|
T m (макс. – мин.) средн. ,ºC |
54.2 – 65.1 59.3 |
58.8 – 62.7 60.7 |
58.0 – 62.5 60.5 |
55.5 – 62.0 58.2 |
|
Разница между мин. и макс. T m , ∆T m , ºC |
10.9 |
3.9 |
4.5 |
6.5 |
|
Шпильки (шп.): количество вариантов, ∆G (kcal.mole -1 ) |
– |
– |
1 шп., ∆G -1.37 |
– |
|
Гомодимеры (д.), количество вариантов, ∆G (kcal.mole -1 ), кол-во спаренных оснований (сп. осн.) |
1 д.: ∆G -14.86, 7 сп. осн. 3 д.: ∆G -7.81 – -8.86
7 д.: ∆G -4.24 – -6.21,
2.42, 2 сп. осн. |
3 д.: ∆G -7.28 – -9.75, 4 – 6 сп. осн. 2 д., ∆G -4.68 – -5.52, 3 – 4 сп. осн. 11 д., ∆G -3.0 – -3.88, 2 – 3 сп. осн. 4 д., ∆G -1.47 – -1.76, 2 сп. осн. |
5 д.: ∆G -5.02 – -6.3, 3 – 4 сп. осн. 7 д.: ∆G -1.34 – - 2.88, 2 сп. осн. |
1 д.: ∆G -17, 7 сп. осн. 1 д.: ∆G -14.42, 6 сп. осн. 2 д.: ∆G -8.13 – -8.77,
5 д.: ∆G -3.34 – -3.52,
|
|
Димеры с BphA1R900, количество вариантов, ∆G (kcal.mole -1 ), кол-во спаренных оснований (сп. осн.) |
4 д.: ∆G -10.87 – -13.66, 5 – 7 сп. осн. 3 д.: ∆G -8.13 – -8.87, 4 сп. осн. 6 д.: ∆G -4.54 – -6.62, 3 – 4 сп. осн. 5 д.: ∆G -3.55 – -3.34, 2 – 3 сп. осн. 6 д.: ∆G -1.34 – -2.39, 2 сп. осн. |
1 д.: ∆G -7.28,
16 д.: ∆G -1.34 – -2.94, 2 – 3 сп. осн. |
1 д.: ∆G -10.13, 6 сп. осн. 3 д.: ∆G -4.45 – -5.4, 3 сп. осн. 10 д.: ∆G -3.07 – -3.91, 2 – 3 сп. осн. 14 д.: ∆G -1.34 – - 2.88, 2 сп. осн. |
– |
|
Разница T m c BphA1R900, ∆T m (макс. – мин.), ∆T m средн., ºC |
-1.5 – 3.1 1.1 |
3.3 – 0.7 2.5 |
2.5 – 0.5 2.3 |
– |
|
Порядковый № АКО (от N-конца белка BphA1), соответствующего 5'-концу праймера |
59 |
73 |
77 |
230 |
|
Порядковый № нуклеотида (от начала гена bphA1 ), соответствующего 5'-концу праймера |
179 |
220 |
232 |
690 |
Примечания. Степень вырожденности праймера рассчитывали, перемножая количество вариантов нуклеотидов в каждой позиции. T m - температура плавления.
Пара праймеров BphA1F462 и BphA1R900 оказалась наименее специфичной к bphA1 генам грамположительных бактерий. Среди данных, найденных с помощью нуклеотидных последовательностей сконструированных праймеров, было 7 генов α-субъединиц БДО бактерий рода Rhodococ-cus и 1 ген bphA1 бактерий рода Arthrobacter . По результатам проверки можно предположить, что с такой же долей вероятности праймеры с будут отжигаться и на гены bphA1 грамотрицательных бактерий: с помощью программы Primer-BLAST было найдено 9 bph -генов бактерий рода Pseudomonas, по 2 гена Burkholderia и Dyella , по 1 гену Comamo-nas , Pandoraea , Cupriavidus , Achromobacter , bphA1 ген некультивируемых бактерий и 9 генов, кодирующих синтетический конструкт BphA. Кроме того, возможен отжиг праймеров на гены больших субъединиц гидроксилирующих диоксигеназ кумола ( cumA1 ), этилбензола ( edoA1 ) и изопропилбензола грамотрицательных бактерий Pseudomonas fluorescens , гены α-субъединиц гидроксилирующих диоксигеназ Polaromonas naphthalenivo-rans и некультивируемой бактерии, на ДНК Pseu-doxanthomonas spadix, на интегративные и конъю-гативные элементы грамотрицательных бактерий Ralstonia и Acidovorax . Размер ожидаемого ПЦР-продукта составил 439 – 454. Вероятен неспецифический отжиг данной пары праймеров на ген рибосомального белка Pirellula staleyi с длиной ожидаемого продукта реакции 1432 п.н.
Заключение
Нами подобраны вырожденные праймеры для амплификации участка гена bphA1 , кодирующего N-концевой домен α-субъединицы БДО с расположенным в нем кластером Риске. Анализ термодинамических параметров и вторичной структуры олигонуклеотидов позволяет предположить, что амплификация фрагмента гена bphA1 с высокой вероятностью пройдет успешно. Все праймеры подходят для детекции генов, кодирующих каталитические субъединицы ферментов подсемейства Б/Т ДО у бактерий порядка Actinomycetales . Для скрининга генов bphA1 более всего подходит пара BphA1F409 и BphA1R900. Планируется экспериментальная проверка праймеров.
Работа выполнена при поддержке гранта РФФИ-Урал №11-04-96028 «Новые физиологические и молекулярно-биологические свойства бактерий-деструкторов (хлор)ароматических соединений».
Список литературы Олигонуклеотидные праймеры для детекции генов, кодирующих большую субъединицу бифенил 2,3-диоксигеназы, бактерий порядка Actinomycetales
- Васильева Г.К., Стрижакова Е.П. Биоремедиация почв и седиментов, загрязненных полихлорированными бифенилами//Микробиол. 2007. T. 76, № 6. С. 725-741.
- Патрушев Л.И. Искусственные генетические системы. М.: Наука, 2004. T. 1: Генная белковая инженерия. 526 с.
- Плотникова Е.Г. и др. Выделение и характеристика новых бактерий, разлагающих полихлорированные бифенилы//Сб. тез. IV Междунар. конф. «Проблемы загрязнения окружающей среды». Пермь, 1998. С. 160.
- Плотникова Е.Г. и др. Бактерии-деструкторы полициклических ароматических углеводородов, выделенные из почв и донных отложений района солеразработок//Микробиол. 2001. Т. 70,. № 1. С. 61-70.
- Плотникова Е.Г. и др. Штамм бактерий Rhodococcus ruber -деструктор полихлорированных бифенилов: пат. № 2262531 Рос. Федерации; опубл. 20.10.05. Бюл. № 29.
- Шумковa Е.С. и др. Скрининг и изучение ключевых генов катаболизма бифенила у бактерий//Вестн. Перм. ун-та. 2008. Вып. 9. Биология.С. 53-57.
- Шумкова Е.С. Генетические и ферментные системы деструкции ароматических соединений бактерий порядка Actinomycetales: автореф. дис. канд. биол. наук. Пермь, 2009. 27 с.
- Compton T. Degenerate primers for DNA amplification//PCR Protocols/Ediors M.A. Innis, D.H. Gelfand, J.J. Sninsky, T.J. White. New York: Academic Press, 1990. P. 39-45.
- Ferraro D. J. et al. Structural investigations of the ferredoxin and terminal oxygenase components of the biphenyl 2,3-dioxygenase from Sphingobium yanoikuyae B1//BMC Structural Biology. 2007. Vol. 7. P. 1170-1182.
- Gibson D.T., Parales R.E. Aromatic hydrocarbon dioxygenases in environmental biotechnology//Curr. Opin. Biotechnol. 2000. Vol. 11. P. 236-243.
- Jakoncic J. et al. The catalytic pocket of the ringhydroxylating dioxygenase from Sphingomonas CHY-1//Biochem. Biophys. Res. Commun. 2007. Vol. 352. P. 861-866.
- Kimura N. et al. Functional analyses of a variety of chimeric dioxygenases construated from two biphenyl dioxygenases that are similar structurally but different functionally//J. Bacteriol. 1997. Vol. 179. P. 3936-3943.
- Kwok S. et al. A guide to the design and use of mismatched and degenerate primers//PCR Methods and Appl. 1994. Vol. 3. P. 39-47.
- Linhart C., Shamir R. The degenerate primer design problem: theory and Applications//J. of Computational Biology. Vol. 12, N 4. 2005. P. 431-456.
- Masai E. et al. Characterization of biphenyl catabolic genes of gram-positive polychlorinated biphenyl degrader Rhodococcus sp. strain RHA1//Appl. Environ. Microbiol. 1995. Vol. 61. P. 2079-2085.
- Mukerjee-Dhar G. et al. bph Genes of the thermophilic PCB degrader, Bacillus sp. JF8: characterization of the divergent ringhydroxylating dioxygenase and hydrolase genes upstream of the Mn-dependent BphC//Microbiol. 2005. Vol. 151. P. 4139-4151.
- Pieper D.H. Aerobic degradation of polychlorinated biphenyls//Appl. Microbiol. Biotech. 2005. Vol. 67. P. 170-191.
- Romine M.F. et al. Complete sequence of a 184-kilobase catabolic plasmid from Sphingomonas aromaticivorans F199//J. Bacteriol. 1999. Vol. 181, № 5. P. 1585-1602.
- Ross G. The public health implications of polychlorinated biphenyls (PCBs) in the environment//Rev. Ecotox. Environ. Safety. 2004. Vol. 59. P. 275-291.
- Seeger M. et al. Dehalogenation, denitration, dehydroxylation, and angular attack on substituted biphenyls and related compounds by a biphenyl dioxygenase//J. Bacteriol. 2001. Vol. 183. P. 3548-3555.
- Suenaga H., et al. Alteration of regiospecificity in biphenyl dioxygenase by active-site engineering//J. Bacteriol. 2002. Vol. 184. P. 3682-3688.
- Taguchi К. et al. Polychlorinated biphenyl/biphenyl degrading gene clusters in Rhodococcus sp. K37, HA99, and TA431 are different from well-known bph-gene clusters of Rhodococci//Biosci. Biotechnol. Biochem. 2007. Vol. 71, № 5. P. 1136-1144.
- Witzig R. et al. Assessment of toluene/biphenyl dioxygenase gene diversity in benzene-polluted soils: links between benzene biodegradation and genes similar to those encoding isopropylbenzene dioxygenases//Appl. Environ. Microbiol. 2006. Vol. 72, N 5. P. 3504-3514.
- Yang X. et al. Characterization and functional analysis of a novel gene cluster involved in biphenyl degradation in Rhodococcus sp. strain R04//J. Appl. Microbiol. 2007. Vol. 103, № 6. P. 2214-2224.
- Zielinski M. et al. The principal determinants for the structure of the substrate-binding pocket are located within a central core of a biphenyl dioxygenase alpha subunit//Microbiol. 2002. Vol. 148. P. 2439-2448.


