Определение эссенциальных и токсичных элементов в моче методом ICP-MS для диагностических исследований и оценки рисков здоровью населения
Автор: Уланова Т.С., Гилева О.В., Стенно Е.В., Вейхман Г.А., Недошитова А.В.
Журнал: Анализ риска здоровью @journal-fcrisk
Рубрика: Экспериментальные модели и инструментальные исследования
Статья в выпуске: 3 (7), 2014 года.
Бесплатный доступ
Представлены результаты разработки методики определения 12 элементов в моче с использованием квадрупольного масс-спектрометра с индуктивно-связанной плазмой Agilent 7500cx (USA) с октопольной реакционно/столкновительной ячейкой (ORS) в реакционном режиме. Образцы мочи анализировались непосредственно после разбавления 1/10 1% водным раствором HNO 3. Правильность результатов подтверждена анализом стандартных образцов мочи Seronorm TM urine (Norway). Разработанная методика позволяет точно и достоверно определять ванадий, хром, марганец, никель, медь, цинк, селен, стронций, кадмий, титан и свинец в образцах мочи. Предел определения для V, Cr, Mn, Ni, Sr, Cd, Tl, Pb составляет 0,1 мкг/дм 3, для Сu 1,0 мкг/дм 3, для Se 5,0 мкг/дм 3, для Sr и Zn 50,0 мкг/дм 3 с погрешностью определения, не превышающей 25 %. Исследования биосубстратов детского населения Пермского края, проживающего в экологически благополучных условиях, выполненные разработанным методом масс-спектрометрии с индуктивно-связанной плазмой, позволили установить фоновые уровни содержания 12 элементов как критериев сравнения для задач гигиенических оценок, эпидемиологических исследований, обследований, экспертиз.
Метод масс-спектрометрии с индуктивно-связанной плазмой (icp-ms), октопольная реакционно/столкновительная ячейка, внутренний стандарт, моча
Короткий адрес: https://sciup.org/14237881
IDR: 14237881 | УДК: 613.9:543.064
Identification of essential and toxic elements in urine by ICP-MS for diagnostic research and health risk assessment
The results of method developing for identifying 12 elements in urine are presented using a quadrupole mass spectrometer with inductively coupled plasma Agilent 7500cx (USA) with octopole reaction/collision cell (ORS) in the reaction mode. Urine samples were analyzed immediately after dilution in 1/10 of 1% aqueous solution of HNO 3. The results’ validity is confirmed by standard analysis of urine samples SeronormTM urine (Norway). The developed method can accurately and reliably identify vanadium, chromium, manganese, nickel, copper, zinc, selenium, strontium, cadmium, lead and titanium in the urine samples. Limit of detection for V, Cr, Mn, Ni, Sr, Cd, Tl, Pb is 0.1 μg/dm 3, for Cu 1.0 μg/dm 3, for Se 5.0 μg/dm 3, for Sr and Zn 50.0 μg/dm 3 with an identification error 25 %. Biological substrates’ study of child population in the Perm Krai, living in ecologically safe conditions, performed by the developed method of mass spectrometry with inductively coupled plasma, allowed to identify background levels of 12 elements as comparison criteria for the problems of hygiene assessments, epidemiological studies, surveys, appraisals.
Текст научной статьи Определение эссенциальных и токсичных элементов в моче методом ICP-MS для диагностических исследований и оценки рисков здоровью населения
но прямые методы определения токсичных соединений и элементов в биологических средах человека являются неоспоримым доказательством неблагоприятного техногенного воздействия, а в совокупности с маркерами эффекта – причиненного вреда здоровью [7, 15].
В настоящее время для высокоточных и селективных определений большого спектра элементов используется метод масс-спектрометрии с индуктивно-связанной плазмой (ICP-MS). Сочетание таких характеристик, как низкие пределы обнаружения, высокая воспроизводимость, широкий диапазон определяемых концентраций, низкий расход анализируемых веществ и возможность выполнения анализа с минимальным объемом, обеспечивает высокую информативность метода для определения микро- и ультрамикросодержаний в биологических жидкостях [12].
С точки зрения доступности наиболее распространенным неинвазивным объектом исследования биологических сред человека является моча. В то же время основной проблемой при определении элементов в моче является высокое содержание солей – хлоридов, сульфатов, фосфатов, которое значительно повышает матричное влияние и ведет к завышению результатов анализа за счет интерференционных помех [6, 8, 11].
Цель данного исследования – разработка высокочувствительного и точного метода количественного определения V, Cr, Mn, Ni, Сu, Zn, As, Se, Sr, Cd, Tl, Pb в моче как маркеров экспозиции в условиях воздействия химических факторов среды обитания.
Материалы и методы. Количественное определение V, Cr, Mn, Ni, Сu, Zn, Se, Sr, Cd, Tl, Pb в образцах мочи осуществляли на квадрупольном масс-спектрометре с индуктивно-связанной плазмой Agilent 7500cx (USA) с октопольной реакционно/столк-новительной ячейкой (ORS). Использование ORS позволяет избавиться от влияния поли-атомных ионов за счет их столкновений или реакций с атомами газа, заполняющими ячейку. В качестве газа ячейки использовали гелий. Экспериментально было установлено значение скорости потока гелия 5,0 мл/мин, позволяющее значительно снизить поли-атомные наложения при сохранении высокого уровня чувствительности. Мощность высокочастотного сигнала 1550 Вт. Для введения проб использовалась двухканальная распылительная камера Скотта. Температура распылительной камеры 2,0 °С. Скорость подачи образца в распылительную камеру составляла 0,4 мл/мин. Скорость работы детектора – ≥ 100 мкс на 1 ион. В качестве газа-реактанта использовался гелий. Для настройки применяли раствор 7Li, 59Co, 89Y и 205Tl в 2 % HNO3 с концентрацией 1 мкг/л для каждого элемента (Tuning Solution, USA). Соотношения 140Ce16O+/140Ce+ + составляли < 1 %, а для 140Ce2+/140Ce+ + < 3 %. Использовали жидкий аргон высокой чистоты 99,99 % (ТУ-2114-005-00204760-99). Максимальная скорость потока аргона составляла 20 л/мин, давление в канале подводки газа 700±20 кПа, Тплаз-мы = 8000–10000 К. Автоматизация процесса проведения анализа обеспечивалась автосэмплером марки G3160B (Germany). В качестве основного стандартного раствора использовали раствор, содержащий 27 элементов с концентрацией 10 мг/л в 5 % водном растворе HNO3 (Multi-Element Calibration Standard-2A, USA). Для приготовления градуировочных растворов и подготовки проб использовали особо чистую HNO3 (Sigma – Aldrich, USA). Концентрации градуировочных растворов для определения Cd и Tl составляли 0,0; 0,1; 0,5; 1,0 мкг/л, для Mn, Ni, Cr, V, Se, Cu – 0,0; 0,1; 0,5; 1,0; 5,0 мкг/л, для As, Sr, Zn – 0,0; 1,0; 5,0; 10,0; 50,0 мкг/л соответственно. Для приготовления растворов внутреннего стандарта (ВС) использовали комплексный стандартный раствор 209Bi, 73Ge, 115 In, 6Li, 45Sc, 159Tb, 89 Yс с концентрацией 10 мг/л в 5 % водном растворе HNO3 (Internal Standard Mix, USA). В качестве внутреннего стандарта для определения Pb и Tl применяли 159Tb, при определении Cd – 115 In, а для остальных элементов – 72Ge, вследствие близости потенциалов ионизации и атомной массы.
Все растворы разбавляли деионизированной водой с удельным сопротивлением 18,2 Mом∙см, очищенной в системе Milli-Q Integral (Millipore SAS, France). Холостую пробу готовили аналогично рабочей. Для подготовки к анализу лабораторной посуды из стекла, тефлона, полипропилена использовали ультразвуковую мойку Elmasonic S 100H (Germany). Посуду выдерживали 20 мин в бидистиллированной воде при 55 °С, далее 20 мин в водном растворе азотной кислоты (1:5) при 55 °С, далее 20 мин в деионизованной воде при 55 °С.
Стандартные образцы мочи SeronormTM urine (LOT 0511545, Sero AS, Billingstad, Norway) разбавляли в 5 мл деионизированной воды.
Отбор проб утренней мочи производили в стерильные полипропиленовые контейнеры на 125 мл с винтовой крышкой (F.L.Medical S.r.l., Torreglia, Italy). Для последующего масс-спектрометрического исследования к 0,5 мл мочи добавляли 4,45 мл
1 % водного раствора HNO 3 и 0,05 мл раствора внутреннего стандарта.
Результаты и их обсуждение. Разработанная методика определения 12 элементов в моче методом масс-спектрометрии с индуктивно-связанной плазмой отличается от действующих в настоящее время МУК 4.1.1483-03 [10] отработанной схемой про-боподготовки для минимизации матричных эффектов, выбором внутреннего стандарта для каждого определяемого элемента, использованием столкновительной ячейки с гелием для коррекции полиатомных интерференций. Методика аттестована центром «Сертимет» (№ 88-16374-102-01.00076) и зарегистрирована в Федеральном информационном фонде по обеспечению единства измерений ФР.1.31.2014.17064.
Диапазоны измерений массовых концентраций V, Cr, Mn, Ni, Сu, Zn, As, Se, Sr, Cd, Tl, Pb и предел обнаружения (LOD) приведены в табл. 1.
Таблица 1
Диапазоны измерений в моче и пределы обнаружения в растворе, мкг/дм3
|
Наименование определяемого элемента |
Массы изотопов, используемых при измерении |
Диапазон измерений в моче, мкг/дм3 |
Показатель точности (границы относительной погрешности при Р = 0,95), ± δ , % |
Предел обнаружения (LOD)в растворе, мкг/дм3 |
|
Ванадий |
51 |
0,1–50,0 |
15–23 |
0,01 |
|
Хром |
53 |
0,1–100,0 |
14–23 |
0,01 |
|
Марганец |
55 |
0,1–100,0 |
14–25 |
0,01 |
|
Никель |
60 |
0,1–100,0 |
15–22 |
0,01 |
|
Медь |
63 |
1,0–200,0 |
14–20 |
0,1 |
|
Цинк |
66 |
50,0–1000 |
13 |
5 |
|
Мышьяк |
75 |
1,0–100,0 |
14 |
0,1 |
|
Селен |
82 |
5,0–500,0 |
16 |
0,5 |
|
Стронций |
88 |
50,0–1500 |
12 |
5 |
|
Кадмий |
111 |
0,1–50,0 |
16–23 |
0,01 |
|
Таллий |
205 |
0,1–50,0 |
15–19 |
0,01 |
|
Свинец |
206 |
0,1–500,0 |
15–23 |
0,01 |
Правильность результатов определения 12 элементов в моче подтверждена анализом стандартных образцах мочи SeronormTM urine ( n = 5, рисунок).
Обобщенные результаты исследований анализа стандартных образцов мочи, полученные с использованием разработанного метода, показывают, что погрешность при определении всех элементов составляет от 2 до 5 %.
Разработанная методика определения была отработана на территориях Пермского края с минимальной антропогенной нагрузкой и позволила получить результаты, представленные в табл. 2.
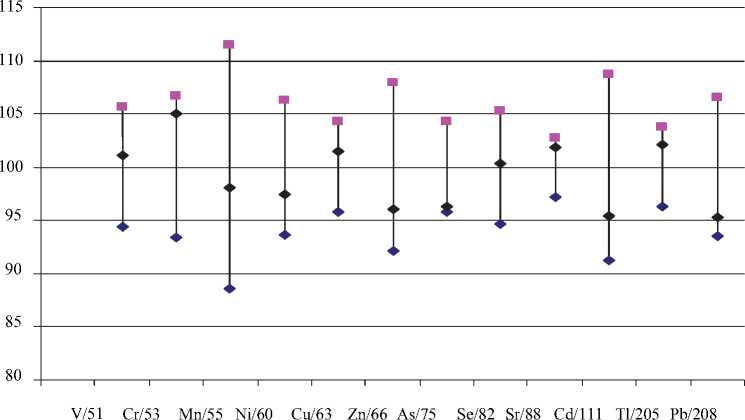
Минимальный уровень аттестованного значения
Максимальный уровень аттестованного значения
Экспериментально найденные значения
Рис. Результаты определения микроэлементов относительно сертифицированных значений в образцах SeronormTM urine
Таблица 2
Фоновые уровни содержания элементов в моче детского населения Пермского края, полученные методом масс-спектрометрии с индуктивно-связанной плазмой (ICP–MS), мкг/дм3
|
Определяемый элемент |
Фоновые уровни ( n = 73), M ± m , мкг/дм3 |
Референтные уровни, мкг/дм3, по Тицу [11] |
|
Марганец |
0,93±0,3 |
0,5–10,0 |
|
Мышьяк |
13,0±2,5 |
5,0–50,0 |
|
Никель |
2,2±0,56 |
0,1–10,0 |
|
Свинец |
1,2±0,17 |
< 80,0 |
|
Стронций |
166,0±26,0 |
20,0–350,0 [10] |
|
Хром |
1,4±0,13 |
0,1–2,0 |
|
Медь |
12,0±2,0 |
2,0–80,0 |
|
Цинк |
240,0±40,0 |
180,0–850,0 |
|
Кадмий |
0,2±0,2 |
0,5–4,7 |
|
Ванадий |
0,6±0,1 |
0,08–0,24 |
На основании выполненных исследований образцов мочи детского населения можно заключить, что разработанная методика позволяет получать достоверные данные, сопоставимые с референтными концентрациями, используемыми в качестве критериаль- ных оценочных величин в клинических исследованиях и доказательной медицине.
Выводы. Таким образом, отработанная схема подготовки образцов, оптимальные элементы внутреннего сравнения, отработанный комплекс инструментальных на- строек масс-спектрометра с индуктивносвязанной плазмой, в том числе октополь-ной реакционно/столкновительной ячейкой, позволили минимизировать матричное и интерференционное влияния солевого состава мочи на этапе пробоподготовки.
Разработанная методика позволяет точно и достоверно определять V, Cr, Mn, Ni, Сu, Zn, As, Se, Sr, Cd, Tl, Pb в образцах мочи, предел определения для V, Cr, Mn, Ni, Sr, Cd, Tl, Pb составляет 0,1 мкг/дм3, для Сu – 1,0 мкг/дм3, для Se – 5,0 мкг/дм3, для
Sr и Zn – 50,0 мкг/дм3 с погрешностью определения, не превышающей 25 %.
Исследования мочи детского населения Пермского края, проживающего в экологически благополучных условиях, выполненные разработанным методом масс-спектрометрии с индуктивно-связанной плазмой, позволили установить фоновые уровни содержания V, Cr, Mn, Ni, Сu, Zn, As, Se, Sr, Cd, Tl, Pb в моче как критерии сравнения для задач гигиенических оценок, эпидемиологических исследований, обследований, экспертиз.
Список литературы Определение эссенциальных и токсичных элементов в моче методом ICP-MS для диагностических исследований и оценки рисков здоровью населения
- Актуальные проблемы управления состоянием окружающей среды и здоровьем населения/Г.Г. Онищенко, В.Б. Гурвич, С.В. Кузьмин, С.В. Ярушин//Уральский медицинский журнал. -2008. -№ 11. -С. 4-10.
- Зайцева Н.В. Диагностика и коррекция экологически обусловленных состояний у детей. Региональные проблемы//Экологически обусловленные заболевания человека: методологические проблемы и пути их решения: материалы пленума/под ред. Ю.А. Рахманина. -М., 2000. -С. 3-5.
- Зайцева Н.В., Май И.В., Клейн С.В. К вопросу установления и доказательства вреда здоровью населения при выявлении неприемлемого риска, обусловленного факторами среды обитания//Анализ риска здоровью. -2013. -№ 2. -С. 14-26.
- Май И.В., Хорошавин В.А., Евдошенко В.С. Алгоритм и методы санитарно-эпидемиологического расследования нарушений прав граждан на благоприятную окружающую среду обитания с этапом оценки риска для здоровья//Здоровье населения и среда обитания. -2010. -№ 11. -С. 28-30.
- Методические подходы к оценке рисков воздействия разнородных факторов среды обитания на здоровье населения на основе эволюционных моделей/Н.В. Зайцева, В.П. Трусов, П.З. Шур, Д.А. Кирьянов, В.М. Чигвинцев, М.Ю. Цинкер//Анализ риска здоровью. -2013. -№ 1. -С. 15-22.
- МУК 4.1.1483-03. Методы контроля. Химические факторы. Определение содержания химических элементов в диагностируемых биосубстратах, препаратах и биологически активных добавках методом масс-спектромерии с индуктивно связанной аргоновой плазмой. -М.: Минздрав России, 2003. -С. 28.
- Определение токсичных веществ в биосредах для установления реальной химической нагрузки/М.Т. Дмитриев, Е.Г. Растянников, А.Г. Малышева [и др.]//Гигиена и санитария. -1986. -№ 3. -С. 48-50.
- Определение химических форм микроэлементов в биологических объектах/Н.Б. Иваненко, Н.Д. Соловьев, А.А. Иваненко, Л.Н. Москвин//Аналитика и контроль. -2012. -Т.16, № 2 -С. 108-133.
- Рахманин Ю.А., Румянцев Г.И., Новиков С.М. Методические проблемы диагностики и профилактики заболеваний, связанных с воздействием факторов окружающей среды//Гигиена и санитария. -2001. -№ 5. -С. 3-7.
- Скальный A.B., Рудаков И.А. Биоэлементы в медицине. -М.: ОНИКС, 2004. -272 с.
- Тиц Н. Клиническое руководство по лабораторным тестам. -М.: ЮНИМЕД-пресс, 2003. -960 с.
- Уланова Т.С. Новые направления в физико-химических исследованиях в рамках социально-гигиенического мониторинга//Гигиенические и медико-профилактические технологии управления рисками здоровью населения. -Пермь, 2011. -С. 41-44.
- Ong C.N., Shen H.M., Chia S.E.Biomarkers for male reproductive health Hazards: are they Available//Toxicology Letters. -2002. -Vol. 134, № 1-3. -С. 17-30.
- Phillips D.H. DNA Adduts as Markers of Exposure and Risk. Mutation Research//Fundamental and Molecular Mechanisms of Mutagenesis. -2005. -Vol. 577, № 1-2 spec. Iss. -P. 284-292.
- Schulte P.A., Talaska G. Validity Criteria fro the Use of Biological Markers of Exposure to Chemical agents in environmental Epidemiology//Toxicology. -1995. Vol. 101, № 1-2. -С. 73-88.
- WHO In formation Fast Sheet. -1997. -№ 170. -Р. 1-3.


