Определение конечных продуктов гликирования у больных стабильной ишемической болезнью сердца в рамках комплексной оценки остаточного сердечно-сосудистого риска
Автор: Объедкова Н.Ю., Маль Г.С.
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: Клинические исследования
Статья в выпуске: 1 т.41, 2026 года.
Бесплатный доступ
Актуальность. Пациенты с ишемической болезнью сердца (ИБС) имеют остаточный (резидуальный) риск наступления нежелательных сосудистых событий. Мультифакторность и гетерогенность его природы требует интегративного подхода к оценке, что является актуальной проблемой кардиологии. Доказана роль липопротеина (а) (Лп(а)) как маркера остаточного риска. В данной статье исследуется роль конечных продуктов гликирования (КПГ) в прогрессировании остаточного риска у пациентов с ИБС. Цель: оценить взаимосвязь индекса аутофлуоресценции КПГ и уровня Лп(а) для определения резидуального риска у пациентов со стабильной ИБС и дислипидемией, получающих интенсивную гиполипидемическую терапию. Материал и методы. Проведено одноцентровое проспективное исследование с участием 87 мужчин от 55 до 75 лет с ИБС и коморбидной патологией. Использованы стандартные лабораторные, включая уровень Лп(а), и инструментальные методы в соответствии с клиническими рекомендациями, а также определено накопление КПГ с помощью вычисления индекса аутофлуоресценции портативным прибором AGE Reader. Проведена коррекция дислипидемии фиксированной комбинацией розувастатина и эзетимиба, по показаниям – алирокумаб. Медиана наблюдения – 12 нед. Статистическая обработка выполнена в программе StatTech 4.9.4 (ООО «Статтех», Россия). Результаты. Участников исследования разделили на подгруппы по значению Лп(а) - 0,5 г/л (n = 41) и < 0,5 г/л (n = 46) в формате определения остаточного риска. Достижение целевых параметров липидограммы фиксированной комбинацией розувастатина и эзетимиба отмечено у 78,2% пациентов (n = 68), на тройной терапии – у 21,8% (n = 19), из них 17,2% (n = 15) принадлежат к подгруппе 1, 4,6% (n = 4) – к подгруппе 2. Индекс аутофлуоресценции на старте составлял 2,8 [2,20; 4,07]. Через 6 нед. на фоне интенсивной гиполипидемической терапии и адекватной терапии коморбидной патологии индекс аутофлуоресценции был равен 2,79 [2,12; 4,00]; через 12 нед. – 2,75 [2,02; 3,88]. По цветовой идентификации прибора индекс аутофлуоресценции красного цвета (очень высокий риск) наблюдался у 54% пациентов на старте исследования (n = 47), через 12 нед. – у 35,6% (n = 31). Исследование показало сильную прямую корреляционную связь с уровнем КПГ на старте и через 12 нед. для подгруппы с значением параметра Лп(а) - 0,5 г/л. ROC-анализ продемонстрировал, что повышение индекса аутофлуоресценции КПГ является статистически значимым предиктором повышенного резидуального риска (AUC = 0,976; 95% ДИ: 0,918–1,000; p < 0,001). Чувствительность и специфичность прогностической модели оценены в 93,3%. Выводы. Индекс аутофлуоресценции КПГ является перспективным маркером комплексной неинвазивной оценки остаточного риска у пациентов со стабильной ИБС и гиперлипопротеинемией (а), что свидетельствует о накопления КПГ как фактора, повышающего остаточный риск.
Резидуальный риск, конечные продукты гликирования, гиперлипопротеинемия (а), ишемическая болезнь сердца
Короткий адрес: https://sciup.org/149150640
IDR: 149150640 | УДК: 616.12-005.4:577.11 | DOI: 10.29001/2073-8552-2025-2895
Determination of advanced glycation end products in patients with stable coronary heart disease as a part of a comprehensive assessment of residual cardiovascular risk
Introduction. Patients with coronary artery disease (CAD) have a residual risk of adverse vascular events. The multifactorial and heterogeneous nature of this risk requires an integrative approach to assessment, which is a pressing issue in cardiology. The role of lipoprotein (a) (Lp(a)) as a marker of residual risk has been demonstrated. In this article the role of advanced glycation end products (AGEs) is being investigated in the progression of residual risk in patients with CAD. Aim: To evaluate the relationship between the autofluorescence index of advanced glycation end products and lipoprotein (a) levels to determine residual risk in patients with stable coronary artery disease and dyslipidemia receiving intensive lipid-lowering therapy. Materials and Methods: A single-center prospective study was conducted involving 87 men aged 55 to 75 years with CAD and comorbidities. Standard laboratory tests, including Lp(a) levels, and instrumental methods in accordance with clinical guidelines were used. AGEs accumulation was also determined by calculating the autofluorescence index using the portable AGE Reader device. Dyslipidemia was corrected with a fixed combination of rosuvastatin and ezetimibe; alirocumab when indicated. The median follow-up was 12 weeks. Statistical processing was performed using StatTech 4.9.4 (StatTech LLC, Russia). Results. Study participants were divided into subgroups based on Lp(a) levels -0.5 g/L (n = 41) and <0.5 g/L (n = 46) assessing residual risk. Lipid profile target parameters were achieved in 78.2% of patients (n = 68) with the fixed-dose combination of rosuvastatin and ezetimibe and in 21,8% (n = 19) with triple therapy, of which 17.2% (n = 15) belonged to subgroup 1 and 4.6% (n = 4) to subgroup 2. Autofluorescence index at baseline: 2.8 [2.20; 4.07]. After 6 weeks of intensive lipid-lowering therapy and adequate treatment of comorbid pathology, the autofluorescence index was 2.79 [2.12; 4.00]; after 12 weeks – 2.75 [2.02; 3.88]. According to the color identification of the device, the red autofluorescence index (very high risk) was observed in 54% of patients at the start of the study (n = 47), and after 12 weeks – in 35.6% (n = 31). The study showed a strong direct correlation with the level of AGEs at the start and after 12 weeks for the group with the Lp(a)-0.5 g/l. ROC analysis demonstrated that an increase in the autofluorescence index is a statistically significant predictor of increased residual risk (AUC = 0.976; 95% CI: 0.918–1.000, p < 0.001). The sensitivity and specificity of the predictive model were estimated at 93.3%. Conclusions: The AGEs autofluorescence index may be used for comprehensive noninvasive assessment of residual risk in patients with stable coronary artery disease and hyperlipoproteinemia (a).
Текст научной статьи Определение конечных продуктов гликирования у больных стабильной ишемической болезнью сердца в рамках комплексной оценки остаточного сердечно-сосудистого риска
В свете современных медико-социальных тенденций совершенствование терапевтических подходов к лечению пациентов с ишемической болезнью сердца (ИБС) является приоритетным направлением развития кардиологии. Стратегия интенсивного снижения уровня атерогенного холестерина липопротеинов низкой плотности (ХС-ЛПНП) принята как один из основополагающих принципов гиполипидемической терапии у больных ИБС. Однако на практике зачастую достижение целевого диапазона атерогенных липопротеинов не всегда возможно, что подтверждают результаты известных многоцентровых исследований [1–3]. Кроме того, приближение к таргетно-му уровню параметров липидограммы вопреки ожиданиям не устраняет полностью так называемый остаточный риск наступления нежелательных сердечно-сосудистых событий, именуемый также резидуальным, который напрямую обусловливает возникновение повторных случаев инфаркта миокарда, острого нарушения мозгового кровообращения по ишемическому типу, тромбоза стента и др. Мультифакториальность и гетерогенность природы остаточного риска требует интегративного подхода к оценке с учетом отсутствия общепризнанных валидированных шкал, учитывающих возможные факторы риска, влияющие на его значение [4]. Так, в мировом научном сообществе широко обсуждается роль ремнантов холестерина, гипертриглицеридемии, липопротеина (а) ((Лп(а)), а также курения, ожирения, метаболического синдрома, сахарного диабета 2-го типа как факторов, потенциально способных увеличивать остаточный риск, однако в настоящий момент отсутствует единый подход к комплексной оценке их синергического действия [5]. В то же время оперативное определение резидуального риска и проведение комплексных корректирующих мероприятий в дальнейшем позволит снизить летальность больных ИБС, увеличить качество и продолжительность жизни пациентов с данной патологией, что непосредственно связано с выполнением целей и задач Национального проекта «Продолжительная и активная жизнь», Федерального проекта «Борьба с сердечно-сосудистыми заболеваниями», направленных на достижение одного из ключевых показателей: увеличение на 10% числа лиц с болезнями системы кровообращения, проживших предыдущий год без острых сердечно-сосудистых событий [6].
Считается, что одним из важнейших компонентов патогенеза резидуального риска, наряду с воспалительным и тромботическим, выступает именно липидный ввиду доминирующей роли избытка циркулирующих проатеро-генных триглицерид-богатых частиц – ремнантов холестерина, липопротеинов промежуточной и очень низкой плотности. Существенный вклад в формирование остаточного кардиоваскулярного риска вносит и такой независимый, генетически детерминированный маркер, как гиперлипопротеинемия (а), – каузальный фактор возможного раннего начала и более злокачественного течения атеросклероза [7]. Концентрация Лп(а) подлежит однократному измерению в течение жизни человека по причине минимальной вариабельности в рамках генетически обусловленного уровня. Важно подчеркнуть, что традиционные терапевтические схемы гиполипидемической терапии не обеспечивают значимого изменения его уровня, а накопленные данные мировой науки на текущий момент свидетельствуют о значимой роли Лп(а) в патогенезе острых коронарных событий у молодых пациентов с субклиническими формами атеросклероза, что может быть детерминировано его выраженными атерогенными и протромботическими свойствами [8–10]. Рутинное измерение уровня Лп(а), к сожалению, до сих пор не вошло в клиническую практику, что потенциально ведет к недостаточной оценке всего комплекса причин возможного повышения уровня остаточного риска, а значит, и вероятности наступления сосудистых катастроф с позиции персонифицированного подхода у конкретного пациента [11].
Согласно актуальным данным, наиболее перспективным режимом гиполипидемической терапии считается применение комбинированных схем с использованием фиксированных комбинаций статина и ингибитора всасывания холестерина, а также ингибиторов пропротеиновой конвертазы субтилизин / кексина типа 9 (иPCSK9), которые, наряду с мощным гиполипидемическим действием, демонстрируют и потенциал к умеренному дозозависимому снижению уровня Лп(а), что в целом выражается в положительном влиянии на морфологическую структуру атеросклеротических бляшек, способствует их стабилизации [12].
С точки зрения актуальных научных знаний также активно разрабатывается проблема определения роли и места конечных продуктов гликирования (КПГ) в прогрессировании широкого спектра внутренней патологии. Данные вещества синтезируются в ходе каскадных многоступенчатых неферментативных реакций гликирования белков, липидов и других веществ с образованием прочных ковалентных связей, интегрирующих тканевые элементы в единые пласты с измененным функционалом: к примеру, волокна эластина связываются ригидными поперечными сшивками, что способствует увеличению жесткости сосудистой стенки, ее ремоделированию, а также усугубляет эндотелиальную дисфункцию, в конечном итоге, усиливая процесс асептического воспаления сосудистой стенки, инфильтрации атерогенными липопротеинами и агрегацию тромбоцитов [13]. Указанные процессы взаимно интегрируют патогенетические детерминанты резидуального риска (липидный, воспалительный, тромботический компоненты), что обусловливает прогрессирование атеросклероза, увеличение частоты макро- и микрососудистых осложнений у пациентов с сахарным диабетом 2-го типа, а также нарастание диастолической дисфункции в самом миокарде, что напрямую ведет к возникновению сосудистых катастроф у пациентов с кардиоваскулярными заболеваниями [14]. В настоящий момент широко обсуждается корреляция содержания КПГ в тканях организма и коже, а накопленные данные убедительно доказывают перспективность неинвазивного способа определения уровня КПГ методом аутофлуоресценции с помощью компактных ридеров, что нашло отражение в предикции ряда заболеваний и состояний: так, по уровню КПГ можно стратифицировать абсолютный суммарный сердечно-сосудистый риск, но не резидуальный риск у пациента с ИБС, что впервые рассматривается именно в настоящем исследовании [15].
Таким образом, ввиду ограниченности интегрированных персонифицированных подходов к оценке остаточного риска у пациентов с ИБС и критической необходимости отдалить возможные нежелательные кардиоваскулярные события, поиск новых маркеров комплексной его оценки является крайне актуальной проблемой медицины, а использование КПГ в аспекте стратификации остаточного риска у пациентов с ИБС создает потенциальные перспективы для совершенствования помощи больным сердечно-сосудистой патологией.
Цель: оценить взаимосвязь индекса аутофлуоресценции КПГ и уровня ЛП(а) для определения резидуального риска у пациентов со стабильной ИБС и дислипидемией, получающих интенсивную гиполипидемическую терапию.
Материал и методы
Проведено одноцентровое проспективное исследование с участием 87 мужчин – пациентов кардиологического кабинета Курской городской больницы № 6 за период с июля 2023 г. по июнь 2025 г., страдающих стабильной ИБС и нетяжелой коморбидной патологией на фоне дислипидемии. Исследование проведено под наблюдением регионального этического комитета (протокол № 3 от 15.03.2023 г.), осуществлено в полном соответствии с принципами Good Clinical Practice (GCP) и Хельсинкской декларации. Процедура включения в исследование предполагала наличие письменного информированного согласия на участие от каждого из пациентов. Критериями включения стали: мужской пол, возраст от 55 до 75 лет, наличие стабильных форм ИБС, дислипидемии, сопутствующей патологии в стадии компенсации (метаболический синдром, сахарный диабет без множественных осложнений, артериальная гипертония). Критерии невключения: женский пол, возраст менее 55 и более 75 лет, тяжелая коморбидная патология в стадии декомпенсации, выраженная гипертриглицеридемия свыше 5 ммоль/л.
На старте каждому участнику выполнили полный объем лабораторных и инструментальных методов исследования в соответствии с актуальными клиническими рекомендациями: оценку общего анализа крови и мочи, липидного профиля, показателей углеводного, азотистого, пуринового обмена в Централизованной клинико-диагностической лаборатории на базе ОБУЗ «Курский онкологический научно-клинический центр им. Г.Е. Остро-верхова», а также измерение уровня Лп(а) турбидиметрическим методом в частной клинико-диагностической лаборатории на автоматическом биохимическом анализаторе Mindray BS-620M (Китай) на личные средства пациентов. Забор крови осуществляли из локтевой вены утром натощак. Из инструментальных методов обследования, помимо рутинных (электрокардиография, эхокардиография), проводили оценку накопления КПГ методом аутофлуоресценции с помощью специального портативного ридера AGE Reader (Diagnoptics Technologies B.V., Нидерланды) трехкратно на коже внутренней поверхности средней трети предплечья с определением среднего значения полученного индекса аутофлуоресценции: данный аппаратно-программный комплекс по уровню КПГ в коже пациента и его возрасту автоматически присваивает полученному числовому значению индекса аутофлуоресценции градацию цвета – от зеленого до красного. Наивысшую степень риска можно интерпретировать при числовом значении искомого параметра выше 3 в соответствии с инструкцией прибора.
Дизайн исследования предполагал распределение общего пула пациентов на подгруппы по детерминирующему признаку – наличию уровня Лп(а) с пограничным значением более 0,5 г/л, который в контексте исследования принимали за ведущий маркер повышенного резидуального риска: подгруппа 1 с гиперлипопротеинемией (а) (Лп(а)+) включала 41 пациента (повышенный остаточный риск). При отсутствии гиперлипопротеинемии (а) (Лп(а)–) в подгруппу 2 (умеренный остаточный риск) включили 46 участников исследования. Медиана наблюдения составила 12 нед. с 3 контрольными точками – визитами, на которых повторно оценивали липидограмму и КПГ.
Всем больным была назначена адекватная терапия основного заболевания и коморбидной патологии в соответствии с актуальными клиническими рекомендациями, в том числе была инициирована интенсивная комбинированная статинотерапия в объеме розувастатина 20 мг и эзетимиба 10 мг в виде фиксированной комбинации, а при отсутствии положительной динамики достижения целевого уровня ХС-ЛПНП через 6 нед. к искомой терапии добавляли иPCSK9 алирокумаб 150 мг подкожно 1 раз в 14 дней.
Статистическую обработку проводили с помощью от- ечественного программного обеспечения – программы StatTech 4.9.4 (ООО «Статтех», Россия). Распределение количественных показателей проверяли на соответствие нормальному распределению по критерию Шапиро – Уилка. Далее количественные показатели описывали в зависимости от полученного результата с помощью средних значений (M) и стандартных отклонений (SD), M ± SD, а в случае отсутствия нормального распределения, – медианой (Ме) и межквартильным промежутком [Q1; Q3], Ме [Q1; Q3]. Сравнение количественных показателей в двух независимых подгруппах проводили по критерию Стьюдента или по критерию Манна – Уитни, категориальные показатели с помощью точного критерия Фишера. Корреляционные связи между двумя количественными показателями оценивали с помощью коэффициента ранговой корреляции Спирмена. Построены однофакторные модели линейной и логистической регрессии. Критический уровень значимости при проверке статистических гипотез принимали равным 0,05.
Результаты
Проведена интегративная оценка клинико-анамнестических характеристик исследуемого пула пациентов. Медиана среднего возраста участников составила 66,50 [64,00; 70,75] года; средние значения окружности талии – 97,73 ± 12,68 см, индекса массы тела – 29,38 ± 3,99 кг/м2. Структурированный анализ анамнестических факторов изучаемых подгрупп в зависимости от наличия гиперли-попротеинемии (а) отражен в таблице 1.
Таблица 1 . Интегративная характеристика исследуемой субпопуляции в зависимости от критерия наличия гиперлипопротеинемии (а) Table 1 . Integrative characteristics of the studied subpopulation depending on the criterion of the presence of hyperlipoproteinemia (a)
|
Факторы |
87 пациентов |
p |
|
|
Подгруппа 1 Лп(а)+, n = 41 |
Подгруппа 2 Лп(а)–, n = 46 |
||
|
Возраст |
65,93 ± 6,13 |
66,80 ± 5,95 |
0,698 |
|
Индекс массы тела |
30,40 ± 3,36 |
28,36 ± 4,40 |
0,164 |
|
Окружность талии |
104,67 ± 11,18 |
90,80 ± 10,24 |
0,001 |
|
Курение, абс. (%) |
15 (36,6) |
13 (28,2) |
0,106 |
|
Инфаркт миокарда, абс. (%) |
25 (61) |
18 (39) |
0,032 |
|
Неконтролируемая артериальная гипертензия, абс. (%) |
19 (46,3) |
24 (52,1) |
0,128 |
|
Сахарный диабет 2-го типа, абс. (%) |
19 (46,3) |
17 (37) |
0,027 |
|
Фибрилляция предсердий, абс. (%) |
6 (14,6) |
5 (10,8) |
0,561 |
|
Мультифокальный атеросклероз, абс. (%) |
11 (26,8) |
6 (13) |
0,047 |
|
Избыточная масса тела, абс. (%) |
19 (46,3) |
23 (50) |
0,678 |
|
Ожирение 1–2-й степени, абс. (%) |
11 (26,8) |
10 (21,7) |
0,325 |
|
Наличие хронической болезни почек, абс. (%) |
2 (4,8) |
3 (6,5) |
0,089 |
Примечание: статистически значимый уровень p < 0,05.
В ходе анализа исследуемой субпопуляции статистически значимыми стали следующие анамнестические характеристики: объем талии, наличие инфаркта миокарда в анамнезе, сахарного диабета 2-го типа, а также мультифокального атеросклероза, где регистрировалось статистически значимое различие у пациентов в подгруппе с гиперлипопротеинемией (а).
В рамках определения липидного профиля в составе общего холестерина (ОХ), холестерина липопротеинов высокой плотности (ХС-ЛПВП), ХС-ЛПНП и уровня триглицеридов (ТГ) на старте исследования достижение целевого значения менее 1,4 ммоль/л по параметру ХС-ЛПНП зарегистрировано не было. В дополнение были проанализированы и сопоставлены численные значения индекса аутофлуоресценции по ведущему фактору ги-перлипопротеинемии (а), определяющего повышение значения остаточного риска. Анализ продемонстрировал статистически значимое различие для уровня индекса аутофлуорсеценции КПГ; в свою очередь при оценке параметров липидного спектра статистически значимых различий между подгруппами зафиксировано не было (табл. 2).
Примечание: ОХ – общий холестерин, ТГ – триглицериды, ХС-ЛП-ВП – липопротеины высокой плотности, ХС-ЛПНП – липопротеины низкой плотности. КПГ – конечные продукты гликирования. Статистически значимый уровень p < 0,05.
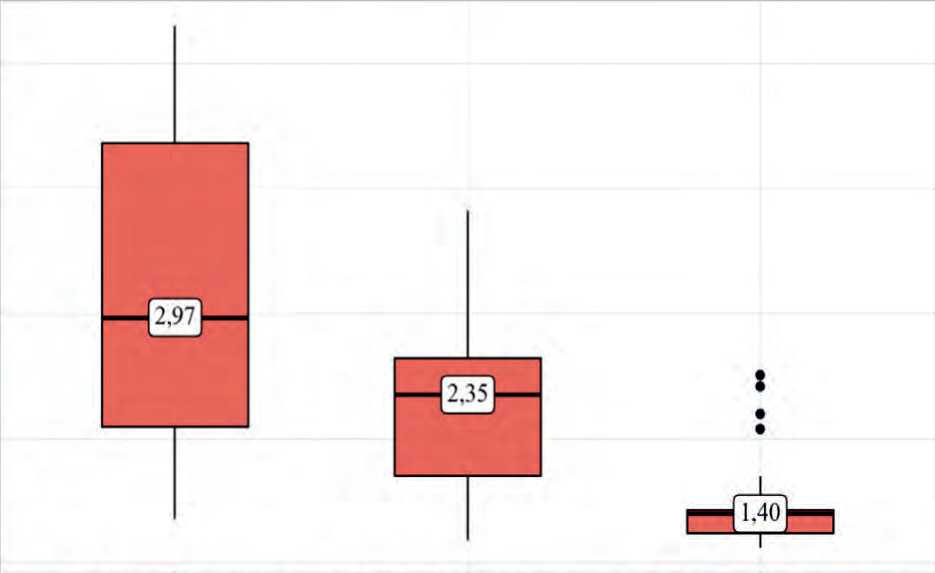
Таблица 2 . Результаты сравнения средних значений показателей липидограммы и конечных продуктов гликирования зависимости от гиперлипопротеинемии (а) на старте исследования
Table 2 . Comparison results of the average values of lipidogram and AGE indicators depending on hyperlipoproteinemia (a) at the start of the study
|
Показатели на старте исследования |
87 пациентов |
p |
|
|
Подгруппа 1 Лп(а)+, n = 41 |
Подгруппа 2 Лп(а)–, n = 46 |
||
|
ОХ |
5,27 ± 1,18 |
4,73 ± 1,47 |
0,277 |
|
ХС-ЛПНП, ммоль/л |
3,33 ± 1,01 |
2,90 ± 1,33 |
0,325 |
|
ТГ |
1,86 ± 0,88 |
1,36 ± 0,56 |
0,073 |
|
ХС-ЛПВП |
1,17 ± 0,37 |
1,10 ± 0,16 |
0,480 |
|
КПГ |
4,00 [3,05; 4,90] |
2,20 [1,85; 2,45] |
< 0,001 |
В ходе проведения коррекции дислипидемии фиксированной комбинацией статина и эзетимиба уже ко 2-му визиту через 6 нед. от начала терапии 78,2% пациентов ( n = 68) достигли целевого значения ХС-ЛПНП, из них 29,9% ( n = 26) принадлежат к подгруппе 1 с гиперлипо-протеинемией (а), 48,3% ( n = 42) к подгруппе 2 без диагностированной гиперлипопротеинемии (а). Оставшиеся 21,8% пациентов ( n = 19), не достигшие целевого значения ХС-ЛПНП, были переведены на тройную терапию и к 3-му визиту через 12 нед. от начала исследования достигли таргетного уровня ХС-ЛПНП менее 1,4 ммоль/л, из них 17,2% ( n = 15) принадлежат к подгруппе 1, 4,6% ( n = 4) – к подгруппе 2. В стартовой фазе исследования среднее значение ХС-ЛПНП по всем участникам исследования составило 2,97 ± 1,15 ммоль/л, через 6 нед. терапии фиксированной комбинацией розувастатина с эзе-тимибом – 2,35 ± 0,71 ммоль/л, через 12 нед. наблюдения – 1,4 ± 0,24 ммоль/л. Динамика достижения целевых значений ХС-ЛПНП на фоне назначения комбинированных схем по визитам представлена на рисунке 1.
Характерно, что среднее значение параметра Лп(а) у когорты пациентов, не достигших целевого значения ХС-ЛПНП с помощью стандартной двухкомпонентной схемы, отличалось от такового у пациентов, достигших таргетного уровня только на тройном режиме терапии с добавлением иPCSK9: 0,5 ± 0,096 против 0,4 ± 0,137 г/л.
В ходе регистрации индекса аутофлуоресценции как главного параметра, отражающего процессы биосинтеза КПГ в коже пациента, с помощью ридера AGE Reader на старте исследования данный индекс составил 2,8 [2,20; 4,07]. Через 6 нед. на фоне комбинированной гиполипи-демической терапии, а также адекватной терапии комор-
ХС-ЛПНП до лечения ХС-ЛПНП через 6 недель ХС-ЛПНП через 12 недель
Рис. 1. Позитивная динамика достижения целевого уровня холестерина липопротеинов низкой плотности у общей исследуемой субпопуляции
Fig. 1. Positive dynamics of achieving the target level of LDL-C in the common studied subpopulation
бидной патологии индекс аутофлуоресценции составил 2,79 [2,12; 4,00], через 12 нед. – 2,75 [2,02; 3,88], что демонстрирует более выраженное снижение при применении более интенсивных схем. Изменения уровня КПГ в подгруппах отражены в таблице 3.
Таблица 3 . Динамика определения индекса аутофлуоресценции конечных продуктов гликирования в изучаемых подгруппах
Table 3 . Dynamics of determination of the autofluorescence index of advanced glycation end products in the studied subgroups
|
Показатели |
Подгруппа 1 Лп(а)+, n = 41 |
Подгруппа 2 Лп(а)–, n = 46 |
p |
|
КПГ до лечения, Me [IQR] |
4,00 [3,05; 4,90] |
2,20 [1,85; 2,45] |
< 0,001 |
|
КПГ через 6 недель, Me [IQR] |
4,00 [3,00; 4,70] |
2,10 [1,85; 2,40] |
< 0,001 |
|
КПГ через 12 недель, Me [IQR] |
3,80 [2,90; 4,55] |
2,00 [1,80; 2,40] |
< 0,001 |
Примечание: статистически значимый уровень p < 0,05.
На основе показаний данного аппаратно-программного комплекса по уровню КПГ и возрасту пациента с автоматическим присвоением градации индексу аутофлуоресценции резидуальный риск можно интерпретировать как очень высокий при значении искомого параметра выше 3. Очевидно, исходя из данных таблицы 3, что более высокие значения индекса аутофлуоресценции зафиксированы в подгруппе 1 у пациентов с гиперлипо-протеинемией (а) на всех этапах исследования. С учетом цветовой идентификации прибора индекс аутофлуоресценции в диапазоне красного цвета (очень высокий риск) наблюдался у 54% пациентов на старте исследования ( n = 47), после проведения коррекции дислипидемии и сопутствующей патологии – у 35,6% ( n = 31) Регистрируемое снижение данного параметра на фоне проводимой терапевтической стратегии коррекции гиперхолестеринемии свидетельствует о перспективности тактики комплексного воздействия для возможной коррекции остаточного риска.
С целью оценки взаимосвязей зарегистрированных изменений уровня КПГ и Лп(а) на старте и финише клинического испытания в зависимости от достижения уровня ХС-ЛПНП на различных режимах терапии определялся коэффициент ранговой корреляции Спирмена, описывалась сила связи по шкале Чеддока (табл. 4).
Таблица 4 . Корреляционные взаимосвязи липопротеина (а) и индекса аутофлуоресценции конечных продуктов гликирования у испытуемых на момент входа в исследование и через 12 недель
Table 4 . Сorrelations between Lp(a) and the autofluorescence index of AGEs in subjects at entry into the study and after 12 weeks
|
Показатель для подгруппы |
Характерис тика корреляцион ной связи |
||
|
ρ |
Теснота связи по шкале Чеддока |
p |
|
|
Лп(а)+ / КПГ до лечения |
0,739 |
Высокая |
< 0,001 |
|
Лп(а)+ / КПГ через 12 недель |
0,762 |
Высокая |
< 0,001 |
|
Лп(а)– / КПГ до лечения |
0,795 |
Высокая |
< 0,001 |
|
Лп(а)– / КПГ через 12 недель |
0,774 |
Высокая |
< 0,001 |
Примечание: Лп(а) – липопротеин (а), КПГ – конечные продукты гликирования, ρ – коэффициент ранговой корреляции Спирмена. Note: Lp(a) – lipoprotein (a), AGEs – advanced glycation end products, ρ – Spearman's rank correlation coefficient.
При оценке взаимозависимости данных параметров была установлена прямая линейная связь уровня КПГ со значением Лп(а) как до, так и после лечения, именно для подгруппы с значением параметра Лп(а) более 0,5 г/л. Линейная связь получена в случае достижения целевого уровня ХС-ЛПНП вне зависимости от режима гиполипи-демической терапии. Наблюдаемая зависимость КПГ от Лп(а) до лечения описывается уравнением парной линейной регрессии: YКПГ до лечения = 3,398 × XЛп(а) + 1,271, после лечения – YКПГ через 12 нед. = 3,355 × XЛ-п(а) + 1,065. Повышение уровня Лп(а) выше порогового сопровождается повышением показателя индекса аутофлуоресценции КПГ, что в совокупности можно интерпретировать как увеличение остаточного риска. Описанные корреляционные взаимосвязи на финише исследования в подгруппе с Лп(а) более 0,5 г/л можно проиллюстрировать диаграммой рассеивания (рис. 2).
При проведении дальнейшей интегральной оценки вклада показателя индекса аутофлуоресценции КПГ в предикцию высокого резидуального риска у пациентов был выполнен ROC-анализ модели однофакторной логистической регрессии прогнозирования высокого резидуального риска (рис. 3).
Повышение индекса аутофлуоресценции КПГ является прогностически значимым предиктором повышенного резидуального риска (AUC = 0,976; 95% ДИ: 0,918–1,000; p < 0,001). Пороговая вероятность в точке cut-off, определенная по критерию Юдена, составила 0,670. Чувствительность и специфичность прогностической модели оценены одинаково – в 93,3%.
Обсуждение
В исследуемой субпопуляции пациентов комплексный анализ анамнестических факторов выявил высокую статистическую значимость ассоциации распространенности инфаркта миокарда, сахарного диабета и мультифокального атеросклероза с гиперлипопротеинемией (а) как важного параметра остаточного риска, что объясняется высокими атерогенными и протромботическими свойствами данной частицы [7, 8]. Следует отметить, что интенсивность синтеза КПГ на биомолекулярном уровне также была выше у пациентов с гиперлипопротеинеми-ей (а), что в общей связи детерминирует более высокий остаточный риск и согласуется с последними научными данными по изучению проблемы резидуального риска [11, 16].
Анализ корреляционной взаимосвязи гиперлипопро-теинемии (а) и высокого значения индекса аутофлуоресценции КПГ у испытуемых на момент входа в исследование и через 12 нед. после достижения целевого значения ХС-ЛПНП демонстрирует высокую тесноту связи по шкале Чеддока. Это подтверждает перспективность неинвазивного динамического определения КПГ, в том числе как интегрального маркера именно остаточного риска, в то время как апробированные методики стратификации суммарного сердечно-сосудистого риска по индексу аутофлуоресценции известны уже длительное время [15]. Отметим важность комплексного определения и других возможных маркеров остаточного риска для данной субпопуляции, поскольку интеграция различных параметров создает персонализированный подход к ведению пациента. Фактически индекс аутофлуоресценции отражает накопление связанных фракций КПГ, образовавших прочные ковалентные связи с эластинами и коллагеном
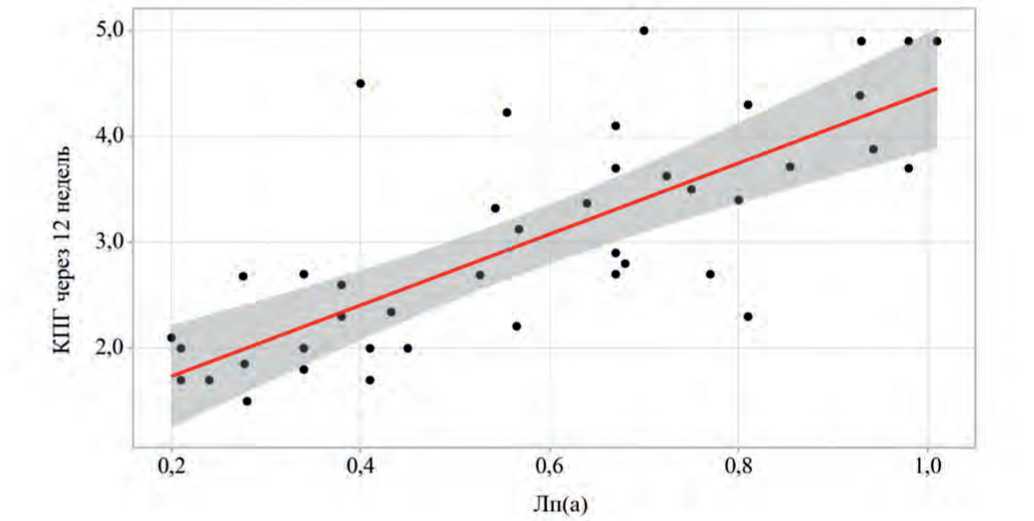
Рис. 2. График линейной зависимости конечных продуктов гликирования через 12 недель от уровня липопротеина (а) в подгруппе 1
Fig. 2. Graph of the linear regression dependence of AGEs after 12 weeks on the level of Lp(a) in the phenotype of combined hypercholesterolemia in the subgroup 1
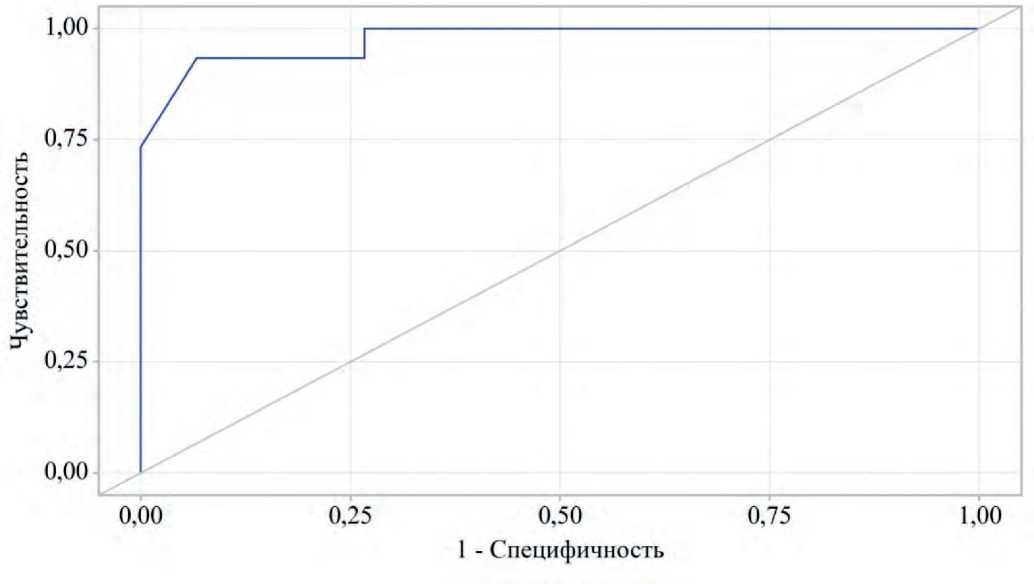
Рис. 3. ROC-кривая, характеризующая дискриминационную способность индекса аутофлуоресценции конечных продуктов гликирования при прогнозировании очень высокого резидуального риска
Fig. 3. ROC curve characterizing the discriminatory ability of advanced glycation end product autofluorescence index in predicting very high residual risk
кожи, что находится в прямой корреляции с количеством КПГ в стенке артериолы, т. к. КПГ способствуют усугублению эндотелиальной дисфункции и запуску фибротиче-ских процессов ремоделирования стенки сосуда. Отсюда на фоне оксидативного стресса и персистирующего низкоинтенсивного воспаления возникают микроповреждения комплекса интима медиа, инфильтрация стенки сосуда атерогенными липопротеинами и повышенная адгезия тромбоцитов; таким образом можно объяснить про- грессирование атеросклероза и наличие потенциальной возможности наступления сосудистых катастроф [19]. Следовательно, три ведущих патогенетических звена остаточного риска (липидный, воспалительный, тромботический компоненты) сходятся воедино в интегральном маркере накопления КПГ [17].
Потенциальная возможность по снижению значения данного показателя может быть объяснена за счет преимущественной оси действия: КПГ – рецептор к КПГ, который может быть представлен трансмембранной или растворимой формой, притом за счет трансмембранной формы осуществляются проатерогенные эффекты, за счет растворимой – индукция провоспалительных факторов; таким образом, существует возможность связывания определенной фракции КПГ и их модуляции на фоне различных воздействий [18].
Статистически значимые корреляционные взаимосвязи, полученные при определении индекса аутофлуоресценции КПГ в ходе исследования, демонстрируют добавочную прогностическую ценность данного показателя при оценке остаточного риска. Преимуществом данной методики является некоторая динамичность показателя, которая была обнаружена в данном исследовании: при постоянном уровне Лп(а) и малой склонности его уровня к изменениям индекс аутофлуоресценции может меняться в ответ на проведение комплексной адекватной терапии ИБС и сопутствующей патологии, удержаниие целевого диапазона липидограммы, артериального давления, глюкозы и т. д.
Ограничения исследования: в проведенном исследовании не было выявлено статистически значимых взаимосвязей в отношении режима терапии (двойная или тройная комбинация) как определяющего фактора изменения значения индекса аутофлуоресценции, важен лишь факт достижения целевого значения ХС-ЛПНП. Однако существуют данные о потенциальной способности препаратов группы иPCSK9 несколько снижать уровень Лп(а) [10]. Возможно, статистически значимые взаимосвязи не были получены в связи с небольшим объемом выборки и недостаточным количеством времени, что создает необходимость продолжать дальнейшие клинические исследования. Кроме того, ограничения исследования могут быть связаны с возможными изменениями кожи пациента (тургор, влажность, возможные повреждения, волосяной покров), которые механически могут препятствовать правильному определению КПГ.
Заключение
Таким образом, определение КПГ можно считать перспективным маркером комплексной неинвазивной оценки остаточного риска у пациентов со стабильной ИБС. Получены статистически значимые корреляционные взаимосвязи между значением индекса аутофлуоресценции КПГ и повышенным уровнем Лп(а) на фоне достижения целевых параметров ХС-ЛПНП. Повышение искомого параметра Лп(а) ассоциировано с меньшей частотой достижения целевых значений атерогенных липопротеинов на стандартной двойной терапии. Исследование показало, что накопление КПГ на фоне гиперлипопротеине-мии (а) – комбинация факторов, которая в совокупности повышает остаточный риск, это позволяет использовать индекс аутофлуоресценции КПГ в качестве прогностического инструмента оценки остаточного риска, наряду с повышенным уровнем Лп(а) более 0,5 г/л. Таким образом, проблема остаточного риска порождает уникальные диагностические и терапевтические вызовы, требующие комплексного подхода к совершенствованию алгоритмов помощи больным ИБС.


