Определение конформационного состава этиленгликоля методом спектроскопии КР и расчетов DFT
Автор: Новиков В.С.
Журнал: Бюллетень науки и практики @bulletennauki
Рубрика: Естественные науки
Статья в выпуске: 10 т.10, 2024 года.
Бесплатный доступ
Целями исследования этиленгликоля (ЭГ), определение линий КР гликолей, которые можно использовать для анализа конформационного и изомерного состава молекул, а также оценка конформационного состава молекул гликолей. По результатам расчетов обнаружено, что линии КР в области около 800 см-1 являются индикаторами присутствия молекул ЭГ в конформациях типа xGy или xG'y , где x и y могут быть t , g или g' . В экспериментальных спектрах КР жидкого ЭГ эта линия высокоинтенсивная, следовательно, в жидком ЭГ молекулы в указанных конформациях присутствуют большом количестве. Этот результат также подтверждается полученными содержаниями молекул ЭГ в различных конформациях на основе расчетов. Для описания области 2600-4000 см-1 спектров КР гликолей требуется учет межмолекулярных взаимодействий.
Спектроскопия комбинационного рассеяния света, гликоли, этиленгликоль, dft
Короткий адрес: https://sciup.org/14131551
IDR: 14131551 | УДК: 538.9 | DOI: 10.33619/2414-2948/107/02
Determination of the conformational composition of ethylene glycol by RAS spectroscopy and DFT calculations
The objectives of the study of ethylene glycol (EG) are to determine the Raman lines of glycols that can be used to analyze the conformational and isomeric composition of molecules, as well as to assess the conformational composition of glycol molecules. Based on the calculations, it was found that the Raman lines in the region of about 800 cm-1 are indicators of the presence of EG molecules in conformations of the xGy or xG'y type, where x and y can be t , g or g' . In the experimental Raman spectra of liquid EG, this line is highly intense, therefore, molecules in the indicated conformations are present in large quantities in liquid EG. This result is also confirmed by the obtained contents of EG molecules in various conformations based on calculations. In order to describe the 2600-4000 cm-1 region of the Raman spectra of glycols, it is necessary to take into account intermolecular interactions.
Текст научной статьи Определение конформационного состава этиленгликоля методом спектроскопии КР и расчетов DFT
Бюллетень науки и практики / Bulletin of Science and Practice
Этиленгликоль (ЭГ, HO-CH 2 -CH 2 -OH) широко используется в химической, пищевой, фармацевтической и косметической промышленностях. Различный конформационный состав образца приводит к различным физико-химическим свойствам и колебательным спектрам конфомаций ЭГ.
Для молекулы ЭГ возможны 27 стабильных конформаций, из которых только 10 уникальны по структуре и колебательным спектрам, а остальные получаются из этих 10 поворотом и (или) отражением. Энергии молекул в различных конформациях сильно отличаются, что приводит к тому, что некоторые конформации намного более вероятны, чем другие.
H2
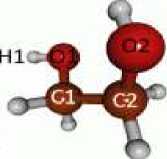
Рисунок 1. Химическая структура молекулы этиленгликоля
Общепринятые обозначения конформаций молекулы ЭГ состоят из трех букв. Первая и третья строчные буквы обозначают торсионные углы H1-O1-C1-C2 и C1-C2-O2-H2 ( транс ( t ), гош ( g ) или гош' ( g' )) соответственно, используя следующую нумерацию атомов в скелете молекулы: H1-O1-C1-C2-O2-H2 (Рисунок 1). Вторая заглавная буква ( T , G или G' ) обозначает торсионный угол O1-C1-C2-O2. Буквы g и G — это гош -конформеры, соответствующие вращению связей по часовой стрелке, а буквы g' и G' - гош -конформеры, соответствующие вращению против часовой стрелки.
Конформационный состав и межмолекулярные взаимодействия молекул ЭГ изучались во многих работах. I. Bakó, T. Grósz, G. Pálinkás, M. C. Bellissent-Funel исследовали структуру жидкого ЭГ методами рентгеноструктурного анализа и дифракции нейтронов при комнатной температуре и установили, что три соседние молекулы образуют три межмолекулярные водородные связи [1].
Расчёты различными ab initio методами, опубликованные в работах, показали, что молекулы ЭГ в конформациях tGg' , gGg' и g'Gg' имеют наименьшие энергии [2-11].
В работах ряда авторов определены следующие наиболее устойчивые конформации ЭГ: tGg' , gGg' , g'Gg' , tTt , tTg и gTg' [2, 6, 11].
В работе J. S. Lomas получен схожий порядок конформаций: tGg' , gGg' , g'Gg' , tTt , tGt и gGg [3].
C. J. Cramer, D. G. Truhlar на основе расчётов в приближении газовой фазы определили следующий порядок конформаций: tGg ', gGg ', g ' Gg ', tTg , gTg ' и gGg [5].
P. E. Kristiansen, K. M. Marstokk, H. Møllendal, L. Parker, L. Niinistö, Schwartz M. используя метод Монте-Карло, получили следующий порядок конформаций молекул ЭГ в водном растворе: tGg , gGg' , tGg' , tGt , tTt и gGg [12, 13].
В различных работах подтвердили преобладание молекулярных конформаций tGg' и gGg' ЭГ: методом микроволновой спектроскопии [14, 15], дифракции электронов для газовой фазы [2], спектроскопии ЯМР для раствора [16] и рентгеноструктурного анализа для жидкой фазы [1].
Rodnikova M. N., Solovei A. B., Solonina I. A. Chopra D. был проведен рентгеноструктурный анализ кристаллического ЭГ и установлено, что в кристаллическом состоянии молекулы ЭГ находятся в конформации tGg' [17, 18]. При этом кристаллическая структура стабилизирована сетью межмолекулярных связей, это также подтверждено в работе [19].
В ряде работ сообщалось об исследованиях конформационного состава молекул ЭГ методом спектроскопии КР [20-24].
Однако авторы этих работ рассматривали только две конформации: «гош» и «транс» относительно торсионного угла О-С-С-О, не принимая во внимание все устойчивые уникальные структурные конформации молекулы ЭГ.
Материал и методы исследования
Регистрация спектров КР гликолей производилась на установке для регистрации спектров КР. Она состоит из лазера Sapphire SF 532 (Coherent Inc., США), двойного монохроматора U1000 (Jobin Yvon, Франция) и фотоумножителя, работающего в режиме счета фотонов. Длина волны возбуждающего излучения была 532 нм. Спектры записывались при 90°-рассеянии со спектральным разрешением 5 см-1.
В данной работе исследовались коммерческие образцы ЭГ чистота образца была не 99% (Sigma-Aldrich, ReagentPlus).
Результаты и обсуждение
При комнатной температуре были записаны поляризованные спектры КР коммерческого образца жидкого ЭГ (Sigma-Aldrich, ReagentPlus, 99%) при параллельном и скрещенном направлениях поляризации возбуждающего и рассеянного излучений. На Рисунке 2 представлены поляризованные спектры КР ЭГ нормированные с учётом разных свойств оптических элементов спектрометра для света с различными направлениями поляризации. Эти спектры использовались для получения неполяризованных спектров гликолей, которые сравнивались с рассчитанными спектрами.
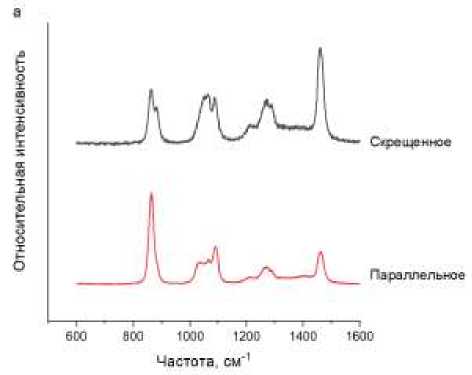
Рисунок 2. Спектры КР ЭГ, записанные при параллельном и скрещенном направлениях поляризации возбуждающего и рассеянного излучений: а – в диапазоне 600-1600 см-1; б – в диапазоне 2600-3100 см-1
Используя анимацию рассчитанных колебаний для ЭГ было определено, что все линии около 800 см-1 относятся к смешанным колебаниям, в основном к комбинации валентных колебаний С-С и С-О связей, линия около 1300 см-1 преимущественно отвечает деформационным колебаниям СН 2 групп.
Были рассчитаны структуры и спектры молекулы ЭГ во всех возможных стабильных онформациях. В Таблице приведены рассчитанные разности энергий относительно наиболее выгодной, относительное содержание (по Больцману, при 298 К) молекул во всех уникальных стабильных конформациях для ЭГ. Обнаружено, что наиболее вероятными конформациями ЭГ при расчётах в приближении газовой фазы являются tGg' (около 48%), gGg' (около 38%) и g'Gg' (около 9%) (Таблица).
Рассчитанное содержание молекул ЭГ в остальных конформациях не превышает 1,5%.
Для трёх наиболее вероятных конформаций молекулы ЭГ порядок совпадает с результатами работ [2-11].
Таблица
ОТНОСИТЕЛЬНЫЕ ЭНЕРГИИ И СОДЕРЖАНИЕ МОЛЕКУЛ ЭГ
В РАЗЛИЧНЫХ КОНФОРМАЦИЯХ
|
Конформация |
Число конформаций в группе |
ΔE, кДж/моль |
Содержание*, % |
|
|
1 |
tGg' |
4 |
0,000 |
48,36 |
|
2 |
gGg' |
4 |
0,621 |
37,64 |
|
3 |
g'Gg' |
2 |
2,436 |
9,05 |
|
4 |
tTg |
4 |
8,928 |
1,32 |
|
5 |
gTg' |
2 |
8,049 |
0,94 |
|
6 |
gTg |
2 |
8,745 |
0,71 |
|
7 |
tGg |
4 |
10,656 |
0,66 |
|
8 |
gGg |
2 |
8,949 |
0,65 |
|
9 |
tGt |
2 |
10,117 |
0,41 |
|
10 |
tTt |
1 |
9,506 |
0,26 |
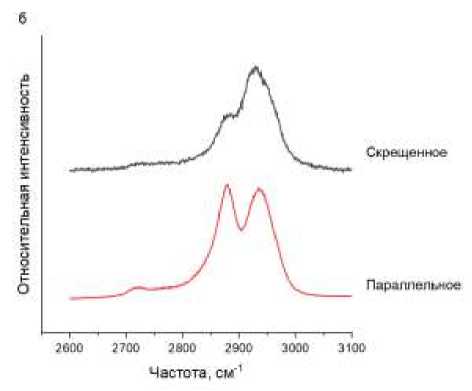
На Рисунке 3 представлены спектры КР всех рассчитанных стабильных конформаций молекул ЭГ, нормированные по интенсивности на максимум наиболее интенсивной линии в области 1400-1600 см (Таблица).
Было обнаружено, что положения максимумов линий в области 800-900 см-1 зависят от конформации молекулы, а линия в диапазоне около 800 см-1 присутствует только в спектрах молекул в конформациях ЭГ типа xGy и xG'y , здесь x и y — это конформеры t , g или g' . Соответственно, спектры молекул в конформациях типа xTy отличаются от спектров других конфрмаций, что может быть использовано для определения конформационного состава молекул ЭГ по спектрам КР.
Линии в области 2800-3100 см-1 отвечают валентным колебаниям CH, CH 2 и CH 3 групп и обертона фундаментальных колебаний. Таким образом, высокочастотный диапазон не может быть хорошо описан расчётами в используемом приближении. Однако, вид рассчитанных спектров КР в этом диапазоне сильно отличается для различных конформаций молекул ЭГ (Рисунок 3).
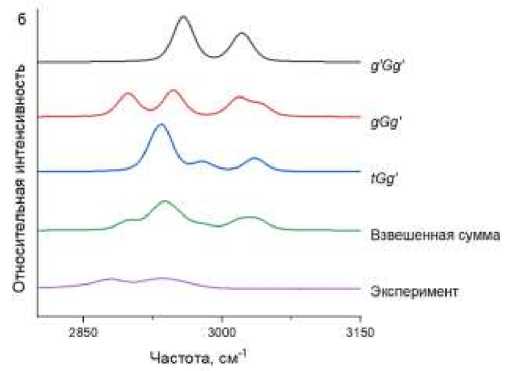
На Рисунке 4 продемонстрированы экспериментальные неполяризованные спектры КР, рассчитанные спектры КР молекул в наиболее вероятных конформациях и взвешенная сумма спектров КР молекул во всех стабильных конформациях с учётом их содержаний (Таблица). Показано, что взвешенная сумма рассчитанных спектров КР описывает основные особенности экспериментальных спектров КР в области 600-1600 см-1.
В диапазоне 2800-3100 см-1 наблюдаются значительные отличия экспериментальных и рассчитанных спектров КР (Рисунок 4). Все наблюдаемые отличия могут быть связаны с влиянием межмолекулярных взаимодействий, в частности межмолекулярных водородных связей, на конформационный состав гликолей и параметры их спектров КР.
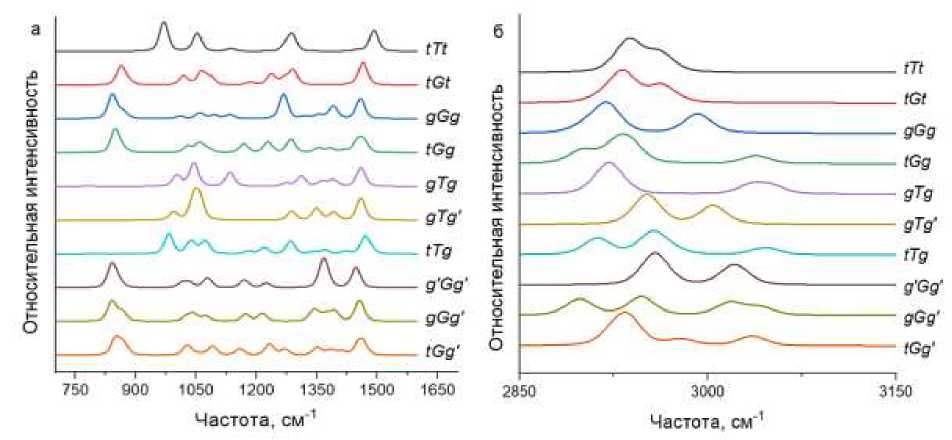
Рисунок 3. Теоретические спектры КР молекул ЭГ во всех стабильных конформациях: а – 6001600 см-1; б – 2800-3100 см-1
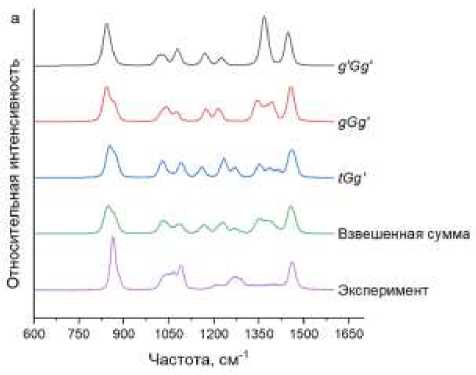
Рисунок 4. Теоретические спектры КР наиболее низких по энергии стабильных конформаций ЭГ, взвешенная сумма спектров КР всех стабильных конформаций ЭГ и экспериментальный спектр КР ЭГ: а – 600-1600 см-1; б – 2800-3100 см-1
Заключение
Таким образом, были рассчитаны структуры, содержания и спектры КР молекул ЭГ во всех стабильных конформациях с использованием метода ТФП в приближении газовой фазы. Рассчитанные спектры описывают экспериментальные спектры КР жидких веществ в области 600-1600 см-1.
На основании данных квантово-химических расчётов сделан вывод, что линии КР в области около 800 см-1 являются индикаторами присутствия молекул ЭГ в конформациях типа xGy или xG'y , где x и y могут быть t , g или g' . В экспериментальных спектрах КР жидкого ЭГ эта линия высокоинтенсивная, следовательно, в жидком ЭГ молекулы в указанных конформациях присутствуют большом количестве. Этот результат также подтверждается полученными содержаниями молекул ЭГ в различных конформациях на основе расчётов.
Некоторые особенности спектров КР гликолей, особенно в спектральной области 26004000 см-1, не могут быть объяснены без учёта межмолекулярных взаимодействий.
Список литературы Определение конформационного состава этиленгликоля методом спектроскопии КР и расчетов DFT
- Bakó I., Grósz T., Pálinkás G., Bellissent-Funel M. C. Ethylene glycol dimers in the liquid phase: A study by x-ray and neutron diffraction // The Journal of chemical physics. 2003. V. 118. №7. P. 3215-3221. https://doi.org/10.1063/1.1536163
- Kazerouni M. R., Hedberg L., Hedberg K. Conformational analysis. 21. Ethane-1, 2-diol. An electron-diffraction investigation, augmented by rotational constants and ab initio calculations, of the molecular structure, conformational composition, SQM vibrational force field, and antigauche energy difference with implications for internal hydrogen bonding // Journal of the American Chemical Society. 1997. V. 119. №35. P. 8324-8331. https://doi.org/10.1021/ja9708631
- Lomas J. S. 1H NMR spectra of ethane-1, 2-diol and other vicinal diols in benzene: GIAO/DFT shift calculations // Magnetic Resonance in Chemistry. 2013. V. 51. №1. P. 32-41. https://doi.org/10.1002/mrc.3899
- Guvench O., MacKerell A. D. Quantum mechanical analysis of 1, 2-ethanediol conformational energetics and hydrogen bonding // The Journal of Physical Chemistry A. 2006. V. 110. №32. P. 9934-9939. https://doi.org/10.1021/jp0623241
- Cramer C. J., Truhlar D. G. Quantum chemical conformational analysis of 1, 2-ethanediol: Correlation and solvation effects on the tendency to form internal hydrogen bonds in the gas phase and in aqueous solution // Journal of the American Chemical Society. 1994. V. 116. №9. P. 3892-3900. https://doi.org/10.1021/ja00088a027
- Howard D. L., Jørgensen P., Kjaergaard H. G. Weak intramolecular interactions in ethylene glycol identified by vapor phase OH− stretching overtone spectroscopy // Journal of the American Chemical Society. 2005. V. 127. №48. P. 17096-17103. https://doi.org/10.1021/ja055827d
- Cheng Y. L., Chen H. Y., Takahashi K. Theoretical Calculation of the OH Vibrational Overtone Spectra of 1-n Alkane Diols (n= 2–4): Origin of Disappearing Hydrogen-Bonded OH Peak // The Journal of Physical Chemistry A. 2011. V. 115. №22. P. 5641-5653. https://doi.org/10.1021/jp202030c
- Csonka G. I., Csizmadia I. G. Density functional conformational analysis of 1, 2-ethanediol // Chemical physics letters. 1995. V. 243. №5-6. P. 419-428. https://doi.org/10.1016/0009-2614(95)00846-V
- Klein R. A. Ab initio conformational studies on diols and binary diol‐water systems using DFT methods. Intramolecular hydrogen bonding and 1: 1 complex formation with water // Journal of computational chemistry. 2002. V. 23. №6. P. 585-599. https://doi.org/10.1002/jcc.10053
- Nagy P. I., Dunn III W. J., Alagona G., Ghio C. Theoretical calculations on 1, 2- ethanediol. Gauche-trans equilibrium in gas-phase and aqueous solution // Journal of the American Chemical Society. 1991. V. 113. №18. P. 6719-6729. https://doi.org/10.1021/ja00018a002
- Bultinck P., Goeminne A., Van de Vondel D. Ab initio conformational analysis of ethylene glycol and 1, 3-propanediol // Journal of Molecular Structure: THEOCHEM. 1995. V. 357. №1-2. P. 19-32. https://doi.org/10.1016/0166-1280(95)04277-D
- Kristiansen P. E., Marstokk K. M., Møllendal H., Parker L., Niinistö L. Microwave Spectrum of HOCH2CD2OH and the Assignment of a Second Hydrogen-Bonded Conformation of Ethylene Glycol // Acta Chem. Scand. 1987. V. 41. P. 403-414.
- Schwartz M. Raman study of the conformational equilibrium of ethylene glycol in dimethyl sulfoxide // Spectrochimica Acta Part A: Molecular Spectroscopy. 1977. V. 33. №11. P. 1025-1032. https://doi.org/10.1016/0584-8539(77)80104-9
- Christen D., Coudert L. H., Suenram R. D., Lovas F. J. The rotational/concerted torsional spectrum of the g′ Ga conformer of ethylene glycol // Journal of Molecular Spectroscopy. 1995. V. 172. №1. P. 57-77. https://doi.org/10.1006/jmsp.1995.1155
- Caminati W. Conformation and hydrogen bond in 1, 2-propanediol // Journal of Molecular Spectroscopy. 1981. V. 86. №1. P. 193-201. https://doi.org/10.1016/0022-2852(81)90117-X
- Chidichimo G., Imbardelli D., Longeri M., Saupe A. Conformation of ethylene glycol dissolved in a nematic-lyotropic solution: An NMR analysis // Molecular Physics. 1988. V. 65. №5. P. 1143-1151. https://doi.org/10.1080/00268978800101651
- Rodnikova M. N., Solovei A. B., Solonina I. A. Structure of crystalline ethylene glycol and a model of its structural rearrangement during melting // Russian Journal of Inorganic Chemistry. 2012. V. 57. P. 252-256. https://doi.org/10.1134/S0036023612020222
- Chopra D., Row T. N. G., Arunan E., Klein R. A. Crystalline ethane-1, 2-diol does not have intra-molecular hydrogen bonding: Experimental and theoretical charge density studies // Journal of Molecular Structure. 2010. V. 964. №1-3. P. 126-133. https://doi.org/10.1016/j.molstruc.2009.11.021
- Fortes A. D., Suard E. Crystal structures of ethylene glycol and ethylene glycol monohydrate // The Journal of chemical physics. 2011. V. 135. №23. https://doi.org/10.1063/1.3668311
- Luo R. S., Jonas J. Raman scattering study of liquid ethylene glycol confined to nanoporous silica glasses // Journal of Raman Spectroscopy. 2001. V. 32. №11. P. 975-978. https://doi.org/10.1002/jrs.786
- Krishnan K., Krishnan R. S. Raman and infrared spectra of ethylene glycol //Proceedings of the indian academy of sciences-section A. New Delhi: Springer India, 1966. V. 64. №2. P. 111-122. https://doi.org/10.1007/BF03047675
- Matsuura H., Hiraishi M., Miyazawa T. Raman spectra and energy difference between rotational isomers of ethylene glycol // Spectrochimica Acta Part A: Molecular Spectroscopy. 1972. V. 28. №12. P. 2299-2304. https://doi.org/10.1016/0584-8539(72)80209-5
- Pruettiangkura P., Ho S., Schwartz M. Thermodynamic Parameters of the Gauche-Trans Equilibrium in Ethylene Glycol // Spectroscopy Letters. 1979. V. 12. №9. P. 679-685. https://doi.org/10.1080/00387017908069193
- Murli C., Lu N., Dong Z., Song Y. Hydrogen bonds and conformations in ethylene glycol under pressure // The Journal of Physical Chemistry B. 2012. V. 116. №41. P. 12574-12580. https://doi.org/10.1021/jp306220q


