Определение лечебной тактики и выбор способа хирургического лечения больных панкреонекрозом
Автор: Лукин А.Ю., Шабунин А.В., Шиков Д.В.
Журнал: Московский хирургический журнал @mossj
Рубрика: Клинические исследования
Статья в выпуске: 3 (31), 2013 года.
Бесплатный доступ
Наибольшее количество послеоперационных специфических осложнений отмечено в группе больных с изменениями, характерными для распространенных некротических и инфильтративных изменений в поджелудочной железе, парапанкреатической и забрюшинной клетчатке. При анализе результатов лечения пришли к выводу, что показатели послеоперационной летальности находятся в зависимости от вариантов моделирования распространения патологических изменений в поджелудочной железе и забрюшинной клетчатке. Наибольшие показатели послеоперационной летальности отмечены в группах пациентов с изменениями в поджелудочной железе и забрюшин- ной клетчатке, характерными для «Модели-3» и «Модели-4». Таким образом, моделирование различных вариантов развития панкреонекроза может быть использовано для прогнозирования течения и исхода заболевания.
Панкреанекроз, некротические изменения парапанкреатической и забрюшинной клетчатки, вития панкреанекрозов
Короткий адрес: https://sciup.org/142211087
IDR: 142211087 | УДК: 616.72
Текст научной статьи Определение лечебной тактики и выбор способа хирургического лечения больных панкреонекрозом
Панкреонекроз – важная проблема неотложной абдоминальной хирургии [1–3]. В структуре основных нозологических форм хирургических стационаров г. Москвы больные острым панкреатитом занимают второе место (25%) после острого аппендицита (29%). По темпам роста острый панкреатит (в течение 2005–2012 гг.) опережает все другие неотложные заболевания органов брюшной полости. Среди всех больных острым панкреатитом пациенты с деструктивными формами составляют 15–25%. Частота инфицированных форм среди больных панкреонекрозом варьирует в широких пределах (25–80%). Общая летальность при остром панкреатите составляет 3–6%; послеоперационная – 11–29%; летальность при гнойно-септических осложнениях достигает 34–62%.
Для панкреонекроза характерно разнообразие форм течения. Неудовлетворительные результаты лечения связаны с несвоевременной диагностикой. С широким использованием современных инструментальных методов (КТ, МРТ) диагностика панкреонекроза в последние годы значительно улучшилась. Однако и эти методы в отсутствии четкого диагностического алгоритма не в состоянии определить оптимальную лечебную тактику. Используемые в настоящее время диагностические критерии не всегда позволяют определить показания к различным способам хирургического лечения. Недостаточно отработаны критерии продолжительности применения миниинвазивных вмешательств и принципы этапного лечения. Предметом дискуссий остаются вопросы определения выбора сроков хирургического лечения, оценки эффективности проводимого лечения при различных формах панкреонекроза [3–9].
На протяжении последних 30-ти лет вопросы тактики лечения панкреонекроза неоднократно пересматривались. Выполнялись травматичные вмешательства. Частью хирургов оптимальной считалась тактика проведения лапаротомии, абдоминизации поджелудочной железы, оментобур-состомии. Ряд хирургов, с появлением миниинвазивных технологий, прилагали усилия к тому, чтобы использовать их в качестве единственного и окончательного способа лечения.
Отправной точкой в стандартизации классификации и лечебной тактики при остром панкреатите следует считать международный консенсус 1992 года в Атланте. Компьютерная томография (КТ) послужила значительному прогрессу диагностики панкреонекроза [10, 11]. Рэнсон и Балтазар в 1981 году предложили использовать КТ для оценки тяжести перипанкреатических изменений в соответствии с ориги- нальной шкалой. В 1990 году авторы модифицировали шкалу с учетом в/в контрастирования и определения объема некроза паренхимы поджелудочной железы.
Следующий этап эволюции взглядов на вопросы лечебной тактики при панкреонекрозе – международный консенсус панкреатологов, принятый в 2002 году в Гайдельбер-ге. Данное руководство не отвечало на все вопросы выбора оптимальной хирургической тактики. В 2010 году Виндзор с соавт. провели анализ 30 различных руководств по лечению острого панкреатита, и лишь в 9 из них имелись общие принципы. В 2012 году международный мультидисциплинарный консенсус определил 19 положений в отношении классификации острого панкреатита, оптимальных способов и сроков вмешательств. В данном консенсусе подчеркнуто преимущественное значение миниинвазивных вмешательств.
Классификации КТ-изменений, а также способов хирургического лечения и хирургических доступов, представленные в различных руководствах, на наш взгляд, сложны для практического применения. Очевидна необходимость дальнейшей разработки диагностических и лечебных алгоритмов, применяемых при панкреонекрозе.
Наша клиника обладает опытом лечения 523 больных панкреонекрозом за период с 2005 по 2012 гг. В лечении всех больных применялась консервативная терапия, эффективность которой определялась клинико-лабораторными данными и результатами инструментальных методов обследования. На основании этих же диагностических методов у 375 больных были определены показания к хирургическому лечению. В обязательном порядке использовали УЗИ и динамическую компьютерную томографию. При поступлении пациентам проводили КТ с болюсным контрастированием для определения исходного объема панкреонекроза, пери-панкреатических изменений и оценки эффективности проводимой терапии. В последующем (каждые 7–10 суток) выполняли повторные КТ-исследования.
С целью изучения достоверности лучевых методов диагностики в 77 случаях проведен сравнительный анализ результатов КТ с характером интраоперационных находок, а также с морфологическими изменениями, выявляемыми при гистологическом изучении биопсийного материала, полученного в ходе хирургических вмешательств (n=55) или (в случае летального исхода) патолого-анатомических исследований (n=22). Выявлено достоверное соответствие между объемом, распространенностью и характером изменений, определяемых при КТ, и интраоперационными находками.
Сравнительный анализ изменений в поджелудочной железе, парапанкреатической и забрюшинной клетчатке, выявляемых при динамической КТ, и результатов морфологического исследования биопсийного материала показал их соответствие во всех случаях.
В ткани поджелудочной железы и жировой клетчатки, оцененной при КТ >25 HU и на операции жизнеспособной, при гистологическом исследовании отмечались междольковый отек и воспалительная инфильтрация. В областях, которые соответствовали 15–25 HU, интраоперационно определялся инфильтрат, а гистологически – отек, воспалительная инфильтрация, очаги жирового некроза, геморрагическое пропитывание, участки тромбоза микроциркуляторного русла. В тех областях, где при КТ плотность соответствовала 0–15 HU, определялись некроз тканей, секвестрация с преобладанием жидкостного компонента.
В соответствии с поставленными задачами в процессе исследования мы пришли к выводу, что среди многочисленных признаков, характеризующих панкреонекроз, существуют определяющие критерии, поддающиеся качественному и количественному анализу. Этими критериями являются: объем первоначального некроза поджелудочной железы, его локализация, а также выраженность, характер и распространенность экстрапанкреатического воспалительно-некротического процесса. Именно объем и локализация некроза поджелудочной железы, парапан-креатической и забрюшинной клетчатки, его изменения в динамике определяют закономерность развития патологического процесса, позволяют прогнозировать развитие осложнений, определять оптимальную лечебную тактику.
Проведенное исследование позволило определить закономерности развития патологических изменений в поджелудочной железе и забрюшинной клетчатке при пан-креонекрозе, что предоставило возможность применить принципы моделирования течения данного заболевания. Наиболее важными следует считать следующие критерии моделирования: объем некроза паренхимы поджелудочной железы; локализация и распространенность некротических и инфильтративных изменений в парапанкреатической и забрюшинной клетчатке, их динамика; объем и локализация жидкостных скоплений, наличие сообщения между ними; наличие признаков секвестрации и абсцедирования. Нами определены основные клинико-морфологические модели панкреонекроза и парапанкреатических изменений (рис. 1):
– «Модель-1» – V некроза поджелудочной железы <30%, или не определяется, парапанкреатический инфильтрат, жидкостное скопление;
– «Модель-2» – V некроза поджелудочной железы 30– 50% в дистальных отделах, парапанкреатический инфильтрат по «левому типу»;
– «Модель-3» – V некроза поджелудочной железы 30– 50% в проксимальных отделах, парапанкреатический инфильтрат по «правому типу»;
– «Модель-4» – V некроза поджелудочной железы 30–50% и более с разобщением жизнеспособных проксимальных и дистальных отделов, парапанкреатический инфильтрат по «правому, центральному и левому типам»;
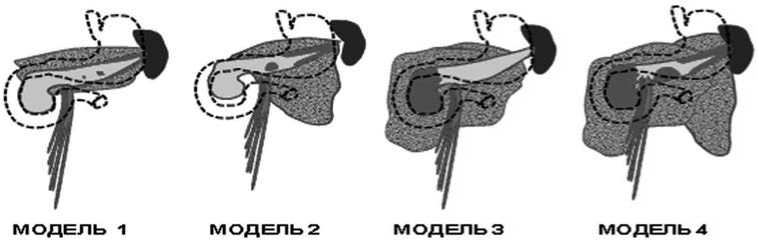
Рис. 1. Клинико-морфологическое моделирование панкреонекроза
служили показанием к пункционно-дренируюшему способу, который был использован в качестве окончательного (рис. 3).
Клинико-морфологические изменения, характерные для «Модели-2», были выявлены у 159 больных. У 53 пациентов в качестве окончательного применен пункционно-дренирующий способ (рис. 4).
В 58 случаях объем некроза ПЖ соответствовал 30–50%. Изменения в
– для всех моделей – характер изменений в забрюшинной клетчатке: «а» – отсутствие жидкостного скопления, «б» – наличие жидкостного скопления.
К наиболее благоприятным вариантам относим мелкоочаговый панкреонекроз, не определяемый при КТ, который сопровождается маловыраженной парапанкреатической инфильтрацией и мелкоочаговый панкреонекроз менее 30% дистальных отделов, при котором формируется пара-панкреатический и забрюшинный инфильтрат по «левому типу». Наиболее тяжелые формы панкреонекроза – крупноочаговый некроз проксимальных отделов, а также крупноочаговый некроз с локализацией в различных отделах железы с поражением главного панкреатического протока, что служит причиной формирования обширных забрюшинных инфильтратов не только по правому и левому, но и по центральному типам.
В ходе проведенного анализа клинико-морфологические изменения, характерные для «Модели-1», выявлены у 191 больного. Из них у 148 пациентов удалось купировать заболевание применением комплексной консервативной терапии (рис. 2).
В 43 случаях клинические и КТ-данные соответствовали «Модели-1», определялись единичные жидкостные скопления объемом более 50 мл. Подобные изменения забрюшинной клетчатке соответство-
б
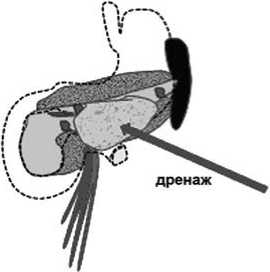
Рис. 3. «Модель-1»: а,б – КТ-данные – жидкостное скопление по переднему контуру в области тела поджелудочной железы до и после дренирования, инфильтрация пара-панкреатической клетчатки; в – схема патологических изменений в поджелудочной железе и забрюшинной клетчатке
в
а б
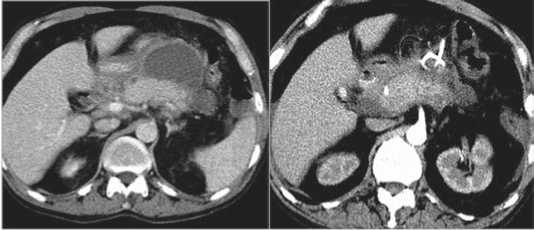
Рис. 2. «Модель-1»: а – КТ данные - визуализируется «изъеден-ность» контура контрастируемой жизнеспособной паренхимы поджелудочной железы, инфильтрация парапанкреатической и забрюшинной клетчатки; б – схема патологических изменений в поджелудочной железе и забрюшинной клетчатке
вали инфильтрату без наличия условий для применения пункционно-дренирующего способа. Отсутствие положительной динамики от проводимой комплексной консервативной терапии, наличие признаков инфицирования служило показанием для применения полостного способа (выполнялись некрсеквестрэктомии) (рис. 5).
У 48 пациентов применение пункционно-дренирующего способа на фоне комплексной консервативной терапии не имело эффекта, в связи с чем применен этапный способ лечения (рис. 6).
У 95 больных выявлены клинико-морфологические изменения, характерные для «Модели-3». В 21 случае удалось купировать заболевание на фоне применения пункционно-дренирующего способа, у 74 больных было применено этапное лечение (рис. 7).
а
в
б
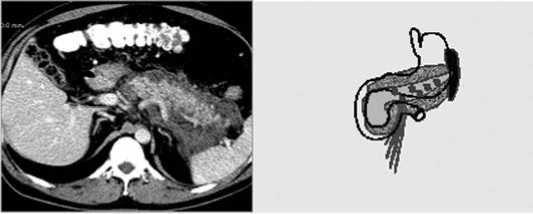
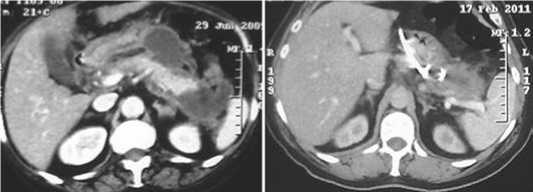
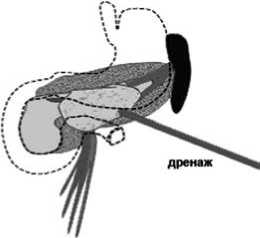
Рис. 4. «Модель-2»: а, б – КТ-данные – в области хвоста поджелудочной железы визуализируется неконтрастируемая зона некроза, жидкостное скопление по переднему контуру поджелудочной железы в области тела, инфильтрация парапанкреатиче-ской клетчатки до и после приме-ненияпункционно-дренирующего способа хирургического лечения; в – схема патологических изменений в поджелудочной железе и забрюшинной клетчатке
а б
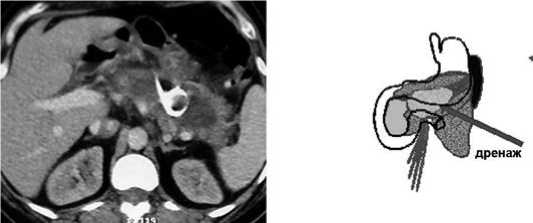
Рис. 6. «Модель-2»: а – КТ-данные - в области хвоста и тела поджелудочной железы визуализируется неконтрастируемая зона некроза, жидкостное скоплениие в зоне секвестрации некроза после применения пункционно-дренирующего способа хирургического лечения, инфильтрация парапанкреатической клетчатки; б – схема патологических изменений в поджелудочной железе и забрюшинной клетчатке
а
б
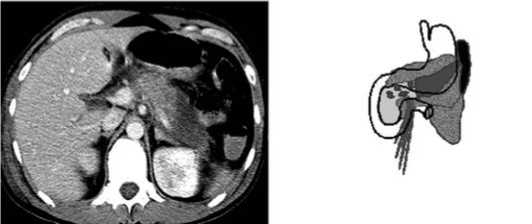
Рис. 5. «Модель-2»: а – КТ-данные - визуализируется неконтра-стируемая зона некроза хвоста и тела поджелудочной железы с инфильтративными изменениями парапанкреатичесокой клетчатки; б – схема патологических изменений в поджелудочной железе и забрюшинной клетчатке
а б
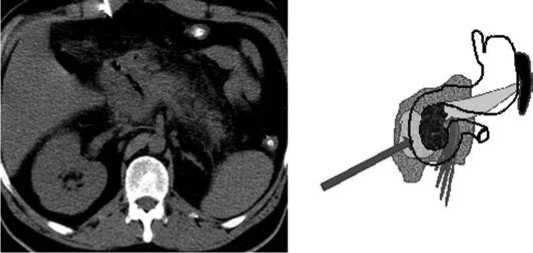
Рис. 7. «Модель-3»: а – КТ-данные – визуализируется некроз и секвестрация головки поджелудочной железы. Неконтрастируемая зона головки поджелудочной железы с газом, инфильтрация пара-панкреатической клетчатки с жидкостным компонентом; б – схема патологических изменений в поджелудочной железе и забрюшинной клетчатке.
В 78 случаях выявлены клинико-морфологические изменения, характерные для «Модели-4», когда по данным КТ определялись различные по объему и локализации некрозы поджелудочной железы с признаками разобщения проксимальных и дистальных жизнеспособных отделов, распространенные изменения в парапанкреатической и забрюшинной клетчатке с незавершенной секвестрацией, жидкостными скоплениями (рис. 8).
Данные патологические изменения служили показанием к применению этапного способа хирургического лечения. Применение миниинвазивных способов лечения в качестве первого этапа способствовало стабилизации состояния больного, отграничению воспалительно-некротического процесса в поджелудочной железе, парапанкреатической и забрюшинной клетчатке, позволяло проводить полостные
б
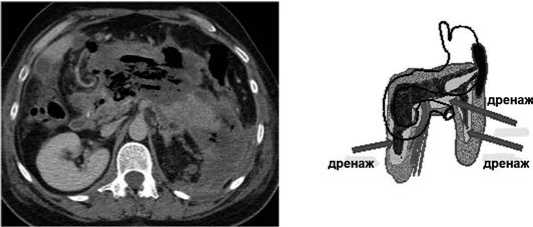
Рис. 8. «Модель-4»: а – КТ-данные некроза головки и тела поджелудочной железы, хвост поджелудочной железы жизнеспособен. Инфильтративные парапанкреатические изменения поджелудочной железы по правому, центральному и левому типам; секвестрация некрозов парапанкреатической и забрюшинной клетчатки с формированием скоплений жидкости с газом; б – схема патологических изменений в поджелудочной железе и забрюшинной клетчатке
вмешательства (полноценную одномоментную секвестрэк-томию) в более поздние сроки.
Результаты лечения больных панкреонекрозом в зависимости от моделирования патологических изменений в поджелудочной железе и забрюшинной клетчатке показаны на диаграмме 1.
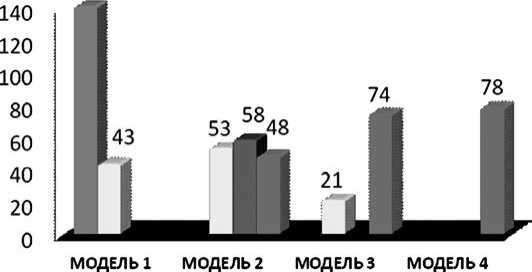
■ КОНСЕРВАТИВНАЯ ТЕРАПИЯ ПДС
■ ПОЛОСТНОЙ СПОСОБ ■ ЭТАПНЫЙ СПОСОБ
Диаграмма 1. Результаты лечения больных панкреонекрозом в зависимости от моделирования патологического процесса
Таким образом, моделирование патологических изменений в поджелудочной железе и забрюшинной клетчатке позволяет определить оптимальные способы лечения больных панкреонекрозом. Выбор способа хирургического вмешательства и сроков его применения диктуется клинико-лабораторными данными, локализацией, распространенностью и характером морфологических изменений в поджелудочной железе, парапанкреатической и забрюшинной клетчатке, наиболее характерные из которых приведены в разработанных моделях панкреонекроза.
Считаем необходимым подчеркнуть, что важнейший этап хирургического лечения – вмешательства, направленные на секвестрэктомию и дренирование зон некроза поджелудочной железы и забрюшинной клетчатки.
Во многих хирургических клиниках полостной способ секвестрэктомии является стандартом в лечении инфицированного панкреонекроза. Способ заключается в лапаротомии (и/или люмботомии) и мануальной секвестрэкто-мии. В практической деятельности предпочтение отдаем органосберегающим принципам. После секвестрэктомии формируется оментобурсостома (и/или люмбостома), с целью создания отграниченного от брюшной полости доступа к зоне секвестрации и проведения ревизий, санаций. Лапа-ростомия с последующими программными секвестрэкто-миями, на наш взгляд, является неприемлемым способом и может быть использована в качестве крайней меры. Например, при синдроме интраабдоминальной гипертензии
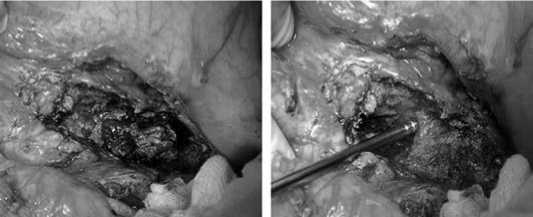
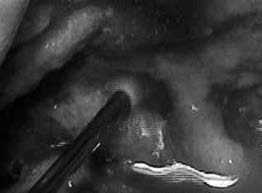
Рис. 9. Полостная секвестрэкто-мия. Использование ультразвукового дезинтегратора или перитоните, а также при измененной анатомии верхних отделов брюшной полости после перенесенных ранее хирургических вмешательств. Наиболее известны два способа санаций: открытый и продолженный лаваж.
В ходе полостной секвестрэктомии, помимо диссекции, мы использовали ультразвуковой дезинтегратор, что позволяло выполнять полноценную секвестрэктомию менее травматично.
Миниинвазивные способы хирургического лечения панкреонекроза имеют неоспоримые преимущества – отсутствие послеоперационных системных проявлений: воспалительной реакции, септического шока, полиорганной недостаточности, а также низкий процент послеоперационных осложнений.
Чрескожные вмешательства (пункционно-дренирующий способ) использован нами в качестве адъювантного в лечении резидуальных очагов некроза и жидкостных скоплений после полостных вмешательств, но чаще применялся как первый этап лечения.
К способу лапароскопической секвестрэктомии относимся сдержанно, ввиду высокого риска развития перитонита и высокой вероятности повторных вмешательств. При данном варианте проведения секвестрэктомии чрезвычайно трудно достигнуть важного принципа – отграничения брюшной полости от зоны некротических изменений в поджелудочной железе и забрюшинной клетчатке.
В 11 случаях («Модель-2» – 5 пациентов, «Модель-3» – 6 пациентов) нами был применен видеоассистированный ретроперитонеоскопический способ секвестрэктомии.
Первым этапом использовали пункционно-дренирующий способ. Далее пункционный канал дилатировали до размера, позволяющего провести жесткий эндоскоп для прямой визуализации, секвестрэктомии и промывания некротической полости. Таким образом, использована методика видеоасси-стированной внебрюшинной секвестрэктомии.
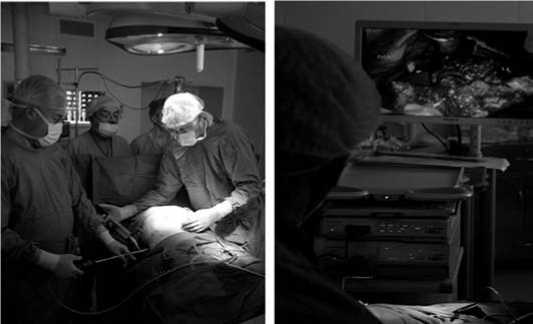
Рис. 10. Проведение видеоассистированной внебрюшинной секве-стрэктомии
а
б
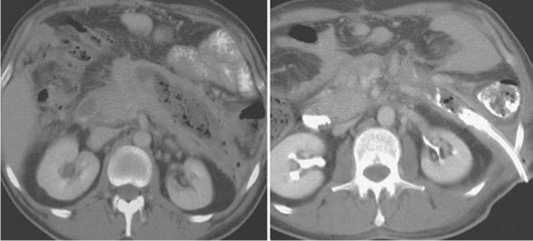
Рис. 11. Результаты применения видеоассистированного ретропе-ритонеоскопического способа секвестрэктомии: а – КТ-данные до ретроперитонеоскопии, секвестрэктомии, дренирования; б – КТ-данные после проведения ретроперитонеоскопии, секвестрэктомии и дренирования
а б
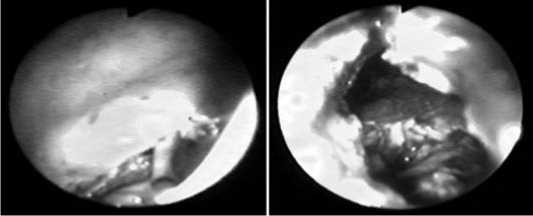
Рис. 12. Эндоскопическая транслюминальная секвестрэктомия: а – гастротомия в зоне задней стенки желудка, прилежащей к полости секвестрации; б – гастротомический доступ расширен, визуализируется секвестр
В 9 случаях («Модель-1» – 2, «Модель-2» – 4, «Модель-3» – 3) применен миниинвазивный способ секвестрэктомий – транслюминальная эндоскопическая секвестрэктомия.
Способ заключается в прямом прохождении в полость некроза через заднюю стенку желудка. Условием для проведения данного вмешательства является локализация фо- куса некроза, жидкостного скопления в непосредственной близости от стенки желудка или ДПК. Доступ определялся по данным Эндо-УЗИ. Секвестрэктомия и санация проводилась посредством специального инструментария и техники. После выполнения гастротомии осуществлялась прямая секвестрэктомия при помощью щипцов и корзин. Для санации полости требовалось от 3 до 6 процедур.
Таким образом, применяемые в лечении инфицированного панкреонекроза и парапанкреатита открытые хирургические вмешательства нередко сопровождаются развитием полиорганной недостаточности, имеют высокий процент послеоперационных осложнений. Мы считаем, что во многих случаях можно ограничиться миниинвазивными вмешательствами при условии проведения адекватной комплексной консервативной терапии.
Разработанные модели панкреонекроза позволяют осуществить выбор оптимального доступа для миниин-вазивного или открытого вмешательства (рис. 13). Для «Модели-1», при необходимости хирургического лечения, оптимально применение пункционно-дренирующего и эндоскопического (транслюминальная секвестрэктомия) способов. Для изменений, характерных для «Модели-2» и «Модели-3», целесообразно использование пункционно-дренирующего внебрюшинного способа соответственно слева и справа, с последующим применением ретропери-тонеоскопии или открытых вмешательств (люмботомия, люмбостомия). В лечении больных с изменениями, характерными для «Модели-4», оптимален этапный способ хирургического лечения: сначала используется один из вариантов миниинвазивных вмешательств (пункционно-дренирующий и ретроперитонеоскопический, транслюминальный способы) или их комбинация. Применение ми-ниинвазивных вмешательств способствует отграничению воспалительно-некротического процесса, профилактике развития полиорганной недостаточности, создает предпосылки к проведению открытых хирургических вмешательств в оптимальные сроки (с 21–28-х суток от начала заболевания) из 2-подреберного или люмботомического доступов (возможно их сочетание).
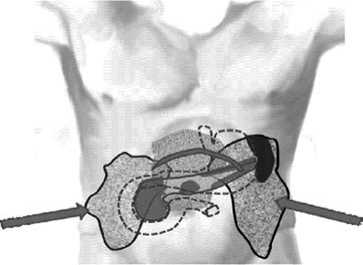
Рис. 13. Выбор доступа в зависимости от модели панкреонекроза
Специфические послеоперационные осложнения у больных панкреонекрозом (n=375)
|
Осложнение |
Модели |
|||
|
«Модель-1» (n=43) |
«Модель-2» (n=159) |
«Модель-3» (n=95) |
«Модель-4» (n=78) |
|
|
Аррозивное кровотечение |
2 (4,7%) |
12 (7,6%) |
3 (3,2%) |
4 (5,1%) |
|
Неполный внутренний дуоденальный свищ |
– |
1 (0,6%) |
1 (1,1%) |
– |
|
Неполный наружный дуоденальный свищ |
– |
– |
6 (6,3%) |
5 (6,4%) |
|
Неполный внутренний толстокишечный свищ |
1 (2,3%) |
4 (2,5%) |
4 (4,2%) |
– |
|
Неполный наружный толстокишечный свищ |
– |
5 (3,1%) |
– |
7 (8,9%) |
|
Спаечная кишечная непроходимость |
– |
3 (1,9%) |
1 (1,1%) |
– |
|
Итого: |
3 (6,9%) |
25 (15,7%) |
15 (15,9%) |
16 (20,5%) |
|
Всего (n=375) |
59 (15,7%) |
|||
Мы проанализировали специфические осложнения, отмеченные в послеоперационном периоде у пациентов с пан-креонекрозом в зависимости от результатов моделирования.
Наибольшее количество послеоперационных специфических осложнений отмечено в группе больных с изменениями, характерными для «Модели-3» и «Модели-4», то есть в случаях распространенных некротических и инфильтративных изменений в поджелудочной железе, парапанкреа-тической и забрюшинной клетчатке.
При анализе результатов лечения больных панкреоне-крозом мы пришли к выводу, что показатели послеоперационной летальности находятся в зависимости от вариантов моделирования распространения патологических изменений в поджелудочной железе и забрюшинной клетчатке.
Наибольшие показатели послеоперационной летальности отмечены в группах пациентов с изменениями в поджелудочной железе и забрюшинной клетчатке, характерными
Таблица 2
Показатели послеоперационной летальности у больных панкреонекрозом в зависимости от вариантов моделирования
|
Вариант моделирования |
Показатели летальности |
|
«Модель-1» (n=43) |
3 (6,9%) |
|
«Модель-2» (n=159) |
23 (14,4%) |
|
«Модель-3» (n=95) |
21 (22,1%) |
|
«Модель-4» (n=78) |
22 (28,2%) |
|
Всего (n=375) |
69 (18,4%) |
Таблица 1
для «Модели-3» и «Модели-4». Таким образом, моделирование различных вариантов развития панкреонекроза может быть использовано для прогнозирования течения и исхода заболевания.
Практическоеприменение в лечениибольных панкреонекрозом клинико-морфологических параллелей позволило определить основные критерии развития патологического процесса в поджелудочной железе и забрюшинной клетчатке. На основании этого разработаны основные модели панкреонекроза и парапанкреатита, что, в свою очередь, предоставило возможность выбора оптимального способа лечения и прогнозирования результатов лечения.
Выводы
Проведенный анализ результатов лечения пациентов с панкреонекрозом послужил основанием для следующих выводов:
– тактика лечения больных панкреонекрозом определяется объемом и локализацией некроза паренхимы поджелудочной железы, расположением и распространенностью патологических изменений в парапанкреатической и забрюшинной клетчатке;
– моделирование течения панкреонекроза с использованием в диагностическом комплексе динамической КТ позволяет осуществить выбор оптимальных способов хирургического лечения, прогнозировать результаты лечения, снизить частоту осложнений и летальных исходов.
Список литературы Определение лечебной тактики и выбор способа хирургического лечения больных панкреонекрозом
- Dellinger E.P., Forsmark C.E., Layer P., E., Petrov M.S., Shimosegawa T., Siriwardena A.K., Uomo G., Whitcomb D.C., Windsor J.A. Determinant based classification of acute pancreatitis severity: an international multidisciplinary consultation//Ann. Surg. 2012. Vol.256 (6). P. 875-880.
- Banks P.A., Bollen T.L., Dervenis C., Gooszen H.G., Johnson C.D., Sarr M.G., Tsiotos G.G., Vege S.S. Acute Pancreatitis Classification Working Group. Classification of acute pancreatitis-2012: revision of the Atlanta classification and definitions by international consensus//Gut. 2013. Vol. 62 (1). P. 102-111.
- Freeman M.L., Werner J., van Santvoort H.C., Baron T.H., Besselink M.G., Windsor J.A., Horvath K.D., van Sonnenberg E., Bollen T.L., Vege S.S. Interventions for necrotizing Pancreatiti. Summary of Multidisciplinary Consensus Conference//Pancreas. 2012. Vol. 41 (8). P. 1176-1194.
- Loveday B.P., Petrov M.S., Connor S. et al. A comprehensive classification of invasive procedures for treating the local complications of acute pancreatitis based on visualization, route, and purpose//Pancreatology. 2011. Vol. 11. P. 406-413. Специфические послеоперационные осложнения у больных панкреонекрозом (n=375)
- Garg P.K., Sharma M., Madan K. et al. Primary conservative treatment results in mortality comparable to surgery in patients with infected pancreatic necrosis//Clin. Gastroenterol. Hepatol. 2010. Vol. 8. P. 1089-1094.
- Kingham T.P., Shamamian P. Management and spectrum of complications in patients undergoing surgical debridement for pancreatic necrosis//Am. Surg. 2008. Vol. 74. P. 1050-1056.
- Ishikawa K., Idoguchi K., Tanaka H., Tohma Y., Ukai I., Watanabe H., Matsuoka T., Yokota J., Sugimoto T. Classification of Acute pancreatitis based on retroperitoneal extension: application of the concept of interfascial planes//Eur. J. Radiol. 2006. Vol. 60(3). P. 445-452.
- Дюжева Т.Г., Джус Е.В., Рамишвили В.Ш., Шефер А.В., Платонова Л.В., Гальперин Э.И. Ранние КТ-признаки прогнозирования различных форм парапанкреонекроза//Анналы хирургической гепатологии. 2009. Т. 14, № 4. С. 54-63.
- Petrov M.S. Abdominal fat: a key player in metabolic acute pancreatitis//Am. J. Gastroenterol. 2013. Vol. 108 (1). P. 140-142.
- Balthazar E.J., Robinson D.L., Megibow A.J. Ranson J.H. Acute pancreatitis: value of CT in establishing prognosis//Radiology. 1990. Vol.174 (2). P. 331-336.
- Mortele K.J., Wiesner W., Intriere L., Shaukas S., Zou K.H., Kalantari B.N., Peres A., van Sounn., Banks enberg E., Ros P.P.A., Silverman S.G. A Modified CT Severity Index for Evaluating Acute Pancreatitis: Improved Correlation with Patient Outcome//Am. J. Roentgenol. 2004. Vol. 183 (5). P. 1261-1265.


